Trắc nghiệm Bài 1. Đốt cháy este không no - Hóa 12
Đề bài
Công thức tổng quát của este không no, đơn chức, mạch hở có 1 liên kết C=C là :
-
A.
CnH2n-4O2
-
B.
CnH2nO4
-
C.
CnH2nO2, n ≥ 2
-
D.
CnH2n-2O2, n ≥ 3
Đốt cháy hoàn toàn x mol este X tạo bởi ancol no, đơn chức, mạch hở và axit không no (chứa một liên kết đôi), đơn chức, mạch hở thu được 11,2 lít CO2 (đktc) và 7,2 gam H2O. Giá trị của x là
-
A.
0,05.
-
B.
0,15.
-
C.
0,10.
-
D.
0,20.
Đốt cháy hoàn toàn m gam este X tạo bởi ancol no đơn chức mạch hở và axit không no (chứa 1 liên kết C=C), đơn chức mạch hở thu được 6,72 lít CO2 (đktc) và 3,6 gam H2O. Giá trị của m là :
-
A.
4,2
-
B.
7,2
-
C.
2,6
-
D.
5,7
Đốt cháy hoàn toàn một lượng este X đơn chức thấy thể tích CO2 thu được bằng thể tích của O2 cần dùng và gấp 1,5 lần thể tích hơi nước (ở cùng đk nhiệt độ, áp suất). Biết X tham gia phản ứng tráng gương. CTCT của X là:
-
A.
HCOOC≡CH.
-
B.
HCOOCH=CHCH3
-
C.
HCOOCH=CH2.
-
D.
HCOOCH2CH3.
Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là:
-
A.
25%
-
B.
27,92%
-
C.
72,08%
-
D.
75%
Hỗn hợp CH3COOC2H5 , HCOOC3H5 và HCOOC3H3. Hỗn hợp X có tỉ khối hơi so với O2 là dX/O2 = 2,7. Đốt cháy hoàn toàn 0,015 mol X ; sau phản ứng thu được hỗn hợp sản phẩm Y. Hấp thụ Y vào dung dịch Ca(OH)2 dư. Kết luận nào dưới đây đúng?
-
A.
Khối lượng bình giảm 3,504
-
B.
Khối lượng bình tăng 3,504
-
C.
Khối lượng dung dịch giảm 5,304
-
D.
Khối lượng dung dịch tăng 2,496
Đốt cháy hoàn toàn 20,1 gam hỗn hợp X gồm 2 este đơn chức, không no (có 1 nối đôi C=C), kế tiếp nhau trong cùng dãy đồng đẳng cần 146,16 lít không khí (đktc), thu được 46,2 gam CO2. Biết rằng trong không khí oxi chiếm 20% về thể tích. Công thức phân tử của 2 este là:
-
A.
C4H6O2 và C5H8O2
-
B.
C5H8O2 và C6H10O2
-
C.
C4H8O2 và C5H10O2
-
D.
C5H10O2 và C6H12O2
Đốt cháy hoàn toàn một este đơn chức, mạch hở X (phân tử có số liên kết p nhỏ hơn 3), thu được thể tích khí CO2 bằng 6/7 thể tích khí O2 đã phản ứng (các thể tích khí đo ở cùng điều kiện). Cho m gam X tác dụng hoàn toàn với 200 ml dung dịch KOH 0,7M thu được dung dịch Y. Cô cạn Y thu được 12,88 gam chất rắn khan. Giá trị của m là
-
A.
7,20.
-
B.
6,66.
-
C.
8,88.
-
D.
10,56.
Đốt cháy hoàn toàn 6,8 gam một este A đơn chức chứa vòng benzen thu được CO2 và H2O. Hấp thụ toàn bộ sản phẩm này vào bình đựng dung dịch Ca(OH)2 lấy dư thấy khối lượng bình tăng 21,2 gam đồng thời có 40 gam kết tủa. Số CTCT có thể có của A
-
A.
2
-
B.
3
-
C.
5
-
D.
6
E là este của axit cacboxylic no đơn chức (X) và ancol không no đơn chức có một nối đôi C=C (Y). Đốt a mol E thu được b mol CO2; đốt a mol X thu được c mol CO2; đốt a mol Y thu được 0,5b mol H2O. Quan hệ giữa b và c là:
-
A.
b= c.
-
B.
b = 2c.
-
C.
c= 2b.
-
D.
b= 3c.
Đốt cháy hoàn toàn 2,01 gam hỗn hợp X gồm axit acrylic, vinyl axetat, metyl metacrylat. Toàn bộ sản phẩm cháy cho qua dung dịch Ca(OH)2 dư, sau phản ứng thu được 9 gam kết tủa và dung dịch X. Vậy khối lượng dung dịch X đã thay đổi so với dung dịch Ca(OH)2 ban đầu là:
-
A.
Giảm 3,87 gam.
-
B.
Tăng 5,13 gam.
-
C.
Tăng 3,96 gam.
-
D.
Giảm 9 gam
Hỗn hợp X gồm 1 este đơn chức, không no có một nối đôi C = C mạch hở (A) và 1 este no, đơn chức mạch hở (B). Đốt cháy hoàn toàn 0,15 mol X rồi cho toàn bộ sản phẩm cháy hấp thụ hoàn toàn vào bình đựng dung dịch Ca(OH)2 dư. Sau phản ứng thấy khối lượng bình tăng 23,9 gam và có 40 gam kết tủa. CTPT của 2 este là:
-
A.
C2H4O2 và C3H4O2
-
B.
C3H6O2 và C5H8O2
-
C.
C2H4O2 và C5H8O2
-
D.
C2H4O2 và C4H6O2
Đốt cháy hoàn toàn 5,4 gam hỗn hợp X gồm axit acrylic, axit oleic, vinyl axetat, metyl acrylat cần vừa đủ V lít O2(đktc). Hấp thụ toàn bộ sản phẩm chát vào nước vôi trong dư, sau khi phản ứng hoàn toàn thu được 30 gam kết tủa. Giá trị của V là
-
A.
8,512.
-
B.
8,736.
-
C.
8,064.
-
D.
8,96.
Đốt cháy hoàn toàn m gam hỗn hợp A gồm 3 este X, Y, Z (đều mạch hở và chỉ chứa chức este, X có khối lượng nhỏ nhất trong A) thu được số mol CO2 lớn hơn số mol H2O là 0,25 mol. Mặt khác, m gam A phản ứng vừa đủ với dung dịch NaOH thu được 22,2 gam hai ancol hơn kém nhau 1 nguyên tử cacbon và hỗn hợp T gồm hai muối. Đốt cháy hoàn toàn T cần vừa đủ 0,275 mol O2, thu được CO2, 0,35 mol Na2CO3 và 0,2 mol H2O. Phần trăm khối lượng của X trong A là
-
A.
28,92%.
-
B.
22,07%.
-
C.
28,43%.
-
D.
42,65%.
Cho X và Y (MX < MY) là hai este đều mạch hở, không phân nhánh và không chứa nhóm chức khác. Đốt cháy X cũng như Y với lượng oxi vừa đủ, luôn thu được CO2 có số mol bằng số mol O2 đã phản ứng. Đun nóng 15,12 gam hỗn hợp E chứa X, Y (số mol của X gấp 1,5 lần số mol Y) cần dùng 200 ml dung dịch KOH 1M, thu được hỗn hợp F chứa 2 ancol và hỗn hợp K chứa 2 muối. Dẫn toàn bộ F qua bình đựng Na dư thấy khối lượng bình tăng 7,6 gam. Đốt cháy hoàn toàn hỗn hợp muối K cần dùng 0,21 mol O2. Phần trăm khối lượng của Y trong hỗn hợp E là
-
A.
58,25%.
-
B.
65,62%.
-
C.
52,38%.
-
D.
47,62%.
Lời giải và đáp án
Công thức tổng quát của este không no, đơn chức, mạch hở có 1 liên kết C=C là :
-
A.
CnH2n-4O2
-
B.
CnH2nO4
-
C.
CnH2nO2, n ≥ 2
-
D.
CnH2n-2O2, n ≥ 3
Đáp án : D
Xem lại phản ứng đốt cháy một số este thường gặp
Este no đơn chức có CTTQ: CnH2nO2
Este không no đơn chức mạch C có 1 liên kết C=C: CnH2n-2O2
Este đơn giản nhất thỏa mãn điều kiện trên: HCOOCH=CH2
Đốt cháy hoàn toàn x mol este X tạo bởi ancol no, đơn chức, mạch hở và axit không no (chứa một liên kết đôi), đơn chức, mạch hở thu được 11,2 lít CO2 (đktc) và 7,2 gam H2O. Giá trị của x là
-
A.
0,05.
-
B.
0,15.
-
C.
0,10.
-
D.
0,20.
Đáp án : C
- Tính số mol CO2, H2O.
- Tìm x.
Đốt cháy este không no chứa 1 nối đôi (CnH2n-2O2 ) có: ${{n}_{este}}~=\text{ }{{n}_{C{{O}_{2}}}}~\text{-}{{n}_{{{H}_{2}}O}}$
$\begin{array}{*{35}{l}}{{n}_{C{{O}_{2}}}}=\text{ }0,5\text{ }mol \\{{n}_{{{H}_{2}}O}}=\text{ }0,4\text{ }mol \\{{n}_{este}}~=\text{ }{{n}_{C{{O}_{2}}}}~\text{-}{{n}_{{{H}_{2}}O}}=\text{ }0,5\text{-}\text{ }0,4=\text{ }0,1\text{ }mol \\\end{array}$
Đốt cháy hoàn toàn m gam este X tạo bởi ancol no đơn chức mạch hở và axit không no (chứa 1 liên kết C=C), đơn chức mạch hở thu được 6,72 lít CO2 (đktc) và 3,6 gam H2O. Giá trị của m là :
-
A.
4,2
-
B.
7,2
-
C.
2,6
-
D.
5,7
Đáp án : B
- Tính số mol este
Đốt cháy este X đơn chức, không no 1 nối đôi: ${{n}_{este}}=\text{ }{{n}_{C{{O}_{2}}}}\text{-}{{n}_{{{H}_{2}}O}}$
- Tính m: m = mH + mC + mO
Este X có CTTQ: CnH2n-2O2
nCO2 = 0,3 mol ; nH2O = 0,2 mol
${{n}_{este}}=\text{ }{{n}_{C{{O}_{2}}}}\text{ - }{{n}_{{{H}_{2}}O}}=0,1mol$
nO = 2.neste = 0,2mol
m = mH + mC + mO = 0,2 . 2 + 0,3 . 12 + 0,2 . 16 = 7,2 gam
Đốt cháy hoàn toàn một lượng este X đơn chức thấy thể tích CO2 thu được bằng thể tích của O2 cần dùng và gấp 1,5 lần thể tích hơi nước (ở cùng đk nhiệt độ, áp suất). Biết X tham gia phản ứng tráng gương. CTCT của X là:
-
A.
HCOOC≡CH.
-
B.
HCOOCH=CHCH3
-
C.
HCOOCH=CH2.
-
D.
HCOOCH2CH3.
Đáp án : C
- Tính số mol của este
Este đơn chức: \({{\text{n}}_X} = \dfrac{1}{2}{n_{{O_{trong este}}}} = \dfrac{1}{2}\left( {{n_{{H_2}O}} + 2{n_{C{O_2}}} - 2{n_{{O_2}}}} \right)\)
- Xác định CTPT của este
\(C = \dfrac{{{n_C}}}{{{n_X}}} = \dfrac{{{n_{C{O_2}}}}}{{{n_X}}}\)
\({H_{hh}} = \dfrac{{{n_H}}}{{{n_X}}} = \dfrac{{2{n_{{H_2}O}}}}{{{n_X}}}\)
\(O = \dfrac{{{n_O}}}{{{n_X}}}\)
- Xác định CTCT của X
Biện luận dựa vào giả thiết xác định CTCT
\( {\text{ }}{n_{C{O_2}}} = {\text{ }}{n_{{O_2}}} = {\text{ }}1,5{n_{{H_2}O}} = {\text{ }}1,5a\)
Bảo toàn O: \({{\text{n}}_X} = \dfrac{1}{2}{n_{{O_{trongeste}}}} = \dfrac{1}{2}\left( {{n_{{H_2}O}} + 2{n_{C{O_2}}} - 2{n_{{O_2}}}} \right) = \dfrac{{a + 2.1,5a - 2.1,5a}}{2} = 0,5a\)
\( C = \dfrac{{{n_C}}}{{{n_X}}} = \dfrac{{{n_{C{O_2}}}}}{{{n_X}}} = 3\)
\({H_{hh}} = \dfrac{{{n_H}}}{{{n_X}}} = \dfrac{{2{n_{{H_2}O}}}}{{{n_X}}} = 4\)
\(O = \dfrac{{{n_O}}}{{{n_X}}} = 2\)
=> X: C3H4O2
X tham gia phản ứng tráng gương => X là este của axit fomic có dạng: HCOOR
=> R: -C2H3
Vậy X: HCOOCH=CH2
Hỗn hợp X gồm vinyl axetat, metyl axetat và etyl fomat. Đốt cháy hoàn toàn 3,08 gam X, thu được 2,16 gam H2O. Phần trăm số mol của vinyl axetat trong X là:
-
A.
25%
-
B.
27,92%
-
C.
72,08%
-
D.
75%
Đáp án : A
- Tính số mol H2O.
- Tìm số mol vinyl axetat.
+) Qui đổi hỗn hợp X gồm: C4H6O2 và C3H6O2 với số mol tương ứng: a, b (mol)
+) Lập hpt 2 ẩn a, b. Tìm a, b => %
$\begin{gathered} {n_{H2O}} = 0,12mol \hfill \\ X:\left\{ \begin{gathered}vinylaxetat:C{H_3}COOCH = C{H_2}:{C_4}{H_6}{O_2} \hfill \\ metylaxetat:C{H_3}COOC{H_3}:{C_3}{H_6}{O_2} \hfill \\etylfomiat:HCOO{C_2}{H_5}:{C_3}{H_6}{O_2} \hfill \\ \end{gathered} \right.\xrightarrow{{Qui\,\,doi}}\left\{ \begin{gathered}{C_4}{H_6}{O_2}:a(mol) \hfill \\{C_3}{H_6}{O_2}:b(mol) \hfill \\ \end{gathered}\right.\hfill\\\left\{\begin{gathered}\xrightarrow{{BTNT:H}}6a + 6b = 0,12.2 \hfill \\86a + 74b = 3,08 \hfill \\ \end{gathered} \right. = > \left\{ \begin{gathered}a = 0,01 \hfill \\b = 0,03 \hfill \\ \end{gathered} \right. \hfill \\\% vinylaxetat = 25\% \hfill \\ \end{gathered} $
Hỗn hợp CH3COOC2H5 , HCOOC3H5 và HCOOC3H3. Hỗn hợp X có tỉ khối hơi so với O2 là dX/O2 = 2,7. Đốt cháy hoàn toàn 0,015 mol X ; sau phản ứng thu được hỗn hợp sản phẩm Y. Hấp thụ Y vào dung dịch Ca(OH)2 dư. Kết luận nào dưới đây đúng?
-
A.
Khối lượng bình giảm 3,504
-
B.
Khối lượng bình tăng 3,504
-
C.
Khối lượng dung dịch giảm 5,304
-
D.
Khối lượng dung dịch tăng 2,496
Đáp án : B
- Tìm dạng tổng quát của hỗn hợp X
\(\left. \begin{array}{*{35}{l}}{{C}_{4}}{{H}_{8}}{{O}_{2}} \\{{C}_{4}}{{H}_{6}}{{O}_{2}}~~~ \\{{C}_{4}}{{H}_{4}}{{O}_{2}} \\\end{array} \right\}=>~{{C}_{4}}{{H}_{n}}{{O}_{2}}\)
- Tính số mol của CO2, H2O
Viết phản ứng cháy tìm CO2, H2O
- Tính các dữ kiện => Đáp án
\(\left. \begin{array}{*{35}{l}}{{C}_{4}}{{H}_{8}}{{O}_{2}} \\{{C}_{4}}{{H}_{6}}{{O}_{2}}~~~ \\{{C}_{4}}{{H}_{4}}{{O}_{2}} \\\end{array} \right\}=>~{{C}_{4}}{{H}_{n}}{{O}_{2}}\)
Có : dX/O2= 2,7 => MX = 86,4g
=> n = 6,4 (C4H6,4O2)
\(\begin{array}{*{20}{l}}{ {n_X} = {\rm{ }}0,015{\rm{ }} = > {\rm{ }}{n_{C{O_2}}} = {\rm{ }}0,06mol{\rm{ }} , {\rm{ }}{n_{{H_2}O}} = {\rm{ }}0,048mol}\\{{n_{CaC{O_3}}}{\rm{ }} = {\rm{ }}{n_{C{O_2}}}{\rm{ }} = {\rm{ }}0,06mol{\rm{ }} = > {\rm{ }}{m_{CaC{O_3}{\rm{ }}}} = {\rm{ }}6g}\\{ = > {\rm{ }}{m_{binh{\rm{ }}tang}} = {\rm{ }}{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}}\\{ = {\rm{ }}0,06.44{\rm{ }} + {\rm{ }}0,048.18}\\\begin{array}{l} = {\rm{ }}3,504{\rm{ }}\left( g \right) < {m_{CaC{O_3}}}\\ = > m{\,_{dung\,dich\,giam}} = 6 - 3,504 = 2,496g\end{array}\end{array}\)
Đốt cháy hoàn toàn 20,1 gam hỗn hợp X gồm 2 este đơn chức, không no (có 1 nối đôi C=C), kế tiếp nhau trong cùng dãy đồng đẳng cần 146,16 lít không khí (đktc), thu được 46,2 gam CO2. Biết rằng trong không khí oxi chiếm 20% về thể tích. Công thức phân tử của 2 este là:
-
A.
C4H6O2 và C5H8O2
-
B.
C5H8O2 và C6H10O2
-
C.
C4H8O2 và C5H10O2
-
D.
C5H10O2 và C6H12O2
Đáp án : B
- Tính số mol H2O
BTKL: ${m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}$
- Xác định CT của các este trong X.
+) S/d pp giá trị trung bình X:
+) BTNT C, H tìm
\(\begin{array}{l} {n_{C{O_2}}} = 1,05mol\\{n_{{O_2}}} = 146,16.\dfrac{{20}}{{100.22,4}} = 1,305mol\\BTKL:{m_X}{\rm{ }} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}} = > {m_{{H_2}O}} = 15,66gam\\ = > {n_{{H_2}O}} = 0,87gam\end{array}\)
\({{C}_{\overline{n}}}{{H}_{2\overline{n}-2}}{{O}_{2}}:a(mol)\xrightarrow{+O2}\left\{ \begin{align}& C{{O}_{2}}:1,05mol \\ & {{H}_{2}}O:0,87mol \\ \end{align} \right.\)
\(\left\{ \begin{gathered}\xrightarrow{{BTNT:C}}a\bar n = 1,05 \hfill \\\xrightarrow{{BTNT:H}}a(\bar n - 1) = 0,87 \hfill \\ \end{gathered} \right. = > \left\{ \begin{gathered}a = 0,18 \hfill \\\bar n = 5,83 \hfill \\ \end{gathered} \right.\)
\(X:\left\{ \begin{array}{l}{C_5}{H_8}{O_2}\\{C_6}{H_{10}}{O_2}\end{array} \right.\)
Đốt cháy hoàn toàn một este đơn chức, mạch hở X (phân tử có số liên kết p nhỏ hơn 3), thu được thể tích khí CO2 bằng 6/7 thể tích khí O2 đã phản ứng (các thể tích khí đo ở cùng điều kiện). Cho m gam X tác dụng hoàn toàn với 200 ml dung dịch KOH 0,7M thu được dung dịch Y. Cô cạn Y thu được 12,88 gam chất rắn khan. Giá trị của m là
-
A.
7,20.
-
B.
6,66.
-
C.
8,88.
-
D.
10,56.
Đáp án : C
Xác định CTPT của X
\({n_{C{O_2}}} = \dfrac{6}{7}{n_{{O_2}{\rm{ }}pu}}\) => CTPT của X
Tính số mol X
Chất rắn gồm: RCOOK (x mol)và KOH dư (0,14 - x)
=> Mối liên hệ giữa R và x => x
nX = x
Tính giá trị m
\(\begin{array}{l}\begin{array}{*{20}{l}}{ {C_x}{H_y}{O_2} + {\rm{ }}(x + \dfrac{y}{4} - 1){O_2} \to xC{O_2} + {\rm{ }}\dfrac{y}{2}{H_2}O}\\{ = > x{\rm{ }} = {\rm{ }}\frac{6}{7}\left( {x{\rm{ }} + \frac{y}{4}{\rm{ }} - 1{\rm{ }}} \right)}\\\begin{array}{l} = > {\rm{ }}2x{\rm{ }} - {\rm{ }}3y{\rm{ }} = {\rm{ }} - 12\\k = \dfrac{{2x - y + 2}}{2} < 3 = > y > 2x - 4\end{array}\end{array}\\ = > x = {\rm{ }}3,y = {\rm{ }}6(t/m)\end{array}\)
X là C3H6O2, chất rắn gồm RCOOK (x mol)và KOH dư (0,14 - x)
Ta có: (R + 83)x + 56 (0,14 - x) = 12,88
=> Rx + 27x = 5,04
+ Với R = 1 => x = 0,18 > 0,14 (loại)
+ Với R = 15 => x = 0,12 < 0,14 (nhận)
=> nX = 0,12mol => m = 8,88g
Khi đề bài xuất hiện từ “chất rắn khan” luôn luôn nghĩ tới trường hợp kiềm dư sau phản ứng.
Đốt cháy hoàn toàn 6,8 gam một este A đơn chức chứa vòng benzen thu được CO2 và H2O. Hấp thụ toàn bộ sản phẩm này vào bình đựng dung dịch Ca(OH)2 lấy dư thấy khối lượng bình tăng 21,2 gam đồng thời có 40 gam kết tủa. Số CTCT có thể có của A
-
A.
2
-
B.
3
-
C.
5
-
D.
6
Đáp án : D
- Tìm số mol CO2, H2O
$\begin{array}{*{20}{l}}{{n_{C{O_2}}} = {\rm{ }}{n_{CaC{O_3}}}}\\{\Delta m \uparrow = {\rm{ }}{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}}\end{array}$
- Xác định CTPT este A
CxHyOz => x : y : z = nC : nH : nO
mO = mA – mC – mH
- Viết CTCT thỏa mãn
$\begin{array}{l} {n_{C{O_2}}} = {n_{CaC{O_3}}} = \frac{{40}}{{100}} = 0,4mol\\\Delta m \uparrow = {m_{C{O_2}}} + {m_{{H_2}O}} < = > 21,2 = 0,4\,\,.\,44 + {m_{{H_2}O}}\\ = > {n_{{H_2}O}} = 0,2mol\\{m_O} = {m_A}{\rm{ }}-{\rm{ }}{m_C}{\rm{ }}-{\rm{ }}{m_H} = 1,6 = > {n_O} = 0,1mol\\A:{C_x}{H_y}{O_z}\\x:y:z = {n_C}:{n_H}:{n_O}= 4:4:1\end{array}$
CTĐGN:(C4H4O)n
Do este đơn chức => n = 2 => Este A: C8H8O2
6 CTCT của A là :
1) CH3COOC6H5
2) HCOOCH2C6H5
3) C6H5COOCH3
4) HCOO-C6H4-CH3 (có 3 đồng phân o-, p-, m-)
Vậy có tất cả 6 CTCT thỏa mãn
Đối với đồng phân chứa vòng benzen cần chú ý các vị trị o,m,p.
E là este của axit cacboxylic no đơn chức (X) và ancol không no đơn chức có một nối đôi C=C (Y). Đốt a mol E thu được b mol CO2; đốt a mol X thu được c mol CO2; đốt a mol Y thu được 0,5b mol H2O. Quan hệ giữa b và c là:
-
A.
b= c.
-
B.
b = 2c.
-
C.
c= 2b.
-
D.
b= 3c.
Đáp án : B
- Viết công thức tổng quát của E, X, Y.
- Viết sơ đồ phản ứng cháy => Tìm mối liên hệ giữa các ẩn
$\begin{align} & \begin{array}{*{35}{l}} X:\text{ }{{C}_{n}}{{H}_{2n+1}}COOH \\ Y:\text{ }{{C}_{m}}{{H}_{2m-1}}OH \\ =>\text{ }E:\text{ }{{C}_{n}}{{H}_{2n+1}}COO{{C}_{m}}{{H}_{2m-1}} \\\end{array} \\ & {{C}_{n}}{{H}_{2n+1}}COO{{C}_{m}}{{H}_{2m-1}}\xrightarrow{+{{O}_{2}}}(n+m+1)C{{O}_{2}} \\& a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\to a(n+m+1)=b \\ & {{C}_{n}}{{H}_{2n+1}}COOH\xrightarrow{+{{O}_{2}}}(n+1)C{{O}_{2}} \\ & a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\to a(n+1)=c \\ & {{C}_{m}}{{H}_{2m-1}}OH\xrightarrow{+{{O}_{2}}}m{{H}_{2}}O \\ & a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\to am=0,5b \\ & \,\,\,\,\,\,\,\,\,a(n+m+1)=b \\ & <=>\underbrace{a(n+1)}_{c}+\underbrace{am}_{0,5b}=b \\ & <=>c=0,5b \\ & <=>b=2c \\ \end{align}$
Đốt cháy hoàn toàn 2,01 gam hỗn hợp X gồm axit acrylic, vinyl axetat, metyl metacrylat. Toàn bộ sản phẩm cháy cho qua dung dịch Ca(OH)2 dư, sau phản ứng thu được 9 gam kết tủa và dung dịch X. Vậy khối lượng dung dịch X đã thay đổi so với dung dịch Ca(OH)2 ban đầu là:
-
A.
Giảm 3,87 gam.
-
B.
Tăng 5,13 gam.
-
C.
Tăng 3,96 gam.
-
D.
Giảm 9 gam
Đáp án : A
- Tính số mol hỗn hợp X
Qui đổi hỗn hợp thành CnH2n-2O2
$\begin{array}{*{20}{l}}{{n_{C{O_2}}}{\rm{ }} = {\rm{ }}{n_{CaC{O_3}}}}\\{BTNT{\rm{ }}C:{n_X} = \frac{{{n_{C{O_2}}}}}{n}}\end{array}$
- Tính n
- Kết luận sự thay đổi khối lượng dung dịch:
+) Tính $\Sigma \left( {{m}_{C{{O}_{2}}}}+{{m}_{{{H}_{2}}O}} \right)$
+) ∆mdd sau pư =$\left( {{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}} \right)$ – (m kết tủa + m khí (nếu có))
· ∆mdd sau pư > 0 → khối lượng dung dịch sau phản ứng tăng
· ∆mdd sau pư < 0 → khối lượng dung dịch sau phản ứng giảm
Các chất trong hỗn hợp đều chứa 2 liên kết pi và 2 nguyên tử oxi.
\(\left. \begin{array}{l}axit{\rm{ }}acrylic:C{H_2} = CH - COOH\\vinyl{\rm{ }}axetat:C{H_3}COOCH = C{H_2}\\metyl{\rm{ }}metacrylat:C{H_2} = C(C{H_3})C{\rm{O}}O - C{H_3}\end{array} \right\rangle = > X:{C_n}{H_{2n - 2}}{O_2}\)
\({{C}_{n}}{{H}_{2n-2}}{{O}_{2}}:\dfrac{2,01}{14n+30}\xrightarrow{+{{O}_{2}}}\left\{ \begin{align}& C{{O}_{2}} \\ & {{H}_{2}}O \\ \end{align} \right.\xrightarrow{+\text{dd}\,\,Ca{{(OH)}_{2}}\,\,}9gam\,\,CaC{{O}_{3}}\)
\(\begin{array}{l}BTNT\,\,C:{n_{CO2}} = {n_{CaCO3}} = {n_{C(X)}} = \dfrac{9}{{100}} = 0,09mol\\ = > {n_{hhX}} = \dfrac{{0,09}}{n}\\ \dfrac{{0,09}}{n}.(14n + 30) = 2,01 < = > n = 3,6\\X:{C_{3,6}}{H_{5,2}}{O_2}:0,025mol\\ = > {n_{{H_2}O}} = 0,065mol\\ {m_{C{O_2}}} + {m_{{H_2}O}} = 0,09.44 + 0,065.18 = 5,13gam\\{\Delta _{mdd{\rm{ }}sau{\rm{ }}pu}} = {\rm{ }}\left( {{m_{C{O_2}}} + {\rm{ }}{m_{{H_2}O}}} \right){\rm{ }}-{\rm{ m}} \downarrow = 5,13 - 9 = - 3,87gam\end{array}\)
∆mdd sau pư < 0 => Khối lượng dung dịch giảm 3,87gam
Hỗn hợp X gồm 1 este đơn chức, không no có một nối đôi C = C mạch hở (A) và 1 este no, đơn chức mạch hở (B). Đốt cháy hoàn toàn 0,15 mol X rồi cho toàn bộ sản phẩm cháy hấp thụ hoàn toàn vào bình đựng dung dịch Ca(OH)2 dư. Sau phản ứng thấy khối lượng bình tăng 23,9 gam và có 40 gam kết tủa. CTPT của 2 este là:
-
A.
C2H4O2 và C3H4O2
-
B.
C3H6O2 và C5H8O2
-
C.
C2H4O2 và C5H8O2
-
D.
C2H4O2 và C4H6O2
Đáp án : D
- Tìm số mol CO2 và H2O
m bình tăng = ${{m}_{C{{O}_{2}}}}+\text{ }{{m}_{{{H}_{2}}O}}$
- Tính số mol mỗi este trong X:
n este không no = ${{n}_{C{{O}_{2}}}}\text{ }{{n}_{{{H}_{2}}O}}$
=> neste no = nhh – neste không no
- BTNT C, H => CTPT của mỗi este
\(\begin{array}{l} X:\underbrace {\left\{ \begin{array}{l}A:{C_n}{H_{2n - 2}}{O_2}(n \ge 3):a\\B:{C_m}{H_{2m}}{O_2}(m \ge 2):b\end{array} \right.}_{0,15mol}\\\left\{ \begin{array}{l}m\,{\,_{binh \uparrow }} = {m_{C{O_2}}} + {m_{{H_2}O}}\\{n_{CO2}} = {n_{CaCO3}} = 0,4\end{array} \right. = > \left\{ \begin{array}{l}{n_{{H_2}O}} = 0,35\\{n_{C{O_2}}} = {n_{CaC{O_3}}} = 0,4\end{array} \right.\\ a = {n_{C{O_2}}} - {n_{{H_2}O}} = 0,05mol = > b = 0,15 - 0,05 = 0,1mol\\ BTNT\,C:\,0,05.n + 0,1.m = 0,4 = > n = 4,m = 2\\\left\{ \begin{array}{l}A:{C_4}{H_6}{O_2}\\B:{C_2}{H_4}{O_2}\end{array} \right.\end{array}\)
Đốt cháy hoàn toàn 5,4 gam hỗn hợp X gồm axit acrylic, axit oleic, vinyl axetat, metyl acrylat cần vừa đủ V lít O2(đktc). Hấp thụ toàn bộ sản phẩm chát vào nước vôi trong dư, sau khi phản ứng hoàn toàn thu được 30 gam kết tủa. Giá trị của V là
-
A.
8,512.
-
B.
8,736.
-
C.
8,064.
-
D.
8,96.
Đáp án : B
Tât cả các chất trong X đều có chứa 2 liên kết pi và có 2 oxi trong phân tử
=> Đặt công thức chung của X là: CnH2n-2O2: a (mol)
BTNT “C”: nCO2 = nCaCO3 = 0,3 (mol)
Ta có:
\(\left\{ \matrix{
\sum {{n_{C{O_2}}} = na = 0,3} \hfill \cr
\sum {{m_{hh}} = (14n + 30)a = 5,4} \hfill \cr} \right. \Rightarrow \left\{ \matrix{
a = ? \hfill \cr
n = ? \hfill \cr} \right.\)
Có: nH2O = nCO2 – nX = ? (mol)
BTNT “O”: 2nX + 2nO2 = 2nCO2 + nH2O => nO2 = ?(mol) => VO2(đktc) = ?
CH2=CH-COOH; C17H33COOH; CH3COOCH=CH2; CH2=CH-COOCH3 => tất cả các chất trong X đều có chứa 2 liên kết pi và có 2 oxi trong phân tử
=> Đặt công thức chung của X là: CnH2n-2O2: a (mol)
BTNT “C”: nCO2 = nCaCO3 = 0,3 (mol)
Ta có:
\(\left\{ \matrix{
\sum {{n_{C{O_2}}} = na = 0,3} \hfill \cr
\sum {{m_{hh}} = (14n + 30)a = 5,4} \hfill \cr} \right. \Rightarrow \left\{ \matrix{
a = 0,04 \hfill \cr
n = 7,5 \hfill \cr} \right.\)
Có: nH2O = nCO2 – nX = 0,3 – 0,04 = 0,26 (mol)
BTNT “O”: 2nX + 2nO2 = 2nCO2 + nH2O
=> 2.0,04 + 2.nO2 = 2.0,3 + 0,26
=> nO2 = 0,39 (mol)
=> VO2(đktc) = 0,39.22,4 = 8,736 (l)
Đốt cháy hoàn toàn m gam hỗn hợp A gồm 3 este X, Y, Z (đều mạch hở và chỉ chứa chức este, X có khối lượng nhỏ nhất trong A) thu được số mol CO2 lớn hơn số mol H2O là 0,25 mol. Mặt khác, m gam A phản ứng vừa đủ với dung dịch NaOH thu được 22,2 gam hai ancol hơn kém nhau 1 nguyên tử cacbon và hỗn hợp T gồm hai muối. Đốt cháy hoàn toàn T cần vừa đủ 0,275 mol O2, thu được CO2, 0,35 mol Na2CO3 và 0,2 mol H2O. Phần trăm khối lượng của X trong A là
-
A.
28,92%.
-
B.
22,07%.
-
C.
28,43%.
-
D.
42,65%.
Đáp án : C
Bảo toàn nguyên tố, bảo toàn khối lượng.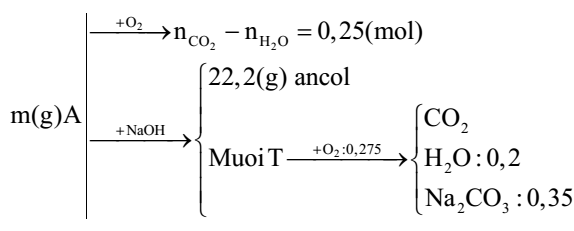
Sơ đồ bài toán:

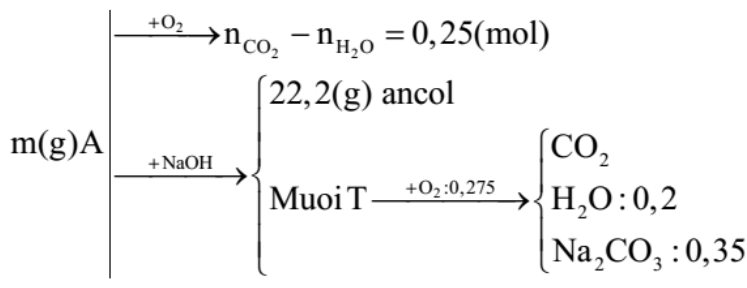
Do các este đều mạch hở và chỉ chứa chức este nên không phải là este của phenol.
- Xét phản ứng đốt muối T:
nCOO = nNaOH = 2nNa2CO3 = 0,7 mol → nO(T) =2nCOO =1,4 mol
BTNT "O": nO(T) + 2nO2(đốt T) = 2nCO2 + nH2O + 3nNa2CO3 → 1,4 + 0,275.2 = 2nCO2 + 0,2 + 0,35.3
→ nCO2 = 0,35 mol
BTKL: m muối =mCO2 + mH2O + mNa2CO3 - mO2(đốt T) =0,35.44 + 0,2.18 + 0,35.106 - 0,275.32 = 47,3 gam
- Xét phản ứng thủy phân A trong NaOH:
BTKL: mA = m muối + m ancol - mNaOH = 47,3 + 22,2 - 0,7.40 = 41,5 gam
- Xét phản ứng đốt A:
Đặt nCO2 = x và nH2O = y (mol)
+ nO(A) = 2nCOO = 1,4 mol. BTKL: mA = mC + mH + mO → 12x + 2y + 1,4.16 = 41,5 (1)
+ nCO2 - nH2O = 0,25 → x - y = 0,25 (2)
Giải hệ (1) và (2) thu được x = 1,4 và y = 1,15
BTNT "O": nO2 (đốt A) = [2nCO2 + nH2O - nO(A)]/2 = (2.1,4 + 1,15 - 1,4)/2 = 1,275 mol
- Xét phản ứng đốt ancol (phản ứng giả sử):
nO2 (đốt ancol) = nO2(đốt A) - nO2(đốt T) = 1,275 - 0,275 = 1 mol
Đặt nCO2 = a; nH2O = b (mol)
BTKL: mCO2 + mH2O = m ancol + mO2(đốt ancol) → 44a + 18b = 22,2 + 32 (3)
BTNT "O": 2nCO2 + nH2O = nO(ancol) + 2nO2 → 2a + b = 0,7 + 2 (4)
Giải (3) và (4) thu được: a = 0,7 và b = 1,3
Nhận thấy: nO(ancol) = nCO2 → Các ancol đều có số C bằng số O → Các ancol chỉ có thể là ancol no
→ n ancol =nH2O - nCO2 = 1,3 - 0,7 = 0,6 mol
→ 1 (CH3OH: u mol) < C tb =0,7: 0,6 = 1,16 < 2 (HO-CH2-CH2-OH: v mol)
nCO2 = u + 2v = 0,7 và u + v = 0,6
Giải được u = 0,5 và v = 0,1
- Phản ứng đốt muối T:
nC(T) = nCO2 + nNa2CO3 = 0,35 + 0,35 = 0,7 mol
nC(T) = nCOO → Số C trong T bằng số nhóm COO
→ 2 muối là HCOONa (n mol) và (COONa)2 (m mol)
m muối =68n + 134m = 47,3; nC(muối) = n + 2m = 0,7
→ n = 0,4 và m = 0,15
Vậy A chứa:
HCOOCH3 (0,2 mol) → mHCOOCH3 = 0,2.60 = 12 gam
(HCOO)2C2H4 (0,1 mol) → m(HCOO)2C2H4 = 0,1.118 = 11,8 gam
(COOCH3)2 (0,15 mol) → m(COOCH3)2 = 0,15.118 = 17,7 gam
Nhận thấy (HCOO)2C2H4 có khối lượng nhỏ nhất → %mX = 11,8/41,5.100% = 28,43%
Cho X và Y (MX < MY) là hai este đều mạch hở, không phân nhánh và không chứa nhóm chức khác. Đốt cháy X cũng như Y với lượng oxi vừa đủ, luôn thu được CO2 có số mol bằng số mol O2 đã phản ứng. Đun nóng 15,12 gam hỗn hợp E chứa X, Y (số mol của X gấp 1,5 lần số mol Y) cần dùng 200 ml dung dịch KOH 1M, thu được hỗn hợp F chứa 2 ancol và hỗn hợp K chứa 2 muối. Dẫn toàn bộ F qua bình đựng Na dư thấy khối lượng bình tăng 7,6 gam. Đốt cháy hoàn toàn hỗn hợp muối K cần dùng 0,21 mol O2. Phần trăm khối lượng của Y trong hỗn hợp E là
-
A.
58,25%.
-
B.
65,62%.
-
C.
52,38%.
-
D.
47,62%.
Đáp án : D
Bảo toàn gốc OH ta có: nOH ancol = nKOH ⟹ nH2 = ½ . nOH ancol
Bảo toàn khối lượng ta tính được mF
Bảo toàn khối lượng ta tính được mmuối
Bảo toàn nguyên tố kali ta có: nCOOK = nKOH
Đặt nCO2 = x mol; nH2O = y mol
Bảo toàn nguyên tố oxi và bảo toàn khối lượng để tìm x và y.
⟹ Số chức este của X và Y
Dùng bảo toàn nguyên tố C kết hợp với dữ kiện nCO2 = nO2 để suy ra số H trong X và Y
Do X và Y mạch hở ⟹ 2 ancol đều đơn chức ⟹ nF = nOH ⟹ MF ⟹ gốc ancol và công thức của X và Y.
Khi đó tính được phần trăm khối lượng của Y trong hỗn hợp E.
Bảo toàn gốc OH ta có: nOH ancol = nKOH = 0,2 mol
-OH + Na → -ONa + ½ H2
⟹ nH2 = ½ . nOH ancol = 0,1 mol
Bảo toàn khối lượng ta có: mF = 7,6 + 0,1.2 = 7,8 (g)
*Bảo toàn khối lượng ta có: mmuối = 15,12 + 0,2.56 - 7,8 = 18,52 (g)
Bảo toàn nguyên tố kali ta có: nCOOK = nKOH = 0,2 mol; nK2CO3 = 0,1 mol
Đặt nCO2 = x mol; nH2O = y mol
Bảo toàn nguyên tố oxi ta có 0,2 . 2 + 0,21 . 2 = 0,1 . 3 + 2x + y
Bảo toàn khối lượng ta có 18,52 + 0,21 . 32 = 0,1 . 138 + 44x + 18y
Giải hệ có x = 0,26 mol và y = 0 mol ⟹ Muối không chứa H ⟹ Muối phải là của axit 2 chức.
⟹ X và Y là este 2 chức ⟹ nX = 0,06 mol ; nY = 0,04 mol
Đặt số C trong gốc axit của X và Y là a và b
Ta có 0,06a + 0,04b = 0,1 + 0,26
Giải phương trình nghiệm nguyên a = 2 và b = 6
⟹ 2 muối là (COOK)2 và KOOCC≡C-C≡CCOOK
Mặt khác, đốt X hay Y đều cho nCO2 = nO2
⟹ X và Y có dạng Cn(H2O)m.
Lại có X và Y đều là este 2 chức → m = 4 → X và Y đều chứa 8H
Do X và Y mạch hở ⟹ 2 ancol đều đơn chức ⟹ nF = nOH = 0,2 mol ⟹ MF = 39 ⟹ chứa CH3OH
Do đó X là CH3OOCCOOC2H5 và Y là CH3OOCC≡C-C≡CCOOC2H5
→ %mY = 47,62%
Luyện tập và củng cố kiến thức Bài 1. Điều chế, ứng dụng, nhận biết este Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Tổng hợp bài tập về chuỗi phản ứng este Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Tổng hợp bài tập về hiệu suất phản ứng este hóa Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 2. Lipit Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 2. Thủy phân chất béo Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Tổng hợp bài tập Este - Lipit hay và khó (phần 1) Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Tổng hợp bài tập Este - Lipit hay và khó (phần 2) Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Ôn tập chương 1 Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1. Đốt cháy este no Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1. Thủy phân este đa chức Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1. Thủy phân este đặc biệt Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1. Thủy phân este đơn giản Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1. Este (Đồng phân - Danh pháp - Tính chất vật lý) Hóa 12 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết










Danh sách bình luận