Trắc nghiệm Ôn tập chương 2 - Hóa 11
Đề bài
Các tính chất không thuộc về tính chất của khí nitơ?
a) Hóa lỏng ở nhiệt độ rất thấp (−1960C)
b) Có khả năng đông nhanh
c) Tan nhiều trong nước
d) Nặng hơn Oxi
e) Kém bền, dễ bị phân hủy thành nitơ nguyên tử
-
A.
a, c, d
-
B.
a, b
-
C.
c, d, e
-
D.
b, c, e
Cho phản ứng N2 + 3H2 $\overset {} \leftrightarrows $ 2NH3 (∆H = -92KJ)
Muốn cho cân bằng của phản ứng nhiệt độ tổng hợp amoniac chuyển dịch sang phải cần phải đồng thời
-
A.
Tăng áp suất và tăng nhiệt độ
-
B.
Tăng áp suất và giảm nhiệt độ
-
C.
Giảm áp suất và giảm nhiệt độ
-
D.
Giảm áp suất và tăng nhiệt độ
Amoniac phản ứng được với tất cả các chất trong nhóm nào sau đây (các điều kiện coi như có đủ)
-
A.
HCl, O2, Cl2, CuO, dung dịch AlCl3
-
B.
H2SO4, PbO, FeO, NaOH
-
C.
HCl, KOH, FeCl3, Cl2
-
D.
KOH, HNO3, CuO, CuCl2
Trong dung dịch, amoniac là một bazơ yếu là do:
-
A.
Amoniac tan nhiều trong nước
-
B.
Phân tử amoniac là phân tử có cực
-
C.
Khi tan trong nước, amoniac kết hợp với nước tạo ra các ion NH4+ và OH-
-
D.
Khi tan trong nước, chỉ một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước tạo ra các ion NH4+ và OH-
Có thể phân biệt muối amoni với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm, vì khi đó:
-
A.
Thoát ra một chất khí màu lục nhạt
-
B.
Thoát ra một chất khí không màu, mùi khai, làm xanh giấy quỳ tím ẩm
-
C.
Thoát ra một chất khí màu nâu đỏ, làm xanh giấy quỳ tím ẩm
-
D.
Thoát ra chất khí không màu, không mùi
Khí nitơ có thể được tạo thành từ phản ứng hóa học nào sau đây?
-
A.
Đốt cháy NH3 trong oxi có chất xúc tác platin
-
B.
Nhiệt phân NH4NO3
-
C.
Nhiệt phân AgNO3
-
D.
Nhiệt phân NH4NO2
Một nhóm học sinh thực hiện thí nghiệm sau: Nhỏ từ từ dung dịch NH3 cho đến dư vào ống nghiệm đựng dung dịch CuSO4. Hiện tượng quan sát đầy đủ và đúng nhất là:
-
A.
Tạo kết tủa màu xanh lam không tan.
-
B.
Chỉ thấy xuất hiện dung dịch màu xanh thẫm.
-
C.
Lúc đầu có kết tủa màu xanh lam, sau đó kết tủa tan dần tạo thành dung dịch màu xanh thẫm.
-
D.
Có kết tủa màu xanh lam tạo thành, có khí màu nâu đỏ thoát ra
Đốt cháy hổn hợp gồm 6,72 lít khí oxi và 7 lít khí amoniac (đo ở cùng điều kiện nhiệt độ và áp suất). Sau phản ứng thu được nhóm các chất là:
-
A.
Khí nitơ và nước
-
B.
Khí oxi, khí nitơ và nước
-
C.
Khí amoniac, khí nitơ và nước
-
D.
Khí nitơ oxit và nước
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro tiheo tỉ lệ 1:3 để điều chế 17 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25%. Các thể tích khí đo được ở đktc.
-
A.
44,8 lít N2 và 134,4 lít H2
-
B.
22,4 lít N2 và 67,2 lít H2
-
C.
22,4 lít N2 và 134,4 lít H2
-
D.
44,8 lít N2 và 67,2 lít H2
Trong những nhận xét dưới đây về muối amoni, nhận xét nào là đúng?
-
A.
Muối amoni là tinh thể ion, phân tử gồm cation amoni và anion hiđroxit
-
B.
Tất cả các muối amoni đều dễ tan trong nước, khi tan điện li hòa toàn thành cation amoni và anion gốc axit.
-
C.
Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hóa đỏ
-
D.
Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra
Trong một bình kín chứa 10 lít nitơ và 10 lít hiđro ở nhiệt độ 0oC và 10 atm. Sau khi phản ứng tổng hợp NH3, lại đưa bình về 0oC. Biết rằng có 60% hiđro tham gia phản ứng, áp suất trong bình sau phản ứng là:
-
A.
10 atm
-
B.
8 atm
-
C.
9 atm
-
D.
8,5 atm
Cho 0,448 lít khí NH3 (đktc) đi qua ống sứ đựng 16 gam CuO nung nóng, thu được chất rắn X (giả sử phản ứng xảy ra hoàn toàn). Phần trăm khối lượng của Cu trong X là
-
A.
85,88%.
-
B.
14,12%.
-
C.
87,63%.
-
D.
12,37%.
Có 4 dung dịch muối riêng biệt: CuCl2, ZnCl2, FeCl3, AlCl3. Nếu thêm dung dịch KOH dư, rồi thêm tiếp dung dịch NH3 dư vào 4 dung dịch trên thì số chất kết tủa thu được là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Phản ứng giữa kim loại magie với axit nitric đặc, giả thiết chỉ tạo ra đinitơ oxit. Tổng các hệ số trong phương trình hóa học bằng:
-
A.
10
-
B.
18
-
C.
24
-
D.
20
Axit nitric đặc, nóng phản ứng được với tất cả các chất trong nhóm nào sau đây?
-
A.
Mg(OH)2, CuO, NH3, Ag
-
B.
Mg(OH)2, CuO, NH3, Pt
-
C.
Mg(OH)2, NH3, CO2, Au
-
D.
CaO, NH3, Au, FeCl2
Hòa tan 1,2 gam kim loại X vào dung dịch HNO3 dư thu được 0,224 lít khí nitơ ở đktc (giả thiết phản ứng chỉ tạo ra khí N2). Vậy X là:
-
A.
Zn
-
B.
Cu
-
C.
Mg
-
D.
Al
Khi bị nhiệt phân, dãy muối nitrat nào sau đây đều cho sản phẩm là kim loại, khí nitơ đioxit và khí oxi?
-
A.
Zn(NO3)2, KNO3, Pb(NO3)2
-
B.
Cu(NO3)2, LiNO3, KNO3
-
C.
Ca(NO3)2, LiNO3, KNO3
-
D.
Hg(NO3)2, AgNO3
Nung nóng hoàn toàn 27,3 gam hổn hợp NaNO3, Cu(NO3)2. Hỗn hợp khí thoát ra được dẫn vào nước dư thấy có 1,12 lít khí (ở đktc) không bị hấp thụ, khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
-
A.
18,8 gam
-
B.
9,4 gam
-
C.
8,6 gam
-
D.
23,5 gam
Để nhận biết ion NO3- người ta thường dùng Cu và dung dịch H2SO4 loãng nhờ
-
A.
Phản ứng tạo ra dung dịch màu xanh và khí không màu làm xanh quỳ tím ẩm.
-
B.
Phản ứng tạo dung dịch màu vàng nhạt.
-
C.
Phản ứng tạo kết tủa màu xanh.
-
D.
Phản ứng tạo dung dịch màu xanh và khí không màu hóa nâu trong không khí.
Cho 2 phản ứng
Fe + 2HCl → FeCl2 + H2↑ (1)
Fe + 4HNO3 →Fe(NO3)3 + NO↑ + 2H2O (2)
Tìm phát biểu đúng
-
A.
H+ ở phản ứng (2) có tính oxi hóa mạnh hơn H+ ở phản ứng (1)
-
B.
H+ là hợp phần oxi hóa ở phản ứng (1), NO3- là hợp phần oxi hóa ở phản ứng (2)
-
C.
Trong 2 phản ứng (1) và (2), axit vừa là chất oxi hóa vừa là môi trường
-
D.
Trong phản ứng (1) Fe thể hiện tính khử yếu, trong phản ứng (2) Fe thể hiện tính khử mạnh
Cho hỗn hợp C và S vào dung dịch HNO3 đặc thu được hỗn hợp khí X và dung dịch Y. Thành phần của X là
-
A.
SO2 và NO2
-
B.
CO2 và SO2
-
C.
SO2 và CO
-
D.
CO2 và NO2
Hoà tan hoàn 12,4 gam hỗn hợp X gồm Fe và Cu bằng dung dịch HNO3 1M vừa đủ, sau phản ứng thu được dung dịch A gồm 2 muối Fe(NO3)3 và Cu(NO3)2 đồng thời thu được hỗn hợp khí Y gồm: 0,1 mol NO và 0,15 mol NO2 (đktc). Phần trăm theo khối lượng Fe có trong hỗn hợp là:
-
A.
22,58%.
-
B.
77,42%.
-
C.
45,16%.
-
D.
54,84%.
Cho sơ đồ chuyển hoá:
${P_2}{O_5}\xrightarrow{{ + KOH dư}}X\xrightarrow{{ + {H_3}P{O_4}}}Y\xrightarrow{{ + KOH}}Z$
Các chất X, Y, Z lần lượt là :
-
A.
K3PO4, K2HPO4, KH2PO4
-
B.
KH2PO4, K2HPO4, K3PO4
-
C.
KH2PO4, K3PO4, K2HPO4
-
D.
K3PO4, KH2PO4, K2HPO4
Trong thành phần của thuốc chuột có hợp chất của photpho là Zn3P2. Khi bả chuột bằng loại thuốc này thì chuột thường chết gần nguồn nước bởi vì khi Zn3P2 vào dạ dày chuột thì sẽ hấp thu một lượng nước lớn và sinh ra đồng thời lượng lớn khí X và kết tủa Y khiến cho dạ dày chuột vỡ ra. Phát biểu nào sau đây không đúng?
-
A.
Kết tủa Y có thể tan được trong dung dịch NaOH đặc
-
B.
Khí X thường xuất hiện ở các nghĩa trang, dễ bốc cháy tạo thành ngọn lửa lập lòe
-
C.
Kết tủa Y có thể tan trong dung dịch NH3
-
D.
Khí X có thể được điều chế trực tiếp từ các đơn chất ở nhiệt độ thường
Cho 200 ml dung dịch H3PO4 0,3M vào 500 ml dung dịch Ba(OH)2 0,16M. Sau khi phản ứng xảy ra hoàn toàn. Khối lượng muối có phân tử khối bé hơn là
-
A.
12,02
-
B.
4,66
-
C.
12,70
-
D.
10,00
Cho H3PO4 tác dụng hết với dung dịch chứa m gam NaOH, sau phản ứng thu được dung dịch X có chứa 1,22m gam chất tan. Các chất tan trong dung dịch X là
-
A.
Na2HPO4, Na3PO4.
-
B.
NaH2PO4, Na2HPO4.
-
C.
Na3PO4, NaOH.
-
D.
NaH2PO4, Na3PO4.
Đốt cháy hoàn toàn 6,2 gam photpho bằng oxi dư rồi cho sản phẩm tạo thành tác dụng vừa đủ với m gam dung dịch NaOH 32% thu được muối Na2HPO4. Giá trị của m là:
-
A.
75
-
B.
50
-
C.
100
-
D.
25
Cho m gam P2O5 vào 1 lít dung dịch hỗn hợp NaOH 0,2M và KOH 0,3M vừa đủ sau phản ứng hoàn toàn thu được dung dịch X. Cô cạn cẩn thận X thu được 35,4 gam hỗn hợp muối khan. Giá trị của m là
-
A.
28,4 gam.
-
B.
7,1 gam.
-
C.
21,3 gam.
-
D.
14,2 gam.
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
-
A.
44,4 gam.
-
B.
39 gam.
-
C.
35,4 gam.
-
D.
37,2 gam.
Trong phòng thí nghiệm N2O được điều chế bằng cách
-
A.
cho Al tác dụng với HNO3 loãng.
-
B.
cho Al tác dụng với HNO3 đặc, nóng.
-
C.
nhiệt phân NH4NO3.
-
D.
cho Mg tác dụng với HNO3 loãng.
Cho các phát biểu sau:
(a) Có thể phân biệt dung dịch NH3 với dung dịch HCl bằng quỳ tím.
(b) Nhỏ dung dịch NH3 đến dư vào dung dịch AlCl3 thu được kết tủa.
(c) CuO tác dụng với dung dịch HNO3 đặc, giải phóng khí NO2.
(d) Nhiệt phân NaNO3 thu được hỗn hợp khí.
Số phát biểu đúng là
-
A.
1
-
B.
4
-
C.
3
-
D.
2
Axit nitric và axit photphoric cùng phản ứng với nhóm các chất sau:
-
A.
CuCl2, NaOH, K2CO3, NH3
-
B.
NaOH, K2O, NH3, Na2CO3
-
C.
KCl, NaOH, K2SO4, NH3
-
D.
CuSO4, MgO, KOH, NH3
Cho các mẫu phân bón sau: KCl, Ca(H2PO4)2, NH4H2PO4 và NH4NO3. Dùng 1 hóa chất nào sau đây có thể phân biệt được các mẫu phân bón trên?
-
A.
dung dịch NaOH
-
B.
dung dịch Ca(OH)2
-
C.
dung dịch BaCl2
-
D.
dung dịch AgNO3
Cho các phát biểu sau:
(a) Khoáng vật chính của photpho trong tự nhiên là pirit, apatit và photphoric.
(b) Các số oxi hóa có thể có của photpho là -3; +3; +5; 0.
(c) Tính chất hóa học điển hình của photpho là tính oxi hóa.
(d) Trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng giữa P2O5 và H2O.
(e) Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của photpho có trong phân.
Số phát biểu không đúng là:
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Lời giải và đáp án
Các tính chất không thuộc về tính chất của khí nitơ?
a) Hóa lỏng ở nhiệt độ rất thấp (−1960C)
b) Có khả năng đông nhanh
c) Tan nhiều trong nước
d) Nặng hơn Oxi
e) Kém bền, dễ bị phân hủy thành nitơ nguyên tử
-
A.
a, c, d
-
B.
a, b
-
C.
c, d, e
-
D.
b, c, e
Đáp án : C
Các tính chất không phải của nitơ là:
c) Tan nhiều trong nước
d) Nặng hơn Oxi
e) Kém bền, dễ bị phân hủy thành nitơ nguyên tử
Cho phản ứng N2 + 3H2 $\overset {} \leftrightarrows $ 2NH3 (∆H = -92KJ)
Muốn cho cân bằng của phản ứng nhiệt độ tổng hợp amoniac chuyển dịch sang phải cần phải đồng thời
-
A.
Tăng áp suất và tăng nhiệt độ
-
B.
Tăng áp suất và giảm nhiệt độ
-
C.
Giảm áp suất và giảm nhiệt độ
-
D.
Giảm áp suất và tăng nhiệt độ
Đáp án : B
Áp dụng nguyên lí chuyển dịch cân bằng:
- Tăng áp suất cân bằng sẽ chuyển theo chiều giảm số phân tử khí và ngược lại
- Phản ứng thu nhiệt cân bằng sẽ chuyển dịch theo chiều thuận nếu tăng nhiệt độ
- Tăng nồng độ các chất cân bằng sẽ chuyển dịch theo chiều giảm nồng độ chất đó
Ảnh hưởng của áp suất:
-Khi tăng áp suất của hệ thì cân bằng chuyển dịch theo chiều giảm số mol khí mà ban đầu có 4 mol sau khi tạo NH3 thì số mol là 2 => Tăng áp suất phản ứng cân bằng sẽ chuyển dịch theo chiều sinh ra là NH3 chiều thuận
-∆H<0: tỏa nhiệt
Vậy để cân bằng chuyển dịch qua bên phải thì phải giảm nhiệt độ
Amoniac phản ứng được với tất cả các chất trong nhóm nào sau đây (các điều kiện coi như có đủ)
-
A.
HCl, O2, Cl2, CuO, dung dịch AlCl3
-
B.
H2SO4, PbO, FeO, NaOH
-
C.
HCl, KOH, FeCl3, Cl2
-
D.
KOH, HNO3, CuO, CuCl2
Đáp án : A
NH3 có tính bazơ nên không phản ứng được với bazơ mạnh
=>NaOH, KOH không phản ứng với NH3 loại B, C, D
Trong dung dịch, amoniac là một bazơ yếu là do:
-
A.
Amoniac tan nhiều trong nước
-
B.
Phân tử amoniac là phân tử có cực
-
C.
Khi tan trong nước, amoniac kết hợp với nước tạo ra các ion NH4+ và OH-
-
D.
Khi tan trong nước, chỉ một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước tạo ra các ion NH4+ và OH-
Đáp án : D
Trong dung dịch, amoniac là một bazơ yếu là do: Khi tan trong nước, chỉ một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước tạo ra các ion NH4+ và OH-
Có thể phân biệt muối amoni với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm, vì khi đó:
-
A.
Thoát ra một chất khí màu lục nhạt
-
B.
Thoát ra một chất khí không màu, mùi khai, làm xanh giấy quỳ tím ẩm
-
C.
Thoát ra một chất khí màu nâu đỏ, làm xanh giấy quỳ tím ẩm
-
D.
Thoát ra chất khí không màu, không mùi
Đáp án : B
Ta có: NH4+ + OH- → NH3 \( \uparrow \)+H2O
=> Để phân biệt muối amoni với các muối khác là người ta cho muối amoni với dung dịch kiềm vì khi đó thoát ra một chất khí không màu, mùi khai, làm xanh giấy quỳ tím ẩm.
Khí nitơ có thể được tạo thành từ phản ứng hóa học nào sau đây?
-
A.
Đốt cháy NH3 trong oxi có chất xúc tác platin
-
B.
Nhiệt phân NH4NO3
-
C.
Nhiệt phân AgNO3
-
D.
Nhiệt phân NH4NO2
Đáp án : D
Ta có PTHH:
A. 2NH3 + 5/2 O2 $\xrightarrow{{{t^o},\operatorname{Pt} }}$ 2NO + 3H2O
B. NH4NO3$\xrightarrow{{{t^o}}}$N2O + 2H2O
C. AgNO3$\xrightarrow{{{t^o}}}$Ag + NO2 + ½ O2
D. NH4NO2$\xrightarrow{{{t^o}}}$N2 + 2H2O
Một nhóm học sinh thực hiện thí nghiệm sau: Nhỏ từ từ dung dịch NH3 cho đến dư vào ống nghiệm đựng dung dịch CuSO4. Hiện tượng quan sát đầy đủ và đúng nhất là:
-
A.
Tạo kết tủa màu xanh lam không tan.
-
B.
Chỉ thấy xuất hiện dung dịch màu xanh thẫm.
-
C.
Lúc đầu có kết tủa màu xanh lam, sau đó kết tủa tan dần tạo thành dung dịch màu xanh thẫm.
-
D.
Có kết tủa màu xanh lam tạo thành, có khí màu nâu đỏ thoát ra
Đáp án : C
Các phản ứng xảy ra
CuSO4 + 2NH3 + H2O → Cu(OH)2 ↓xanh lam + (NH4)2SO4
Cu(OH)2 + NH3 + H2O → [Cu(NH3)4](OH)2 (dd màu xanh thẫm)
=> Lúc đầu có kết tủa màu xanh lam, sau đó kết tủa tan dần tạo thành dung dịch màu xanh thẫm
Đốt cháy hổn hợp gồm 6,72 lít khí oxi và 7 lít khí amoniac (đo ở cùng điều kiện nhiệt độ và áp suất). Sau phản ứng thu được nhóm các chất là:
-
A.
Khí nitơ và nước
-
B.
Khí oxi, khí nitơ và nước
-
C.
Khí amoniac, khí nitơ và nước
-
D.
Khí nitơ oxit và nước
Đáp án : B
+) Xét tỉ lệ tìm ra chất dư, chất hết
+) Tính theo chất hết
Phản ứng: 4NH3 + 3O2 → 2N2 + 6H2O
Xét tỉ lệ thể tích: $\dfrac{{{n_{N{H_3}}}}}{4} = \dfrac{7}{4} < \dfrac{{{n_{{O_2}}}}}{3} = \dfrac{{6,72}}{3}$ => dư oxi.
Do đó, các chất thu được sau phản ứng là khí nitơ, nước được tạo thành và khí oxi dư.
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro tiheo tỉ lệ 1:3 để điều chế 17 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25%. Các thể tích khí đo được ở đktc.
-
A.
44,8 lít N2 và 134,4 lít H2
-
B.
22,4 lít N2 và 67,2 lít H2
-
C.
22,4 lít N2 và 134,4 lít H2
-
D.
44,8 lít N2 và 67,2 lít H2
Đáp án : A
+) Tính số mol NH3 thu được nếu H = 100% => số mol các khí cần tìm
${m_{N{H_3}}}$ thu được nếu H = 100% $ = \dfrac{{17}}{{25\% }} = 68\,gam$
=> ${n_{N{H_3}}}$= 4 mol
N2 + 3H2 $\overset {} \leftrightarrows $ 2NH3
2 $ \leftarrow $ 6 $ \leftarrow $4 mol
=> ${n_{{H_2}}} = 6\,mol \Rightarrow {V_{{H_2}}} = 134,4$ lít
=> ${n_{{N_2}}} = 2{\text{ }}mol \Rightarrow {V_{{N_2}}}{\text{ = }}44,8$ lít
Trong những nhận xét dưới đây về muối amoni, nhận xét nào là đúng?
-
A.
Muối amoni là tinh thể ion, phân tử gồm cation amoni và anion hiđroxit
-
B.
Tất cả các muối amoni đều dễ tan trong nước, khi tan điện li hòa toàn thành cation amoni và anion gốc axit.
-
C.
Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hóa đỏ
-
D.
Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra
Đáp án : B
A sai vì muối amoni là tinh thể ion, phân tử gồm cation amoni và anion gốc axit
C sai vì khí làm quì hóa xanh
D sai vì khi nhiệt phân muối amoni chưa chắc ra khi amoniac.
VD: NH4NO2 $\xrightarrow{{{t^o}}}$ N2 + 2H2O
Trong một bình kín chứa 10 lít nitơ và 10 lít hiđro ở nhiệt độ 0oC và 10 atm. Sau khi phản ứng tổng hợp NH3, lại đưa bình về 0oC. Biết rằng có 60% hiđro tham gia phản ứng, áp suất trong bình sau phản ứng là:
-
A.
10 atm
-
B.
8 atm
-
C.
9 atm
-
D.
8,5 atm
Đáp án : B
+) $\dfrac{{{n_H}_{_2}}}{{{n_N}_{_2}}} = \dfrac{3}{1}$
+) Hiđro phản ứng là 60% từ đó tính tổng thể tích khí phản ứng
+) Sau phản ứng thể tích khí giảm bằng ½ thể tích khí phản ứng
=> Vgiảm
=> Vsau phản ứng
+) áp dụng CT: $\dfrac{{{V_1}}}{{{V_2}}} = \dfrac{{{n_1}}}{{{n_2}}} = \dfrac{{{p_1}}}{{{p_2}}}$
N2+3H2 $\overset {} \leftrightarrows $ 2NH3
Theo PT tổng hợp NH3 thì $\dfrac{{{n_H}_{_2}}}{{{n_N}_{_2}}} = \dfrac{3}{1}$
Thể tích H2 phản ứng là 6 lít => VN2 = 2 lit
Tổng thể tích khí phản ứng là 8 lit
Sau phản ứng thể tích khí giảm bằng ½ thể tích khí phản ứng
=> Vgiảm = 4 lit
=> Vsau phản ứng = 10 + 10 − 4 = 16 lit
$\dfrac{{{V_1}}}{{{V_2}}} = \dfrac{{{n_1}}}{{{n_2}}} = \dfrac{{{p_1}}}{{{p_2}}} \Rightarrow \dfrac{{20}}{{16}} = \dfrac{{10}}{{{p_2}}} \Rightarrow {p_2} = 8\,atm$
Cho 0,448 lít khí NH3 (đktc) đi qua ống sứ đựng 16 gam CuO nung nóng, thu được chất rắn X (giả sử phản ứng xảy ra hoàn toàn). Phần trăm khối lượng của Cu trong X là
-
A.
85,88%.
-
B.
14,12%.
-
C.
87,63%.
-
D.
12,37%.
Đáp án : D
+) Xét chất hết, chất dư
+) nCu = 1,5.nNH3 => mCu
+) mX = mCu + mCuO dư
nCuO = 0,2 mol ; nNH3 = 0,02 mol
3CuO + 2NH3 $\xrightarrow{{{\text{t}^\text{0}}}}$ 3Cu + N2 + 3H2O
0,03 $ \leftarrow $ 0,02
nCu = 0,03 mol => mCu = 1,92 gam
mX = mCu + mCuO dư = 1,92 + (0,2 – 0,03).80 = 15,52 gam
=> %mCu trong X = $\dfrac{{1,92}}{{15,52}}.100\% = 12,37\% $
Có 4 dung dịch muối riêng biệt: CuCl2, ZnCl2, FeCl3, AlCl3. Nếu thêm dung dịch KOH dư, rồi thêm tiếp dung dịch NH3 dư vào 4 dung dịch trên thì số chất kết tủa thu được là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Đáp án : A
+) KOH dư sẽ không kết tủa với ion Zn2+,Al3+, Cr3+ .
+) NH3 có khả năng tạo phức với ion: Cu2+, Ag+, Zn2+ hòa tan kết tủa.
Khi cho KOH dư
$\begin{gathered}\text{C}{\text{u}^{\text{2 + }}}\text{ + 2O}{\text{H}^\text{ - }}\xrightarrow{{}}\text{Cu(OH}{\text{)}_\text{2}} \downarrow \hfill \\\text{Z}{\text{n}^{\text{2 + }}}\text{ + 4O}{\text{H}^\text{ - }}\xrightarrow{{}}\text{4Zn(OH)}_\text{4}^{\text{2 - }} \hfill \\\text{F}{\text{e}^{\text{3 + }}}\text{ + 3O}{\text{H}^\text{ - }}\xrightarrow{{}}\text{Fe(OH}{\text{)}_\text{3}} \downarrow \hfill \\\text{A}{\text{l}^{\text{3 + }}}\text{ + 4O}{\text{H}^\text{ - }}\xrightarrow{{}}\text{Al(OH)}_\text{4}^\text{ - } \hfill \\ \end{gathered} $
Thêm tiếp NH3 thì NH3 sẽ tạo phức với Cu2+, Zn2+
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
=> chỉ còn kết tủa Fe(OH)3
Phản ứng giữa kim loại magie với axit nitric đặc, giả thiết chỉ tạo ra đinitơ oxit. Tổng các hệ số trong phương trình hóa học bằng:
-
A.
10
-
B.
18
-
C.
24
-
D.
20
Đáp án : C
Sử dụng phương pháp cân bằng electron
Ta có PTHH:
10HNO3 + 4Mg → 5H2O + 4Mg(NO3)2 + N2O
Axit nitric đặc, nóng phản ứng được với tất cả các chất trong nhóm nào sau đây?
-
A.
Mg(OH)2, CuO, NH3, Ag
-
B.
Mg(OH)2, CuO, NH3, Pt
-
C.
Mg(OH)2, NH3, CO2, Au
-
D.
CaO, NH3, Au, FeCl2
Đáp án : A
HNO3 không phản ứng được với Pt loại B
HNO3 không phản ứng được với CO2, Au loại C
HNO3 không phản ứng được với Au loại D
Hòa tan 1,2 gam kim loại X vào dung dịch HNO3 dư thu được 0,224 lít khí nitơ ở đktc (giả thiết phản ứng chỉ tạo ra khí N2). Vậy X là:
-
A.
Zn
-
B.
Cu
-
C.
Mg
-
D.
Al
Đáp án : C
Gọi kim loại là X; kim loại có số oxi hóa là +n
+) Sử dụng bảo toàn e
+) biện luận theo x để tìm M của kim loại
Gọi kim loại là X; kim loại có số oxi hóa là +n
X → X+n + ne
0,01/n ← 0,01 mol
2N+5 + 10e →N20
0,01←0,02 mol
=> MX = 12n
|
x |
1 |
2 |
3 |
|
MM |
12 (l) |
24 |
36(l) |
Vậy M là Mg
Khi bị nhiệt phân, dãy muối nitrat nào sau đây đều cho sản phẩm là kim loại, khí nitơ đioxit và khí oxi?
-
A.
Zn(NO3)2, KNO3, Pb(NO3)2
-
B.
Cu(NO3)2, LiNO3, KNO3
-
C.
Ca(NO3)2, LiNO3, KNO3
-
D.
Hg(NO3)2, AgNO3
Đáp án : D
$\underbrace {K,Na,Ca,}_I\underbrace {Mg,Al,Zn,Fe,Ni,Sn,Pb,Cu}_{II},\underbrace {Hg,Ag,Au}_{III}$
+) Nhóm I nhiệt phân tạo muối nitrit và oxi: VD 2KNO3$\xrightarrow{{{t^ \circ }}}$ 2KNO2 + O2↑
+) Nhóm II nhiệt phân tạo oxit lim loại, khí NO2 và oxi: VD 2Cu(NO3)2 $\xrightarrow{{{t^ \circ }}}$2CuO + 4NO2 ↑+ O2↑
+) Nhóm III nhiệt phân tạo lim loại, khí NO2 và oxi: VD 2AgNO3$\xrightarrow{{{t^ \circ }}}$2Ag + 2NO2 ↑+ O2↑
$\underbrace {K,Na,Ca,}_I\underbrace {Mg,Al,Zn,Fe,Ni,Sn,Pb,Cu}_{II},\underbrace {Hg,Ag,Au}_{III}$
Nhiệt phân cho sản phẩm kim loại, khí nitơ đioxit và khí oxi là kim loại nhóm III.
PTHH:
\[Hg{(N{O_3})_2}\,\,\xrightarrow{{{t^o}}}\,\,Hg\,\, + \,\,2N{O_2} \uparrow \,\, + {O_2} \uparrow \]
\[2AgN{O_3}\,\,\xrightarrow{{{t^o}}}\,\,2Ag\,\, + \,\,2N{O_2} \uparrow \,\, + {O_2} \uparrow \]
=> dãy muối cho sản phẩm kim loại, khí nitơ đioxit và khí oxi là: Hg(NO3)2, AgNO3
Nung nóng hoàn toàn 27,3 gam hổn hợp NaNO3, Cu(NO3)2. Hỗn hợp khí thoát ra được dẫn vào nước dư thấy có 1,12 lít khí (ở đktc) không bị hấp thụ, khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
-
A.
18,8 gam
-
B.
9,4 gam
-
C.
8,6 gam
-
D.
23,5 gam
Đáp án : A
Gọi số mol của NaNO3, Cu(NO3)2 lần lượt là x và y
+) Tính số mol NO2 và O2 sinh ra theo a và b
+) Khí không bị hấp thụ là O2 còn dư
=> nO2 dư => a
=> mCu(NO3)2
Gọi số mol của NaNO3, Cu(NO3)2 lần lượt là x và y
NaNO3 → NaNO2 + ½ O2
a → 0,5a
Cu(NO3)2→ CuO + 2NO2 + ½ O2
b → 2b → 0,5b
Hỗn hợp khí gồm nNO2 = 2b mol, nO2 = 0,5.(a + b)
Hấp thụ hỗn hợp khí vào nước
4NO2 + O2 + 2H2O → 4HNO3
2b → 0,5b
Khí không bị hấp thụ là O2 còn dư
=> nO2 dư = 0,5.(a +b) - 0,5b = 0,5a = 0,05 mol
=> a = 0,1 mol
=> mCu(NO3)2 = (27,3 – 85.0,1) = 18,8 gam
Để nhận biết ion NO3- người ta thường dùng Cu và dung dịch H2SO4 loãng nhờ
-
A.
Phản ứng tạo ra dung dịch màu xanh và khí không màu làm xanh quỳ tím ẩm.
-
B.
Phản ứng tạo dung dịch màu vàng nhạt.
-
C.
Phản ứng tạo kết tủa màu xanh.
-
D.
Phản ứng tạo dung dịch màu xanh và khí không màu hóa nâu trong không khí.
Đáp án : D
Để nhận biết ion NO3- người ta thường dùng Cu và dung dịch H2SO4 loãng nhờ phản ứng tạo dung dịch màu xanh và khí không màu hóa nâu trong không khí.
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
Cho 2 phản ứng
Fe + 2HCl → FeCl2 + H2↑ (1)
Fe + 4HNO3 →Fe(NO3)3 + NO↑ + 2H2O (2)
Tìm phát biểu đúng
-
A.
H+ ở phản ứng (2) có tính oxi hóa mạnh hơn H+ ở phản ứng (1)
-
B.
H+ là hợp phần oxi hóa ở phản ứng (1), NO3- là hợp phần oxi hóa ở phản ứng (2)
-
C.
Trong 2 phản ứng (1) và (2), axit vừa là chất oxi hóa vừa là môi trường
-
D.
Trong phản ứng (1) Fe thể hiện tính khử yếu, trong phản ứng (2) Fe thể hiện tính khử mạnh
Đáp án : B
A sai vì H+ ở phản ứng (2) không có sự thay đổi số oxi hóa
B đúng vì: 2H+ + 2e → H2 => H+ là hợp phần oxi hóa
$\mathop N\limits^{ + 5} + 3{\text{e}} \to \mathop N\limits^{ + 2} $ =>NO3- là hợp phần oxi hóa
C sai vì ở phản ứng (1) HCl không có vai trò là môi trường
D sai vì 2 phản ứng không kết luận được Fe khử yếu hay khử mạnh
Cho hỗn hợp C và S vào dung dịch HNO3 đặc thu được hỗn hợp khí X và dung dịch Y. Thành phần của X là
-
A.
SO2 và NO2
-
B.
CO2 và SO2
-
C.
SO2 và CO
-
D.
CO2 và NO2
Đáp án : D
C + 4HNO3 đặc → 2H2O + 4NO2 + CO2
S + 2HNO3 đặc → H2SO4 + 2NO2
2 khí thu được là CO2 và NO2
Hoà tan hoàn 12,4 gam hỗn hợp X gồm Fe và Cu bằng dung dịch HNO3 1M vừa đủ, sau phản ứng thu được dung dịch A gồm 2 muối Fe(NO3)3 và Cu(NO3)2 đồng thời thu được hỗn hợp khí Y gồm: 0,1 mol NO và 0,15 mol NO2 (đktc). Phần trăm theo khối lượng Fe có trong hỗn hợp là:
-
A.
22,58%.
-
B.
77,42%.
-
C.
45,16%.
-
D.
54,84%.
Đáp án : A
+) Sử dụng phương pháp bảo toàn e cho các nguyên tố: Cu; Fe; NO; NO2
nCu = x mol; nFe = y mol
=> mX = 64x + 56y = 12,4 (1)

Bảo toàn electron: n e cho = n e nhận = 2x + 3y = 0,45 mol (2)
Giải hệ (1) và (2) => x = 0,15 và y = 0,05
=> nFe = 0,05 mol
=> $\% {m_{Fe}} = \dfrac{{0,05.56}}{{12,4}}.100\% = 22,58\% $
Cho sơ đồ chuyển hoá:
${P_2}{O_5}\xrightarrow{{ + KOH dư}}X\xrightarrow{{ + {H_3}P{O_4}}}Y\xrightarrow{{ + KOH}}Z$
Các chất X, Y, Z lần lượt là :
-
A.
K3PO4, K2HPO4, KH2PO4
-
B.
KH2PO4, K2HPO4, K3PO4
-
C.
KH2PO4, K3PO4, K2HPO4
-
D.
K3PO4, KH2PO4, K2HPO4
Đáp án : D
Ta có: P2O5 +6 KOH dư →2 K3PO4 +3H2O
=> X là K3PO4
2K3PO4 +H3PO4 → 3K2HPO4
Hoặc: K3PO4 +2H3PO4 → 3KH2PO4
=> Y là K2HPO4 hoặc KH2PO4
Y + KOH → Z và X; Y; Z là các chất khác nhau mà KH2PO4 + KOH →2 K2HPO4 +H2O tức Y + KOH → Z
=> Y là KH2PO4, Z là K2HPO4
Trong thành phần của thuốc chuột có hợp chất của photpho là Zn3P2. Khi bả chuột bằng loại thuốc này thì chuột thường chết gần nguồn nước bởi vì khi Zn3P2 vào dạ dày chuột thì sẽ hấp thu một lượng nước lớn và sinh ra đồng thời lượng lớn khí X và kết tủa Y khiến cho dạ dày chuột vỡ ra. Phát biểu nào sau đây không đúng?
-
A.
Kết tủa Y có thể tan được trong dung dịch NaOH đặc
-
B.
Khí X thường xuất hiện ở các nghĩa trang, dễ bốc cháy tạo thành ngọn lửa lập lòe
-
C.
Kết tủa Y có thể tan trong dung dịch NH3
-
D.
Khí X có thể được điều chế trực tiếp từ các đơn chất ở nhiệt độ thường
Đáp án : D
PTHH: Zn3P2 + 6H2O → 2PH3 + 3Zn(OH)2
=> khí X là PH3 và kết tủa Y là Zn(OH)2
X không thể tạo ra từ H2 + P
Cho 200 ml dung dịch H3PO4 0,3M vào 500 ml dung dịch Ba(OH)2 0,16M. Sau khi phản ứng xảy ra hoàn toàn. Khối lượng muối có phân tử khối bé hơn là
-
A.
12,02
-
B.
4,66
-
C.
12,70
-
D.
10,00
Đáp án : B
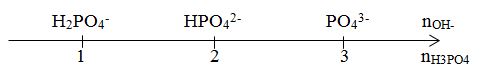
+) tỉ lệ \(\frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}}\)
+) Đối chiếu với sơ đổ quy kết muối
+) Viết PTHH, đặt ẩn giải hệ
${n_{{H_3}P{O_4}}}$= 0,06 mol
${n_{Ba{{(OH)}_2}}}$= 0,08 mol $ \Rightarrow {n_{O{H^ - }}}$= 0,16 mol
\(\frac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}} = \frac{{0,16}}{{0,06}} = 2,67\)
Ta thấy 2 < 2,67 <3 $ \Rightarrow $ Tạo 2 muối $HPO_4^{2 - }$ (x mol) và $PO_4^{3 - }$(y mol)
BT nguyên tố P: ${n_{{H_3}P{O_4}}} = {n_{HPO_4^{2 - }}} + {n_{PO_4^{3 - }}}$ => x + y = 0,06 (1)
BT điện tích: ${n_{O{H^ - }}} = 2.{n_{HPO_4^{2 - }}} + 3.{n_{PO_4^{3 - }}}$ => 2x + 3y = 0,16 (2)
Từ (1) và (2) => x = 0,02 mol; y = 0,04 mol
Ta có:
${n_{BaHP{O_4}}} = {n_{HPO_4^{2 - }}}$= 0,02 mol $ \Rightarrow $${m_{BaHP{O_4}}}$= 0,02.233 = 4,66 gam
${n_{B{a_3}{{(P{O_4})}_2}}} = \dfrac{1}{2}{n_{PO_4^{3 - }}}$= 0,02 mol $ \Rightarrow $${m_{B{a_3}{{(P{O_4})}_2}}} = $0,02.601 = 12,02 gam
Cho H3PO4 tác dụng hết với dung dịch chứa m gam NaOH, sau phản ứng thu được dung dịch X có chứa 1,22m gam chất tan. Các chất tan trong dung dịch X là
-
A.
Na2HPO4, Na3PO4.
-
B.
NaH2PO4, Na2HPO4.
-
C.
Na3PO4, NaOH.
-
D.
NaH2PO4, Na3PO4.
Đáp án : C
+) Gán giá trị m là 20 gam, từ đó tính số mol NaOH và Khối lượng chất rắn.
+) Giả sử OH- hết ta có PTHH: H+ + OH- → H2O
Sau đó áp dụng bảo toàn khối lượng để tính lại số mol H+, so sánh với OH- xem giả sử đúng hay sai
+) Kết luận chất tan.
Coi m =20 gam
nNaOH =0,5 mol
mChất rắn =24,4 gam
Giả sử OH- hết
Ta thấy bản chất phản ứng: H+ + OH- → H2O
0,5\( \leftarrow \) 0,5 →0,5
BT khối lượng: \({m_{{H_3}P{O_4}}} + {m_{NaOH}} = {m_{{H_2}O}}\) + m chất rắn
- ${m_{{H_3}P{O_4}}}$ + 0,5*40 = 0,5*18 + 24,4
- \({n_{{H_3}P{O_4}}} = 0,1367mol\)
\({n_{{H^ + }}}\) phản ứng = 0,1367*3=0,41 mol < 0,5. Vậy OH- dư
- Chất tan là: Na3PO4 và NaOH
Đốt cháy hoàn toàn 6,2 gam photpho bằng oxi dư rồi cho sản phẩm tạo thành tác dụng vừa đủ với m gam dung dịch NaOH 32% thu được muối Na2HPO4. Giá trị của m là:
-
A.
75
-
B.
50
-
C.
100
-
D.
25
Đáp án : B
Bảo toàn nguyên tố
Do phản ứng chỉ tạo ra ${N{a_2}HP{O_4}}$ nên :
$2{n_P} = 2{n_{N{a_2}HP{O_4}}} = {n_{NaOH}}$ (bảo toàn nguyên tố)
=> ${n_{NaOH}} = \dfrac{{2.6,2}}{{31}} = 0,4{\text{ }}mol$
=> Khối lượng dung dịch NaOH cần dùng là: $m = \dfrac{{0,4.40.100}}{{32}} = 50\,gam$
Cho m gam P2O5 vào 1 lít dung dịch hỗn hợp NaOH 0,2M và KOH 0,3M vừa đủ sau phản ứng hoàn toàn thu được dung dịch X. Cô cạn cẩn thận X thu được 35,4 gam hỗn hợp muối khan. Giá trị của m là
-
A.
28,4 gam.
-
B.
7,1 gam.
-
C.
21,3 gam.
-
D.
14,2 gam.
Đáp án : D
+) Vừa đủ => OH- hết : OH- + H+ → H2O => \({n_{O{H^ - }}} = {n_{{H_2}O}}\)
+) Bảo toàn khối lượng: ${m_{{H_3}P{O_4}}} + {m_{NaOH}} + {m_{KOH}} = $ mmuối $ + {m_{{H_2}O}}$
Xét H3PO4 phản ứng với bazơ
Vừa đủ => OH- hết : OH- + H+ → H2O => nH2O = nOH = 0,5 mol
Bảo toàn khối lượng : ${m_{{H_3}P{O_4}}} + {m_{NaOH}} + {m_{KOH}} = $ mmuối $ + {m_{{H_2}O}}$
=> ${m_{{H_3}P{O_4}}}$ + 0,2*40+0,3*56= 35,4 + 0,5*18
${n_{{H_3}P{O_4}}} = 0,2\,gam \Rightarrow {n_{{P_2}{O_5}}} = \dfrac{1}{2}{n_{{H_3}P{O_4}}} = 0,1\,mol$
=> m = 14,2 gam
Đốt cháy hoàn toàn 6,2 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
-
A.
44,4 gam.
-
B.
39 gam.
-
C.
35,4 gam.
-
D.
37,2 gam.
Đáp án : C
Gọi công thức trung bình của bazơ và làm tương tự như cho 1 bazơ tác dụng với P2O5
2P → P2O5 → 2H3PO4
0,2 → 0,2
${n_{{H_3}P{O_4}}} = 0,2{\text{ }}mol$
${n_{O{H^ - }}} = 0,5{\text{ }}mol \Rightarrow 2 < \dfrac{{{n_{O{H^ - }}}}}{{{n_{{H_3}P{O_4}}}}} = 2,5 < 3$
=> Muối gồm: \(\left\{ \begin{array}{l}N{a_2}HP{O_4} = xmol\\N{a_3}P{O_4} = ymol\end{array} \right.\)
Các phản ứng xảy ra:
2MOH + H3PO4 → M2HPO4 + 2H2O
2x \( \leftarrow \) x \( \leftarrow \)x
3MOH + H3PO4 → M3PO4 + 3H2O
3y \( \leftarrow \) y \( \leftarrow \)y
Ta có hệ phương trình:\(\left\{ \begin{array}{l}2x + 3y = 0,5\\x + y = 0,2\end{array} \right.\)
=> Muối gồm : 0,1 mol M2HPO4 và 0,1 mol M3PO4
mmuối $ = {m_K} + {m_{Na}} + {m_{HPO_4^{2 - }}} + {m_{PO_4^{3 - }}} = 35,4\,gam$
Trong phòng thí nghiệm N2O được điều chế bằng cách
-
A.
cho Al tác dụng với HNO3 loãng.
-
B.
cho Al tác dụng với HNO3 đặc, nóng.
-
C.
nhiệt phân NH4NO3.
-
D.
cho Mg tác dụng với HNO3 loãng.
Đáp án : C
Dựa vào phương pháp điều chế N2O trong phòng thí nghiệm.
Trong phòng thí nghiệm, người ta điều chế N2O bằng phương pháp nhiệt phân muối NH4NO3:
NH4NO3 \(\xrightarrow{{{t^o}}}\) N2O + 2H2O
Cho các phát biểu sau:
(a) Có thể phân biệt dung dịch NH3 với dung dịch HCl bằng quỳ tím.
(b) Nhỏ dung dịch NH3 đến dư vào dung dịch AlCl3 thu được kết tủa.
(c) CuO tác dụng với dung dịch HNO3 đặc, giải phóng khí NO2.
(d) Nhiệt phân NaNO3 thu được hỗn hợp khí.
Số phát biểu đúng là
-
A.
1
-
B.
4
-
C.
3
-
D.
2
Đáp án : D
(a) đúng, vì NH3 làm quỳ tím hóa xanh còn HCl làm quỳ tím hóa đỏ
(b) đúng vì AlCl3 + 3NH3 + 3H2O → 3NH4Cl + Al(OH)3 ↓ (kết tủa không bị hòa tan bởi NH3 dư)
(c) sai vì Cu có hóa trị cao nhất nên không có phản ứng oxi hóa khử với HNO3 mà chỉ xảy ra phản ứng trao đổi: CuO + 2HNO3 → Cu(NO3)2 + H2O
(d) sai vì nhiệt phân NaNO3 chỉ thu được 1 khí là O2. PTHH: NaNO3 → NaNO2 + O2
→ 2 phát biểu đúng
Axit nitric và axit photphoric cùng phản ứng với nhóm các chất sau:
-
A.
CuCl2, NaOH, K2CO3, NH3
-
B.
NaOH, K2O, NH3, Na2CO3
-
C.
KCl, NaOH, K2SO4, NH3
-
D.
CuSO4, MgO, KOH, NH3
Đáp án : B
Vì axit nitric và axit photphoric đều là axit nên đều mang tính chất hóa học chung của axit. Từ đó xác định các chất phản ứng được với cả 2 axit này.
Axit nitric và axit photphoric cùng phản ứng với nhóm các chất: NaOH, K2O, NH3, Na2CO3
Các phương trình hóa học xảy ra:
NaOH + HNO3 → NaNO3 + H2O
K2O + 2HNO3 → 2KNO3 + H2O
NH3 + HNO3 → NH4NO3
Na2CO3 + 2HNO3 → 2NaNO3 + CO2 + H2O
H3PO4 + 3NaOH → Na3PO4 + 3H2O
2H3PO4 + 3K2O → 2K3PO4 + 3H2O
3NH3 + H3PO4 → (NH4)3PO4
3Na2CO3 + 2H3PO4 → 2Na3PO4 + 3CO2 + 3H2O
Cho các mẫu phân bón sau: KCl, Ca(H2PO4)2, NH4H2PO4 và NH4NO3. Dùng 1 hóa chất nào sau đây có thể phân biệt được các mẫu phân bón trên?
-
A.
dung dịch NaOH
-
B.
dung dịch Ca(OH)2
-
C.
dung dịch BaCl2
-
D.
dung dịch AgNO3
Đáp án : B
Chọn hóa chất sao cho hiện tượng xảy ra giữa các chất khác nhau.
Cho dung dịch Ca(OH)2 vào các dung dịch trên:
- Nếu xuất hiện kết tủa trắng thì đó là Ca(H2PO4)2:
Ca(H2PO4)2 + 2Ca(OH)2 → Ca3(PO4)2 + 4H2O
- Nếu vừa xuất hiện chất khí có mùi khai và kết tủa trắng thì đó là NH4H2PO4
2NH4H2PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 2NH3 + 6H2O
- Nếu xuất hiện chất khí có mùi khai thì đó là NH4NO3:
2NH4NO3 + Ca(OH)2 → Ca(NO3)2 + 2NH3 + 2H2O
Cho các phát biểu sau:
(a) Khoáng vật chính của photpho trong tự nhiên là pirit, apatit và photphoric.
(b) Các số oxi hóa có thể có của photpho là -3; +3; +5; 0.
(c) Tính chất hóa học điển hình của photpho là tính oxi hóa.
(d) Trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng giữa P2O5 và H2O.
(e) Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của photpho có trong phân.
Số phát biểu không đúng là:
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đáp án : C
Dựa vào trạng thái tự nhiên, số oxi hóa và tính chất của photpho và hợp chất của photpho để xác định các phát biểu không đúng.
(a) Phát biểu không đúng vì khoáng vật của photpho không phải là pirit.
(b) Phát biểu đúng.
(c) Phát biểu không đúng vì photpho có cả tính oxi hóa và tính khử.
(d) Phát biểu không đúng vì trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng P và HNO3 đặc.
(e) Phát biểu không đúng vì độ dinh dưỡng của phân lân được đánh giá bằng tỉ lệ phần trăm khối lượng P2O5 tương ứng với lượng P có trong thành phần của nó.
Vậy số phát biểu không đúng là 4.
Luyện tập và củng cố kiến thức Tổng hợp bài tập nitơ - photpho Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 12. Phân bón hóa học Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 11. Hợp chất của photpho Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 11. Axit photphoric và muối photphat Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 10. Photpho Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Tổng hợp bài tập tính oxi hóa của HNO3 Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 9. Axit nitric và muối nitrat Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 8. Muối amoni Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 8. Amoniac Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 7. Nitơ Hóa 11 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết










Danh sách bình luận