Đề kiểm tra 1 tiết Hóa 11 chương 2: Cacbon - Silic - Đề số 1
Đề bài
Thành phần chính của khí than ướt là
-
A.
\(CO,C{O_2},{H_2},{N_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{H_2},N{O_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Thành phần chính của khí than khô là
-
A.
\(CO,C{O_2},{H_2},N{O_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{N_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Silic tác dụng với chất nào sau đây ở nhiệt độ thường
-
A.
O2
-
B.
F2
-
C.
Cl2
-
D.
Br2
Số oxi hóa cao nhất của silic thể hiện ở hợp chất nào sau đây
-
A.
SiO2
-
B.
SiF4
-
C.
SiH4
-
D.
A, B đúng
Cấu hình electron của nguyên tử cacbon là :
-
A.
1s22s22p1
-
B.
1s22s22p2
-
C.
1s22s22p3
-
D.
1s22s22p4
Thêm từ từ từng giọt của 100 ml dung dịch chứa Na2CO3 1,2M và NaHCO3 0,6M vào 200 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch nước vôi trong dư vào dung dịch X thì thu được bao nhiêu gam kết tủa ?
-
A.
8 gam
-
B.
10 gam
-
C.
12 gam
-
D.
6 gam
Phản ứng dùng để khắc hình, khắc chữ lên thủy tinh là phản ứng giữa SiO2 với:
-
A.
H2SO4
-
B.
HCl
-
C.
HNO3
-
D.
HF
Chọn câu trả lời đúng: Trong các phản ứng hoá học, cacbon
-
A.
chỉ thể hiện tính khử.
-
B.
vừa thể hiện tính khử vừa thể hiện tính oxi hóa.
-
C.
chỉ thể hiện tính oxi hoá.
-
D.
không thể hiện tính khử và tính oxi hoá.
Sục từ từ khí CO2 vào 100,0 ml dung dịch chứa đồng thời NaOH 1M, Ba(OH)2 0,5M và BaCl2 0,7M. Thể tích khí CO2 cần sục vào (đktc) để kết tủa thu được là lớn nhất là
-
A.
2,8 lít
-
B.
2,24 lít
-
C.
3,136 lít
-
D.
2,688 lít
Nhỏ rất từ từ đến hết 200ml dung dịch X chứa đồng thời H2SO4 aM và HCl 0,15M vào 100ml dung dịch chứa đồng thời NaOH 0,5M và Na2CO3 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,448 lít khí (đktc). Giá trị của a là:
-
A.
0,4
-
B.
0,1
-
C.
0,3
-
D.
0,2
Cho 4,48 lít khí CO (ở đktc) từ từ đi qua ống sứ nung nóng đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng là:
-
A.
FeO; 75%
-
B.
Fe3O4; 75%
-
C.
Fe2O3; 65%
-
D.
Fe2O3; 75%
Có các axit sau: HCl, H2SiO3, H2CO3.Sắp xếp theo chiều tính axit tăng dần của 3 axit trên
-
A.
HCl, H2CO3, H2SiO3
-
B.
H2SiO3, H2CO3, HCl
-
C.
HCl, H2SiO3, H2CO3
-
D.
H2CO3, H2SiO3, HCl
Cho các chất: O2 (1), NaOH (2), Mg (3), Na2CO3 (4), SiO2 (5), HCl (6), CaO (7), Al (8), ZnO (9), H2O (10), NaHCO3 (11), KMnO4 (12), HNO3 (13), Na2O (14). Cacbon đioxit phản ứng trực tiếp được với bao nhiêu chất?
-
A.
5 .
-
B.
6.
-
C.
7.
-
D.
8.
Khí CO2 điều chế trong phòng TN thường lẫn khí HCl và hơi nước. Để loại bỏ HCl và hơi nước ra khỏi hỗn hợp, ta dùng
-
A.
Dung dịch NaOH đặc.
-
B.
Dung dịch Na2CO3 bão hoà và dung dịch H2SO4 đặc.
-
C.
Dung dịch H2SO4 đặc.
-
D.
Dung dịch NaHCO3 bão hoà và dung dịch H2SO4 đặc.
Than được dùng làm chất độn cao su, sản xuất mực in, xi đánh giầy là:
-
A.
than chì
-
B.
than muội
-
C.
than gỗ
-
D.
than cốc
Dung dịch đậm đặc của hợp chất nào sau đây được gọi là thủy tinh lỏng
-
A.
Na2SiO3 và K2SiO3
-
B.
SiO2 và K2SiO3
-
C.
NaOH và Na2SiO3
-
D.
KOH và K2SiO3
Một loại thủy tinh có chứa 13% Na2O; 11,7% CaO; 75,3% SiO2 về khối lượng. Thành phần của thủy tinh này được viết dưới dạng hợp chất các oxit là
-
A.
Na2O.CaO.6SiO2
-
B.
2Na2O.6CaO.6SiO2
-
C.
2Na2O.CaO.6SiO2
-
D.
Na2O.6CaO.SiO2
Cho 3,60 gam cacbon tác dụng với 8,10 gam nhôm. Khối lượng nhôm cacbua tạo thành nếu hiệu suất của phản ứng 70% là
-
A.
5,76 gam
-
B.
7,56 gam
-
C.
10,08 gam
-
D.
10,80 gam
Có 5 lọ mất nhãn đựng 5 chất bột màu trắng: NaCl, Na2CO3, Na2SO4, BaCO3, BaSO4. Chỉ dùng nước và khí CO2 thì có thể nhận được mấy chất
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Thực hiện các thí ngiệm sau
TN1: cho (a + b) mol CaCl2 vào dd X
TN2: cho (a + b) mol Ca(OH)2 vào dd X
Khối lượng kết tủa thu được trong 2 TN là
-
A.
Bằng nhau.
-
B.
Ở TN1 < ở TN2.
-
C.
Ở TN1 > ở TN2.
-
D.
Không so sánh được.
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
-
A.
NaOH và Al(OH)3.
-
B.
NaOH, NaAlO2 và Al(OH)3.
-
C.
NaAlO2 và BaCO3.
-
D.
Ba(OH)2, NaOH và BaCO3.
Khí X được dùng nhiều trong ngành sản xuất nước giải khát và bia rượu. Tuy nhiên, việc gia tăng nồng độ khí X trong không khí là nguyên nhân làm trái đất nóng lên. Khí X là
-
A.
N2.
-
B.
O2.
-
C.
H2.
-
D.
CO2.
Cho 3,36 lít khí CO (đktc) phản ứng vừa đủ với 20 gam hỗn hợp X gồm CuO và MgO. Phần trăm khối lượng của MgO trong X là
-
A.
80%.
-
B.
60%.
-
C.
20%.
-
D.
40%.
Thuốc nổ đen là hỗn hợp
-
A.
KNO3, C và S.
-
B.
KNO3 và S.
-
C.
KClO3, C và S.
-
D.
KClO3 và S.
Trong các chất sau, chất có độ cứng lớn nhất là
-
A.
silic.
-
B.
kim cương.
-
C.
than chì.
-
D.
thạch anh.
Một chất Y có tính chất sau:
- Không màu, rất độc.
- Cháy trong không khí với ngọn lửa màu xanh và sinh ra chất khí làm đục nước vôi trong. Y là:
-
A.
H2.
-
B.
CO.
-
C.
Cl2.
-
D.
CO2.
Oxit nào sau đây không tạo muối?
-
A.
CO2.
-
B.
Mn2O7.
-
C.
CO.
-
D.
SiO2.
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
-
A.
1 lít.
-
B.
1,5 lít.
-
C.
0,8 lít.
-
D.
2 lít.
Dẫn luồng khí CO dư qua hỗn hợp Al2O3; CuO; MgO; Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được chất rắn là
-
A.
Al2O3, Cu, Mg, Fe.
-
B.
Al, Fe, Cu, Mg.
-
C.
Al2O3, Fe2O3, Cu, MgO.
-
D.
Al2O3, Cu; MgO; Fe.
Kim cương và than chì là các dạng
-
A.
đồng hình của cacbon.
-
B.
đồng vị của cacbon.
-
C.
thù hình của cacbon.
-
D.
đồng phân của cacbon.
Lời giải và đáp án
Thành phần chính của khí than ướt là
-
A.
\(CO,C{O_2},{H_2},{N_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{H_2},N{O_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Đáp án : A
Thành phần chính của khí than ướt là CO, CO2, H2, N2
Thành phần chính của khí than khô là
-
A.
\(CO,C{O_2},{H_2},N{O_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{N_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Đáp án : C
Thành phần chính của khí than than khô là CO, CO2, N2
Silic tác dụng với chất nào sau đây ở nhiệt độ thường
-
A.
O2
-
B.
F2
-
C.
Cl2
-
D.
Br2
Đáp án : B
Silic tác dụng được với F2 ở nhiệt độ thường.
Số oxi hóa cao nhất của silic thể hiện ở hợp chất nào sau đây
-
A.
SiO2
-
B.
SiF4
-
C.
SiH4
-
D.
A, B đúng
Đáp án : D
Số oxi hóa cao nhất của Si trong hợp chất là +4 => thể hiện trong SiO2 và SiF4
Cấu hình electron của nguyên tử cacbon là :
-
A.
1s22s22p1
-
B.
1s22s22p2
-
C.
1s22s22p3
-
D.
1s22s22p4
Đáp án : B
C (Z = 6) có cấu hình e: 1s22s22p2
Thêm từ từ từng giọt của 100 ml dung dịch chứa Na2CO3 1,2M và NaHCO3 0,6M vào 200 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch nước vôi trong dư vào dung dịch X thì thu được bao nhiêu gam kết tủa ?
-
A.
8 gam
-
B.
10 gam
-
C.
12 gam
-
D.
6 gam
Đáp án : D
- Tính số mol Na2CO3 và NaHCO3 có trong X
Tính số mol Na2CO3 và NaHCO3 => tỉ lệ phản ứng khi phản ứng với HCl
Đặt nNaHCO3 phản ứng = x mol => nNa2CO3 phản ứng = 2x mol
Các phản ứng: Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
${{n}_{HCl}}=\text{ }2.{{n}_{N{{a}_{2}}C{{O}_{3}}}}+\text{ }{{n}_{NaHC{{O}_{3}}}}$
=> số mol Na2CO3 và NaHCO3
- Tính khối lượng kết tủa
${{n}_{CaC{{O}_{3}}}}=\text{ }{{n}_{CO_{3}^{2-}}}+\text{ }{{n}_{HCO_{3}^{-}}}$
- Ta có
\(\begin{gathered}
\begin{array}{*{20}{l}}
{{n_{C{O_3}^{2 - }}}{\text{ }} = {\text{ }}0,12mol} \\
{{n_{HC{O_3}^ - }}{\text{ }} = {\text{ }}0,06{\text{ }}mol}
\end{array} \hfill \\
= > {n_{C{O_3}^{2 - }}}:{n_{HC{O_3}^ - }} = 2:1 \hfill \\
\end{gathered} \)
- Khi cho từ từ 100 ml dung dịch vào HCl thì cả 2 chất đều phản ứng đồng thời theo tỉ lệ mol
Na2CO3 : NaHCO3 = 1,2 : 0,6 = 2 : 1
- Đặt x là số mol NaHCO3 phản ứng => nNa2CO3 = 2x mol
Các phản ứng: Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
=> nHCl = 0,2 = 2.2x + x => x = 0,04 mol
\(\begin{array}{*{20}{l}}
{{n_{C{O_3}^{2 - }\,pu}}{\text{ }} = {\text{ }}0,08mol = > {n_{C{O_3}^{2 - }\,trong\,X}} = 0,12 - 0,08 = 0,04mol} \\
{{n_{HC{O_3}^ - \,pu}}{\text{ }} = {\text{ }}0,04{\text{ }}mol = > {n_{HC{O_3}^ - \,trong\,X}} = 0,06 - 0,04 = 0,02mol}
\end{array}{\text{ }}\)
Khi cho nước vôi trong vào X thì tạo kết tủa CaCO3 có
${{n}_{CaC{{O}_{3}}}}=\text{ }{{n}_{CO_{3}^{2-}}}+\text{ }{{n}_{HCO_{3}^{-}}}$ = 0,06 mol => m kết tủa = 6 gam
Phản ứng dùng để khắc hình, khắc chữ lên thủy tinh là phản ứng giữa SiO2 với:
-
A.
H2SO4
-
B.
HCl
-
C.
HNO3
-
D.
HF
Đáp án : D
Phản ứng dùng để khắc hình, khắc chữ lên thủy tinh là phản ứng giữa SiO2 với HF
SiO2 + HF → SiF4 + 2H2O
Chọn câu trả lời đúng: Trong các phản ứng hoá học, cacbon
-
A.
chỉ thể hiện tính khử.
-
B.
vừa thể hiện tính khử vừa thể hiện tính oxi hóa.
-
C.
chỉ thể hiện tính oxi hoá.
-
D.
không thể hiện tính khử và tính oxi hoá.
Đáp án : B
Trong các phản ứng hoá học, cacbon vừa thể hiện tính khử vừa thể hiện tính oxi hóa.
Sục từ từ khí CO2 vào 100,0 ml dung dịch chứa đồng thời NaOH 1M, Ba(OH)2 0,5M và BaCl2 0,7M. Thể tích khí CO2 cần sục vào (đktc) để kết tủa thu được là lớn nhất là
-
A.
2,8 lít
-
B.
2,24 lít
-
C.
3,136 lít
-
D.
2,688 lít
Đáp án : B
nBa2+ > ½.nOH- => kết tủa cực đại khi OH- tạo hết thành CO32-
+) nCO2 = nCO32- = nBa2+
nOH- = 0,2 mol
nBa2+ = 0,12 mol > ½.nOH- => kết tủa cực đại khi OH- tạo hết thành CO32-
=> nBaCO3 max = 0,1 mol
=> nCO2 = nCO32- = nBa2+ = 0,1 mol => V = 2,24 lít
Nhỏ rất từ từ đến hết 200ml dung dịch X chứa đồng thời H2SO4 aM và HCl 0,15M vào 100ml dung dịch chứa đồng thời NaOH 0,5M và Na2CO3 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,448 lít khí (đktc). Giá trị của a là:
-
A.
0,4
-
B.
0,1
-
C.
0,3
-
D.
0,2
Đáp án : D
- Chú ý thứ tự xảy ra phản ứng
H+ + OH- → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → H2O + CO2
- Tính số mol H+
\({n_{{H^ + }}} = {\text{ }}2{n_{{H_2}S{O_4}}} + {\text{ }}{n_{HCl}} = {\text{ }}{n_{O{H^ - }}} + {\text{ }}{n_{C{O_3}^{2 - }}} + {\text{ }}{n_{C{O_2}}}\)
- Thứ tự phản ứng :
H+ + OH- → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → H2O + CO2
\([{n_{{H^ + }}} = {\text{ }}2{n_{{H_2}S{O_4}}} + {\text{ }}{n_{HCl}} = {\text{ }}{n_{O{H^ - }}} + {\text{ }}{n_{C{O_3}^{2 - }}} + {\text{ }}{n_{C{O_2}}}\)
=> 0,2.(2a + 0,15) = 0,05 + 0,04 + 0,02
=> a = 0,2M
Cho 4,48 lít khí CO (ở đktc) từ từ đi qua ống sứ nung nóng đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng là:
-
A.
FeO; 75%
-
B.
Fe3O4; 75%
-
C.
Fe2O3; 65%
-
D.
Fe2O3; 75%
Đáp án : D
+) Mkhí sau phản ứng = 40 => khí sau phản ứng gồm CO2 (x mol) và CO dư (y mol)
+) Bảo toàn C: nCO ban đầu = nCO2 + nCO dư => PT(1)
\(\bar M = \frac{{44x + 28y}}{{x + y}} = 40\) => PT(2)
+) nO trong oxit = nCO2
+) mFe = moxit – mO trong oxit
nCO ban đầu = 0,2 mol
Mkhí sau phản ứng = 40 => khí sau phản ứng gồm CO2 (x mol) và CO dư (y mol)
Bảo toàn C: nCO ban đầu = nCO2 + nCO dư => x + y = 0,2 (1)
\(\bar M = \frac{{44x + 28y}}{{x + y}} = 40\,\,\,(2)\)
Từ (1) và (2) => nCO2 = 0,15 mol và nCO dư = 0,05 mol
=> %CO2 = 75%
Ta có: nO trong oxit = nCO2 = 0,15 mol
mFe = moxit – mO trong oxit => nFe = (8 – 0,15.16) : 56 = 0,1 mol
Gọi công thức của oxit là FexOy
=> x : y = 0,1 : 0,15 = 2 : 3
Có các axit sau: HCl, H2SiO3, H2CO3.Sắp xếp theo chiều tính axit tăng dần của 3 axit trên
-
A.
HCl, H2CO3, H2SiO3
-
B.
H2SiO3, H2CO3, HCl
-
C.
HCl, H2SiO3, H2CO3
-
D.
H2CO3, H2SiO3, HCl
Đáp án : B
Theo chiều tính axit tăng dần của 3 axit trên là: H2SiO3, H2CO3, HCl
Cho các chất: O2 (1), NaOH (2), Mg (3), Na2CO3 (4), SiO2 (5), HCl (6), CaO (7), Al (8), ZnO (9), H2O (10), NaHCO3 (11), KMnO4 (12), HNO3 (13), Na2O (14). Cacbon đioxit phản ứng trực tiếp được với bao nhiêu chất?
-
A.
5 .
-
B.
6.
-
C.
7.
-
D.
8.
Đáp án : C
CO2 phản ứng được với: NaOH, Mg, Na2CO3, CaO, H2O, Na2O, Al
Khí CO2 điều chế trong phòng TN thường lẫn khí HCl và hơi nước. Để loại bỏ HCl và hơi nước ra khỏi hỗn hợp, ta dùng
-
A.
Dung dịch NaOH đặc.
-
B.
Dung dịch Na2CO3 bão hoà và dung dịch H2SO4 đặc.
-
C.
Dung dịch H2SO4 đặc.
-
D.
Dung dịch NaHCO3 bão hoà và dung dịch H2SO4 đặc.
Đáp án : D
Xem lại lí thuyết hợp chất cacbon
A loại vì NaOH phản ứng với CO2 và HCl
B loại vì Na2CO3 phản ứng với CO2 và HCl
C loại vì H2SO4 đặc chỉ tách được nước, không tách được CO2và HCl.
D đúng vì NaHCO3 chỉ phản ứng với HCl sinh ra khí CO2 và H2SO4 hút nước.
NaHCO3 + HCl →NaCl + CO2 + H2O
Than được dùng làm chất độn cao su, sản xuất mực in, xi đánh giầy là:
-
A.
than chì
-
B.
than muội
-
C.
than gỗ
-
D.
than cốc
Đáp án : B
Than được dùng làm chất độn cao su, sản xuất mực in, xi đánh giầy là than muội.
Dung dịch đậm đặc của hợp chất nào sau đây được gọi là thủy tinh lỏng
-
A.
Na2SiO3 và K2SiO3
-
B.
SiO2 và K2SiO3
-
C.
NaOH và Na2SiO3
-
D.
KOH và K2SiO3
Đáp án : A
Thủy tinh lỏng là dung dịch đậm đặc của Na2SiO3 và K2SiO3
Một loại thủy tinh có chứa 13% Na2O; 11,7% CaO; 75,3% SiO2 về khối lượng. Thành phần của thủy tinh này được viết dưới dạng hợp chất các oxit là
-
A.
Na2O.CaO.6SiO2
-
B.
2Na2O.6CaO.6SiO2
-
C.
2Na2O.CaO.6SiO2
-
D.
Na2O.6CaO.SiO2
Đáp án : A
Công thức thủy tinh có dạng: xNa2O.yCaO.zSiO2
$x{\rm{ }}:{\rm{ }}y{\rm{ }}:{\rm{ }}z{\rm{ }} = \,\frac{{\% N{a_2}O}}{{{M_{N{a_2}O}}}}:\frac{{\% CaO}}{{{M_{CaO}}}}:\frac{{\% Si{{\rm{O}}_2}}}{{{M_{Si{{\rm{O}}_2}}}}}$
Công thức thủy tinh có dạng: xNa2O.yCaO.zSiO2
$x{\rm{ }}:{\rm{ }}y{\rm{ }}:{\rm{ }}z{\rm{ }} = \,\frac{{\% N{a_2}O}}{{{M_{N{a_2}O}}}}:\frac{{\% CaO}}{{{M_{CaO}}}}:\frac{{\% Si{{\rm{O}}_2}}}{{{M_{Si{{\rm{O}}_2}}}}}\,\, = \,\,\frac{{13}}{{62}}:\frac{{11,7}}{{56}}:\frac{{75,3}}{{60}} = 0,21:0,21:1,255 = 1:1:6$
Cho 3,60 gam cacbon tác dụng với 8,10 gam nhôm. Khối lượng nhôm cacbua tạo thành nếu hiệu suất của phản ứng 70% là
-
A.
5,76 gam
-
B.
7,56 gam
-
C.
10,08 gam
-
D.
10,80 gam
Đáp án : B
+) 3C + 4Al $\xrightarrow{{{t}^{o}}}$ Al4C3
Xét tỉ lệ, biện luân chất dư, chất hết
+) nAl4C3 lí thuyết = nAl / 4
+) nAl4C3 thực tế = nAl4C3 lí thuyết . H
nC = 0,3 mol; nAl = 0,3 mol
3C + 4Al $\xrightarrow{{{t}^{o}}}$ Al4C3
Xét tỉ lệ : \(\frac{{{n_C}}}{3} = \frac{{0,3}}{3} = 0,1\,\, > \,\,\frac{{{n_{Al}}}}{4} = \frac{{0,3}}{4} = 0,075\) => phản ứng tính theo Al
nAl4C3 lí thuyết = nAl / 4 = 0,075 mol
H = 70% => nAl4C3 thực tế = 0,075.70/100 = 0,0525 mol => mAl4C3 = 7,56 gam
không xét tỉ lệ dư thừa => tính nhầm hiệu suất theo C => chọn nhầm C
Có 5 lọ mất nhãn đựng 5 chất bột màu trắng: NaCl, Na2CO3, Na2SO4, BaCO3, BaSO4. Chỉ dùng nước và khí CO2 thì có thể nhận được mấy chất
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đáp án : D
|
|
NaCl |
Na2CO3 |
Na2SO4 |
BaCO3 |
BaSO4 |
|
Nước |
tan |
tan |
tan |
Không tan |
Không tan |
|
CO2 |
Không ht |
Không ht |
Không ht |
Hòa tan kết tủa, tạo dung dịch Ba(HCO3)2 trong suốt |
Không ht |
|
Ba(HCO3)2 |
Không ht |
↓ trắng, tan khi sục CO2 |
↓ trắng, không tan khi sục CO2 |
|
|
Vậy dùng nước và CO2 ta có thể nhận biết được cả 5 dung dịch
Dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Thực hiện các thí ngiệm sau
TN1: cho (a + b) mol CaCl2 vào dd X
TN2: cho (a + b) mol Ca(OH)2 vào dd X
Khối lượng kết tủa thu được trong 2 TN là
-
A.
Bằng nhau.
-
B.
Ở TN1 < ở TN2.
-
C.
Ở TN1 > ở TN2.
-
D.
Không so sánh được.
Đáp án : B
TN1: chỉ có Na2CO3 phản ứng: nCaCO3 = nNa2CO3
TN2: cả 2 chất đều phản ứng
NaHCO3 + Ca(OH)2 → CaCO3 ↓ + NaOH + H2O
Na2CO3 + Ca(OH)2 → CaCO3 ↓ + 2NaOH
TN1: chỉ có Na2CO3 phản ứng: nCaCO3 = nNa2CO3 = b mol
TN2: cả 2 chất đều phản ứng
NaHCO3 + Ca(OH)2 → CaCO3 ↓ + NaOH + H2O
a → a → a
Na2CO3 + Ca(OH)2 → CaCO3 ↓ + 2NaOH
b → b → b
=> ở TN2 thu được kết tủa nhiều hơn ở TN1
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
-
A.
NaOH và Al(OH)3.
-
B.
NaOH, NaAlO2 và Al(OH)3.
-
C.
NaAlO2 và BaCO3.
-
D.
Ba(OH)2, NaOH và BaCO3.
Đáp án : B
Dựa vào các phản ứng hóa học => xác định sản phẩm sau phản ứng
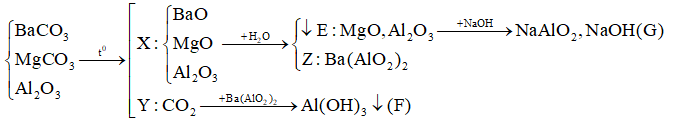
(Vì E tan 1 phần trong kiềm => trong E chứa Al2O3 còn dư => dung dịch Z không còn Ba(OH)2
Khí X được dùng nhiều trong ngành sản xuất nước giải khát và bia rượu. Tuy nhiên, việc gia tăng nồng độ khí X trong không khí là nguyên nhân làm trái đất nóng lên. Khí X là
-
A.
N2.
-
B.
O2.
-
C.
H2.
-
D.
CO2.
Đáp án : D
CO2 được dùng nhiều trong ngành sản xuất nước giải khát và bia rượu, tuy nhiên, việc gia tăng nồng độ khí X trong không khí là nguyên nhân làm trái đất nóng lên.
Cho 3,36 lít khí CO (đktc) phản ứng vừa đủ với 20 gam hỗn hợp X gồm CuO và MgO. Phần trăm khối lượng của MgO trong X là
-
A.
80%.
-
B.
60%.
-
C.
20%.
-
D.
40%.
Đáp án : D
Khi cho CO qua hỗn hợp CuO và MgO chỉ có CuO phản ứng. Viết PTHH xảy ra, tính mol CuO theo mol CO, từ đó tính được % CuO và suy ra được %MgO còn lại.
nCO(đktc) = 3,36 :22,4 = 0,15 (mol)
Khi cho CO qua hỗn hợp CuO và MgO chỉ có CuO phản ứng
CO + CuO \(\xrightarrow{{{t^0}}}\) Cu + H2O
0,15 → 0,15 (mol)
nCuO = 0,15 (mol) => mCuO = 0,15.80 = 12 (g)
%CuO = (mCuO : mhh).100% = (12 : 20).100% = 60%
=> %MgO = 100% -%CuO = 40%.
Thuốc nổ đen là hỗn hợp
-
A.
KNO3, C và S.
-
B.
KNO3 và S.
-
C.
KClO3, C và S.
-
D.
KClO3 và S.
Đáp án : A
Thuốc nổ đen là hỗn hợp của muôi kali nitrat, cacbon và lưu huỳnh
Thuốc nổ đen là hỗn hợp gồm KNO3, C và S.
Trong các chất sau, chất có độ cứng lớn nhất là
-
A.
silic.
-
B.
kim cương.
-
C.
than chì.
-
D.
thạch anh.
Đáp án : B
Kim cương
+ tinh thể trong suốt, không màu, không dẫn điện, dẫn nhiệt kém
+ cúng nhất trong tất cả các chất
Một chất Y có tính chất sau:
- Không màu, rất độc.
- Cháy trong không khí với ngọn lửa màu xanh và sinh ra chất khí làm đục nước vôi trong. Y là:
-
A.
H2.
-
B.
CO.
-
C.
Cl2.
-
D.
CO2.
Đáp án : B
CO là khí có những tính chất thỏa mãn với đề bài:
- Không màu, rất độc
- Cháy trong không khí với ngọn lửa màu xanh và sinh ra khí làm đục nước vôi trong:
2CO + O2 → 2CO2 (nhiệt độ)
CO2+ Ca(OH)2 → CaCO3 + H2O
Oxit nào sau đây không tạo muối?
-
A.
CO2.
-
B.
Mn2O7.
-
C.
CO.
-
D.
SiO2.
Đáp án : C
CO là một oxit trung tính nên không có khả năng tạo muối.
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
-
A.
1 lít.
-
B.
1,5 lít.
-
C.
0,8 lít.
-
D.
2 lít.
Đáp án : A
Bảo toàn nguyên tố C.
Bảo toàn nguyên tố C ta có: nCO2 thu được = nCO + nCO2 bđ
Hay V CO2 thu được = VCO + VCO2 bđ = 1 lít
Dẫn luồng khí CO dư qua hỗn hợp Al2O3; CuO; MgO; Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn thu được chất rắn là
-
A.
Al2O3, Cu, Mg, Fe.
-
B.
Al, Fe, Cu, Mg.
-
C.
Al2O3, Fe2O3, Cu, MgO.
-
D.
Al2O3, Cu; MgO; Fe.
Đáp án : D
CO khử được các oxit của KL đứng sau Al trong dãy hoạt động hóa học.
CO khử được các oxit CuO, Fe2O3 nên sau phản ứng thu được chất rắn là: Al2O3, Cu, MgO, Fe.
Kim cương và than chì là các dạng
-
A.
đồng hình của cacbon.
-
B.
đồng vị của cacbon.
-
C.
thù hình của cacbon.
-
D.
đồng phân của cacbon.
Đáp án : C
Kim cương và than chì là hai dạng thù hình của cacbon.
>> 2K9 Học trực tuyến - Định hướng luyện thi TN THPT, ĐGNL, ĐGTD ngay từ lớp 11 (Xem ngay) cùng thầy cô giáo giỏi trên Tuyensinh247.com. Bứt phá điểm 9,10 chỉ sau 3 tháng, tiếp cận sớm các kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1









