Đề kiểm tra 15 phút Hóa 11 chương 5: Hidrocacbon no - Đề số 1
Đề bài
Phản ứng đặc trưng của hiđrocacbon no là :
-
A.
Phản ứng tách.
-
B.
Phản ứng thế.
-
C.
Phản ứng cộng.
-
D.
Cả A, B và C.
Khi đốt cháy hoàn toàn V lít C2H6 (đktc) thu được 44 gam CO2 và 27 gam H2O. Giá trị của V là :
-
A.
8,96.
-
B.
11,20.
-
C.
13,44.
-
D.
15,68.
Sản phẩm của phản ứng thế clo (1:1, ánh sáng) vào 2,2-đimetylpropan là :
(1) (CH3)3CCH2Cl (2) CH3C(CH2Cl)2CH3 (3) CH3ClC(CH3)3
-
A.
(1) và (2).
-
B.
(2) và (3).
-
C.
(2).
-
D.
(1).
Khi clo hóa C5H12 với tỉ lệ mol 1:1 thu được 3 sản phẩm thế monoclo. Danh pháp IUPAC của ankan đó là
-
A.
1-metylbutan.
-
B.
2-metylbutan.
-
C.
pentan
-
D.
2, 2 -đimetylpropan.
Đốt cháy hoàn toàn một hiđrocacbon A. Sản phẩm thu được hấp thụ hoàn toàn vào 200 ml dung dịch Ca(OH)2 0,2M thấy thu được 3 gam kết tủa. Lọc bỏ kết tủa, cân lại phần dung dịch thấy khối lượng tăng lên so với ban đầu là 0,28 gam. Hiđrocacbon trên có CTPT là
-
A.
C5H12.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là :
-
A.
3.
-
B.
4.
-
C.
2.
-
D.
5.
Crackinh hoàn toàn 6,6 gam propan được hỗn hợp X gồm hai hiđrocacbon. Dẫn toàn bộ X qua bình đựng 400 ml dung dịch brom a mol/l thấy khí thoát ra khỏi bình có tỉ khối so metan là 1,1875. Giá trị a là :
-
A.
0,5M.
-
B.
0,25M.
-
C.
0,175M.
-
D.
0,1M.
Cho các chất sau :
C2H6 (I) C3H8 (II) n-C4H10 (III) i-C4H10 (IV)
Nhiệt độ sôi tăng dần theo dãy là :
-
A.
(III) < (IV) < (II) < (I).
-
B.
(III) < (IV) < (II) < (I).
-
C.
(I) < (II) < (IV) < (III).
-
D.
(I) < (II) < (III) < (IV).
Cho các chất sau :
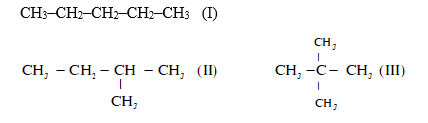
Thứ tự tăng dần nhiệt độ sôi của các chất là :
-
A.
I < II < III.
-
B.
II < I < III.
-
C.
III < II < I.
-
D.
II < III < I.
Trong phòng thí nghiệm, người ta điều chế CH4 bằng phản ứng
-
A.
crackinh n-butan.
-
B.
cacbon tác dụng với hiđro.
-
C.
nung natri axetat với vôi tôi xút.
-
D.
điện phân dung dịch natri axetat.
$A{l_4}{C_3} + {\text{ }}{H_2}O \to X + {\text{ }}Al{\left( {OH} \right)_3}$. X là
-
A.
CH4
-
B.
C2H6
-
C.
C3H8
-
D.
C3H6
Từ CH4 (các chất vô cơ và điều kiện có đủ) có thể điều chế các chất nào sau đây?
-
A.
CH3Cl
-
B.
C2H6
-
C.
C3H8
-
D.
Cả 3 chất trên
Lời giải và đáp án
Phản ứng đặc trưng của hiđrocacbon no là :
-
A.
Phản ứng tách.
-
B.
Phản ứng thế.
-
C.
Phản ứng cộng.
-
D.
Cả A, B và C.
Đáp án : B
Xem lại lí thuyết phản ứng halogen hóa của ankan
Phản ứng đặc trưng của hiđrocacbon no là phản ứng thế
Khi đốt cháy hoàn toàn V lít C2H6 (đktc) thu được 44 gam CO2 và 27 gam H2O. Giá trị của V là :
-
A.
8,96.
-
B.
11,20.
-
C.
13,44.
-
D.
15,68.
Đáp án : B
Áp dụng công thức : nankan = nH2O – nCO2
nCO2 = 1 mol ; nH2O = 1,5 mol
Áp dụng công thức : nankan = nH2O – nCO2 = 1,5 – 1 = 0,5 mol
=> VC2H6 = 0,5.22,4 = 11,2 lít
Sản phẩm của phản ứng thế clo (1:1, ánh sáng) vào 2,2-đimetylpropan là :
(1) (CH3)3CCH2Cl (2) CH3C(CH2Cl)2CH3 (3) CH3ClC(CH3)3
-
A.
(1) và (2).
-
B.
(2) và (3).
-
C.
(2).
-
D.
(1).
Đáp án : D
Xem lại lí thuyết phản ứng halogen hóa của ankan
2,2-đimetylpropan: (CH3)3C-CH3 => chỉ có 1 vị trí thế Cl
(CH3)3C-CH3 + Cl2 → (CH3)3C-CH2Cl + HCl
Khi clo hóa C5H12 với tỉ lệ mol 1:1 thu được 3 sản phẩm thế monoclo. Danh pháp IUPAC của ankan đó là
-
A.
1-metylbutan.
-
B.
2-metylbutan.
-
C.
pentan
-
D.
2, 2 -đimetylpropan.
Đáp án : C
- Viết đồng phân ankan
- Xét các vị trí thế clo của mỗi đồng phân
C5H12 có 3 đồng phân:
$\overset{1}{\mathop{C}}\,{{H}_{3}}-\overset{2}{\mathop{C}}\,{{H}_{2}}-\overset{3}{\mathop{C}}\,{{H}_{2}}-C{{H}_{2}}-C{{H}_{3}}$ : có 3 vị trí thế Clo (1, 2, 3), vị trí C4 giống C2 và C5 giống C1
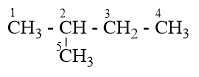
có 4 vị trí thế Clo (1, 2, 3, 4), vị trí C5 giống C1
(CH3)3C – CH3 : chỉ có 1 vị trí thế Clo vì 4 nhóm CH3 đều giống nhau
Đốt cháy hoàn toàn một hiđrocacbon A. Sản phẩm thu được hấp thụ hoàn toàn vào 200 ml dung dịch Ca(OH)2 0,2M thấy thu được 3 gam kết tủa. Lọc bỏ kết tủa, cân lại phần dung dịch thấy khối lượng tăng lên so với ban đầu là 0,28 gam. Hiđrocacbon trên có CTPT là
-
A.
C5H12.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Đáp án : A
- Trường hợp 1 : Ca(OH)2 dư, chỉ xảy ra phản ứng tạo kết tủa :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
+) mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}$
- Trường hợp 2 : Ca(OH)2 phản ứng hết :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
+) mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}$
Theo giả thiết ta có : Do đó có hai trường hợp xảy ra :
TH1: Ca(OH)2 dư, chỉ xảy ra phản ứng tạo kết tủa :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}=0,28\,\,gam\Rightarrow {{m}_{{{H}_{2}}O}}=0,28+3-0,03.44=\,\,1,96\,\,gam$
$\Rightarrow {{n}_{{{H}_{2}}O}}=0,1088\,\,mol\Rightarrow {{n}_{H}}=0,217\,\,mol\Rightarrow {{n}_{C}}:{{n}_{H}}=0,03:0,217=1:7,3\,\,(loại).$
TH2 : Ca(OH)2 phản ứng hết :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
0,02 0,01
$\Rightarrow {{n}_{C{{O}_{2}}}}=0,05\,\,mol.$
mdung dịch tăng = ${{m}_{{{H}_{2}}O}}+{{m}_{C{{O}_{2}}}}-{{m}_{CaC{{O}_{3}}}}=0,28\,\,gam\Rightarrow {{m}_{{{H}_{2}}O}}=0,28+3-0,05.44=\,\,1,08\,\,gam$
$\Rightarrow {{n}_{{{H}_{2}}O}}=0,06\,\,mol\Rightarrow {{n}_{H}}=0,12\,\,mol\Rightarrow {{n}_{C}}:{{n}_{H}}=0,05:0,12=5:12\,$
Vậy CTPT của ankan là C5H12
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là :
-
A.
3.
-
B.
4.
-
C.
2.
-
D.
5.
Đáp án : C
- Xác định số nguyên tử C trong X
Số C = \(\frac{{{n_{C{O_2}}}}}{{{n_X}}}\)
- Xác định CTPT của X
X chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử
=> X là ankan
=> số vị trí thế monoclo
- Đốt cháy 1 thể tích X sinh ra 6 thể tích CO2 => trong X có 6 nguyên tử C
- Vì X chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử
=> X là ankan C6H14 có công thức phân tử là (CH3)2 - CH – CH(CH3)2
=> có 2 vị trí thế monoclo
Crackinh hoàn toàn 6,6 gam propan được hỗn hợp X gồm hai hiđrocacbon. Dẫn toàn bộ X qua bình đựng 400 ml dung dịch brom a mol/l thấy khí thoát ra khỏi bình có tỉ khối so metan là 1,1875. Giá trị a là :
-
A.
0,5M.
-
B.
0,25M.
-
C.
0,175M.
-
D.
0,1M.
Đáp án : B
+) ${{n}_{{{C}_{3}}{{H}_{8}}}}={{n}_{C{{H}_{4}}}}={{n}_{{{C}_{2}}{{H}_{4}}}}$
+) Sau khi qua bình đựng brom khí thoát ra khỏi bình có nên ngoài CH4 còn có C2H4 dư.
+) Từ $\bar{M}=19$ => a
+) nC2H4 phản ứng với Br2 = nBr2
Các phản ứng xảy ra :
C3H8 $\xrightarrow{{}}$ CH4 + C2H4 (1)
C2H4 + Br2 $\xrightarrow{{}}$ C2H4Br2 (2)
Theo (1) và giả thiết ta có : ${{n}_{{{C}_{3}}{{H}_{8}}}}={{n}_{C{{H}_{4}}}}={{n}_{{{C}_{2}}{{H}_{4}}}}=\frac{6,6}{44}=0,15\,\,mol$
Sau khi qua bình đựng brom khí thoát ra khỏi bình có $\overline{M}=1,1875.16=19$ nên ngoài CH4 còn có C2H4 dư.
Gọi nC2H4 dư = a mol
$\bar{M}=\frac{16.0,15+28a}{0,15+a}=19\,\,=>\,\,a=0,05\,\,mol$
=> nC2H4 phản ứng với Br2 = 0,15 – 0,05 = 0,1 mol => nBr2 = 0,1 mol
=> CM Br2 = $\frac{0,1}{0,4}=0,25M$
Cho các chất sau :
C2H6 (I) C3H8 (II) n-C4H10 (III) i-C4H10 (IV)
Nhiệt độ sôi tăng dần theo dãy là :
-
A.
(III) < (IV) < (II) < (I).
-
B.
(III) < (IV) < (II) < (I).
-
C.
(I) < (II) < (IV) < (III).
-
D.
(I) < (II) < (III) < (IV).
Đáp án : C
Khi cấu trúc phân tử càng gọn thì tonc, tos càng cao và ngược lại.
Vì phân tử i-C4H10 có cấu trúc cồng kềnh hơn n-C4H10 nên tos nhỏ hơn: (IV) < (III)
Nhiệt độ sôi tăng dần khi tăng khối lượng phân tử => (I) < (II) < (IV) < (III)
Cho các chất sau :
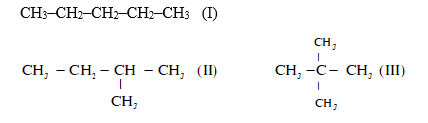
Thứ tự tăng dần nhiệt độ sôi của các chất là :
-
A.
I < II < III.
-
B.
II < I < III.
-
C.
III < II < I.
-
D.
II < III < I.
Đáp án : C
Khi cấu trúc phân tử càng cồng kềnh thì tonc, tos càng thấp và ngược lại.
Cả 3 chất đều có 5C => tos phụ thuộc vào cấu trúc phân tử. Phân tử càng cồng kềnh thì nhiệt độ sôi càng thấp
=> (III) có cấu trúc cồng kềnh nhất => (III) < (II) < (I)
Trong phòng thí nghiệm, người ta điều chế CH4 bằng phản ứng
-
A.
crackinh n-butan.
-
B.
cacbon tác dụng với hiđro.
-
C.
nung natri axetat với vôi tôi xút.
-
D.
điện phân dung dịch natri axetat.
Đáp án : C
Trong phòng thí nghiệm, CH4 được điều chế bằng cách nung natri axetat với vôi tôi xút
$A{l_4}{C_3} + {\text{ }}{H_2}O \to X + {\text{ }}Al{\left( {OH} \right)_3}$. X là
-
A.
CH4
-
B.
C2H6
-
C.
C3H8
-
D.
C3H6
Đáp án : A
$A{l_4}{C_3} + {\text{12}}{H_2}O \to 3C{H_4} + {\text{ 4}}Al{\left( {OH} \right)_3}$
Từ CH4 (các chất vô cơ và điều kiện có đủ) có thể điều chế các chất nào sau đây?
-
A.
CH3Cl
-
B.
C2H6
-
C.
C3H8
-
D.
Cả 3 chất trên
Đáp án : D
Xem lại phương pháp điều chế và ứng dụng của metan
$C{H_4} + C{l_2}\xrightarrow{{as}}C{H_3}Cl + HCl$
$C{H_4}\xrightarrow{{1500^\circ C,\,xt}}{C_2}{H_2}\xrightarrow{{ + {H_2}(Ni,t^\circ )}}{C_2}{H_6}$
$C{H_4}\xrightarrow{{1500^\circ C,\,xt}}{C_2}{H_2}\xrightarrow{{đime{\text{ }}hóa}}{C_4}{H_4}\xrightarrow{{ + {H_2}(Ni,t^\circ )}}{C_4}{H_{10}}\xrightarrow{{crackinh}}{C_3}{H_6}\xrightarrow{{ + {H_2}(Ni,t^\circ )}}{C_3}{H_8}$
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1










Danh sách bình luận