Đề thi học kì 2 Hóa 11 - Đề số 3
Đề bài
Cho các hợp chất sau: CCl3COOH, CH3COOH, CBr3COOH, CF3COOH. Chất có tính axit mạnh nhất là
-
A.
CCl3COOH.
-
B.
CH3COOH.
-
C.
CBr3COOH.
-
D.
CF3COOH.
Cho sơ đồ
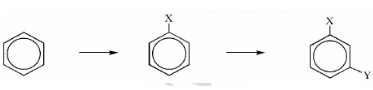
Nhóm X, Y phù hợp sơ đồ trên là
-
A.
X (-CH3), Y (-NO2)
-
B.
X (-NO2), Y (-CH3)
-
C.
X (-NH2), Y (-CH3)
-
D.
A, C đều đúng
Hiện nay nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là
-
A.
etanol.
-
B.
etan.
-
C.
axetilen.
-
D.
etilen.
Cho các chất: CH2=CH-CH=CH2; CH3-CH2-CH=C(CH3)2; CH3-CH=CH-CH=CH2; CH3-CH=CH2; CH3-CH=CH-COOH. Số chất có đồng phân hình học là :
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
1.
Có thể tạo ra CH3COOH từ
-
A.
CH3CHO.
-
B.
C2H5OH.
-
C.
CH3CCl3.
-
D.
Tất cả đều đúng.
Chất nào sau đây làm mất màu dung dịch KMnO4 khi đun nóng?
-
A.
benzen
-
B.
toluen
-
C.
propan
-
D.
metan
Tên thay thế của hợp chất có công thức dưới đây là
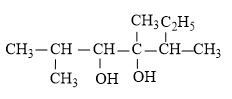
-
A.
3,4,6-trimetylheptan-4,5-điol
-
B.
2,4-đimetyl-5-etylhexan-3,4-điol
-
C.
2,4,5-trimetylheptan-3,4-điol
-
D.
3,5-đimetyl-2-etylhexan-3,4-điol
Trong các chất: ancol propylic, anđehit fomic, axit butiric và etilen glycol, chất có nhiệt độ sôi nhỏ nhất là
-
A.
ancol propylic
-
B.
anđehit fomic
-
C.
axit butiric
-
D.
etilen glycol
Khi đun nóng hh gồm CH3OH với HCl đặc có thể thu được hợp chất có tên là:
-
A.
metylclorua
-
B.
clometan
-
C.
đimetyl ete
-
D.
A và B đều đúng
Ảnh hưởng của nhóm -OH đến gốc C6H5- trong phân tử phenol thể hiện qua phản ứng giữa phenol với
-
A.
dung dịch NaOH.
-
B.
Na kim loại.
-
C.
nước Br2.
-
D.
H2 (Ni, nung nóng).
Ancol no X có công thức đơn giản nhất là C2H5O. Công thức phân tử của X là
-
A.
C4H10O
-
B.
C2H5O
-
C.
C6H15O3
-
D.
C4H10O2
Có thể dùng một chất nào trong các chất dưới đây để nhậnn biết được các chất: ancol etylic, glixerol, dung dịch anđehit axetic đựng trong ba lọ mất nhãn?
-
A.
Cu(OH)2/OH-
-
B.
Quỳ tím
-
C.
Kim loại Na
-
D.
dd AgNO3/NH3.
Sản phẩm chính của phản ứng nào sau đây có đồng phân hình học?
-
A.
\(CH \equiv CH + HCl \to C{H_2} = CHCl\)
-
B.
\(CH \equiv C - C{H_3} + HCl \to C{H_2} = CCl - C{H_3}\)
-
C.
\(C{H_3}C \equiv CC{H_3} + HCl \to C{H_3}CH = CClC{H_3}\)
-
D.
\(C{H_3}C \equiv CC{H_3} + 2{H_2} \to C{H_3}C{H_2}C{H_2}C{H_3}\)
Trong dãy đồng đẳng của các axit đơn chức no, HCOOH là axit có độ mạnh trung bình, còn lại là axit yếu (điện li không hoàn toàn). Dung dịch axit axetic có nồng độ 0,001 mol/l có pH là
-
A.
3 < pH < 7.
-
B.
< 3.
-
C.
3.
-
D.
10-3
Để chuyển hóa ankin thành anken ta thực hiện phản ứng cộng H2 trong điều kiện có xúc tác
-
A.
Ni, t0
-
B.
Mn, t0
-
C.
Pd/PbCO3, t0
-
D.
Fe, t0
Trong các nhận xét dưới đây, nhận xét nào sai ?
-
A.
Tất cả các ankan đều có công thức phân tử CnH2n+2.
-
B.
Tất cả các chất có công thức phân tử CnH2n+2 đều là ankan.
-
C.
Tất cả các ankan đều chỉ có liên kết đơn trong phân tử.
-
D.
Tất cả các chất chỉ có liên kết đơn trong phân tử đều là ankan.
Ankin C6H10 có bao nhiêu đồng phân có phản ứng với dung dịch AgNO3/NH3?
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Đốt cháy hoàn toàn 1 mol ankađien A cần 7 mol oxi. Công thức phân tử của A là
-
A.
C4H6
-
B.
C5H8
-
C.
C3H4
-
D.
C6H10
Mô hình thí nghiệm dùng để điều chế chất khí Z:
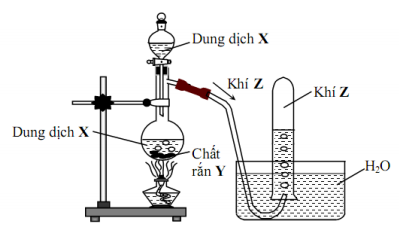
Phương trình hóa học nào sau đây phù hợp với mô hình trên?
-
A.
CaC2 + 2H2O → Ca(OH)2 + C2H2↑.
-
B.
Al4C3 + 12HCl → 4AlCl3 + 3CH4↑.
-
C.
H2SO4 đặc + Na2SO3 rắn SO2↑ + Na2SO4 + H2O.
-
D.
CH3COONa rắn + NaOH rắn CH4↑ + Na2CO3.
Phản ứng đặc trưng của hiđrocacbon no là :
-
A.
Phản ứng tách.
-
B.
Phản ứng thế.
-
C.
Phản ứng cộng.
-
D.
Cả A, B và C.
Hiđro hóa hoàn toàn buta-1,3-đien, thu được:
-
A.
butan
-
B.
isobutan
-
C.
isopentan
-
D.
pentan
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1:1), số dẫn xuất monoclo tối đa sinh ra là
-
A.
3
-
B.
4
-
C.
5
-
D.
2
Cho 2,4 gam hỗn hợp C2H2, C3H8, C2H6, C4H6 và H2 đi qua bột Ni nung nóng, sau một thời gian thu được hỗn hợp khí X. Đốt cháy hoàn toàn X cần vừa đủ V lít khí O2 (đktc), thu được 3,36 lít CO2 (đktc). Gía trị của V là
-
A.
6,72.
-
B.
10,08.
-
C.
7,84.
-
D.
8,96.
Crackinh 1 ankan A thu được hỗn hợp sản phẩm B gồm 5 hiđrocacbon có khối lượng mol trung bình là 36,25 gam/mol, hiệu suất phản ứng là 60%. Công thức phân tử của A là :
-
A.
C4H10.
-
B.
C5H12.
-
C.
C3H8.
-
D.
C2H6.
Khi đốt cháy hoàn toàn một hiđrocacbon A thu được 1,12 lít CO2 (đktc) và 1,08 gam H2O. A có phân tử khối là 72 và khi cho tác dụng với clo (có askt) thì thu được bốn dẫn xuất monocle. A có tên gọi là:
-
A.
isopentan
-
B.
2, 2-đimetylpropan
-
C.
neopentan
-
D.
pentan
Hỗn hợp X gồm 2 anken kế tiếp nhau trong dãy đồng đẳng. Trộn một thể tích hỗn hợp X với một lượng vừa đủ khí oxi để được một hỗn hợp Y rồi đen đốt cháy hoàn toàn thì thu được sản phẩm khí và hơi Z. Tỉ khối của Y so với Z là 744 : 713. Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. Công thức phân tử của 2 anken là
-
A.
C5H10 và C6H12.
-
B.
C3H6 và C2H4.
-
C.
C4H8 và C5H10.
-
D.
C3H6 và C4H8.
Cho etan qua xúc tác (ở nhiệt độ cao) thu được một hỗn hợp X gồm etan, etilen, axetilen và H2. Tỷ khối của hỗn hợp X đối với etan là 0,4. Hãy cho biết nếu cho 0,4 mol hỗn hợp X qua dung dịch Br2 dư thì số mol Br2 đã phản ứng là bao nhiêu ?
-
A.
0,24 mol
-
B.
0,6 mol
-
C.
0,4 mol
-
D.
0,32 mol.
Đốt cháy hoàn toàn m gam ankin X thu được m gam nước. Công thức phân tử của X là
-
A.
C2H2.
-
B.
C3H4.
-
C.
C4H6.
-
D.
C5H8.
Dẫn 11,2 lít hỗn hợp khí X gồm axetilen và propin vào dung dịch AgNO3/NH3 dư (các phản ứng xảy ra hoàn toàn), sau phản ứng thu được 92,1 gam kết tủa. Phần trăm số mol axetilen trong X là
-
A.
70%.
-
B.
30%.
-
C.
60%.
-
D.
40%.
Đốt cháy hết 9,18 gam 2 đồng đẳng của benzen A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là :
-
A.
15,654.
-
B.
15,465.
-
C.
15,546.
-
D.
15,456.
Tiến hành trùng hợp 10,4 gam stiren được hỗn hợp X gồm polistiren và stiren dư. Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung dịch KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp stiren là
-
A.
60%
-
B.
75%
-
C.
80%
-
D.
83,33%
Cho 18,4 gam X gồm glixerol và một ancol no đơn chức Y tác dụng với Na dư thu được 5,6 lít khí hiđro (đktc). Lượng hiđro do Y sinh ra bằng 2/3 lượng hiđro do glixerol sinh ra. Công thức phân tử của Y là
-
A.
CH3OH
-
B.
C2H5OH
-
C.
C3H7OH
-
D.
C4H9OH
Đun ancol X đơn chức với H2SO4 đặc thu được hợp chất hữu cơ Y có dY/ X = 1,75. Công thức phân tử của X là
-
A.
C3H5OH
-
B.
C3H7OH
-
C.
C4H7OH
-
D.
C4H9OH
Chất nào sau đây có nhiệt độ sôi thấp nhất ?
-
A.
axetanđehit
-
B.
metan
-
C.
phenol
-
D.
propan-1-ol
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ A thu được 0,4 mol CO2 và 0,4 mol H2O. Biết A chỉ chứa một loại nhóm chức và 0,05 mol A tham gia phản ứng tráng gương thì tạo ra 0,1 mol Ag. Công thức cấu tạo thu gọn của A là
-
A.
C3H7CHO.
-
B.
CH3CHO.
-
C.
C2H5CHO.
-
D.
C2H3CHO.
Hợp chất A chứa C, H, O có M < 90 đvC. A tham gia phản ứng tráng bạc và có thể tác dụng với H2 (xt Ni) sinh ra ancol chứa C bậc IV trong phân tử. Công thức của A là
-
A.
(CH3)2CHCHO.
-
B.
(CH3)2CH-CH2CHO.
-
C.
(CH3)3C-CH2CHO.
-
D.
(CH3)3CCHO.
Hỗn hợp X gồm axit HCOOH và axit CH3COOH (tỉ lệ mol 1:1). Lấy 5,3 gam hỗn hợp X tác dụng với 5,75 gam C2H5OH (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất của các phản ứng este hoá đều bằng 80%). Giá trị của m là
-
A.
10,12 g
-
B.
6,48 g
-
C.
8,10 g
-
D.
16,20 g
Dẫn V lít (ở đktc) hỗn hợp X gồm axetilen và hiđro có khối lượng là m gam đi qua ống sứ đựng bột niken nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z được 2,24 lít khí CO2 (đktc) và 4,5 gam H2O. Tính giá trị của m.
-
A.
5,6 gam
-
B.
5,4 gam
-
C.
5,8 gam
-
D.
6,2 gam
Hiđro hóa hoàn toàn m gam hỗn hợp X gồm 2 anđehit mạch hở, thu được hỗn hợp Y. Cho Y vào bình đựng Na (dư 25% so với lượng phản ứng), thu được 11,2 lít H2 (đktc) và hỗn hợp rắn Z. Đốt cháy hoàn toàn Z thu được Na2CO3, H2O và 16,5 gam CO2. Mặt khác, cho 0,3 mol X tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được a gam kết tủa. Giá trị của a là
-
A.
86,4.
-
B.
97,2.
-
C.
108,0.
-
D.
129,6.
M là hỗn hợp gồm 3 ancol đơn chức X, Y, Z có số nguyên tử cacbon liên tiếp nhau, đều mạch hở (MX < MY < MZ); X và Y no, Z không no (có 1 liên kết đôi C=C). Chia M thành 3 phần bằng nhau.
- Đốt cháy hoàn toàn phần 1 thu được 45,024 lít khí CO2 (đktc) và 46,44 gam H2O
- Phần 2 làm mất màu vừa đủ dung dịch chứa 16 gam Br2
- Đun nóng phần 3 với H2SO4 đặc ở 140oC thu được 18,752 gam hỗn hợp 6 ete (T). Đốt cháy hoàn toàn T thu được 1,106 mol CO2 và 1,252 mol H2O.
Hiệu suất tạo ete của X, Y, Z lần lượt là
-
A.
50%; 40%; 35%.
-
B.
50%; 60%; 40%.
-
C.
60%; 40%; 35%.
-
D.
60%; 50%; 35%.
Lời giải và đáp án
Cho các hợp chất sau: CCl3COOH, CH3COOH, CBr3COOH, CF3COOH. Chất có tính axit mạnh nhất là
-
A.
CCl3COOH.
-
B.
CH3COOH.
-
C.
CBr3COOH.
-
D.
CF3COOH.
Đáp án : D
Chất có tính axit mạnh nhất là CF3COOH vì F có độ âm điện lớn nhất => hút e mạnh nhất
Cho sơ đồ

Nhóm X, Y phù hợp sơ đồ trên là
-
A.
X (-CH3), Y (-NO2)
-
B.
X (-NO2), Y (-CH3)
-
C.
X (-NH2), Y (-CH3)
-
D.
A, C đều đúng
Đáp án : B
Vì Y nằm ở vị trí meta so với X
Nên X phải là nhóm hút electron để các nhóm thế tiếp theo thế vào vị trí meta.
Vì Y nằm ở vị trí meta so với X
Nên X phải là nhóm hút electron để các nhóm thế tiếp theo thế vào vị trí meta.
=> X là -NO2 => Y là -CH3
Hiện nay nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là
-
A.
etanol.
-
B.
etan.
-
C.
axetilen.
-
D.
etilen.
Đáp án : D
Nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là etilen
2CH2=CH2 + O2 $\xrightarrow{P\text{d}C{{l}_{2}},CuC{{l}_{2}}}$ 2CH3CHO
Cho các chất: CH2=CH-CH=CH2; CH3-CH2-CH=C(CH3)2; CH3-CH=CH-CH=CH2; CH3-CH=CH2; CH3-CH=CH-COOH. Số chất có đồng phân hình học là :
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
1.
Đáp án : C
Những chất có đồng phân là CH3-CH=CH-CH=CH2; CH3-CH=CH-COOH
Có thể tạo ra CH3COOH từ
-
A.
CH3CHO.
-
B.
C2H5OH.
-
C.
CH3CCl3.
-
D.
Tất cả đều đúng.
Đáp án : D
Có thể tạo ra CH3COOH từ CH3CHO, C2H5OH, CH3CCl3
CH3CHO + $\frac{1}{2}$O2 $\xrightarrow{xt,{{t}^{o}}}$ CH3COOH
CH3CH2OH + O2 $\xrightarrow[25-{{30}^{o}}C]{men\,\,giấm}$ CH3COOH + H2O
CH3CCl3 + 3NaOH → CH3COOH + 3NaCl + H2O
Chất nào sau đây làm mất màu dung dịch KMnO4 khi đun nóng?
-
A.
benzen
-
B.
toluen
-
C.
propan
-
D.
metan
Đáp án : B
Xem lại lí thuyết toluen
Chất nào sau đây làm mất màu dung dịch KMnO4 khi đun nóng toluen
PTHH: 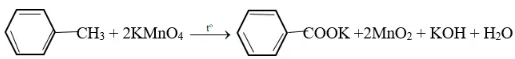
Tên thay thế của hợp chất có công thức dưới đây là

-
A.
3,4,6-trimetylheptan-4,5-điol
-
B.
2,4-đimetyl-5-etylhexan-3,4-điol
-
C.
2,4,5-trimetylheptan-3,4-điol
-
D.
3,5-đimetyl-2-etylhexan-3,4-điol
Đáp án : C
+ Chọn mạch chính đi qua C chứa nhóm OH
+ Đánh số C từ vị trí gần nhóm OH nhất
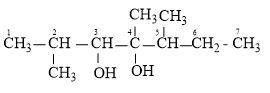
=> Tên gọi: 2,4,5-trimetylheptan-3,4-điol
Trong các chất: ancol propylic, anđehit fomic, axit butiric và etilen glycol, chất có nhiệt độ sôi nhỏ nhất là
-
A.
ancol propylic
-
B.
anđehit fomic
-
C.
axit butiric
-
D.
etilen glycol
Đáp án : B
Theo chiều giảm nhiệt độ sôi : axit > ancol > anđehit
=> chất có nhiệt độ sôi nhỏ nhất là anđehit fomic
Khi đun nóng hh gồm CH3OH với HCl đặc có thể thu được hợp chất có tên là:
-
A.
metylclorua
-
B.
clometan
-
C.
đimetyl ete
-
D.
A và B đều đúng
Đáp án : D
Xem lại lí thuyết phản ứng của ancol với axit
CH3OH + HCl → CH3Cl + H2O
CH3Cl có tên là metylclorua và clometan
Ảnh hưởng của nhóm -OH đến gốc C6H5- trong phân tử phenol thể hiện qua phản ứng giữa phenol với
-
A.
dung dịch NaOH.
-
B.
Na kim loại.
-
C.
nước Br2.
-
D.
H2 (Ni, nung nóng).
Đáp án : C
Nhóm -OH ảnh hưởng đến gốc C6H5- khiến cho dễ thế vào vòng benzen của phenol hơn so với benzen C6H6.
- Nhóm -OH ảnh hưởng đến gốc C6H5- khiến phản ứng thế vào vòng benzen của phenol dễ dàng hơn so với benzen C6H6
⟹ Phản ứng thể hiện sự ảnh hưởng này là phản ứng của phenol với Br2
- So sánh phản ứng của phenol và benzen với Br2:
C6H5OH + 3Br2 (dd) → C6H2OHBr3 ↓ + 3HBr (không cần xúc tác)
C6H6 + Br2 (khan) → C6H5Br + HBr (xúc tác bột sắt)
Ancol no X có công thức đơn giản nhất là C2H5O. Công thức phân tử của X là
-
A.
C4H10O
-
B.
C2H5O
-
C.
C6H15O3
-
D.
C4H10O2
Đáp án : D
Ancol no X có công thức đơn giản nhất là C2H5O => CTPT dạng (C2H5O)n
n = 2 => Công thức phân tử của X là C4H10O2
Có thể dùng một chất nào trong các chất dưới đây để nhậnn biết được các chất: ancol etylic, glixerol, dung dịch anđehit axetic đựng trong ba lọ mất nhãn?
-
A.
Cu(OH)2/OH-
-
B.
Quỳ tím
-
C.
Kim loại Na
-
D.
dd AgNO3/NH3.
Đáp án : A
Xem lại lí thuyết phản ứng oxi hóa hoàn toàn anđehit
- Dùng Cu(OH)2/OH-
|
|
C2H5OH |
C3H5(OH)3 |
CH3CHO |
|
Cu(OH)2/OH- (to thường) |
Không phản ứng |
Phức màu xanh |
Không phản ứng |
|
Cu(OH)2/OH- đun nóng |
Không phản ứng |
|
Kết tủa đỏ gạch |
Sản phẩm chính của phản ứng nào sau đây có đồng phân hình học?
-
A.
\(CH \equiv CH + HCl \to C{H_2} = CHCl\)
-
B.
\(CH \equiv C - C{H_3} + HCl \to C{H_2} = CCl - C{H_3}\)
-
C.
\(C{H_3}C \equiv CC{H_3} + HCl \to C{H_3}CH = CClC{H_3}\)
-
D.
\(C{H_3}C \equiv CC{H_3} + 2{H_2} \to C{H_3}C{H_2}C{H_2}C{H_3}\)
Đáp án : C
CH2=CHCl; CH2=CCl-CH3 không có đphh vì a và b giống nhau ( đều là H)
CH3CH2CH2CH3 không có liên kết đôi => không có đphh
Trong dãy đồng đẳng của các axit đơn chức no, HCOOH là axit có độ mạnh trung bình, còn lại là axit yếu (điện li không hoàn toàn). Dung dịch axit axetic có nồng độ 0,001 mol/l có pH là
-
A.
3 < pH < 7.
-
B.
< 3.
-
C.
3.
-
D.
10-3
Đáp án : A
+) CH3COOH là axit yếu phân li không hoàn toàn ra H+
=> So sánh [H+] với [CH3COOH]
=> PH
Ta có phương trình phân li: CH3COOH $ \rightleftharpoons $ CH3COO- + H+
Mà [CH3COOH] = 0,001 M nên [H+] < [CH3COOH] =0,001 M
→ pH > 3 → 3 < pH < 7
Để chuyển hóa ankin thành anken ta thực hiện phản ứng cộng H2 trong điều kiện có xúc tác
-
A.
Ni, t0
-
B.
Mn, t0
-
C.
Pd/PbCO3, t0
-
D.
Fe, t0
Đáp án : C
Xem lại lí thuyết phản ứng cộng ankin
Để chuyển hóa ankin thành anken ta thực hiện phản ứng cộng H2 trong điều kiện có xúc tác Pd/PbCO3 đun nóng
VD: CH≡C–CH2–CH3 + H2 \(\xrightarrow{{Pd/PbC{O_3}}}\) CH2=CH–CH2–CH3
Trong các nhận xét dưới đây, nhận xét nào sai ?
-
A.
Tất cả các ankan đều có công thức phân tử CnH2n+2.
-
B.
Tất cả các chất có công thức phân tử CnH2n+2 đều là ankan.
-
C.
Tất cả các ankan đều chỉ có liên kết đơn trong phân tử.
-
D.
Tất cả các chất chỉ có liên kết đơn trong phân tử đều là ankan.
Đáp án : D
Nhận xét sai là: Tất cả các chất chỉ có liên kết đơn trong phân tử đều là ankan.
Ví dụ như chất CH3 – O – CH3 đều chỉ có các liên kết đơn nhưng không phải là ankan.
Ankin C6H10 có bao nhiêu đồng phân có phản ứng với dung dịch AgNO3/NH3?
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Đáp án : B
Có phản ứng với dung dịch AgNO3/NH3 => có nối 3 đầu mạch
- CH≡C-CH2-CH2-CH2-CH3
- (CH3)2CH-CH2-C≡CH
- CH3-CH2-CH(CH3)-C≡CH
- (CH3)3C-C≡CH
Đốt cháy hoàn toàn 1 mol ankađien A cần 7 mol oxi. Công thức phân tử của A là
-
A.
C4H6
-
B.
C5H8
-
C.
C3H4
-
D.
C6H10
Đáp án : B
Ankadien có CTPT CnH2n-2
Phản ứng:
\(\begin{array}{l}{C_n}{H_{2n - 2}} + \dfrac{{3n - 1}}{2}{O_2} \to nC{O_2} + (n - 1){H_2}O\\ \to {n_{{O_2}}} = \dfrac{{3n - 1}}{2}{n_{ankadien}}\end{array}\)
Ankadien có CTPT CnH2n-2
Phản ứng:
\(\begin{array}{l}{C_n}{H_{2n - 2}} + \dfrac{{3n - 1}}{2}{O_2} \to nC{O_2} + (n - 1){H_2}O\\ \to {n_{{O_2}}} = \dfrac{{3n - 1}}{2}{n_{ankadien}}\\7 = \dfrac{{3n - 1}}{2}.1 \to n = 5\end{array}\)
CTPT của A là C5H8
Mô hình thí nghiệm dùng để điều chế chất khí Z:

Phương trình hóa học nào sau đây phù hợp với mô hình trên?
-
A.
CaC2 + 2H2O → Ca(OH)2 + C2H2↑.
-
B.
Al4C3 + 12HCl → 4AlCl3 + 3CH4↑.
-
C.
H2SO4 đặc + Na2SO3 rắn SO2↑ + Na2SO4 + H2O.
-
D.
CH3COONa rắn + NaOH rắn CH4↑ + Na2CO3.
Đáp án : B
Thu khí Z bằng cách đẩy nước nên khí Z phải hầu như không tan trong nước và không phản ứng với nước.
Thu khí Z bằng cách đẩy nước nên khí Z phải hầu như không tan trong nước và không phản ứng với nước.
A loại vì CaC2 tác dụng với H2O không cần nhiệt độ, H2O không được gọi là dung dịch
B phù hợp
C loại vì SO2 là khí độc không thu bằng cách đẩy nước
D loại vì chất tham gia đều là chất rắn còn mô hình thí nghiệm là chất rắn tác dụng với chất lỏng
Phản ứng đặc trưng của hiđrocacbon no là :
-
A.
Phản ứng tách.
-
B.
Phản ứng thế.
-
C.
Phản ứng cộng.
-
D.
Cả A, B và C.
Đáp án : B
Xem lại lí thuyết phản ứng halogen hóa của ankan
Phản ứng đặc trưng của hiđrocacbon no là phản ứng thế
Hiđro hóa hoàn toàn buta-1,3-đien, thu được:
-
A.
butan
-
B.
isobutan
-
C.
isopentan
-
D.
pentan
Đáp án : A
\({H_2}C = CH - CH = C{H_2} + 2{H_2}\underrightarrow {{t^0},xt}{H_3}C - C{H_2} - C{H_2} - C{H_3}\)
Sản phẩm là butan.
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1:1), số dẫn xuất monoclo tối đa sinh ra là
-
A.
3
-
B.
4
-
C.
5
-
D.
2
Đáp án : D
Từ đặc điểm cấu tạo của X và tỉ lệ thể tích X và CO2 để xác định được công thức cấu tạo của X.
Từ công thức cấu tạo của X ta xác định được số dẫn xuất monoclo tối đa sinh ra khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1:1).
X là hiđrocacbon mạch hở chỉ chứa liên kết σ => X là ankan
Mà đốt 1 thể tích X thu được 6 thể tích CO2 nên phân tử X có chứa 6 nguyên tử C => C6H14
Mà X có chứa 2 nguyên tử C bậc 3 => CH3-CH(CH3)-CH(CH3)-CH3
Các vị trí nguyên tử Cl có thể thế vào:
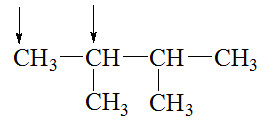
Vậy có tối đa 2 dẫn xuất monoclo được sinh ra.
Cho 2,4 gam hỗn hợp C2H2, C3H8, C2H6, C4H6 và H2 đi qua bột Ni nung nóng, sau một thời gian thu được hỗn hợp khí X. Đốt cháy hoàn toàn X cần vừa đủ V lít khí O2 (đktc), thu được 3,36 lít CO2 (đktc). Gía trị của V là
-
A.
6,72.
-
B.
10,08.
-
C.
7,84.
-
D.
8,96.
Đáp án : A
+) BTNT C: nC =nCO2
+) mhh= mC + mH => mH => nH
+) BTNT H: nH2O = nH : 2
+) BTNT O: 2n O2 = 2nCO2 + nH2O => VO2
BTNT C: nC =nCO2 = 0,15 mol => mC = 1,8 gam
mhh= mC + mH => mH = 2,4 – 1,8 = 0,6 gam => nH = 0,6 mol
BTNT H: nH2O = nH : 2 = 0,3 mol
BTNT O: 2n O2 = 2nCO2 + nH2O = 0,15. 2 + 0,3 = 0,6 mol
=> nO2 = 0,3 mol => VO2 = 6,72 lít
Crackinh 1 ankan A thu được hỗn hợp sản phẩm B gồm 5 hiđrocacbon có khối lượng mol trung bình là 36,25 gam/mol, hiệu suất phản ứng là 60%. Công thức phân tử của A là :
-
A.
C4H10.
-
B.
C5H12.
-
C.
C3H8.
-
D.
C2H6.
Đáp án : A
+) nankan phản ứng = nkhí tăng
+) nhh B = nA + nkhí tăng
+) bảo toàn khối lượng ta có :${{m}_{A}}=\text{ }{{m}_{B}}~<=>{{n}_{A}}.{{M}_{A}}=\text{ }{{n}_{B}}.{{\overline{M}}_{B}}\,\,=>\,\,{{M}_{A}}=\frac{{{\text{n}}_{B}}{{\overline{M}}_{B}}}{{{\text{n}}_{A}}}$
Giả nankan ban đầu = 1 mol
H = 60% => nankan phản ứng = 0,6 mol => nkhí tăng = 0,6 mol
=> nhh B = nA + nkhí tăng = 1 + 0,6 = 1,6 mol
Áp dụng định luật bảo toàn khối lượng ta có :
${{m}_{A}}=\text{ }{{m}_{B}}~<=>{{n}_{A}}.{{M}_{A}}=\text{ }{{n}_{B}}.{{\overline{M}}_{B}}\,\,=>\,\,{{M}_{A}}=\frac{{{\text{n}}_{B}}{{\overline{M}}_{B}}}{{{\text{n}}_{A}}}=\frac{1,6.36,25}{1}=58\,\,gam/mol$
Vậy CTPT của ankan A là C4H10
Khi đốt cháy hoàn toàn một hiđrocacbon A thu được 1,12 lít CO2 (đktc) và 1,08 gam H2O. A có phân tử khối là 72 và khi cho tác dụng với clo (có askt) thì thu được bốn dẫn xuất monocle. A có tên gọi là:
-
A.
isopentan
-
B.
2, 2-đimetylpropan
-
C.
neopentan
-
D.
pentan
Đáp án : A
+) Bảo toàn khối lượng cho A: mA = mC +mH
=> nA
+) Từ số mol của A, CO2 và H2O => CTPT của A
+) Từ các CTCT của A, xét CTCT có khả năng tạo 4 dẫn xuất monoclo
nCO2 = 0,05 mol
nH2O = 0,06 mol
Bảo toàn khối lượng cho A ta có:
mA = mC +mH =0,05*12+0,06*2=0,72 gam
=> nA = 0,01 mol
${C_x}{H_y} + (x + \dfrac{y}{4}){O_2} \to xC{O_2} + \dfrac{y}{2}{H_2}O$
0,01 0,05 0,06
=> x = 0,05/0,01 = 5
=> y = 0,06 . 2/0,01 = 12
Vậy CTPT của A là: C5H12
Do A tác dụng với clo thu được bốn dẫn xuất monoclo nên A là: CH3-CH(CH3)-CH2-CH3 (isopentan)
Hỗn hợp X gồm 2 anken kế tiếp nhau trong dãy đồng đẳng. Trộn một thể tích hỗn hợp X với một lượng vừa đủ khí oxi để được một hỗn hợp Y rồi đen đốt cháy hoàn toàn thì thu được sản phẩm khí và hơi Z. Tỉ khối của Y so với Z là 744 : 713. Các thể tích khí đo ở cùng điều kiện nhiệt độ, áp suất. Công thức phân tử của 2 anken là
-
A.
C5H10 và C6H12.
-
B.
C3H6 và C2H4.
-
C.
C4H8 và C5H10.
-
D.
C3H6 và C4H8.
Đáp án : B
CnH2n + 1,5nO2 → nCO2 + nH2O
1 mol → 1,5n → n → n
Y gồm 1 mol CnH2n và 1,5n mol O2
Z gồm CO2 (n mol) và H2O (n mol)
dY/Z = MY / MZ
Gọi công thức phân tử chung cho 2 anken là CnH2n có 1 mol
CnH2n + 1,5nO2 → nCO2 + nH2O
1 mol → 1,5n → n → n
Y gồm 1 mol CnH2n và 1,5n mol O2
Z gồm CO2 (n mol) và H2O (n mol)
${d_{Y/Z}} = {\rm{ }}\frac{{\frac{{1.14n{\rm{ }} + {\rm{ }}1,5n.32}}{{1 + 1,5n}}}}{{\frac{{44n{\rm{ }} + {\rm{ }}18n}}{{n + n}}}} = \frac{{744}}{{713}}\,\, = > \,\,n = 2,4$
=> 2 anken là C2H4 và C3H6
Cho etan qua xúc tác (ở nhiệt độ cao) thu được một hỗn hợp X gồm etan, etilen, axetilen và H2. Tỷ khối của hỗn hợp X đối với etan là 0,4. Hãy cho biết nếu cho 0,4 mol hỗn hợp X qua dung dịch Br2 dư thì số mol Br2 đã phản ứng là bao nhiêu ?
-
A.
0,24 mol
-
B.
0,6 mol
-
C.
0,4 mol
-
D.
0,32 mol.
Đáp án : B
C2H6 → C2H4 + H2
p/ ứng (mol) a a a
C2H6 → C2H2 + H2
p/ ứng (mol) b b b
hỗn hợp X gồm C2H6 dư (0,4-a-b) mol
C2H4 a mol; C2H2 b mol; H2 (a+b) mol
\(\begin{gathered}{d_{X/e\tan }} = 0,4 \to {M_X} = 12 \hfill \\\frac{{30}}{{0,4 + a + 2b}} = 12 \to a + 2b = 0,6 \hfill \\ \end{gathered} \)
C2H6 → C2H4 + H2
p/ ứng (mol) a a a
C2H6 → C2H2 + H2
p/ ứng (mol) b b b
hỗn hợp X gồm C2H6 dư (0,4-a-b) mol
C2H4 a mol; C2H2 b mol; H2 (a+b) mol
Ta có:
\(\begin{gathered}{d_{X/e\tan }} = 0,4 \to {M_X} = 12 \hfill \\ \frac{{30}}{{0,4 + a + 2b}} = 12 \to a + 2b = 0,6(mol) \hfill \\ {n_{B{r_2}}} = {n_{{C_2}{H_4}}} + 2{n_{{C_2}{H_2}}} = a + 2b = 0,6(mol) \hfill \\ \end{gathered} \)
Đốt cháy hoàn toàn m gam ankin X thu được m gam nước. Công thức phân tử của X là
-
A.
C2H2.
-
B.
C3H4.
-
C.
C4H6.
-
D.
C5H8.
Đáp án : C
+) Bảo toàn khối lượng: mankin X = mC + mH
+) nC = nCO2
+) nC : nH = 2m/27 : 2m/18
nH2O = m / 18
Bảo toàn khối lượng: mankin X = mC + mH => mC = m – 2.m/18 = 8m/9
=> nC = nCO2 = 2m/27
=> nC : nH = 2m/27 : 2m/18 = 2 : 3
=> CTĐGN của X là C2H3 => CTPT của X là C4H6
Dẫn 11,2 lít hỗn hợp khí X gồm axetilen và propin vào dung dịch AgNO3/NH3 dư (các phản ứng xảy ra hoàn toàn), sau phản ứng thu được 92,1 gam kết tủa. Phần trăm số mol axetilen trong X là
-
A.
70%.
-
B.
30%.
-
C.
60%.
-
D.
40%.
Đáp án : D
nkết tủa = nankin
Gọi nC2H2 = x mol; nC3H4 = y mol
=> x + y = 0,5 (1)
nkết tủa = nankin => nAg2C2 = x mol; nC3H3Ag = y mol
=> 240x + 147y = 92,1 (2)
Từ (1) và (2) => x = 0,2; y = 0,3
=> %nC2H2 = 40%
Đốt cháy hết 9,18 gam 2 đồng đẳng của benzen A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là :
-
A.
15,654.
-
B.
15,465.
-
C.
15,546.
-
D.
15,456.
Đáp án : D
$ + ){m_H} = 2.{n_{{H_2}O}}$
$ + ){m_C} = {m_{hi{\text{dr}}oc{\text{a}}cbon}} - {m_H}$
Đặt công thức phân tử trung bình của A và B là: ${C_{\overline n }}{H_{2\overline n - 6}}$
${n_{{H_2}O}} = \frac{{8,1}}{{18}} = 0,45\,\,mol \Rightarrow {m_H} = 0,45.2\,\, = 0,9\,\,gam$
$\Rightarrow {m_C} = 9,18 - 0,9 = 8,28\,\,gam \Rightarrow {n_{C{O_2}}} = {n_C} = \frac{{8,28}}{{12}} = 0,69\,\,mol.$
Vậy thể tích CO2 thu được là : 0,69.22,4=15,456 lít.
Tiến hành trùng hợp 10,4 gam stiren được hỗn hợp X gồm polistiren và stiren dư. Cho X tác dụng với 200 ml dung dịch Br2 0,15M, sau đó cho dung dịch KI dư vào thấy xuất hiện 1,27 gam iot. Hiệu suất trùng hợp stiren là
-
A.
60%
-
B.
75%
-
C.
80%
-
D.
83,33%
Đáp án : B
n stiren = 0,1 mol
n I2 = 0,005 mol
=> n Br2 dư => n Br2 phản ứng (cộng với stiren) => n stiren dư => H%
Ta có: n stiren = 0,1 mol
n I2 = 1,27/254 = 0,005 mol
=> n Br2 dư = 0,005 mol
=> n Br2 phản ứng (cộng với stiren)= 0,2. 0,15 - 0,005 = 0,025mol
=> n stiren dư = 0,025
=> Hiệu suất = (0,1-0,025) / 0,1= 75%
Cho 18,4 gam X gồm glixerol và một ancol no đơn chức Y tác dụng với Na dư thu được 5,6 lít khí hiđro (đktc). Lượng hiđro do Y sinh ra bằng 2/3 lượng hiđro do glixerol sinh ra. Công thức phân tử của Y là
-
A.
CH3OH
-
B.
C2H5OH
-
C.
C3H7OH
-
D.
C4H9OH
Đáp án : B
Sơ đồ phản ứng
C3H5(OH)3 $\xrightarrow{{ + Na}}$ H2
a mol 1,5a mol
ROH $\xrightarrow{{ + Na}}$ H2
b mol 0,5b mol
+) nH= 1,5.nC3H5(OH)3 + 0,5.nROH
Sơ đồ phản ứng
C3H5(OH)3 $\xrightarrow{{ + Na}}$ H2
a mol 1,5a mol
ROH $\xrightarrow{{ + Na}}$ H2
b mol 0,5b mol
+) nH= 1,5.nC3H5(OH)3 + 0,5.nROH
Ta có phương trình : nH= 1,5a + 0,5b =$\frac{{5,6}}{{22,4}}$ = 0,25 (1) và 0,5b =$\frac{2}{3}$ .1,5a (2)
Từ (1) và (2) suy ra a = 0,1 ; b = 0,2 mol
mX = 0,1 . 92 + 0,2 . (R + 17) = 18,4 => R = 29 (C2H5). Vậy ancol Y là C2H5OH
Đun ancol X đơn chức với H2SO4 đặc thu được hợp chất hữu cơ Y có dY/ X = 1,75. Công thức phân tử của X là
-
A.
C3H5OH
-
B.
C3H7OH
-
C.
C4H7OH
-
D.
C4H9OH
Đáp án : C
+) dY/ X = 1,5 > 1 nên Y là ete
+) dY/ X = $\frac{{2R + 16}}{{R + 17}}$ = 1,75 => R = 55 (C4H7)
Vì dY/ X = 1,75 > 1 nên Y là ete
Ta có sơ đồ : 2ROH $\xrightarrow{{{H_2}S{O_4}\,\,đặc,\,\,{t^o}}}$ ROR
dY/ X = $\frac{{2R + 16}}{{R + 17}}$ = 1,75 => R = 55 (C4H7). Vậy công thức phân tử của X là C4H7OH
Chất nào sau đây có nhiệt độ sôi thấp nhất ?
-
A.
axetanđehit
-
B.
metan
-
C.
phenol
-
D.
propan-1-ol
Đáp án : B
Chất có nhiệt độ sôi thấp nhất là metan.
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ A thu được 0,4 mol CO2 và 0,4 mol H2O. Biết A chỉ chứa một loại nhóm chức và 0,05 mol A tham gia phản ứng tráng gương thì tạo ra 0,1 mol Ag. Công thức cấu tạo thu gọn của A là
-
A.
C3H7CHO.
-
B.
CH3CHO.
-
C.
C2H5CHO.
-
D.
C2H3CHO.
Đáp án : A
Bảo toàn nguyên tố, bảo toàn khối lượng.
BTNT C, H: nC = nCO2 = 0,4 mol; nH = 2nH2O = 0,8 mol
BTKL: mO(A) = mA - mC - mH = 7,2 - 0,4.(12+2) = 1,6 gam
=> nO = 0,1 mol
=> nC : nH : nO = 4 : 8 : 1. Mà nAg : nA = 2 : 1 => Phân tử A có chứa 1 nhóm -CHO
=> A có CTPT C4H8O, CTCT là C3H7CHO
Hợp chất A chứa C, H, O có M < 90 đvC. A tham gia phản ứng tráng bạc và có thể tác dụng với H2 (xt Ni) sinh ra ancol chứa C bậc IV trong phân tử. Công thức của A là
-
A.
(CH3)2CHCHO.
-
B.
(CH3)2CH-CH2CHO.
-
C.
(CH3)3C-CH2CHO.
-
D.
(CH3)3CCHO.
Đáp án : D
Xem lại lí thuyết phản ứng oxi hóa hoàn toàn anđehit
A có khả năng tráng bạc => A chứa gốc –CHO
Ancol chứa C bậc IV => có dạng (CH3)3C-R-CHO
Vì M < 90 => 57 + R + 29 < 90 => R = 0
=> A là (CH3)3CCHO.
Hỗn hợp X gồm axit HCOOH và axit CH3COOH (tỉ lệ mol 1:1). Lấy 5,3 gam hỗn hợp X tác dụng với 5,75 gam C2H5OH (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất của các phản ứng este hoá đều bằng 80%). Giá trị của m là
-
A.
10,12 g
-
B.
6,48 g
-
C.
8,10 g
-
D.
16,20 g
Đáp án : B
+) Vì số mol ancol lớn hơn số mol axit nên ancol dư.
+) Số mol ancol pư = số mol axit
Áp dụng định luật bảo toàn khối lượng : mancol + maxit = meste + mnước
Vì số mol ancol lớn hơn số mol 2 axit nên ancol dư.
Số mol ancol pư = số mol 2 axit = 0,1 mol. áp dụng định luật bảo toàn khối lượng có
mancol + maxit = meste + mnước => 0,1.46 + 5,3 = meste + 0,1.18 => meste = 8,10 gam
H = 80% nên meste thu được = $\frac{{8,10.80}}{{100}}$= 6,48 gam.
Dẫn V lít (ở đktc) hỗn hợp X gồm axetilen và hiđro có khối lượng là m gam đi qua ống sứ đựng bột niken nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z được 2,24 lít khí CO2 (đktc) và 4,5 gam H2O. Tính giá trị của m.
-
A.
5,6 gam
-
B.
5,4 gam
-
C.
5,8 gam
-
D.
6,2 gam
Đáp án : C
\(X\xrightarrow{{Ni}}\left\{ \begin{gathered}\xrightarrow{{AgN{O_3}/N{H_3}}}{C_2}{H_2}:0,05\,\,mol \hfill \\\xrightarrow{{B{r_2}}}{C_2}{H_4}:0,1\,\,mol \hfill \\ \to Z\left\{ \begin{gathered}{H_2} \hfill \\{C_2}{H_6} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}{H_2}O:0,25 \hfill \\C{O_2}:0,1 \hfill \\ \end{gathered} \right.\xrightarrow{{BTNT\,:H + C}}\left\{ \begin{gathered}{H_2}:0,1 \hfill \\ {C_2}{H_6}:0,05 \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \right.\)
Giải bài toán theo sơ đồ sau:
\(X\xrightarrow{{Ni}}\left\{ \begin{gathered}\xrightarrow{{AgN{O_3}/N{H_3}}}{C_2}{H_2}:0,05\,\,mol \hfill \\\xrightarrow{{B{r_2}}}{C_2}{H_4}:0,1\,\,mol \hfill \\\to Z\left\{ \begin{gathered}{H_2} \hfill \\ {C_2}{H_6} \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}{H_2}O:0,25 \hfill \\C{O_2}:0,1 \hfill \\\end{gathered} \right.\xrightarrow{{BTNT\,:H + C}}\left\{ \begin{gathered}{H_2}:0,1 \hfill \\{C_2}{H_6}:0,05 \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \right.\)
BTKL: \({m_X} = {m_{{C_2}{H_2}}} + {m_{{C_2}{H_4}}} + {m_{{C_2}{H_6}}} + {m_{{H_2}}} = 5,8gam\)
Hiđro hóa hoàn toàn m gam hỗn hợp X gồm 2 anđehit mạch hở, thu được hỗn hợp Y. Cho Y vào bình đựng Na (dư 25% so với lượng phản ứng), thu được 11,2 lít H2 (đktc) và hỗn hợp rắn Z. Đốt cháy hoàn toàn Z thu được Na2CO3, H2O và 16,5 gam CO2. Mặt khác, cho 0,3 mol X tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được a gam kết tủa. Giá trị của a là
-
A.
86,4.
-
B.
97,2.
-
C.
108,0.
-
D.
129,6.
Đáp án : D
+) Từ nH2 => nNa phản ứng => nNa dư
+) ∑nNa ban đầu = nNa phản ứng + nNa dư
+) Bảo toàn Na => ${n_{N{a_2}C{O_3}}} = \dfrac{{{n_{Na\,ban{\text{đ}}ầu}}}}{2}$
+) Bảo toàn C => ${n_C} = {n_{N{a_2}C{O_3}}} + {n_{C{O_2}}}$
Y có dạng: R(OH)a ($\dfrac{1}{a}$ mol) => số C trong Y
+) Biện các ancol trong Y => anđehit trong Z
nH2 = 0,5 mol => nNa phản ứng = 1 mol
=> nNa dư = 0,25 mol
=> ∑nNa ban đầu = 1 + 0,25 = 1,25 mol
Bảo toàn Na => ${n_{N{a_2}C{O_3}}} = \dfrac{{{n_{Na\,ban{\text{đ}}ầu}}}}{2} = 0,625{\text{ }}mol$
Bảo toàn C => ${n_C} = {n_{N{a_2}C{O_3}}} + {n_{C{O_2}}} = 1$
Y có dạng: R(OH)a (($\dfrac{1}{a}$ mol)
=> số C $ = \dfrac{{{n_C}}}{{{n_Y}}} = \dfrac{1}{{\dfrac{1}{a}}} = a$
Vậy Y chứa các ancol có số C = số mol OH
Mặt khác, Y tạo ra từ anđehit nên các ancol đều bậc 1
=> CH3OH và C2H4(OH)2
=> X gồm HCHO và (CHO)2
=> nAg = 4.nX = 1,2
=> mAg = 129,6
M là hỗn hợp gồm 3 ancol đơn chức X, Y, Z có số nguyên tử cacbon liên tiếp nhau, đều mạch hở (MX < MY < MZ); X và Y no, Z không no (có 1 liên kết đôi C=C). Chia M thành 3 phần bằng nhau.
- Đốt cháy hoàn toàn phần 1 thu được 45,024 lít khí CO2 (đktc) và 46,44 gam H2O
- Phần 2 làm mất màu vừa đủ dung dịch chứa 16 gam Br2
- Đun nóng phần 3 với H2SO4 đặc ở 140oC thu được 18,752 gam hỗn hợp 6 ete (T). Đốt cháy hoàn toàn T thu được 1,106 mol CO2 và 1,252 mol H2O.
Hiệu suất tạo ete của X, Y, Z lần lượt là
-
A.
50%; 40%; 35%.
-
B.
50%; 60%; 40%.
-
C.
60%; 40%; 35%.
-
D.
60%; 50%; 35%.
Đáp án : B
Vì Z chứa 1 liên kết đôi => đốt cháy Z thu được ${n_{{H_2}O}} = {n_{C{O_2}}}$
=> ${n_X} + {n_Y} = {n_{{H_2}O}}-{n_{C{O_2}}}$
+) ${n_Z} = {n_{B{r_2}}}$
+) Tính số C trung bình của hỗn hợp M => các ancol trong M
Đặt x, y, z là số mol X, Y, Z đã phản ứng
=> ${n_{ete}} = {n_{{H_2}O}} = \dfrac{{{n_{ancol{\text{ }}pư}}}}{2} = \dfrac{{x + y + z}}{2}$
+) Bảo toàn khối lượng: mX + mY + mZ = mete + mH2O => PT (1)
+) Từ số mol CO2 khi đốt T => PT (2)
+) Từ số mol H2O khi đốt T => PT (3)
(1), (2), (3) => x; y; z => hiệu suất
Đốt phần 1 thu được: ${n_{C{O_2}}} = 2,01{\text{ }}mol$ và ${n_{{H_2}O}} = 2,58{\text{ }}mol$
Vì Z chứa 1 liên kết đôi => đốt cháy Z thu được ${n_{{H_2}O}} = {n_{C{O_2}}}$
=> ${n_X} + {n_Y} = {n_{{H_2}O}}-{n_{C{O_2}}} = 0,57$
${n_Z} = {n_{B{r_2}}} = 0,1$
=> nM = 0,67 => số C = 3
Vậy M chứa:
X là C2H5OH: 0,1 mol
Y là C3H7OH: 0,47 mol
Z là C4H7OH: 0,1 mol
(số C = 3 nên nX = nZ)
Đặt x, y, z là số mol X, Y, Z đã phản ứng
=> ${n_{ete}} = {n_{{H_2}O}} = \dfrac{{{n_{ancol{\text{ }}pư}}}}{2} = \dfrac{{x + y + z}}{2}$
Bảo toàn khối lượng: mX + mY + mZ = mete + mH2O
=> 46x + 60y + 72z = 18,752 + 18.(x+y+z)/2 (1)
Đốt T thu được:
${n_{C{O_2}}} = 2x + 3y + 4z = 1,106\,\left( 2 \right)$
${n_{{H_2}O}} = 3x + 4y + 4z-\dfrac{{x + y + z}}{2} = 1,252\,\left( 3 \right)$
Giải hệ (1), (2), (3) => x = 0,05; y = 0,282; z = 0,04
=> H(X) = 50%; H(Y) = 60%; H(Z) = 40%
Các bài khác cùng chuyên mục
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1

















