Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
Đề bài
Không thể điều chế CH4 bằng phản ứng nào ?
-
A.
Nung muối natri malonat với vôi tôi xút
-
B.
Canxi cacbua tác dụng với nước
-
C.
Nung natri axetat với vôi tôi xút
-
D.
Điện phân dung dịch natri axetat
Cho các chất sau: pentan; hex-1-en, etilen, metan, propen, isobutan. Số các chất làm mất màu dung dịch KMnO4 ở ngay điều kiện thường là
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
1
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
-
A.
có kết tủa xanh.
-
B.
có kết tủa nâu đen.
-
C.
có kết tủa trắng.
-
D.
có kết tủa vàng.
Hợp chất C5H10 có bao nhiêu đồng phân anken?
-
A.
4.
-
B.
5.
-
C.
6.
-
D.
7.
Các ankan không tham gia loại phản ứng nào ?
-
A.
Phản ứng thế.
-
B.
Phản ứng cộng.
-
C.
Phản ứng tách.
-
D.
Phản ứng cháy.
Áp dụng quy tắc Mac-cốp-nhi-cốp vào trường hợp nào sau đây ?
-
A.
Phản ứng cộng của Br2 với anken đối xứng.
-
B.
Phản ứng cộng của HX vào anken đối xứng.
-
C.
Phản ứng trùng hợp của anken.
-
D.
Phản ứng cộng của HX vào anken bất đối xứng.
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
-
A.
anken.
-
B.
ankan.
-
C.
ankan và xicloankan.
-
D.
ankin.
Hợp chất hexa-2,4-đien có bao nhiêu đồng phân hình học ?
-
A.
2.
-
B.
5.
-
C.
4.
-
D.
3.
Công thức phân tử tổng quát của ankin là
-
A.
CnH2n-2 (n ≥ 3).
-
B.
CnH2n-2 (n ≥ 2).
-
C.
CnH2n-6 (n ≥ 4).
-
D.
CnH2n (n ≥ 2).
Cho propin qua nước có HgSO4 ở 80oC tạo ra sản phẩm là
-
A.
CH3–C(OH)=CH2.
-
B.
CH3–C(=O)–CH3.
-
C.
CH3–CH2–CHO.
-
D.
Sản phẩm khác.
Công thức tổng quát của anken là
-
A.
CnH2n (n ≥ 2).
-
B.
CnH2n+2 (n ≥ 1).
-
C.
CnH2n-2 (n ≥ 2).
-
D.
CnH2n (n ≥ 1)
$A{l_4}{C_3} + {\text{ }}{H_2}O \to X + {\text{ }}Al{\left( {OH} \right)_3}$. X là
-
A.
CH4
-
B.
C2H6
-
C.
C3H8
-
D.
C3H6
Trùng hợp but-2-en, sản phẩm thu được có cấu tạo là
-
A.
(-CH2-CH2-CH2-CH2-)n.
-
B.
[-CH(CH3)-CH(CH3)-]n.
-
C.
[-CH(CH3)=CH(CH3)-]n.
-
D.
[-CH2-CH(C2H5)-]n.
Phần trăm khối lượng cacbon trong phân tử ankan Y bằng 83,33%. Công thức phân tử của Y là :
-
A.
C2H6.
-
B.
C3H8.
-
C.
C4H10.
-
D.
C5H12.
Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C5H12 ?
-
A.
3 đồng phân.
-
B.
4 đồng phân.
-
C.
5 đồng phân.
-
D.
6 đồng phân.
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là :
-
A.
3.
-
B.
4.
-
C.
2.
-
D.
5.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai hiđrocacbon thuộc cùng dãy đồng đẳng cần dùng 6,16 lít O2 và thu được 3,36 lít CO2 (các thể tích khí đo ở đktc). Giá trị của m là
-
A.
2,3 gam.
-
B.
23 gam.
-
C.
3,2 gam.
-
D.
32 gam.
Khi crackinh hoàn toàn một ankan X thu được hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 29. Công thức phân tử của X là:
-
A.
C6H14.
-
B.
C3H8.
-
C.
C4H10.
-
D.
C5H12
X là anken trong phân tử có 3 nguyên tử cacbon no. Số công thức cấu tạo của X là
-
A.
3.
-
B.
4.
-
C.
6.
-
D.
5.
Cho hỗn hợp X gồm etilen và H2 có tỉ khối so với H2 bằng 4,25. Dẫn X qua bột niken nung nóng (hiệu suất phản ứng 75%) thu được hỗn hợp Y. Tỉ khối của Y so với H2 (các thể tích đo ở cùng điều kiện) là
-
A.
5,23.
-
B.
9,71.
-
C.
5,35.
-
D.
10,46.
Anken thích hợp để điều chế ancol (CH3CH2)3C-OH là
-
A.
3-etylpent-2-en.
-
B.
3-etylpent-3-en.
-
C.
3-etylpent-1-en.
-
D.
3,3- đimetylpent-1-en.
Đime hóa 6,72 lít axetilen (nhiệt độ, xúc tác cần thiết) thu được 4,48 lít hỗn hợp X gồm axetilen và vinyl axetilen. Cho toàn bộ X qua dung dịch AgNO3 trong NH3 dư thu được m gam kết tủa. Các thể tích đo ở đktc. Giá trị m là
-
A.
24,0.
-
B.
39,9
-
C.
72,0
-
D.
15,9
Phân biệt các chất metan, etilen, axetilen bằng phương pháp hóa học, ta dùng
-
A.
dd AgNO3/NH3 và nước brom.
-
B.
dung dịch AgNO3/NH3
-
C.
dd NaOH.
-
D.
dd KMnO4
Trong bình kín (ở 210oC) đựng hỗn hợp A (gồm 2 ankin X và Y là đồng đẳng liên tiếp, MX < MY). Thêm một lượng không khí vừa đủ (khi đó áp suất trong bình đạt 0,81 atm) rồi bật tia lửa điện để đốt cháy hết X và Y rồi đưa bình về 210oC, thấy áp suất trong bình = 0,836 atm. Biết trong không khí chứa 80% thể tích N2, còn lại là O2. CTPT của Y là
-
A.
C2H2
-
B.
C3H4
-
C.
C6H10
-
D.
C4H6
Cho 0,448 lít (đktc) một anken ở thể khí vào một bình kín dung tích 11,2 lít chứa sẵn 11,52 gam không khí (M = 28,8). Đốt cháy hoàn toàn hỗn hợp trong bình, sau phản ứng giữ bình ở nhiệt độ 136oC, áp suất bình đo được là 1,26 atm. Biết rằng sau phản ứng cháy còn dư oxi. Công thức của anken là
-
A.
C3H6.
-
B.
C4H8.
-
C.
C2H4.
-
D.
C5H10.
Lời giải và đáp án
Không thể điều chế CH4 bằng phản ứng nào ?
-
A.
Nung muối natri malonat với vôi tôi xút
-
B.
Canxi cacbua tác dụng với nước
-
C.
Nung natri axetat với vôi tôi xút
-
D.
Điện phân dung dịch natri axetat
Đáp án : B
Không thể điều chế CH4 bằng phản ứng canxicacbua tác dụng với nước vì
$Ca{C_2} + 2{H_2}O \to {C_2}{H_2} + Ca{(OH)_2}$
Cho các chất sau: pentan; hex-1-en, etilen, metan, propen, isobutan. Số các chất làm mất màu dung dịch KMnO4 ở ngay điều kiện thường là
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
1
Đáp án : B
Các anken phản ứng được với dung dịch KMnO4 ở ngay điều kiện thường
=> hex-1-en, etilen, propen
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
-
A.
có kết tủa xanh.
-
B.
có kết tủa nâu đen.
-
C.
có kết tủa trắng.
-
D.
có kết tủa vàng.
Đáp án : D
Cho axetilen vào dung dịch AgNO3 :
CH≡CH + 2AgNO3 + 2NH3 → CAg≡CAg ↓vàng nhạt + 2NH4NO3
=> phản ứng tạo kết tủa vàng nhạt
Hợp chất C5H10 có bao nhiêu đồng phân anken?
-
A.
4.
-
B.
5.
-
C.
6.
-
D.
7.
Đáp án : C
Xem lại lí thuyết anken
Số đồng phân anken bao gồm đồng phân cấu tạo và đồng phân hình học
Các đồng phân cấu tạo mạch hở của C5H10 là:
- CH2=CH-CH2-CH2-CH3
- CH3-CH=CH-CH2-CH3 (có đphh)
- CH2=CH(CH3)-CH2-CH3
- (CH3)2C=CH-CH3
- (CH3)2CH-CH=CH2
=> C5H10 có 6 đồng phân anken
Các ankan không tham gia loại phản ứng nào ?
-
A.
Phản ứng thế.
-
B.
Phản ứng cộng.
-
C.
Phản ứng tách.
-
D.
Phản ứng cháy.
Đáp án : B
Xem lại lí thuyết phản ứng halogen hóa của ankan
Các ankan không tham gia loại phản ứng cộng
Áp dụng quy tắc Mac-cốp-nhi-cốp vào trường hợp nào sau đây ?
-
A.
Phản ứng cộng của Br2 với anken đối xứng.
-
B.
Phản ứng cộng của HX vào anken đối xứng.
-
C.
Phản ứng trùng hợp của anken.
-
D.
Phản ứng cộng của HX vào anken bất đối xứng.
Đáp án : D
Quy tắc Mac-côp-nhi-côp được dùng trong phản ứng cộng HX và anken bất đối xứng (xem ưu tiên X vào C nào…)
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
-
A.
anken.
-
B.
ankan.
-
C.
ankan và xicloankan.
-
D.
ankin.
Đáp án : B
X thuộc dãy đồng đẳng của ankan.
Hợp chất hexa-2,4-đien có bao nhiêu đồng phân hình học ?
-
A.
2.
-
B.
5.
-
C.
4.
-
D.
3.
Đáp án : D
Xét các nhóm liên kết với mỗi cacbon ở vị trí liên kết đôi
Hexa-2,4-đien: CH3-CH=CH-CH=CH-CH3
Cả 2 nối đôi đều có đồng phân hình học và cấu tạo phân tử đối xứng => có 3 đồng phân là cis-cis; trans-trans và cis-trans
Công thức phân tử tổng quát của ankin là
-
A.
CnH2n-2 (n ≥ 3).
-
B.
CnH2n-2 (n ≥ 2).
-
C.
CnH2n-6 (n ≥ 4).
-
D.
CnH2n (n ≥ 2).
Đáp án : B
Công thức phân tử tổng quát của ankin là CnH2n-2 (n ≥ 2).
Cho propin qua nước có HgSO4 ở 80oC tạo ra sản phẩm là
-
A.
CH3–C(OH)=CH2.
-
B.
CH3–C(=O)–CH3.
-
C.
CH3–CH2–CHO.
-
D.
Sản phẩm khác.
Đáp án : B
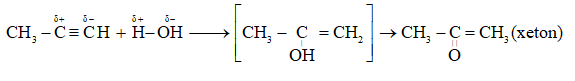
Công thức tổng quát của anken là
-
A.
CnH2n (n ≥ 2).
-
B.
CnH2n+2 (n ≥ 1).
-
C.
CnH2n-2 (n ≥ 2).
-
D.
CnH2n (n ≥ 1)
Đáp án : A
Công thức tổng quát của anken là CnH2n (n ≥ 2).
$A{l_4}{C_3} + {\text{ }}{H_2}O \to X + {\text{ }}Al{\left( {OH} \right)_3}$. X là
-
A.
CH4
-
B.
C2H6
-
C.
C3H8
-
D.
C3H6
Đáp án : A
$A{l_4}{C_3} + {\text{12}}{H_2}O \to 3C{H_4} + {\text{ 4}}Al{\left( {OH} \right)_3}$
Trùng hợp but-2-en, sản phẩm thu được có cấu tạo là
-
A.
(-CH2-CH2-CH2-CH2-)n.
-
B.
[-CH(CH3)-CH(CH3)-]n.
-
C.
[-CH(CH3)=CH(CH3)-]n.
-
D.
[-CH2-CH(C2H5)-]n.
Đáp án : B
Phương trình trùng hợp but-2-en: nCH3-CH=CH-CH3 → (-CH(CH3)-CH(CH2)-)n
Phần trăm khối lượng cacbon trong phân tử ankan Y bằng 83,33%. Công thức phân tử của Y là :
-
A.
C2H6.
-
B.
C3H8.
-
C.
C4H10.
-
D.
C5H12.
Đáp án : D
ankan Y : CnH2n+2
$\% {m_C} = \frac{{12n}}{{12n + 2n + 2}}.100\%$.
=> n => Công thức phân tử của Y
Gọi công thức phân tử của ankan Y có dạng CnH2n+2
$\% {m_C} = \frac{{12n}}{{12n + 2n + 2}}.100\% = 83,33\% \,\, = > \,\,n = 5$.
=> Công thức phân tử của Y là C5H12
Có bao nhiêu đồng phân cấu tạo có công thức phân tử là C5H12 ?
-
A.
3 đồng phân.
-
B.
4 đồng phân.
-
C.
5 đồng phân.
-
D.
6 đồng phân.
Đáp án : A
- Đồng phân mạch thẳng: C – C – C – C – C
- Đồng phân mạch nhánh:
+ cắt 1C:
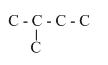
+ cắt 2C:
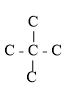
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2 (ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2 (theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là :
-
A.
3.
-
B.
4.
-
C.
2.
-
D.
5.
Đáp án : C
- Xác định số nguyên tử C trong X
Số C = \(\frac{{{n_{C{O_2}}}}}{{{n_X}}}\)
- Xác định CTPT của X
X chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử
=> X là ankan
=> số vị trí thế monoclo
- Đốt cháy 1 thể tích X sinh ra 6 thể tích CO2 => trong X có 6 nguyên tử C
- Vì X chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử
=> X là ankan C6H14 có công thức phân tử là (CH3)2 - CH – CH(CH3)2
=> có 2 vị trí thế monoclo
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai hiđrocacbon thuộc cùng dãy đồng đẳng cần dùng 6,16 lít O2 và thu được 3,36 lít CO2 (các thể tích khí đo ở đktc). Giá trị của m là
-
A.
2,3 gam.
-
B.
23 gam.
-
C.
3,2 gam.
-
D.
32 gam.
Đáp án : A
Bảo toàn nguyên tố O : $2.{{n}_{{{O}_{2}}}}=2.{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}$
Bảo toàn nguyên tố C và H : nC (trong X) = nCO2; nH (trong X) = 2.nH2O
Bảo toàn khối lượng : mX = mC (trong X) + mH (trong X)
nO2 = 0,275 mol ; nCO2 = 0,15 mol
Bảo toàn nguyên tố O : $2.{{n}_{{{O}_{2}}}}=2.{{n}_{C{{O}_{2}}}}+{{n}_{{{H}_{2}}O}}=>\,\,{{n}_{{{H}_{2}}O}}=2.{{n}_{{{O}_{2}}}}-2.{{n}_{C{{O}_{2}}}}=2.0,275-2.0,15=0,25mol$
Bảo toàn nguyên tố C và H : nC (trong X) = nCO2 = 0,15 mol ; nH (trong X) = 2.nH2O = 0,5 mol
Bảo toàn khối lượng : mX = mC (trong X) + mH (trong X) = 12.0,15 + 0,5 = 2,3 gam
Khi crackinh hoàn toàn một ankan X thu được hỗn hợp Y (các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất); tỉ khối của Y so với H2 bằng 29. Công thức phân tử của X là:
-
A.
C6H14.
-
B.
C3H8.
-
C.
C4H10.
-
D.
C5H12
Đáp án : A
Crackinh hoàn toàn thu được hỗn hợp Y, MY = 58 nên sẽ có 1 chất có M lớn hơn 58 và 1 chất có M nhỏ hơn.
Crackinh hoàn toàn thu được hỗn hợp Y, MY = 58 nên sẽ có 1 chất có M lớn hơn 58 và 1 chất có M nhỏ hơn.
Xét 4 đáp án chỉ có C6H14 mới tạo ra sản phẩm có M lớn hơn 58
(Nếu là C5H12 có M = 72, crackinh ra cả 2 sản phẩm đều có M nhỏ hơn hoặc bằng 58 => không thỏa mãn)
X là anken trong phân tử có 3 nguyên tử cacbon no. Số công thức cấu tạo của X là
-
A.
3.
-
B.
4.
-
C.
6.
-
D.
5.
Đáp án : D
Anken X có 3 nguyên tử C no và 2 nguyên tử C không no (2C ở nối đôi) => X là anken có 5C => X là C5H10
=> số công thức cấu tạo của X là 5
1. C=C-C-C-C
2. C-C=C-C-C
3. C=C(C)-C-C
4. (C)2C=C-C
5. (C)2C-C=C
Cho hỗn hợp X gồm etilen và H2 có tỉ khối so với H2 bằng 4,25. Dẫn X qua bột niken nung nóng (hiệu suất phản ứng 75%) thu được hỗn hợp Y. Tỉ khối của Y so với H2 (các thể tích đo ở cùng điều kiện) là
-
A.
5,23.
-
B.
9,71.
-
C.
5,35.
-
D.
10,46.
Đáp án : A
+) Giả sử lấy 1 mol hỗn hợp X. Gọi nC2H4 = x mol; nH2 = y mol => PT(1)
+) \({\bar M_X} = \frac{{28x + 2y}}{{x + y}} \) => PT(2)
+) hiệu suất phản ứng tính theo chất hết (khi coi H = 100%)
+) nC2H4 phản ứng = nhỗn hợp khí giảm => nY
+) Áp dụng công thức: \(\frac{{{{\bar M}_X}}}{{{{\bar M}_Y}}} = \frac{{{n_Y}}}{{{n_X}}}\,\, = > \,\,{\bar M_Y} = \frac{{{n_X}.{{\bar M}_X}}}{{{n_Y}}}\)
Giả sử lấy 1 mol hỗn hợp X. Gọi nC2H4 = x mol; nH2 = y mol
=> x + y = 1 (1)
\({\bar M_X} = \frac{{28x + 2y}}{{x + y}} = 4,25.2\) (2)
Từ (1) và (2) => x = 0,25 mol; y = 0,75 mol
C2H4 + H2 → C2H6
=> hiệu suất phản ứng tính theo C2H4
=> nC2H4 phản ứng = nhỗn hợp khí giảm = 0,25.0,75 = 0,1875 mol
=> nY = 1 – 0,1875 = 0,8125 mol
Áp dụng công thức: \(\frac{{{{\bar M}_X}}}{{{{\bar M}_Y}}} = \frac{{{n_Y}}}{{{n_X}}}\,\, = > \,\,{\bar M_Y} = \frac{{{n_X}.{{\bar M}_X}}}{{{n_Y}}} = \frac{{1.8,5}}{{0,8125}} = 10,46\,\, = > \,\,{d_{Y/{H_2}}} = 5,23\)
Anken thích hợp để điều chế ancol (CH3CH2)3C-OH là
-
A.
3-etylpent-2-en.
-
B.
3-etylpent-3-en.
-
C.
3-etylpent-1-en.
-
D.
3,3- đimetylpent-1-en.
Đáp án : A
+) Phản ứng của anken sinh ra ancol là phản ứng của anken với nước
+) Viết CTCT của ancol, vận dụng quy tắc Mac-cốp-nhi-cốp xác định anken ban đầu
Khi anken tác dụng vs nước thì sp tạo thành sẽ tuân theo quy tắc Mac-côp-nhi-côp
=> nhóm OH thế vào C bậc cao hơn, H sẽ thế vào C bậc thấp hơn.
Viết CTCT của sp, xác định được mạch chính chứa nhóm OH có 5C, mà nhóm OH đã thế vào C ở vị trí thứ 3 nên H sẽ thế vào C ở vị trí thứ 2. Vậy lk đôi ở vị trí thứ 2 => chất ban đầu là 3-etylpent-2-en.
Đime hóa 6,72 lít axetilen (nhiệt độ, xúc tác cần thiết) thu được 4,48 lít hỗn hợp X gồm axetilen và vinyl axetilen. Cho toàn bộ X qua dung dịch AgNO3 trong NH3 dư thu được m gam kết tủa. Các thể tích đo ở đktc. Giá trị m là
-
A.
24,0.
-
B.
39,9
-
C.
72,0
-
D.
15,9
Đáp án : B
+) Đặt số mol của C4H4 trong hỗn hợp X là x mol
+) Từ PT: 2CH ≡ CH → CH ≡ C – CH = CH2
=> tính số mol của C2H2 phản ứng => số mol C2H2 dư
${n_{{C_2}{H_2}}}\,\, = \,\,\frac{{6,72}}{{22,4}}\,\, = \,\,0,3\,\,mol$
Đặt số mol của C4H4 trong hỗn hợp X là x mol
2CH ≡ CH → CH ≡ C – CH = CH2
2x ← x
$\begin{array}{l}{n_{{C_2}{H_2}(X)}} = 0,3 - 2{\rm{x}}mol\\{n_X}= \frac{{4,48}}{{22,4}} = 0,2\,mol \to {n_{{C_2}{H_2}(X)}} + {n_{{C_4}{H_4}(X)}} = 0,2 \to 0,3 - 2{\rm{x}}+ x = 0,2 \to x =0,1\\ \to {n_{{C_2}{H_2}(X)}}= 0,3 - 2.0,1= 0,1\,mol;\,{n_{{C_4}{H_4}(X)}} = 0,1\,mol\end{array}$
CH ≡ CH → CAg ≡ CAg
0,1 → 0,1
CH ≡ C – CH = CH2 → CAg ≡ C – CH = CH2
0,1 → 0,1
m↓ = 0,1.240 + 0,1.159 = 39,9 gam
Phân biệt các chất metan, etilen, axetilen bằng phương pháp hóa học, ta dùng
-
A.
dd AgNO3/NH3 và nước brom.
-
B.
dung dịch AgNO3/NH3
-
C.
dd NaOH.
-
D.
dd KMnO4
Đáp án : A
|
|
Metan (CH4) |
Etilen (CH2 = CH2) |
Axetilen (CH º CH) |
|
AgNO3/NH3 |
x |
x |
↓ vàng |
|
dung dịch Br2 |
x |
mất màu |
|
Phương trình hóa học
CH≡CH + 2AgNO3 + 2NH3 → Ag–C≡C–Ag ↓(vàng) + 2NH4NO3
CH2=CH2 + Br2 → CH2Br–CH2Br
Trong bình kín (ở 210oC) đựng hỗn hợp A (gồm 2 ankin X và Y là đồng đẳng liên tiếp, MX < MY). Thêm một lượng không khí vừa đủ (khi đó áp suất trong bình đạt 0,81 atm) rồi bật tia lửa điện để đốt cháy hết X và Y rồi đưa bình về 210oC, thấy áp suất trong bình = 0,836 atm. Biết trong không khí chứa 80% thể tích N2, còn lại là O2. CTPT của Y là
-
A.
C2H2
-
B.
C3H4
-
C.
C6H10
-
D.
C4H6
Đáp án : C
+) Gọi nCO2 = a mol; nH2O = b mol
+) nankin = nCO2 – nH2O => nankin = a – b
+) Bảo toàn O: 2.nO2 = 2.nCO2 + nH2O
+) nhh trước pứ = nankin + nO2 + nN2
+) nhh sau phản ứng = nCO2 + nH2O + nN2
Từ công thức $pV = n.R.T{\rm{ }} = > \frac{{{p_t}}}{{{p_s}}} = \frac{{{n_t}}}{{{n_s}}}\,\,$
Ở 210oC, nước ở thể hơi => coi như là 1 khí gây áp suất trong bình
Vì lượng không khí dùng vừa đủ => hỗn hợp sau phản ứng gồm CO2, H2O và N2
Gọi nCO2 = a mol; nH2O = b mol
=> nankin = nCO2 – nH2O => nankin = a – b
Bảo toàn O: 2.nO2 = 2.nCO2 + nH2O => nO2 = a + 0,5b
Trong không khí: nN2 = 4.nO2 = 4a + 2b
=> nhh trước pứ = nankin + nO2 + nN2 = a – b + a + 0,5b + 4a + 2b = 6a + 1,5b
nhh sau phản ứng = nCO2 + nH2O + nN2 = a + b + 4a + 2b = 5a + 3b
Từ công thức $pV = n.R.T{\rm{ }} = > \frac{{{p_t}}}{{{p_s}}} = \frac{{{n_t}}}{{{n_s}}}\,\, = > \,\,\frac{{0,81}}{{0,836}} = \frac{{6a + 1,5b}}{{5a + 3b}}\,\, = > \,a = 1,21b$
=> nankin = a – b = 1,21b – b = 0,21b mol
=> số C trung bình = nCO2 / nankin = 1,21 / 0,21 = 5,76
=> 2 ankin X và Y là C5H8 và C6H10
Cho 0,448 lít (đktc) một anken ở thể khí vào một bình kín dung tích 11,2 lít chứa sẵn 11,52 gam không khí (M = 28,8). Đốt cháy hoàn toàn hỗn hợp trong bình, sau phản ứng giữ bình ở nhiệt độ 136oC, áp suất bình đo được là 1,26 atm. Biết rằng sau phản ứng cháy còn dư oxi. Công thức của anken là
-
A.
C3H6.
-
B.
C4H8.
-
C.
C2H4.
-
D.
C5H10.
Đáp án : C
+) Ở nhiệt độ 136oC, nước ở thể hơi.
+) nkhí sau phản ứng = PV / RT
CnH2n + 1,5nO2 → nCO2 + nH2O
+) hỗn hợp khí sau phản ứng gồm CO2 (0,02n mol); H2O (0,02n mol); N2 (0,32 mol); O2 dư (0,08 – 0,03n mol)
nanken = 0,02 mol; nkk = 0,4 mol => nN2 = 0,32 mol; nO2 = 0,08 mol
Ở nhiệt độ 136oC, nước ở thể hơi.
nkhí sau phản ứng = PV / RT = 1,26.11,2 / (0,082.409) = 0,42 mol
CnH2n + 1,5nO2 → nCO2 + nH2O
0,02 → 0,03n → 0,02n → 0,02n
=> hỗn hợp khí sau phản ứng gồm CO2 (0,02n mol); H2O (0,02n mol); N2 (0,32 mol); O2 dư (0,08 – 0,03n mol)
=> 0,02n + 0,02n + 0,32 + 0,08 – 0,03n = 0,42 => n = 2
=> anken cần tìm là C2H4
Các bài khác cùng chuyên mục
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1

















