Bài 40.16* trang 64 SBT hóa học 11
Giải bài 40.16* trang 64 sách bài tập hóa học 11. Hỗn hợp khí A chứa 2 anken kế tiếp nhau trong dãy đồng đẳng...
Đề bài
Hỗn hợp khí A chứa 2 anken kế tiếp nhau trong dãy đồng đẳng. Tỉ khối của A đối với khí nitơ là 1,35.
1. Xác định công thức phân tử 2 anken.
2. Nếu hiđrat hoá một lượng hỗn hợp A (giả sử hiệu suất là 100%) thì được hỗn hợp ancol B, trong đó tỉ lệ về khối lượng giữa ancol bậc một và ancol bậc hai là 43 : 50.
Hãy cho biết tên và phần trăm về khối lượng của từng ancol trong hỗn hợp B.
Phương pháp giải - Xem chi tiết
1. Dựa vào tỉ khối hơi của A => Biểu diễn khối lượng mol 2 anken theo ẩn n (\( \Rightarrow \) CnH2n < 37,8 < Cn+1H2n+2) => n => CTPT 2 anken.
2. +) Giả sử trong 1 mol hỗn hợp A có x mol C3H6 và (1 - x) mol C2H4
+) Dựa vào dữ kiện "Tỉ khối của A đối với khí nitơ là 1,35" => x
+) Khi hiđrat hóa hoàn toàn 1 mol A:
CH2 = CH2 + H2O \( \to \) CH3 - CH2 - OH
0,3 mol 0,3 mol
CH3 - CH = CH2 + H2O\( \to \) CH3 - CH2 - CH2 - OH
a mol a mol
CH3 - CH = CH2 + H2O \( \to \) 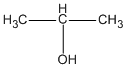
(0,7 - a) mol (0,7 - a) mol
+) Dựa vào dữ kiện "tỉ lệ về khối lượng giữa ancol bậc một và ancol bậc hai là 43 : 50" => a
+) Hỗn hợp B gồm CH3 - CH2 - OH ; CH3 - CH2 - CH2 - OH và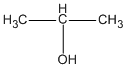
+) Tìm số mol từng chất trong B => phần trăm về khối lượng của chúng.
Lời giải chi tiết
1. Hỗn hợp khí A chứa CnH2n và Cn+1H2n+2 với phân tử khối trung bình là : 1,35.28 = 37,8
\( \Rightarrow \) CnH2n < 37,8 < Cn+1H2n+2
\( \Rightarrow \) 14n < 37,8 < 14n + 14
1,70 < n < 2,70 \( \Rightarrow \) n = 2.
CTPT của 2 anken là C2H4 và C3H6.
2. Giả sử trong 1 mol hỗn hợp A có x mol C3H6 và (1 - x) mol C2H4 :
42x + 28(1 - x) = 37,8 \( \Rightarrow \) x = 0,7
Như vậy, trong 1 mol hỗn hợp A có 0,7 mol C3H6 và 0,3 mol C2H4.
Giả sử hiđrat hoá hoàn toàn 1 mol A :
CH2 = CH2 + H2O \( \to \) CH3 - CH2 - OH
0,3 mol 0,3 mol
CH3 - CH = CH2 + H2O\( \to \) CH3 - CH2 - CH2 - OH
a mol a mol
CH3 - CH = CH2 + H2O \( \to \) 
(0,7 - a) mol (0,7 - a) mol
Tỉ lệ khối lượng giữa ancol bậc I so với ancol bậc II :
\(\dfrac{{46.0,3 + 60{\rm{a}}}}{{60(0,7 - a)}} = \dfrac{{43}}{{50}} \Rightarrow a = 0,2\)
Hỗn hợp B gồm 0,3 mol CH3 - CH2 - OH ; 0,2 mol CH3 - CH2 - CH2 - OH và 0,5 mol  ; có khối lượng tổng cộng là 55,8 g.
; có khối lượng tổng cộng là 55,8 g.
% về khối lượng etanol (ancol etylic) là : \(\dfrac{{0,3.46}}{{55,8}}.100\% = 24,7\% \)
% về khối lượng của propan-1-ol (ancol propylic) là : \(\dfrac{{0,2.60}}{{55,8}}.100\% = 21,5\% \)
Propan-2-ol (ancol isopropylic) chiếm : \(\dfrac{{0,5.60}}{{55,8}}.100\% = 53,8\% \)
Riêng câu 2 cũng có thể lập luận như sau :
Phần trăm khối lượng của ancol bậc II (ancol isopropylic) :
\(\dfrac{{50}}{{43 + 50}}.100\% = 53,8\% \)
Vậy phần trăm khối lượng của 2 ancol bậc I là 46,2%.
Nếu dùng 1 mol A (37,8 g) thì lượng H2O là 1 mol (18 g) và khối lượng hỗn hợp B là 37,8 + 18, = 55,8 (g), trong đó 0,3 mol C2H4 tạo ra 0,3 mol ancol etylic.
Phần trăm khối lượng của ancol etylic là \(\dfrac{{0,3.46}}{{55,8}}.100\% = 24,7\% \) và của ancol propylic là 46,2% - 24,7% = 21,5%.
Loigiaihay.com













Danh sách bình luận