Trắc nghiệm Bài 24. Tính chất của oxi - Hóa học 8
Đề bài
Trong các câu sau, câu nào sai?
-
A.
Oxygen nặng hơn không khí.
-
B.
Oxygen là chất khí không màu, không mùi, không vị.
-
C.
Oxygen tan nhiều trong nước.
-
D.
Oxygen chiếm 1/5 thể tích không khí.
Chất rắn màu vàng cháy trong bình đựng khí oxi với ngọn lửa sáng xanh, có khí không màu, mùi hắc bay ra là hiện tượng của phản ứng:
-
A.
S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
-
B.
4P + 5O2 $\xrightarrow{{{t}^{o}}}$ 2P2O5
-
C.
C + O2 $\xrightarrow{{{t}^{o}}}$ CO2
-
D.
3Fe + 2O2 $\xrightarrow{{{t}^{o}}}$ Fe3O4
Cần bao nhiêu gam oxi để đốt cháy hết 2 mol lưu huỳnh?
-
A.
16 gam.
-
B.
32 gam.
-
C.
64 gam.
-
D.
48 gam.
Chất nào sau đây cháy mạnh trong khí oxi, sáng chói, tạo ra các hạt nóng chảy màu nâu?
-
A.
Fe.
-
B.
CH4.
-
C.
P.
-
D.
H2.
Người ta điều chế oxi trong phòng thí nghiệm bằng cách nào sau đây?
-
A.
Chưng cất phân đoạn không khí lỏng.
-
B.
Điện phân nước.
-
C.
Điện phân dung dịch NaOH.
-
D.
Nhiệt phân KClO3 với xúc tác MnO2.
Chất nào sau đây dùng để điều chế khí oxi trong công nghiệp?
-
A.
CaCO3.
-
B.
H2O.
-
C.
KMnO4.
-
D.
KClO3.
Đốt cháy 6,2 gam P trong bình chứa 6,72 lít khí oxi (đktc) tạo thành P2O5.
Chất nào còn dư, chất nào hết?
-
A.
P còn dư, O2 phản ứng hết.
-
B.
P hết, O2 dư.
-
C.
Cả 2 chất vừa đủ.
-
D.
Tất cả đều sai.
Khối lượng chất tạo thành là bao nhiêu?
-
A.
15,4 gam.
-
B.
16 gam.
-
C.
14,2 gam.
-
D.
13,3 gam.
Tính số gam kali clorat cầm thiết để điều chế được 48 gam khí oxi?
-
A.
183,75 gam
-
B.
122,5 gam
-
C.
147 gam
-
D.
196 gam.
Đốt cháy hoàn toàn 24 kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 tạo thành (ở điều kiện tiêu chuẩn)
-
A.
43904 lít.
-
B.
49388 lít.
-
C.
43988 lít.
-
D.
44904 lít
Đốt cháy m1 gam nhôm bằng 6,72 lít khí oxi (đktc) vừa đủ, thu được m2 gam Al2O3. Hòa tan toàn bộ lượng Al2O3 ở trên vào dung dịch chứa m3 gam H2SO4 vừa đủ thu được sản phẩm là Al2(SO4)3 và H2O. Tính m1 + m2 + m3
-
A.
70 gam.
-
B.
80 gam.
-
C.
90 gam.
-
D.
60 gam.
Đốt cháy m1 gam kẽm bằng khí oxi vừa đủ, thu được 12,15 gam ZnO. Hòa tan toàn bộ lượng ZnO ở trên vào dung dịch chứa m2 gam HCl vừa đủ thu được sản phẩm là ZnCl2 và nước. Tính m1 + m2
-
A.
20,7 gam.
-
B.
10,95 gam.
-
C.
9,75 gam.
-
D.
10,35 gam
Đốt cháy hoàn toàn 32 gam khí metan (CH4) cần V lít khí oxi (đktc), thu được khí CO2 và H2O. Giá trị của V là
-
A.
22,4 lít.
-
B.
89,6 lít.
-
C.
44,8 lít.
-
D.
67,2 lít.
Đốt cháy hoàn toàn m1 gam khí etilen (C2H4) cần 7,392 lít khí oxi (đktc), thu được m2 gam khí CO2 và m3 gam H2O. Tính m1 + m2 + m3
-
A.
19,36 gam.
-
B.
10,59 gam.
-
C.
10,12 gam.
-
D.
16,72 gam.
Đốt cháy 7,8 gam khí axetilen (C2H2) trong khí oxi, thu được 11,2 lít khí CO2 (đktc) và m2 gam H2O. Giá trị m2 là
-
A.
5,4 gam.
-
B.
9,0 gam.
-
C.
4,5 gam.
-
D.
2,7 gam.
Khí được con người sử dụng để hô hấp là:
-
A.
H2.
-
B.
O2.
-
C.
N2.
-
D.
CO2.
Oxi phản ứng với nhóm chất nào dưới đây ?
-
A.
C, Cl2, Na.
-
B.
C, C2H2, Cu.
-
C.
Na, C4H10, Au.
-
D.
Au, N2, Mg.
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi có hiện tượng gì xảy ra ?
-
A.
Tàn đóm tắt ngay
-
B.
Không có hiện tượng gì
-
C.
Tàn đóm tắt dần
-
D.
Tàn đóm bùng cháy
Trong điều kiện bình thường, khí oxi là đơn chất hoạt động hóa học ở mức độ:
-
A.
yếu
-
B.
rất yếu
-
C.
bình thường
-
D.
mạnh
Mỗi giờ 1 người lớn trung bình hít vào 0,5 m3 không khí, cơ thể giữ lại 1/3 lượng oxi có trong đó. Vậy thực tế trong 1 ngày đêm, cơ thể người cần 1 lượng khí oxi là:
-
A.
4 m3
-
B.
12 m3
-
C.
0,8 m3
-
D.
6 m3
Các phát biểu sau đây là đúng hay sai?
1. Khí oxygen tan nhiều trong nước.
2. Oxygen ở thể rắn hay lỏng có màu xanh nhạt.
3. Ở điều kiện thường, oxygen là chất khí.

Khi đốt bếp than, bếp lò, muốn ngọn lửa cháy to hơn, ta thường thổi hoặc quạt mạnh vào bếp. Đúng hay Sai?
Cho các từ/ cụm từ sau: sự cháy, sự sống, đốt cháy nhiên liệu, hô hấp. Em hãy bấm chọn từ/ cụm từ thích hợp và kéo thả vào chỗ trống để hoàn thành đoạn văn dưới đây:
Khí oxygen cần thiết cho quá trình nào sau đây?
-
A.
Đông đặc.
-
B.
Hô hấp.
-
C.
Nóng chảy.
-
D.
Quang hợp.
Để phân biệt hai chất khí là oxygen và carbon dioxide, em nên lựa chọn cách nào dưới đây?
-
A.
Oxygen duy trì sự sống và sự cháy.
-
B.
Quan sát màu sắc của hai khí đó.
-
C.
Ngửi mùi của hai khí đó.
-
D.
Dẫn từng khí vào cây nên đang cháy, khí nào làm nến cháy tiếp thì đó là oxygen, khí làm nến tắt là carbon dioxide.
Nhiệt độ lạnh nhất trên Trái Đất ghi lại được là -89oC, khi đó oxygen ở thể gì?
-
A.
Rắn
-
B.
Lỏng
-
C.
Khí
-
D.
Lỏng và rắn
Thợ lặn đeo bình có khí gì khi lặn xuống biển?
-
A.
Khí oxygen
-
B.
Khí nitrogen
-
C.
Khí carbon dioxit
-
D.
Tất cả các đáp án trên.
Tại sao khi phun chất từ bình cứu hoả vào đám cháy thì đám cháy lại bị đập tắt?
-
A.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí carbon dioxide. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
B.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí carbon monoxide. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
C.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí nitrogen. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
D.
Tất cả các đáp án trên.
Em hãy lựa chọn đáp án đúng và hoàn thành đoạn văn dưới đây:
Tại sai các đầm nuôi tôm thường lắp hệ thống quạt nước?
Do oxygen
trong nước và việc nuôi tôm, cá số lượng lớn làm cho lượng oxygen trong ao đầm nuôi rất ít. Chính vì vậy, người ta phải dùng giải phát quạt để sũ khí liên tục vào nước giúp cho oxygen
hơn trong nước, từ đó cá tôm có đủ oxygen để
.
Cho các từ sau: suy hô hấp, carbon monoxide, oxygen, gây mê. Em hãy bấm chọn các từ thích hợp và kéo thả vào chỗ trống trong đoạn văn sau:
Một lần, bạn An vào viện thăm ông ngoại đang phải cấp cứu. Khi vào viện, An thấy trên mũi ông đang phải đeo chiếc mặt nạ dưỡng khí. Mặt nạ đó được kết nối với một bình được làm bằng thép rất chắc chân. Bạn An thắc mắc rằng:
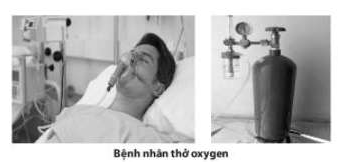
Nếu là oxygen thì tại sao trong không khí đã có oxygen rồi tại sao phải dùng thêm bình khí oxygen? Em hãy giải đáp thắc mắc giúp bạn An bằng cách bấm chọn từ thích hợp và kéo thả vào chỗ trống trong đoạn văn dưới đây:
Lời giải và đáp án
Trong các câu sau, câu nào sai?
-
A.
Oxygen nặng hơn không khí.
-
B.
Oxygen là chất khí không màu, không mùi, không vị.
-
C.
Oxygen tan nhiều trong nước.
-
D.
Oxygen chiếm 1/5 thể tích không khí.
Đáp án : C
Câu sai là: Oxi tan nhiều trong nước.
Oxi là chất khí ít tan trong nước.
Chất rắn màu vàng cháy trong bình đựng khí oxi với ngọn lửa sáng xanh, có khí không màu, mùi hắc bay ra là hiện tượng của phản ứng:
-
A.
S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
-
B.
4P + 5O2 $\xrightarrow{{{t}^{o}}}$ 2P2O5
-
C.
C + O2 $\xrightarrow{{{t}^{o}}}$ CO2
-
D.
3Fe + 2O2 $\xrightarrow{{{t}^{o}}}$ Fe3O4
Đáp án : A
Chất rắn màu vàng là S, S cháy trong bình đựng khí oxi với ngọn lửa sáng xanh, có khí không màu, mùi hắc bay ra là hiện tượng của phản ứng: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
Cần bao nhiêu gam oxi để đốt cháy hết 2 mol lưu huỳnh?
-
A.
16 gam.
-
B.
32 gam.
-
C.
64 gam.
-
D.
48 gam.
Đáp án : C
PTHH: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
+) Tính số mol O2 theo S
PTHH: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
Tỉ lệ PT: 1mol 1mol
Phản ứng: 2mol → 2mol
=> Khối lượng oxi cần dùng là: ${{m}_{{{O}_{2}}}}=n.M=2.32=64\,gam$
Chất nào sau đây cháy mạnh trong khí oxi, sáng chói, tạo ra các hạt nóng chảy màu nâu?
-
A.
Fe.
-
B.
CH4.
-
C.
P.
-
D.
H2.
Đáp án : A
Fe cháy mạnh trong khí oxi, sáng chói, tạo ra các hạt nóng chảy màu nâu là Fe3O4
PTHH: 3Fe + 2O2 $\xrightarrow{{{t}^{o}}}$ Fe3O4
Người ta điều chế oxi trong phòng thí nghiệm bằng cách nào sau đây?
-
A.
Chưng cất phân đoạn không khí lỏng.
-
B.
Điện phân nước.
-
C.
Điện phân dung dịch NaOH.
-
D.
Nhiệt phân KClO3 với xúc tác MnO2.
Đáp án : D
- O2 điều chế bằng phản ứng phân hủy những hợp chất giàu oxi và không bền nhiệt như KMnO4, KClO3, H2O2,…
2KMnO4 $\xrightarrow{{{t}^{o}}}$ K2MnO4 + MnO2 + O2
2KClO3 $\xrightarrow[Mn{{O}_{2}}]{{{t}^{o}}}$ 2KCl + 3O2
Chất nào sau đây dùng để điều chế khí oxi trong công nghiệp?
-
A.
CaCO3.
-
B.
H2O.
-
C.
KMnO4.
-
D.
KClO3.
Đáp án : B
Điều chế khí oxi trong công nghiệp, người ta điện phân nước: 2H2O → 2H2 + O2
Đốt cháy 6,2 gam P trong bình chứa 6,72 lít khí oxi (đktc) tạo thành P2O5.
Chất nào còn dư, chất nào hết?
-
A.
P còn dư, O2 phản ứng hết.
-
B.
P hết, O2 dư.
-
C.
Cả 2 chất vừa đủ.
-
D.
Tất cả đều sai.
Đáp án: B
Tính số mol của Photpho và số mol oxi
+) Viết phương trình phản ứng
+) Xét tỉ lệ phản ứng số mol chia cho hệ số phản ứng => chất dư, chất hết
Số mol của Photpho là: ${{n}_{P}}=\dfrac{{{m}_{P}}}{{{M}_{P}}}=\dfrac{6,2}{31}=0,2\,mol$
Số mol oxi là: ${{n}_{{{O}_{2}}}}=\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3\,mol$
Phương trình phản ứng: 4P + 5O2 $\xrightarrow{{{t}^{o}}}$ 2P2O5
Xét tỉ lệ phản ứng số mol chia cho hệ số phản ứng, ta có: $\dfrac{0,2}{4}<\dfrac{0,3}{5}$
=> oxi dư, P phản ứng hết => phản ứng tính theo O
Khối lượng chất tạo thành là bao nhiêu?
-
A.
15,4 gam.
-
B.
16 gam.
-
C.
14,2 gam.
-
D.
13,3 gam.
Đáp án: C
Tính số mol chất tạo thành ta dựa vào số mol chất phản ứng vừa đủ
Khối lượng chất tạo thành ta dựa vào số mol của Photpho, là chất phản ứng vừa đủ
4P + 5O2 $\xrightarrow{{{t}^{o}}}$ 2P2O5
4mol 2mol
0,2mol ?mol
Số mol P2O5 tạo thành là: ${{n}_{{{P}_{2}}{{O}_{5}}}}=\dfrac{0,2.2}{4}=0,1\,mol$
Khối lượng P2O5 tạo thành là: ${{m}_{{{P}_{2}}{{O}_{5}}}}={{n}_{{{P}_{2}}{{O}_{5}}}}.{{M}_{{{P}_{2}}{{O}_{5}}}}=0,1.(31.2+16.5)=14,2\,gam$
Tính số gam kali clorat cầm thiết để điều chế được 48 gam khí oxi?
-
A.
183,75 gam
-
B.
122,5 gam
-
C.
147 gam
-
D.
196 gam.
Đáp án : B
+) Tính số mol khí oxi thu được
+) Viết PTHH => tính KClO3 cần dùng theo số mol oxi
Số mol khí oxi thu được là: ${{n}_{{{O}_{2}}}}=\frac{48}{32}=1,5\,mol$
PTHH: 2KClO3 $\xrightarrow{{{t}^{o}}}$ 2KCl + 3O2
Tỉ lệ theo PT: 2mol 3mol
Phản ứng: 1mol ← 1,5mol
=> Khối lượng KClO3 cần dùng là: ${{m}_{KCl{{O}_{3}}}}=n.M=1.(39+35,5+16.3)=122,5\,gam$
Đốt cháy hoàn toàn 24 kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 tạo thành (ở điều kiện tiêu chuẩn)
-
A.
43904 lít.
-
B.
49388 lít.
-
C.
43988 lít.
-
D.
44904 lít
Đáp án : C
+) Từ % tạp chất => tính % cacbon => số mol của C và S trong than đá
+) Viết PTHH 2 phản ứng cháy của C và S
+) Tính số mol CO2 và SO2 theo PTHH
Trong than đá chứa: Cacbon (x%), lưu huỳnh (0,5%) và tạp chất khác (1,5%)
=> x = 100 – 0,5 – 1,5 = 98 (%)
=> trong 24 kg than đá chứa: 24.98% = 23,52 kg = 23520 gam cacbon; 24.0,5% = 0,12 kg = 120 gam lưu huỳnh; 24.1,5% = 0,36 kg = 360 gam tạp chất khác
=> số mol C là: ${{n}_{C}}=\dfrac{23520}{12}=1960\,mol$
Số mol S là: ${{n}_{S}}=\dfrac{120}{32}=3,75\,mol$
PTHH: C + O2 $\xrightarrow{{{t}^{o}}}$ CO2
Tỉ lệ PT: 1mol 1mol
Phản ứng: 1960mol → 1960mol
=> Thể tích khí CO2 sinh ra là: ${{V}_{C{{O}_{2}}}}=22,4.1960=43904$ lít
PTHH: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2
Tỉ lệ PT: 1mol 1mol
Phản ứng: 3,75mol → 3,75mol
=> Thể tích khí SO2 sinh ra là: ${{V}_{S{{O}_{2}}}}=22,4.3,75=84$ lít
=> tổng thể tích khí thu được là: $V={{V}_{C{{O}_{2}}}}+{{V}_{S{{O}_{2}}}}=43904+84=43988$ lít
Đốt cháy m1 gam nhôm bằng 6,72 lít khí oxi (đktc) vừa đủ, thu được m2 gam Al2O3. Hòa tan toàn bộ lượng Al2O3 ở trên vào dung dịch chứa m3 gam H2SO4 vừa đủ thu được sản phẩm là Al2(SO4)3 và H2O. Tính m1 + m2 + m3
-
A.
70 gam.
-
B.
80 gam.
-
C.
90 gam.
-
D.
60 gam.
Đáp án : C
+) Tính số mol khí oxi
+) Viết PTHH => số mol Al2O3 thu được và số mol Al phản ứng => m2 và m1
+) Viết PTHH Al2O3 tác dụng với H2SO4 => số mol H2SO4 phản ứng => m3
Số mol khí oxi là: ${{n}_{{{O}_{2}}}}=\frac{6,72}{22,4}=0,3\,mol$
PTHH: 4Al + 3O2 $\xrightarrow{{{t}^{o}}}$ 2Al2O3
Tỉ lệ PT: 4mol 3mol 2mol
Phản ứng: 0,4mol ← 0,3mol → 0,2mol
=> Khối lượng Al2O3 thu được là: m2 = ${{m}_{A{{l}_{2}}{{O}_{3}}}}=0,2.102=20,4\,gam$
Khối lượng Al phản ứng là: m1 = mAl = 0,4.27 = 10,8 gam
Lấy 0,2 mol Al2O3 tác dụng với H2SO4
PTHH: Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tỉ lệ PT: 1mol 3mol
Phản ứng: 0,2mol → 0,6mol
=> Khối lượng H2SO4 phản ứng là: ${{m}_{3}}={{m}_{{{H}_{2}}S{{O}_{4}}}}=0,6.98=58,8\,gam$
=> m1 + m2 + m3 = 10,8 + 20,4 + 58,8 = 90 gam
Đốt cháy m1 gam kẽm bằng khí oxi vừa đủ, thu được 12,15 gam ZnO. Hòa tan toàn bộ lượng ZnO ở trên vào dung dịch chứa m2 gam HCl vừa đủ thu được sản phẩm là ZnCl2 và nước. Tính m1 + m2
-
A.
20,7 gam.
-
B.
10,95 gam.
-
C.
9,75 gam.
-
D.
10,35 gam
Đáp án : A
+) Tính số mol ZnO thu được
+) Viết PTHH => số mol Zn phản ứng theo số mol ZnO => m1
+) Viết PTHH ZnO tác dụng với HCl => tính số mol HCl phản ứng theo số mol ZnO => m2
Số mol ZnO thu được là: ${{n}_{ZnO}}=\frac{12,15}{81}=0,15\,mol$
PTHH: 2Zn + O2 $\xrightarrow{{{t}^{o}}}$ 2ZnO
Tỉ lệ PT: 2mol 1mol 2mol
Phản ứng: 0,15mol ← 0,15mol
=> Khối lượng Zn phản ứng là: m1 = mZn = 0,15.65 = 9,75 gam
Lấy 0,15 mol ZnO cho vào dung dịch HCl
PTHH: ZnO + 2HCl → ZnCl2 + H2O
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,15mol → 0,3mol
=> Khối lượng HCl phản ứng là: mHCl = m2 = 0,3.36,5 = 10,95 gam
=> m1 + m2 = 9,75 + 10,95 = 20,7 gam
Đốt cháy hoàn toàn 32 gam khí metan (CH4) cần V lít khí oxi (đktc), thu được khí CO2 và H2O. Giá trị của V là
-
A.
22,4 lít.
-
B.
89,6 lít.
-
C.
44,8 lít.
-
D.
67,2 lít.
Đáp án : B
+) Tính số mol khí CH4
+) Viết PTHH => tính số mol khí oxi cần dùng theo CH4
Số mol khí CH4 là: ${{n}_{C{{H}_{4}}}}=\frac{32}{12+4}=2\,mol$
PTHH: CH4 + 2O2 $\xrightarrow{{{t}^{o}}}$ CO2 + 2H2O
Tỉ lệ PT: 1mol 2mol
Phản ứng: 2mol → 4mol
=> thể tích khí oxi cần dùng là: ${{V}_{{{O}_{2}}}}=22,4.n=22,4.4=89,6$ lít
Đốt cháy hoàn toàn m1 gam khí etilen (C2H4) cần 7,392 lít khí oxi (đktc), thu được m2 gam khí CO2 và m3 gam H2O. Tính m1 + m2 + m3
-
A.
19,36 gam.
-
B.
10,59 gam.
-
C.
10,12 gam.
-
D.
16,72 gam.
Đáp án : D
+) Tính số mol khí O2
+) Viết PTHH => tính số mol C2H4, CO2, H2O theo số mol khí O2 => m1, m2, m3
Số mol khí O2 là: ${{n}_{{{O}_{2}}}}=\frac{7,392}{22,4}=0,33\,mol$
Ta có PTHH: C2H4 + 3O2 2CO2 + 2H2O
Theo phương trình cứ 3 mol O2 thì đốt cháy hết 1 mol C2H4
Theo đầu bài………………0,33 mol O2…...$\frac{{0,33}}{3}$= 0,11mol C2H4
Áp dụng định luật bảo toàn khối lượng ta có: m C2H4 + mO2 = mCO2 + mH2O
=> mCO2 + mH2O = 0,11.28 + 0,33.32=13,64
=> m1 + m2 + m3 = m C2H4 + mCO2 + mH2O = 13,64 + 3,08= 16,72 gam
Đốt cháy 7,8 gam khí axetilen (C2H2) trong khí oxi, thu được 11,2 lít khí CO2 (đktc) và m2 gam H2O. Giá trị m2 là
-
A.
5,4 gam.
-
B.
9,0 gam.
-
C.
4,5 gam.
-
D.
2,7 gam.
Đáp án : C
+) Tính số mol khí CO2
+) Vì đầu bài cho 2 số liệu số mol của chất phản ứng C2H2 và chất sản phẩm CO2 => tính toán theo chất sản phẩm
+) Viết PTHH và tính số mol H2O theo CO2
Số mol khí C2H2 là: ${{n}_{{{C}_{2}}{{H}_{2}}}}=\frac{7,8}{12.2+2}=0,3\,mol$
Số mol khí CO2 là: ${{n}_{C{{O}_{2}}}}=\frac{11,2}{22,4}=0,5\,mol$
Vì đầu bài cho 2 số liệu số mol của chất phản ứng C2H2 và chất sản phẩm CO2 => tính toán theo chất sản phẩm
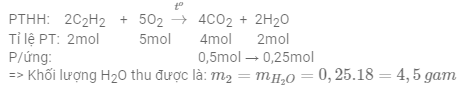
Khí được con người sử dụng để hô hấp là:
-
A.
H2.
-
B.
O2.
-
C.
N2.
-
D.
CO2.
Đáp án : B
Con người hít khí O2 vào cơ thể để hô hấp
Oxi phản ứng với nhóm chất nào dưới đây ?
-
A.
C, Cl2, Na.
-
B.
C, C2H2, Cu.
-
C.
Na, C4H10, Au.
-
D.
Au, N2, Mg.
Đáp án : B
Dựa vào tính chất hóa học của oxi trong sgk hóa 8 – trang 81
A. Loại Cl2 không pư.
B. Thỏa mãn
PTHH minh họa: C + O2 \(\xrightarrow{{{t^0}}}\) CO2
C2H2 + 5/2O2 \(\xrightarrow{{{t^0}}}\) 2CO2 + H2O
2Cu + O2 \(\xrightarrow{{{t^0}}}\) 2CuO
B, D. Loại Au không pư.
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi có hiện tượng gì xảy ra ?
-
A.
Tàn đóm tắt ngay
-
B.
Không có hiện tượng gì
-
C.
Tàn đóm tắt dần
-
D.
Tàn đóm bùng cháy
Đáp án : D
Dựa vào dấu hiệu hiện tượng nhận biết ra khí oxi.
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi thì tàn đóm bùng cháy.
Trong điều kiện bình thường, khí oxi là đơn chất hoạt động hóa học ở mức độ:
-
A.
yếu
-
B.
rất yếu
-
C.
bình thường
-
D.
mạnh
Đáp án : D
Trong điều kiện bình thường, khí oxi là đơn chất hoạt động hóa học ở mức độ: mạnh
Mỗi giờ 1 người lớn trung bình hít vào 0,5 m3 không khí, cơ thể giữ lại 1/3 lượng oxi có trong đó. Vậy thực tế trong 1 ngày đêm, cơ thể người cần 1 lượng khí oxi là:
-
A.
4 m3
-
B.
12 m3
-
C.
0,8 m3
-
D.
6 m3
Đáp án : C
Dựa vào thành phần của không khí ta có: VO2 = 1/5Vkk
Vì O2 chiếm 20% thể tích không khí nên trong 0,5 m3 có chứa lượng O2 là: \({V_{{O_2}}} = \frac{{20\% }}{{100\% }}.0,5 = 0,1{m^3}\)
Cơ thể người giữ lại 1/3 lượng oxi nên 1 giờ cơ thể người giữ lại lượng O2 có trong không khí là: \({V_{{O_2}giu\,lai}} = \frac{1}{3}{V_{{O_2}}} = \frac{{0,1}}{3}\,{m^3}\)
1 ngày đêm có 24 giờ nên cơ thể người cần 1 lượng oxi là: \({V_{{O_2}\,can}} = 24 \times {V_{{O_2}giu\,lai}} = 24 \times \frac{{0,1}}{3} = 0,8\,{m^3}\)
Các phát biểu sau đây là đúng hay sai?
1. Khí oxygen tan nhiều trong nước.
2. Oxygen ở thể rắn hay lỏng có màu xanh nhạt.
3. Ở điều kiện thường, oxygen là chất khí.
1. Khí oxygen tan nhiều trong nước.
2. Oxygen ở thể rắn hay lỏng có màu xanh nhạt.
3. Ở điều kiện thường, oxygen là chất khí.
Ý (2), (3) đúng.
Ý (1) sai vì oxygen tan ít trong nước.

Khi đốt bếp than, bếp lò, muốn ngọn lửa cháy to hơn, ta thường thổi hoặc quạt mạnh vào bếp. Đúng hay Sai?
Khi thổi hoặc quạt sẽ cung cấp thêm khí oxi. Thổi hoặc quạt càng mạnh càng nhiều khí oxy, vì thế sự diễn ra cháy càng mạnh hơn và tỏa nhiều nhiệt hơn.
=> Đáp án: Đúng
Cho các từ/ cụm từ sau: sự cháy, sự sống, đốt cháy nhiên liệu, hô hấp. Em hãy bấm chọn từ/ cụm từ thích hợp và kéo thả vào chỗ trống để hoàn thành đoạn văn dưới đây:
Thông thường, ở đâu có oxygen thì ở đó có sự sống. Oxygen không chỉ cần thiết cho quá trình hô hấp của động vật, thực vật trên Trái Đất, mà còn không thể thiếu cho quá trình đốt cháy nhiên liệu để thắp sáng, cung cấp nhiệt,… Nếu không ó oxygen thì sự cháy không thể xảy ra.
Khí oxygen cần thiết cho quá trình nào sau đây?
-
A.
Đông đặc.
-
B.
Hô hấp.
-
C.
Nóng chảy.
-
D.
Quang hợp.
Đáp án : B
Oxygen là thành phần quan trọng nhất đối với hoạt động hô hấp của con người, động vật và thực vật.
Để phân biệt hai chất khí là oxygen và carbon dioxide, em nên lựa chọn cách nào dưới đây?
-
A.
Oxygen duy trì sự sống và sự cháy.
-
B.
Quan sát màu sắc của hai khí đó.
-
C.
Ngửi mùi của hai khí đó.
-
D.
Dẫn từng khí vào cây nên đang cháy, khí nào làm nến cháy tiếp thì đó là oxygen, khí làm nến tắt là carbon dioxide.
Đáp án : D
Oxygen duy trì sự cháy, còn carbon dioxide thì không.
Nhiệt độ lạnh nhất trên Trái Đất ghi lại được là -89oC, khi đó oxygen ở thể gì?
-
A.
Rắn
-
B.
Lỏng
-
C.
Khí
-
D.
Lỏng và rắn
Đáp án : C
Nhiệt độ lạnh nhất trên Trái Đất ghi lại được là -89oC, khi đó oxygen ở thể khí. Không thể là thể lỏng hay thể rắn vì oxygen hóa lỏng ở -183oC, hóa rắn ở -218oC.
Thợ lặn đeo bình có khí gì khi lặn xuống biển?
-
A.
Khí oxygen
-
B.
Khí nitrogen
-
C.
Khí carbon dioxit
-
D.
Tất cả các đáp án trên.
Đáp án : A
Oxygen là thành phần quan trọng đối với hoạt động hô hấp của con người, động vật, thực vật. Ngoài ra, nhờ tính dễ nén, oxygen được nén vào những bình khí đặc biệt cùng một số khí khác và được dùng trong y tế, chinh phục độ cao hay khám phá đại dương…
Tại sao khi phun chất từ bình cứu hoả vào đám cháy thì đám cháy lại bị đập tắt?
-
A.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí carbon dioxide. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
B.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí carbon monoxide. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
C.
Chất từ bình cứu hoả phun vào đám cháy là bọt khí nitrogen. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
-
D.
Tất cả các đáp án trên.
Đáp án : A
Chất từ bình cứu hoả phun vào đám cháy là bọt khí carbon dioxide. Chất này đã ngăn cách chất cháy với oxygen trong không khí nên sự cháy đã được dập tắt.
Em hãy lựa chọn đáp án đúng và hoàn thành đoạn văn dưới đây:
Tại sai các đầm nuôi tôm thường lắp hệ thống quạt nước?
Do oxygen
trong nước và việc nuôi tôm, cá số lượng lớn làm cho lượng oxygen trong ao đầm nuôi rất ít. Chính vì vậy, người ta phải dùng giải phát quạt để sũ khí liên tục vào nước giúp cho oxygen
hơn trong nước, từ đó cá tôm có đủ oxygen để
.
Do oxygen
trong nước và việc nuôi tôm, cá số lượng lớn làm cho lượng oxygen trong ao đầm nuôi rất ít. Chính vì vậy, người ta phải dùng giải phát quạt để sũ khí liên tục vào nước giúp cho oxygen
hơn trong nước, từ đó cá tôm có đủ oxygen để
.
Tại sai các đầm nuôi tôm thường lắp hệ thống quạt nước?
Do oxygen ít tan trong nước và việc nuôi tôm, cá số lượng lớn làm cho lượng oxygen trong ao đầm nuôi rất ít. Chính vì vậy, người ta phải dùng giải phát quạt để sũ khí liên tục vào nước giúp cho oxygen tan nhiều hơn trong nước, từ đó cá tôm có đủ oxygen để hô hấp.
Cho các từ sau: suy hô hấp, carbon monoxide, oxygen, gây mê. Em hãy bấm chọn các từ thích hợp và kéo thả vào chỗ trống trong đoạn văn sau:
Khí oxygen trong bình khí sẽ có tác dụng hỗ trợ cho những bệnh nhân mắc các triệu chứng như suy hô hấp, ngạt thở, bệnh tim, chứng rối loạn thở. Ngoài ra, trong y tế, các bác sĩ sẽ cho bệnh nhân thở oxygen khi ngộ độc carbon monoxide, đặc biệt khi cần gây mê bệnh nhân để thực hiện phẫu thuật.
Một lần, bạn An vào viện thăm ông ngoại đang phải cấp cứu. Khi vào viện, An thấy trên mũi ông đang phải đeo chiếc mặt nạ dưỡng khí. Mặt nạ đó được kết nối với một bình được làm bằng thép rất chắc chân. Bạn An thắc mắc rằng:

Nếu là oxygen thì tại sao trong không khí đã có oxygen rồi tại sao phải dùng thêm bình khí oxygen? Em hãy giải đáp thắc mắc giúp bạn An bằng cách bấm chọn từ thích hợp và kéo thả vào chỗ trống trong đoạn văn dưới đây:
Trong không khí có oxygen nhưng hàm lượng oxygen thấp, cơ quan hô hấp của người bệnh lại hoạt động yếu nên oxygen trong không khí không đáp ứng đủ nhu cầu của người bệnh. Oxygen trong bình là oxygen có hàm lượng cao (gần 100%), đảm bảo cho người bệnh vẫn có đủ oxygen cho tế bào mặc dù hô hấp yếu.
Luyện tập và củng cố kiến thức Bài 25. Sự oxi hóa - Phản ứng hóa hợp - Ứng dụng của oxi Hóa học 8 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 26. Oxit Hóa học 8 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 27. Điều chế khí oxi - Phản ứng phân hủy Hóa học 8 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 28. Không khí - Sự cháy Hóa học 8 với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
- Trắc nghiệm Tổng hợp bài tập hòa tan kim loại và chất rắn vào dung dịch axit - Hóa học 8
- Trắc nghiệm Tổng hợp bài tập hòa tan một chất vào nước và vào dung dịch cho sẵn - Hóa học 8
- Trắc nghiệm Tổng hợp bài tập pha trộn 2 dung dịch có xảy ra phản ứng - Hóa học 8
- Trắc nghiệm Tổng hợp bài tập pha trộn 2 dung dịch không xảy ra phản ứng - Hóa học 8
- Trắc nghiệm Bài 43. Pha chế dung dịch - Hóa học 8










Danh sách bình luận