 Giải bài tập hóa học 11, Hóa 11 - Để học tốt hóa học 11
Giải bài tập hóa học 11, Hóa 11 - Để học tốt hóa học 11
 Bài 3. Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
Bài 3. Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
Lý thuyết Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
pH càng nhỏ thì dung dịch có độ axit càng lón. pH càng lớn thì dung dịch có độ bazơ càng lớn.
I. NƯỚC LÀ CHẤT ĐIỆN LI YẾU
1. Sự điện li của nước
Thực nghiệm cho ta nhận thấy, nước là chất điện ly cực yếu:
H2O \(\rightleftharpoons \) H+ + OH- (1)
Tích số ion của nước :
K H2O= [H+][OH-] =10-14 M (đo ở 25oC)
2. Ý nghĩa tích số ion của nước
- Môi trường trung tính có : [H+] = [OH–] và pH = 7 ;
- Môi trường axit có : [H+] > [OH–] và pH < 7 ;
- Môi trường bazơ có : [H+] < [OH–] và pH > 7.
- pH càng nhỏ thì dung dịch có độ axit càng lớn. pH càng lớn thì dung dịch có độ bazơ càng lớn.
II. KHÁI NIỆM VỀ pH. CHẤT CHỈ THỊ AXIT - BAZO
1. Khái niệm về pH

2. Chất chỉ thị axit – bazơ
- Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
- Dựa vào sự chuyển màu của giấy quỳ và dung dịch phenolphtalein xác định được môi trường của dung dịch, dựa vào màu của giấy chỉ thị vạn năng có thể xác định được gần đúng giá tri pH của dung dịch.
Ta có: Nếu [H+] = 1,0.10–a M thì pH = a.
=> pH = -lg [H+]
Ví dụ : [H+] = 10-3M pH = 3 : Môi trường axit.
pH + pOH = 14
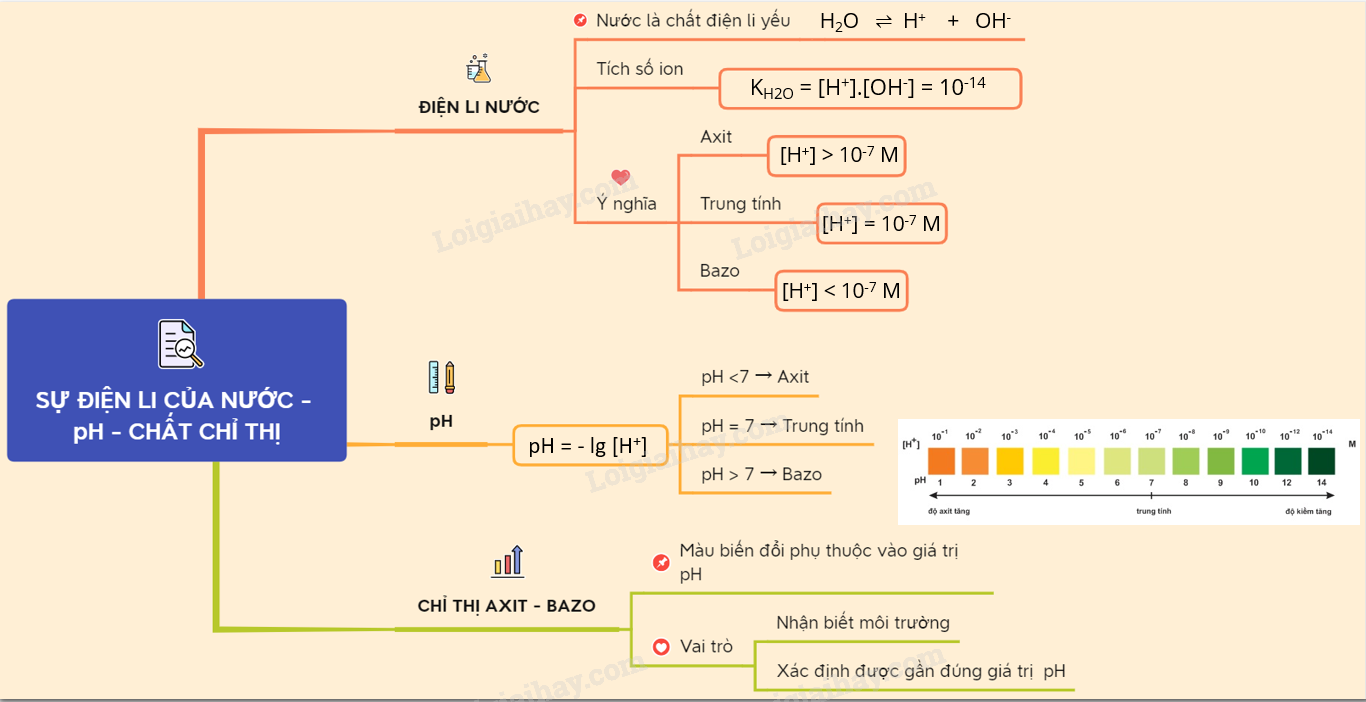
Sơ đồ tư duy: Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
Loigiaihay.com












Danh sách bình luận