 Giải bài tập hóa học 11, Hóa 11 - Để học tốt hóa học 11
Giải bài tập hóa học 11, Hóa 11 - Để học tốt hóa học 11
 Bài 35. Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
Bài 35. Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
Lý thuyết Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
1. Đồng đẳng, đồng phân, danh pháp, cấu tạo.
I. ĐỒNG ĐẰNG, ĐỒNG PHÂN, DANH PHÁP, CẤU TẠO
1. Đồng đằng
- Công thức chung dãy đồng đẳng của benzen: CnH2n-6 (n ≥ 6)
- Tên gọi chung là aren.
- Công thức đơn giản nhất là benzen (C6H6).
- Các ankyl benzen thương gặp là toluen C6H5CH3, xilen C6H4(CH3)2, cumen C6H5CH(CH3)2, …
2. Danh pháp
- Khi coi vòng benzen là mạch chính thì các nhóm ankyl đính với nó là mạch nhánh (còn gọi là nhóm thế).
- Tên gọi: Tên vị trí – tên nhánh + benzen
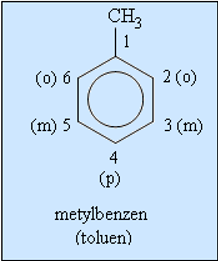
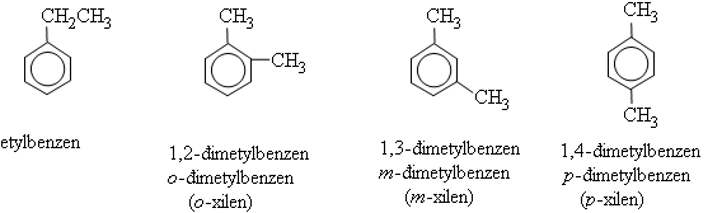
3. Đồng phân
- Đồng phân gồm: Đồng phân vị trí nhóm ankyl trong vòng benzen và đồng phân mạch cacbon của nhánh.
+ Nếu 2 nhóm thế ở 2 C lân cận ta có đồng phân ortho (viết tắt o-) hoặc đánh số 1,2.
+ Nếu 2 nhóm thế cách nhau 1 nguyên tử cacbon (1 đỉnh tam giác) gọi là đồng phân meta (viết tắt m-) hoặc 1,3.
+ Nếu 2 nhóm thế ở 2 nguyên tử cacbon đối đỉnh gọi là đồng phân para (viết tắt p-) hoặc 1,4.
Ví dụ: Các đồng phân của diclobenzen (C6H4Cl2).
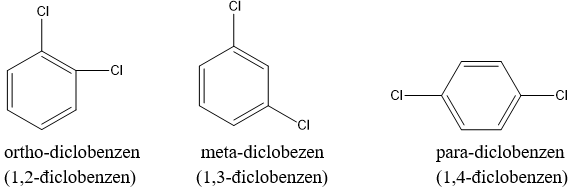
4. Cấu tạo
- Cấu trúc phân tử benzen: Sáu nguyên tử C trong phân tử liên kết với nhau tạo vòng 6 cạnh, 3 liên kết đôi tạo hệ liên hợp chung cho cả vòng benzen. Các nguyên tử trong phân tử cùng nằm trên mặt phẳng.
- Biểu diễn cấu tạo benzen:
![]()
II. TÍNH CHẤT VẬT LÍ
Bezen là chất lỏng, không màu, có mùi thơm đặc trưng, nhẹ hơn nước và không tan trong nước nhưng tan nhiều trong dung môi hữu cơ như rượu, ete, xeton
III. TÍNH CHẤT HÓA HỌC
1. Phản ứng thế
- Phản ứng thế H ở nhân thơm bởi các tác nhân như halogen X2/Fe; HNO3/H2SO4 đặc… tuân theo quy tắc thế vào vòng benzen.
C6H6 + Br2 → C6H5Br + HBr (Fe, tº)
C6H6 + HNO3 → C6H5NO2 + H2O (H2SO4 đặc, tº)
- Quy tắc thế vào vòng benzen:
+ Nếu vòng benzen đã có sẵn nhóm thế loại I (-OH, ankyl, -NH2, …) thì phản ứng thế xảy ra dễ hơn so với benzen và ưu tiên thế vào vị trí o- và p-.
+ Nếu vòng benzen đã có sẵn nhóm thế loại II (-COOH, -CHO, -CH=CH2) thì phản ứng thế xảy ra khó hơn so với benzen và ưu tiên thế vào vị trí m-.
2. Phản ứng cộng: R
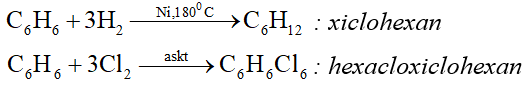
3. Phản ứng oxi hóa
- Phản ứng cháy tỏa nhiều nhiệt và cho nhiều muội than.
- Benzen không làm mất màu KMnO4
- Ankylbenzen tác dụng với dung dịch KMnO4/to (hoặc K2Cr2O7) bị oxi hóa không hoàn toàn nhóm ankyl, trong đó CH3 chuyển thành nhóm – COOH.
C6H5-CH3 + 2KMnO4 → C6H5COOK + 2MnO2 + KOH + H2O
IV. STIREN C8H8 (hay: vinybenzen, phenyletilen)
- Stiren là chất lỏng không màu, nhẹ hơn nước, không tan trong nước.
![]()
- Tính chất hóa học:
+ Tính chất thơm tương tự ankylbenzen: có phản ứng thế H ở nhân thơm, oxi hóa Cα ở nhánh.
+ Tính chất không no của nhóm vinyl tương tự anken: cộng halogen, cộng hiđro halogenua, trùng hợp, làm mất màu dung dịch KMnO4.
V. NAPHTALEN
- CTPT C10H8 và có công thức cấu tạo ![]()
- Naphtalen là chất rắn màu trắng, thăng hoa ngay ở nhiệt độ thường, có mùi đặc trưng, không tan trong nước, tan trong dung môi hữu cơ.
- Naphtalen có tính thơm tương tự benzen: Naphtalen tham gia từng phản ứng thế dễ dàng hơn benzen và thường ưu tiên thế nguyên tử H ở vị trí Cα (vị trí C số 1 của vòng), có phản ứng cộng H2/(Ni, to) tạo C10H12 (tralin) hoặc C10H18 (đecanlin).
Sơ đồ tư duy: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
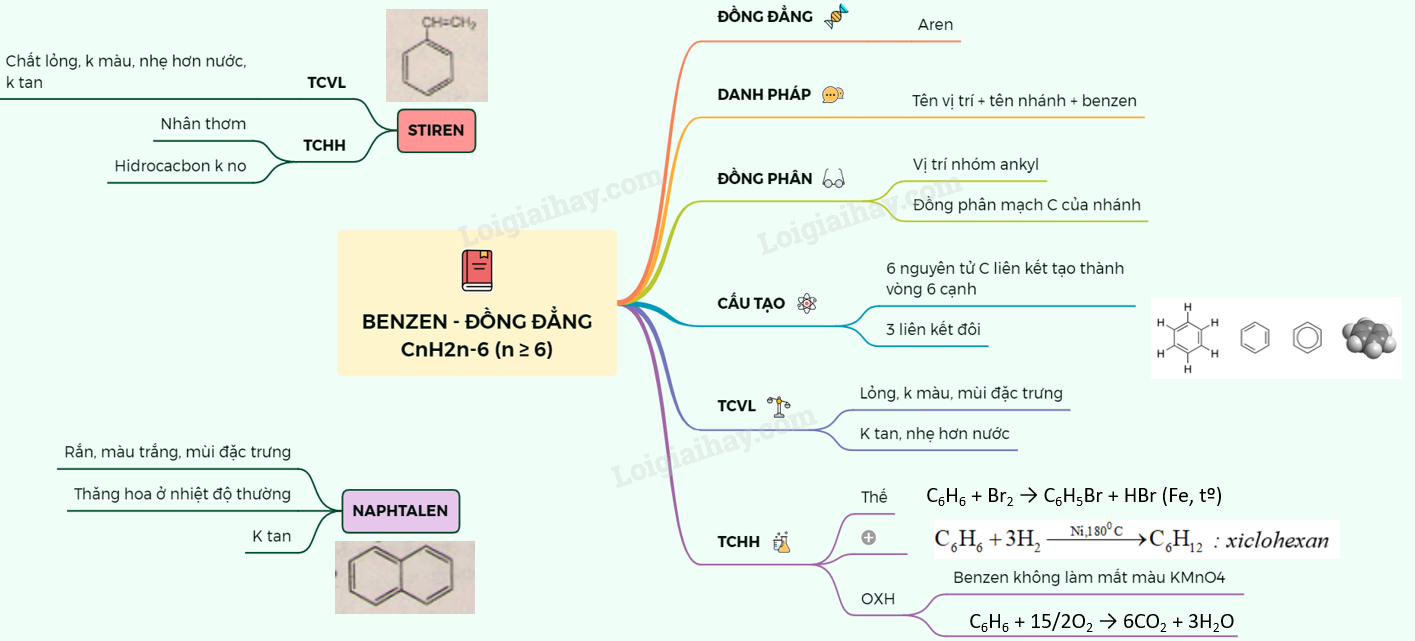
Loigiaihay.com












Danh sách bình luận