30 bài tập về đốt cháy chất béo có lời giải
Làm đề thiCâu hỏi 1 :
Đốt cháy hoàn toàn m gam một triglixerit X cần dùng 1,61 mol O2, thu được 1,14 mol CO2 và 1,06 mol H2O. Cho 26,58 gam X tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
- A 18,28 gam.
- B 27,14 gam.
- C 27,42 gam.
- D 25,02 gam.
Đáp án: C
Phương pháp giải:
Bảo toàn nguyên tố
Bảo toàn khối lượng
Lời giải chi tiết:
Hướng dẫn giải
Bảo toàn nguyên tố O ta có
→ nO(X) =0,12 → nCOOH(X) =0,06 mol
Bảo toàn khối lượng ta có
mX +mO2 =mCO2 + mH2O → m + 1,61.32 = 1,14.44 + 1,06.18 → m =17,72 g
17,72 g X có 0,06 mol COOH → 26,58 g X có 0,09 mol COOH
→ 26,58 g X + 0,09 mol NaOH → muối + 0,03 mol C3H5(OH)3
Bảo toàn khối lượng có 26,58 + 0,09.40 = mmuối + 0,03.92 → mmuối =27,42
Đáp án C
Câu hỏi 2 :
Đốt cháy hoàn toàn 17,72 g một chất béo (triglixerit) cần 1,61 mol O2 thu được CO2 và 1,06 mol H2O. Mặt khác cho 26,58 g chất béo này vào vừa đủ dd NaOH thì thu được lượng muối là
- A 18,56g
- B 27,42 g
- C 27,14g
- D 18,28g
Đáp án: B
Phương pháp giải:
Phương pháp :
Bảo toàn khối lượng
Bảo toàn nguyên tố
nchất béo = 1/6 . nO(chất béo)
Lời giải chi tiết:
Hướng dẫn giải;
Bảo toàn khối lượng ta có 17,72 + 1,61.32 = mCO2+ 1,06.18 → mCO2 = 50,16 → nCO2= 1,14 mol
Bảo toàn O có nO(chất béo) + 2nO2 = 2nCO2 +nH2O → nO( chất béo ) =0,12 → nchất béo =0,02 mol
→ 26,58 g chất béo có số mol :0,03 mol→ phản ứng với 0,09mol NaOH
Ta có chất béo + 0,09 mol NaOH → muối + 0,03 mol C3H5(OH)3
Bảo toàn khối lượng mmuối =26,58 + 0,09.40 -0,03.92 =27,42 g
Đáp án B
Câu hỏi 3 :
Đốt cháy hoàn toàn triglixerit X thu được x mol CO2 và y mol H2O với x = y + 4a. Nếu thủy phân hoàn toàn X thu được hỗn hợp glicerol, axit oleic, axit stearic. Số nguyên tử H trong X là :
- A 106
- B 102
- C 108
- D 104
Đáp án: A
Phương pháp giải:
Mối liên hệ độ bất bão hòa k của chất X: CxHyOz với H2O và CO2 :
nX = (nH2O – nCO2) / ( k – 1)
Lời giải chi tiết:
nCO2 – nH2O = x – y = 4a = 4nX
=>X có 5 liên kết pi (3 COO và 2 oleic)
=> X có dạng (Oleic)2(Stearin)
Đáp án A
Câu hỏi 4 :
Đốt cháy hoàn toàn 0,1 mol triglixerit X ta thu được 250,8 gam CO2 và 90 gam H2O. Mặt khác 0,1 mol X phản ứng vừa đủ với V lít dung dịch Br2 1M. Giá trị của V là
- A 0,7.
- B 0,3.
- C 0,5.
- D 0,4.
Đáp án: C
Phương pháp giải:
nCO2 => Số C; nH2O => Số H
=> CTPT => Độ bất bão hòa: k = (2C + 2 – H)/2 => Số liên kết π có khả năng phản ứng với Br2: k - 3
Lời giải chi tiết:
nCO2 = 5,7 mol
nH2O = 5 mol
Số C = 5,7/0,1 =57
Số H = 10/0,1 = 100
Vậy công thức phân tử của chất béo đó là C57H100O6. Độ bất bão hòa: k = (2C + 2 – H)/2 = (57.2+2-100)/2 = 8
Số liên kết π có khả năng phản ứng với Br2: 8 – 3 (trong 3 gốc COO) = 5
=> nBr2 = 0,5 mol => V = 0,5 lít
Đáp án C
Câu hỏi 5 :
Đốt cháy hoàn toàn 17,72 gam một chất béo (triglixerit) cần 1,61 mol O2 thu được CO2 và 1,06 mol nước. Mặt khác, cho 26,58 gam chất béo này tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối thu được là:
- A 18,56 gam
- B 27,42 gam
- C 18,28 gam
- D 27,14 gam
Đáp án: B
Phương pháp giải:
+ BTKL => mCO2 = m chất béo + mO2 – mH2O
+ BTNT O: nO(chất béo) = 2nCO2 + nH2O – 2nO2 => n chất béo = nO(chất béo)/6
Khi cho chất béo tác dụng với NaOH vừa đủ:
nNaOH = 3n chất béo
n glixerol = n chất béo
BTKL: m muối = m chất béo + mNaOH – m glixerol
Lời giải chi tiết:
BTKL => mCO2 = m chất béo + mO2 – mH2O = 17,72 + 1,61.32 – 1,06.18 = 50,16 gam => nCO2 = 1,14 mol
BTNT O: nO(chất béo) = 2nCO2 + nH2O – 2nO2 = 1,14.2 + 1,06 – 1,61.2 = 0,12 mol
=> n chất béo = nO(chất béo)/6 = 0,02 mol
Khi cho chất béo tác dụng với NaOH vừa đủ:
nNaOH = 3n chất béo = 0,06 mol
n glixerol = n chất béo = 0,02 mol
BTKL: m muối = m chất béo + mNaOH – m glixerol = 17,72 + 0,06.40 – 0,02.92 = 18,28 gam
Tỉ lệ:
17,72 gam chất béo thu được 18,28 gam muối
26,58 gam 27,42 gam
Đáp án B
Câu hỏi 6 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của b là
- A 60,36.
- B 54,84.
- C 57,12.
- D 53,16.
Đáp án: B
Phương pháp giải:
X + O2 → CO2 + H2O
a gam 4,83 mol 3,42 mol 3,18 mol
BTKL => a
BTNT O: nO(X) = 2nCO2+nH2O-2nO2
=> nX = nO/6 (Vì X chứa 6O)
\(\begin{gathered}
{(\overline R COO)_3}{C_3}{H_5} + 3NaOH \to 3\overline R COONa + {C_3}{H_5}{(OH)_3} \hfill \\
\xrightarrow{{BTKL}}b = a + {m_{NaOH}} - {m_{{C_3}{H_5}{{(OH)}_3}}} \hfill \\
\end{gathered} \)
Lời giải chi tiết:
X + O2 → CO2 + H2O
a gam 4,83 mol 3,42 mol 3,18 mol
BTKL => a = 3,42.44+3,18.18-4,83.32 = 52,16 gam
BTNT O: nO(X) = 2nCO2+nH2O-2nO2 = 0,36 mol
=> nX = 0,36/6 = 0,06 mol (Vì X chứa 6O)
\(\begin{gathered}
{(\overline R COO)_3}{C_3}{H_5} + 3NaOH \to 3\overline R COONa + {C_3}{H_5}{(OH)_3} \hfill \\
\xrightarrow{{BTKL}}b = a + {m_{NaOH}} - {m_{{C_3}{H_5}{{(OH)}_3}}} = 53,16 + 40.0,18 - 0,06.92 = 54,84\,gam \hfill \\
\end{gathered} \)
Đáp án B
Câu hỏi 7 :
Đốt cháy hoàn toàn m gam một triglixerit X cần vừa đủ x mol O2, sau phản ứng thu được CO2 và y mol H2O. Biết m=78x-103y. Nếu cho a mol X tác dụng với dung dịch nước Br2 dư thì lượng Br2 phản ứng tối đa là 0,15 mol. Giá trị của a là
- A 0,20
- B 0,15
- C 0,08
- D 0,05
Đáp án: D
Phương pháp giải:
Gọi CTTQ của X là CnH2n+2-2kO6 viết PTHH đốt cháy X:
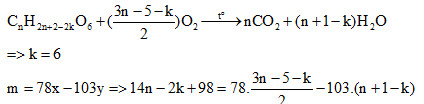
=> k => Số liên kết pi ở gốc hiđrocacbon => a
Lời giải chi tiết:
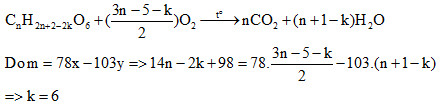
=> Ở gốc hiđrocacbon có 3 liên kết pi
=> nX = nBr2/3 = 0,05 mol
Đáp án D
Câu hỏi 8 :
Đốt cháy hoàn toàn m gam chất béo X (chứa triglixerit của axit stearic,axit panmitic và các axit béo tự do đó). Sau phản ứng thu được 13,44 lít CO2 (đktc) và 10,44 gam nước. Xà phòng hoá m gam X (H=90%) thì thu được khối lượng glixerol là
- A 0,92 gam.
- B 1,656 gam.
- C 0,828 gam.
- D 2,484 gam.
Đáp án: C
Phương pháp giải:
CxH2x-4O6 → xCO2 + (x-2) H2O
a ax a(x-2)
CyH2y O2 → yCO2 + yH2O
b by by
\(\left\{ \begin{array}{l}{\rm{ax}} + by = 0,6\\a(x - 2) + by = 0,58\end{array} \right. \to a\)
Lời giải chi tiết:
CxH2x-4O6 → xCO2 + (x-2) H2O
a ax a(x-2)
CyH2y O2 → yCO2 + yH2O
b by by
\(\left\{ \begin{array}{l}{\rm{ax}} + by = 0,6\\a(x - 2) + by = 0,58\end{array} \right. \to a=0,01\)
nglixerol = ntriglixerit = 0,01 mol
=> mglixerol = 0,01.92 = 0,92 gam
Vì H = 90% => mglixerol = 0,92.90% = 0,828 gam
Đáp án C
Câu hỏi 9 :
Đốt cháy hòan toàn m gam 1 chất béo cần 1,61 mol O2, sinh ra 1,14 mol CO2 và 1,06 mol H2O. Cho 7,088 gam chất béo tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
- A 7,312 gam
- B 7,612 gam
- C 7,412 gam
- D 7,512 gam
Đáp án: A
Phương pháp giải:
Bảo toàn khối lượng tính được khối lượng của chất béo. Bảo toàn nguyên tố O suy ra số mol O trong chất béo. Từ đó suy đó số mol chất béo. Tính được số mol NaOH tham gia phản ứng và áp dụng bảo toàn khối lượng suy ra khối lượng muối.
Lời giải chi tiết:
Bảo toàn khối lượng m = 1,14.44+ 1,06.18 – 1,61.32 = 17,72 g
Bảo toàn nguyên tố O suy ra nO (chất béo) = 2.1,14+1,06 – 1,61.2=0,12 mol
Suy ra nchất béo = 0,12/6 = 0,02 mol
nNaOH = 3.nchất béo =0,06 mol, nGlixerol =0,02 mol
Áp dụng bảo toàn khối lượng: mmuối = 17,72+0,06.40 – 0,02.92=18,28 gam
Suy ra nếu cho 7,088 gam chất béo tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là 7,312 gam
Đáp án A
Câu hỏi 10 :
Đốt cháy hoàn toàn 0,06 mol hỗn hợp X gồm ba triglixerit cần vừa đủ 4,77 mol O2, thu được 3,14 mol H2O. Mặt khác, hiđro hóa hoàn toàn 78,9 gam X (xúc tác Ni, to), thu được hỗn hợp Y. Đun nóng Y với dung dịch KOH vừa đủ, thu được glixerol và m gam muối. Giá trị của m là
- A 86,10.
- B 57,40.
- C 83,82.
- D 57,16.
Đáp án: A
Phương pháp giải:
- Bảo toàn O: 6nX + 2nO2 = 2nCO2 + nH2O => nCO2 = ?
- Bảo toàn khối lượng: mX + mO2 = mCO2 + mH2O => mX = ?
- \({n_X} = {\rm{ }}{{{n_{H2}}_O - {\rm{ }}{n_C}_{O2}} \over {1{\rm{ }} - {\rm{ }}k}} = > {\rm{ }}k{\rm{ }} = {\rm{ }}5\)
=> X cộng được 2H2
\({M_X} = {{{m_X}} \over {{n_X}}} = ?\)
- X + 2H2 →Y
=> mY = mX + mH2 = ?
Y + 3KOH → Muối + C3H5(OH)3
Bảo toàn khối lượng => m muối = mY + mKOH - mC3H5(OH)3 = ? gam
Lời giải chi tiết:
- Bảo toàn O: 6nX + 2nO2 = 2nCO2 + nH2O => nCO2 = 3,38
- Bảo toàn khối lượng: mX + mO2 = mCO2 + mH2O => mX = 52,6
- \({n_X} = {\rm{ }}{{{n_{H2}}_O - {\rm{ }}{n_C}_{O2}} \over {1{\rm{ }} - {\rm{ }}k}} = > {\rm{ }}k{\rm{ }} = {\rm{ }}5\)
=> X cộng được 2H2
\({M_X} = {{{m_X}} \over {{n_X}}} = {{52,6} \over {0,06}}\)
Khi mX = 78,9 thì nX = 0,09:
- X + 2H2 →Y
=> mY = mX + mH2 = 79,26
Y + 3KOH → Muối + C3H5(OH)3
Bảo toàn khối lượng => m muối = mY + mKOH - mC3H5(OH)3 = 86,1 gam
Đáp án A
Câu hỏi 11 :
Đốt cháy hoàn toàn 0,1 mol một chất béo X thu được CO2 và H2O hơn kém nhau 0,6 mol. Thể tích dung dịch Br2 0,5M tối đa để phản ứng hết với 0,03 mol chất béo X là
- A 120 ml.
- B 240 ml.
- C 360 ml.
- D 160 ml.
Đáp án: B
Phương pháp giải:
Đốt cháy hợp chất hữu cơ X : CxHyOz có độ bất bão hòa k ta có:
\({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}}\)
Theo dữ kiện đề bài => k = ?
nBr2 = nliên kết pi mach ngoài
Lời giải chi tiết:
Gọi công thức của chất béo là: (RCOO)3C3H5: 0,1 (mol)
Gọi k là số liên kết pi có trong chất béo
Áp dụng công thức ta có:
\(\begin{gathered}
{n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \hfill \\
\Rightarrow 0,1 = \frac{{0,6}}{{k - 1}} \hfill \\
\Rightarrow k = 7 \hfill \\
\end{gathered} \)
Vì X là chất béo (là este của glixerol và các axit béo) => có 3 liên kết pi trong 3 nhóm –COO trong phân tử.
=> còn 4 liên kết pi ngoài mạch C
=> 1 mol X có thể công tối đa với 4 mol C
=> 0,03 mol chất béo X có thể cộng tối đa với 0,03.4 = 0,12 (mol) Br2
=> VBr2 = nBr2: CM = 0,12 : 0,5 = 0,24 (lít) = 240 (ml)
Đáp án B
Câu hỏi 12 :
Đốt cháy 34,32 gam chất béo X bằng lượng oxi vừa đủ, thu được 96,8 gam CO2 và 36,72 gam H2O. Mặt khác 0,12 mol X làm mất màu tối đa V ml dung dịch Br2 1M. Giá trị của V là
- A 120 ml.
- B 360 ml.
- C 240 ml.
- D 480 ml.
Đáp án: C
Phương pháp giải:
Tính số mol CO2 và H2O từ đó suy ra số mol C và H.
mO(X) = mX – mC – mH => nO(X)
=> nX = nO(X) : 6
Xác định số C và H trong X.
Vậy CTPT của X là C55H102O6 có k = (2C + 2 – H) : 2 = ?
Mà có chứa 3 liên kết π trong gốc COO nên ở ngoài gốc hidrocacbon còn (k – 3) liên kết π.
Lời giải chi tiết:
nCO2 = 2,2 mol => nC = 2,2 mol; nH2O = 2,04 mol => nH = 4,08 mol
mO(X) = mX – mC – mH = 34,32 – 2,2.12 – 2,04.2 = 3,84 gam => nO(X) = 3,84 : 16 = 0,24 mol
=> nX = nO(X) : 6 = 0,04 mol
Số C = 2,2 : 0,04 = 55
Số H = 4,08 : 0,04 = 102
Vậy CTPT của X là C55H102O6 có k = (2C + 2 – H) : 2 = (2.55 + 2 – 102) : 2 = 5
Mà có chứa 3 liên kết π trong gốc COO nên ở ngoài gốc hidrocacbon còn 2 liên kết π.
Do đó 1 phân tử X có khả năng với 2 phân tử Br2.
=> nBr2 = 2nX = 2.0,12 = 0,24 mol
Đáp án C
Câu hỏi 13 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của b là
- A 53,16
- B 57,12
- C 60,36
- D 54,84
Đáp án: D
Phương pháp giải:
*Phản ứng cháy:
BTKL: mX = mCO2 + mH2O – mO2 = ?
BTNT “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = ?
=> nX = nO(X) : 6 = ?
*Phản ứng thủy phân trong NaOH:
X + 3NaOH → Muối + C3H5(OH)3
nNaOH = 3nX = ?
nGlixerol = nX = ?
BTKL: m muối = mX + mNaOH – mglixerol = ?
Lời giải chi tiết:
*Phản ứng cháy:
BTKL: mX = mCO2 + mH2O – mO2 = 3,42.44 + 3,18.18 – 4,83.32 = 53,16 gam
BTNT “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = 3,42.2 + 3,18 – 4,83.2 = 0,36 mol
=> nX = nO(X) : 6 = 0,36 : 6 = 0,06 mol
*Phản ứng thủy phân trong NaOH:
X + 3NaOH → Muối + C3H5(OH)3
nNaOH = 3nX = 0,06.3 = 0,18 mol
nGlixerol = nX = 0,06 mol
BTKL: m muối = mX + mNaOH – mglixerol = 53,16 + 0,18.40 – 0,06.92 = 54,84 gam
Đáp án D
Câu hỏi 14 :
Đốt cháy hoàn toàn m gam một triglixerit X cần dùng 1,61 mol O2, thu được 1,14 mol CO2 và 1,06 mol H2O. Cho 26,58 gam X tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
- A 18,28 gam.
- B 27,14 gam.
- C 27,42 gam.
- D 25,02 gam.
Đáp án: C
Phương pháp giải:
Bảo toàn nguyên tố O ta có: nO(X) = 2nCO2 + nH2O – 2nO2 → nCOOH(X)
Bảo toàn khối lượng ta có
mX + mO2 = mCO2 + mH2O → m
Tính tỉ lệ suy ra số mol COOH trong 26,58 gam X => nNaOH và n glixerol
Bảo toàn khối lượng: m muối = mX + mNaOH – mC3H5(OH)3
Lời giải chi tiết:
Bảo toàn nguyên tố O ta có
→ nO(X) = nO(X) = 2nCO2 + nH2O – 2nO2 = 0,12 → nCOOH(X) = 0,06 mol
Bảo toàn khối lượng ta có
mX + mO2 = mCO2 + mH2O → m + 1,61.32 = 1,14.44 + 1,06.18 → m = 17,72 g
17,72 g X có 0,06 mol COOH → 26,58 g X có 0,09 mol COOH
→ 26,58 g X + 0,09 mol NaOH → muối + 0,03 mol C3H5(OH)3
Bảo toàn khối lượng: m muối = mX + mNaOH – mC3H5(OH)3 = 26,58 + 0,09.40 – 0,03.92 = 27,42 gam
Đáp án C
Câu hỏi 15 :
Đốt cháy hoàn toàn m gam triglixerit X cần 1,61 mol O2, sinh ra 1,14 mol CO2 và 1,06 mol H2O. Cho 7,088 gam X tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
- A 7,312 gam.
- B 7,412 gam.
- C 7,612 gam.
- D 7,512 gam.
Đáp án: A
Phương pháp giải:
*Phản ứng đốt cháy m gam X:
BTNT “O”: nO(X) = 2nCO2 + nH2O – 2nO2
=> nX = nO(X) : 6
mX = mCO2 + mH2O – mO2
Tỉ lệ: mX = ? gam X tương ứng với nX = ? mol
=> 7,088 gam ? mol
=> nNaOH = 3nX; nglixerol = nX
BTKL: m muối = mX + mNaOH – m glixerol
Lời giải chi tiết:
*Phản ứng đốt cháy m gam X:
BTNT “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = 1,14.2 + 1,06 – 1,61.2 = 0,12 mol
=> nX = nO(X) : 6 = 0,02 mol
mX = mCO2 + mH2O – mO2 = 1,14.44 + 1,06.18 – 1,61.32 = 17,72 gam
Tỉ lệ: 17,72 gam X tương ứng với 0,02 mol X
=> 7,088 gam 0,008 mol
=> nNaOH = 3nX = 0,008.3 = 0,024 mol; nglixerol = nX = 0,008 mol
BTKL: m muối = mX + mNaOH – m glixerol = 7,088 + 0,024.40 – 0,008.92 = 7,312 gam
Đáp án A
Câu hỏi 16 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch NaOH, thu được b gam muối. Giá trị của b là
- A 57,12.
- B 53,16.
- C 60,36.
- D 54,84.
Đáp án: D
Phương pháp giải:
BTNT: “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = ? (mol)=> nX = 1/6nO(X) = ? (mol)
BTKL ta có: a = mX = mC + mH + mO = ? (g)
Đặt công thức chung của X: (RCOO)3C3H5
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
mmuối = mX + mNaOH – mC3H5(OH)3 = ?
Lời giải chi tiết:
BTNT: “O”: nO(X) = 2nCO2 + nH2O – 2nO2 = 3,42.2 + 3,18.1 – 4,83.2 = 0,36 (mol)
=> nX = 1/6nO(X) = 0,36/6 = 0,06 (mol)
BTKL ta có: a = mX = mC + mH + mO = 3,42.12 + 2.3,18 + 0,36.16 = 53,16 (g)
Đặt công thức chung của X: (RCOO)3C3H5
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
0,06 → 0,18 → 0,06 (mol)
mmuối = mX + mNaOH – mC3H5(OH)3 = 53,16 + 0,18.40 – 0,06.92 = 54,84 (g)
Đáp án D
Câu hỏi 17 :
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác, khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư nung nóng, thu được dung dịch chứa a gam muối. Giá trị của a là
- A 8,34
- B 7,63
- C 4,87
- D 9,74
Đáp án: A
Phương pháp giải:
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3
mdd giảm = mkết tủa - mH2O – mCO2 → nH2O
→ X có nC = nCO2 và nH = 2nH2O → CTPT của X
Bảo toàn khối lượng tìm mmuối
Lời giải chi tiết:
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3 = 0,255 mol
mdd giảm = mkết tủa - mH2O – mCO2 → 25,5 - mH2O - 0,255.44 = 9,87 → nH2O = 0,245 mol
→ X có nC = nCO2 =0,255 mol và nH = 2nH2O = 2.0,245 =0,49 mol
→ nO = \(\frac{{4,03 - 0,255.12 - 0,49.1}}{{16}} = 0,03\) mol
Vì X là triglixerit nên X có 6 O trong CTPT → \({n_X} = \frac{{{n_O}}}{6} = 0,005 \Rightarrow \left\{ \begin{gathered}C = \frac{{0,255}}{{0,005}} = 51 \hfill \\H = \frac{{0,49}}{{0,005}} = 98 \hfill \\\end{gathered} \right.\)
→ X : C51H98O6
Xét 8,06 g X + NaOH → muối + glixerol thì
nX = \(\frac{{8,06}}{{12.51 + 98.1 + 16.6}} = 0,01\) →nNaOH = 3nX =0,03 mol và nglixerol = nX = 0,01 mol
Bảo toàn khối lượng có mmuối = mX + mNaOH – mglixerol = 8,06 + 0,03.40 – 0,01 .92 =8,34 g
Đáp án A
Câu hỏi 18 :
Đốt cháy hoàn toàn m gam chất béo X (chứa triglixerit của axit stearic, axit panmitic). Sau phản ứng thu được 20,16 lit khí CO2 (dktc) và 15,66g nước . Xà phòng hóa m gam X (H = 90%) thì thu được khối lượng glyxerol là :
- A 2,760g
- B 1,242g
- C 1,380g
- D 2,484g
Đáp án: B
Phương pháp giải:
Biện luận công thức este dựa vào số liên kết pi trong phân tử
=> CnH2n+2-2kO2m (m là số nhóm COO ; k là số liên kết pi trong phân tử)
Bài toán hiệu suất : mThực tế = mLT.H%
Lời giải chi tiết:
Este của axit no đơn chức (axit stearic và axit panmitic) và glyxerol
=> este này có 3 liên kết pi nằm trong 3 nhóm COO-
=> Công thức tổng quát của este là CnH2n - 4O6
- Phản ứng cháy : CnH2n – 4O6 + O2 → nCO2 + (n – 2)H2O
- Theo phương trình, nCO2 – nH2O = 2neste
Có : nCO2 = 20,16 : 22,4 = 0,9 mol ; nH2O = 15,66 : 18 = 0,87 mol
=> neste = ½ (0,9 – 0,87) = 0,015 mol
- Phản ứng xà phòng hóa : Este + 3NaOH → 3Muối + Glycerol
Mol 0,015 → 0,015
Vì hiệu suất phản ứng là 90% => nGlycerol thực = nGlycerol LT. H% = 0,015.90% = 0,0135 mol
=> mGlyxerol = 0,0135.92 = 1,242g
Đáp án B
Câu hỏi 19 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,26 mol O2, thu được 2,28 mol CO2 và 39,6 gam nước. Mặt khác thủy phân hoàn toàn a gam X trong dung dịch NaOH đun nóng, thu được dung dịch chứa b gam muối. Giá trị của b là
- A 31,92
- B 36,72
- C 40,40
- D 35,60
Đáp án: B
Phương pháp giải:
a g X + 3,26 mol O2 → 2,28 mol CO2 + 39,6 gam nước
Bảo toàn khối lượng → a
Bảo toàn nguyên tố O → nX
X + 3NaOH → muối + C3H5(OH)3
Bảo toàn khối lượng → mmuối
Lời giải chi tiết:
Ta có a g X + 3,26 mol O2 → 2,28 mol CO2 + 39,6 gam nước
Bảo toàn khối lượng có a + 3,26.32 = 2,28.44 + 39,6 → a = 35,6 gam
Bảo toàn nguyên tố O có nO(X) + 2nO2 = 2nCO2 + nH2O → nO(X) + 2.3,26 = 2.2,28 + 2,2 → nO(X) = 0,24 mol
Vì X là triglixerit nên X chứa 6 O trong công thức phân tử nên nX = 0,04 mol
Ta có a gam X + 3NaOH → muối + C3H5(OH)3
Ta có nNaOH = 3nX = 3.0,04 =0,12 mol
nC3H5(OH)3 = 0,04 mol
Bảo toàn khối lượng có mX + mNaOH =mmuối + mC3H5(OH)3 → 35,6 + 0,12.40 = 0,04.92 + mmuối → mmuối = 36,72 g
Đáp án B
Câu hỏi 20 :
Đốt cháy hoàn toàn m gam chất béo no X thu được 4,539 mol CO2 và 4,361 mol H2O. Thủy phân hết m gam X trong dung dịch NaOH thu được 74,226 gam muối. Tổng số nguyên tử trong X là
- A 57
- B 155
- C 173
- D 806
Đáp án: B
Phương pháp giải:
Gọi số mol của X là a mol và số mol O2 là b mol
X + O2 → CO2 +H2O
Bảo toàn khối lượng có m + mO2 = mCO2 + mH2O →pt (1)
Bảo toàn O có pt (2)
X + 3a mol NaOH → muối + a mol C3H5(OH)3
Bảo toàn khối lượng có pt(3)
Giải (1),(2),(3) có m ; a và b → MX = 806 → xác định CTPT của X
Lời giải chi tiết:
Gọi số mol của X là a mol và số mol O2 là b mol
X + O2 → CO2 +H2O
Bảo toàn khối lượng có m + mO2 = mCO2 + mH2O →m + 32b = 44.4,539 + 4,361.18 = 278,214 (1)
Bảo toàn O có 6a + 2b = 2.4,539 + 4,361 = 13,439 (2)
X + 3a mol NaOH → muối + a mol C3H5(OH)3
Bảo toàn khối lượng có m + 3a.40 = 74,226 + 92a (3)
Giải (1),(2),(3) có m = 71,734; a= 0,089 mol và b = 6,4525 mol
→ MX = 806
X có số C = nCO2 :nX = 4,539 : 0,089 = 51
Số H = 2nH2O : nX = 2.4,361 : 0,089 = 98
→ số O = (806 – 12.51 – 98 ) : 16 = 6
→ tổng số nguyên tử tron X là 51 + 98 + 6 = 155
Đáp án B
Câu hỏi 21 :
Đốt cháy hoàn toàn m gam một triglixerit X cần 9,016 lít O2 thu được 6,384 lít CO2 và 4,77 g H2O. Mặt khác m gam X phản ứng vừa đủ với x gam Brom (trong dung môi CCl4). Biết thể tích các khí đo ở đktc. Giá trị của x là:
- A 1,6
- B 5,6
- C 4,8
- D 3,2
Đáp án: A
Phương pháp giải:
- Gọi công thức của X là (RCOO)3C3H5 có k liên kết pi
Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O
=> nO(X) => nX
Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k
Có 3 pi trong 3 gốc COO => số liên kết pi còn lại sẽ nằm trong gốc hidrocacbon (Có thể phản ứng được với Br2/CCl4)
=> số mol Br2 => x
Lời giải chi tiết:
- Gọi công thức của X là (RCOO)3C3H5 có k liên kết pi
nO2 = 9,016 : 22,4 = 0,4025 mol ; nCO2 = 6,384 : 22,4 = 0,285 mol ; nH2O = 0,265 mol
Bảo toàn nguyên tố O: nO(X) + 2nO2 = 2nCO2 + nH2O
=> nO(X) = 0,03 mol = 6n(X) => nX = 0,005 mol
Mặt khác: (k – 1).nX = (nCO2 – nH2O) => k = 5
Có 3 pi trong 3 gốc COO => 2 pi còn lại sẽ nằm trong gốc hidrocacbon (Có thể phản ứng được với Br2/CCl4)
=> nBr2 = 2.nX = 2.0,005 = 0,01 mol
=> mBr2 = x = 0,01.160 = 1,6g
Đáp án A
Câu hỏi 22 :
X là Trieste của một ancol no mạch hở và 3 axit cacboxylic mạch hở đơn chức. Đốt cháy hoàn toàn a mol X thu được b mol CO2 và c = 0,5 mol H2O. Biết rằng b – c = 5a. Mặt khác a mol X phản ứng tối đa với dung dịch chứa 0,15 mol Br2. Đốt cháy hoàn toàn 5,92 gam X cần V lít khí O2 đktc. Giá trị của V là
- A 5,712 lít
- B 4,032 lít
- C 7,616 lít
- D 4,3008 lít
Đáp án: C
Phương pháp giải:
áp dụng công thức tính độ bất bão hòa k đối với 1 chất hữu cơ CxHyOz: a (mol)
Ta có \({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \to a = \frac{{b - c}}{{k - 1}} \to a = \frac{{5a}}{{k - 1}} \Rightarrow k = 6\) → X có 6 liên kết pi trong đó có 3 liên kết pi trong nhóm COO, 3 liên kết pi trong gốc axit → X + 3Br2 → a → b
X + O2 → CO2 +H2O
Bảo toàn O → nO2
Bảo toàn khối lượng → mX
Lời giải chi tiết:
áp dụng công thức tính độ bất bão hòa k đối với 1 chất hữu cơ CxHyOz: a (mol)
Ta có \({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \to a = \frac{{b - c}}{{k - 1}} \to a = \frac{{5a}}{{k - 1}} \Rightarrow k = 6\) → X có 6 liên kết pi trong đó có 3 liên kết pi trong nhóm COO, 3 liên kết pi trong gốc axit
→ X + 3Br2 → nX = 0,15 : 3 =0,05 mol = a
→ b = 5a + c = 5.0,05 + 0,5 = 0,75 mol
X + O2 → CO2 +H2O
Bảo toàn O có 6nX + 2nO2 = 2nCO2 + nH2O = 2.0,75 + 0,5 = 2 → nO2 = (2 – 6.0,05) : 2 = 0,85 mol
Bảo toàn khối lượng mX + mO2 = mCO2 + mH2O → mX + 0,85.32 = 0,75.44 + 0,5.18 →mX = 14,8 g
5,92 g X có n = 5,92 : 14,8 . 0,05 = 0,02 mol
→nO2 = 0,02 : 0,05 . 0,85 = 0,34 mol → V = 7,616 lít
Đáp án C
Câu hỏi 23 :
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác, khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH (dư) đun nóng, thu được dung dịch chứa m gam muối. Giá trị của m là
- A 4,87.
- B 8,34.
- C 7,63.
- D 9,74.
Đáp án: A
Phương pháp giải:
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3
mdd giảm = mkết tủa - mH2O – mCO2 → nH2O
→ X có nC = nCO2 và nH = 2nH2O → CTPT của X
Bảo toàn khối lượng tìm mmuối
Lời giải chi tiết:
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3 = 0,255 mol
mdd giảm = mkết tủa - mH2O – mCO2 → 25,5 - mH2O - 0,255.44 = 9,87 → nH2O = 0,245 mol
→ X có nC = nCO2 =0,255 mol và nH = 2nH2O = 2.0,245 =0,49 mol
→ nO = \(\frac{{4,03 - 0,255.12 - 0,49.1}}{{16}} = 0,03\) mol
Vì X là triglixerit nên X có 6 O trong CTPT
→ \({n_X} = \frac{{{n_O}}}{6} = 0,005 \Rightarrow \left\{ \begin{gathered}
C = \frac{{0,255}}{{0,005}} = 51 \hfill \\
H = \frac{{0,49}}{{0,005}} = 98 \hfill \\
\end{gathered} \right.\)
→ X : C51H98O6
Xét 8,06 g X + NaOH → muối + glixerol thì
nX = \(\frac{{8,06}}{{12.51 + 98.1 + 16.6}} = 0,01\) → nNaOH = 3nX =0,03 mol và nglixerol = nX = 0,01 mol
Bảo toàn khối lượng có mmuối = mX + mNaOH – mglixerol = 8,06 + 0,03.40 – 0,01 .92 =8,34 g
Đáp án A
Câu hỏi 24 :
Đốt cháy hoàn toàn 13,728 gam một triglixerit X cần vừa đủ 27,776 lít O2 (đktc) thu được số mol CO2 và số mol H2O hơn kém nhau 0,064. Mặt khác, hiđro hóa hoàn toàn một lượng X cần 0,096 mol H2 thu được m gam chất hữu cơ Y. Xà phòng hóa hoàn toàn m gam Y bằng dung dịch NaOH thu được dung dịch chứa a gam muối. Giá trị của a là
- A 11,424.
- B 42,720.
- C 41,376.
- D 42,528.
Đáp án: B
Phương pháp giải:
X + O2 → x mol CO2 + y mol H2O
Bảo toàn khối lượng có mX + mO2 = mCO2 + mH2O → pt ẩn x và y
Mà x – y = 0,064 mol nên giải được x và y
Bảo toàn O có nO(X) + 2nO2 = 2nCO2 + nH2O → nO(X) → nX → MX
Lập CTPT của X theo nCO2 và nH2O → số liên kết ∏ của X → tỉ lệ của X với H2 phản ứng
X + 0,096 mol H2 → Y → nX =nY → mX →mY
Y + 3NaOH → a gam muối + C3H5(OH)3 → BTKL : mmuối
Lời giải chi tiết:
X + O2 → x mol CO2 + y mol H2O
nO2 = 1,24 mol
Bảo toàn khối lượng có mX + mO2 = mCO2 + mH2O → 13,728 + 1,24.32 = 44x + 18y (1)
Mà x – y = 0,064 mol nên x = 0,88 mol và y = 0,816 mol
Bảo toàn O có nO(X) + 2nO2 = 2nCO2 + nH2O → nO(X) = 2.0,88 + 0,816 – 2.1,24 =0,096 mol
Vì X là triglixerit nên nO(X) = 6nX → nX = 0,016 mol → MX = 13,728 : 0,016 = 858 (g/mol)
X có số C = nCO2 : nX = 55 và số H = 2nH2O : nX = 102 → X là C55H102O6
→ X cộng tối đa với 2H2 → no
X + 0,096 mol H2 → Y → nX = 0,048 mol → mX =41,184 gam→mY = 41,184 + 0,096.2 =41,376 gam và nY =nX =0,048 mol
Y + 3NaOH → a gam muối + C3H5(OH)3
nNaOH = 3nY = 0,048.3 =0,144 mol và nC3H5(OH)3 = 0,048 mol
→ BTKL : mmuối = mY + mNaOH – mC3H5(OH)3 = 41,376 + 0,144.40 – 0,048.92 = 42,72 gam
Đáp án B
Câu hỏi 25 :
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư đun nóng thu được dung dịch chứa a gam muối. Giá trị của a là
- A 7,63
- B 4,87
- C 9,74
- D 8,34
Đáp án: D
Phương pháp giải:
Xét phản ứng 4,03 g X +O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
Bảo toàn nguyên tố C → nCO2
Lập phương trình mdd giảm → mH2O
BTKL → mO2 → bảo toàn O → nO(X) → nX = 1/6 .nO(X)
→ số mol của 8,06 g X
BTKL mmuối = mX + mNaOH – mC3H5(OH)3
Lời giải chi tiết:
Xét phản ứng 4,03 g X +O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
→ nCaCO3 = nCO2 = 0,255 mol
mdd giảm = - mCO2 - mH2O + mCaCO3 = - 0,255.44 – mH2O + 25,5 = 9,87 → mH2O = 4,41 gam → nH2O = 0,245 mol
BTKL có mO2 = mCO2 + mH2O – mX = 0,255.44 + 4,41 – 4,03 = 11,6 g → nO2= 0,3625 mol
Bảo toàn O có 2nO2 + nO(X) = 2nCO2 + nH2O → nO(X) = 0,03 mol
Vì X là triglixerit nên nX = 1/6 .nO(X) = 0,005 mol
→ 8,06 g X có số mol là 0,005.8,06 : 4,03 = 0,01 mol
0,01 mol X + 0,03 mol NaOH → muối + 0,01 mol C3H5(OH)3
BTKL mmuối = mX + mNaOH – mC3H5(OH)3 = 8,06 + 0,03.40 – 0,01.92 = 8,34 gam
Đáp án D
Câu hỏi 26 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 0,32 mol O2 thu được 0,228 mol CO2 và 0,208 mol H2O. Mặt khác, cho a gam X vào 45 ml dung dịch hỗn hợp gồm NaOH 0,1M và KOH 0,1M sau phản ứng hoàn toàn cô cạn dung dịch thu được chất rắn chứa m gam muối khan. Giá trị của m là
- A 3,768.
- B 3,712.
- C 2,808.
- D 3,692.
Đáp án: C
Phương pháp giải:
BTNT "O": 6nX + 2nO2 = 2nCO2 + nH2O → nX = ? (mol)
BTKL ta có: mX + mO2 = mCO2 + mH2O → a = ? (g)
→ Phân tử khối của X là: MX = ? (g/mol)
Đặt CTPT của X có dang: (RCOO)3C3H5
Ta thấy: nX > 3nOH- → bazo pư hết, X dư. Mọi tính toán theo số mol OH-
(RCOO)3C3H5 + 3OH- → 3RCOO- + C3H5(OH)3
BTKL ta có: mX pư + mNaOH + mKOH = mmuối + mC3H5(OH)3
Lời giải chi tiết:
BTNT "O": 6nX + 2nO2 = 2nCO2 + nH2O → nX = (0,228.2 + 0,208 - 2.0,32)/6 = 0,004 (mol)
BTKL ta có: mX + mO2 = mCO2 + mH2O → a + 0,32.32 = 0,228.44 + 0,208.18 → a = 3,536 (g)
→ Phân tử khối của X là: MX = 3,536 : 0,004 = 884 (g/mol)
nKOH = nNaOH = 0,045.0,1 = 0,0045 (mol) → ∑ nOH- = 0,009 (mol)
Đặt CTPT của X có dang: (RCOO)3C3H5: 0,004 (mol)
Ta thấy: nX > 3nOH- → bazo pư hết, X dư. Mọi tính toán theo số mol OH-
(RCOO)3C3H5 + 3OH- → 3RCOO- + C3H5(OH)3
0,003 ← 0,009 → 0,003 (mol)
→ nX pư = nC3H5(OH)3 = nOH-/3 = 0,003 (mol)
BTKL ta có: mX pư + mNaOH + mKOH = mmuối + mC3H5(OH)3
→ 0,003.884 + 0,0045. 40 + 0,0045.56 = mmuối + 0,003.92
→ mmuối = 2,808 (g)
Đáp án C
Câu hỏi 27 :
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 7,8 mol O2 thu được 5,5 mol CO2 và 5,2 mol H2O. Mặt khác cho a gam X phản ứng với vừa đủ dung dịch Br2. Số mol Br2 tham gia phản ứng là:
- A 0,2
- B 0,1
- C 0,4
- D 0,3
Đáp án: B
Phương pháp giải:
Bảo toàn nguyên tố oxi: nO(X) + 2nO2 = 2nCO2 + nH2O => nO(X) => nX
Gọi số liên kết pi trong X là k
=> Khi đốt cháy X thì thu được sản phẩm: nCO2 – nH2O = (k – 1)nX => k
Biện luận => số liên kết pi có thể phản ứng được với Br2 => nBr2
Lời giải chi tiết:
Bảo toàn nguyên tố oxi: nO(X) + 2nO2 = 2nCO2 + nH2O
=> nO(X) = 0,6 mol
Vì X là triglixerit => 3 nhóm COO => 6 nguyên tử oxi
=> nX = 1/6.nO(X) = 0,1 mol
Gọi số liên kết pi trong X là k
=> Khi đốt cháy X thì thu được sản phẩm: nCO2 – nH2O = (k – 1)nX
=> k = 4. Có 3 liên kết pi trong 3 nhóm COO
=> có 1 liên kết pi ở gốc hiđrocacbon (C=C)
=> nBr2 = nX = 0,1 mol
Đáp án B
Câu hỏi 28 :
Đốt cháy hoàn toàn 17,16 gam triglixerit X, thu được H2O và 1,1 mol CO2. Cho 17,16 gam X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và m gam muối. Mặt khác, 17,16 gam X tác dụng được tối đa với 0,04 mol Br2 trong dung dịch. Giá trị của m là
- A 18,28.
- B 18,48.
- C 16,12.
- D 17,72.
Đáp án: D
Phương pháp giải:
- Bảo toàn khối lượng
- Sử dụng công thức: nCO2 - nH2O = (k-1).nX
Lời giải chi tiết:
Đặt số mol H2O là a mol, số mol của X là b mol, k là số liên kết pi.
+ nCO2 - nH2O = (k-1).nX => 1,1 - a = (k - 1).b (1)
+ nBr2 = (k - 3).b = 0,04 (2)
+ BTKL: mX = mC + mH + mO => 12.1,1 + 2a + 16.6b = 17,16 (3)
Từ (1), (2) và (3) => a = 1,02; b = 0,02; k = 5
- Xét phản ứng thủy phân:
nGlixerol = nX = 0,02 mol; nNaOH = 3nX = 0,06 mol
BTKL: mX + mNaOH = m muối + m Glixerol => 17,16 + 0,06.40 = m + 0,02.92 => m = 17,72 gam
Đáp án D
Câu hỏi 29 :
Đốt cháy hoàn toàn 13,728 gam triglixerit X, thu được a mol hỗn hợp Y gồm CO2 và H2O. Cho toàn bộ hỗn hợp Y qua cacbon nung đỏ, thu được 2,364 mol hỗn hợp Z gồm CO, H2 và CO2. Cho hỗn hợp Z qua dung dịch Ba(OH)2 dư thu được 202,516 gam kết tủa. Cho 13,728 gam X tác dụng được tối đa với 0,032 mol Br2 trong dung dịch. Giá trị của m là
- A 14,648
- B 14,784
- C 14,176
- D 14,624
Đáp án: C
Phương pháp giải:
- Tính số mol CO2 từ số mol kết tủa
- Suy ra tổng số mol CO và H2
- Áp dụng bảo toàn electron, tìm số mol C
- Suy ra giá trị của a.
- Quy đổi hỗn hợp X thành (HCOO)3C3H5, CH2 và H2O
- Lập phương trình khối lượng X (1)
- Lập phương trình giá trị của a (2)
- Từ (1) và (2) tìm ra số mol (HCOO)3C3H5 và CH2
- Tìm số mol NaOH và glixerol.
- Bảo toàn khối lượng để tìm khối lượng muối
Lời giải chi tiết:
Dẫn hỗn hợp Z qua dung dịch Ba(OH)2 dư thì \({n_{C{O_2}}} = {n_{BaC{{\rm{O}}_3}}} = 1,028\,\,mol\)
\( \to {n_{CO}} + {n_{{H_2}}} = 2,364 - 1,028 = 1,336\)mol
Xét quá trình trao đổi electron của phản ứng giữa C với CO2 và H2O
C → C+4 + 4eC+4 + 2e → C+2
2H+ + 2e → H2
Áp dụng bảo toàn electron: \(4{n_C} = 2{n_{CO}} + 2{n_{{H_2}}}\)
\( \to {n_C} = \frac{{2.1,336}}{4} = 0,668\,\,mol\)
→ a = 2,364 – 0,668 = 1,696 mol
Quy đổi hỗn hợp X thành (HCOO)3C3H5 (x mol), CH2 (y mol) và H2 (-0,032 mol)
→ mX = 176x + 14y – 0,032.2 = 13,728 (1)
\({n_{C{O_2}}} + {n_{{H_2}O}} = (6{\rm{x}} + y) + (4{\rm{x}} + y - 0,032) = 1,696\)(2)
Từ (1) và (2) → x = 0,016 mol; y = 0,784 mol
Ta có: nNaOH = 3x = 0,048 mol; \({n_{{C_3}{H_5}{{(OH)}_3}}} = x = 0,016\,\,mol\)
Áp dụng bảo toàn khối lượng cho phản ứng: mX + mNaOH = mmuối + mglixerol
→ mmuối = 13,728 + 0,048.40 – 92.0,016 = 14,176 gam
Đáp án C
Câu hỏi 30 :
Đốt cháy hoàn toàn x mol một triglixerit X cần vừa đủ 0,77 mol khí O2 thu được 9,00 gam H2O. Nếu thủy phân hoàn toàn x mol X trong dung dịch KOH đun nóng thu được dung dịch chứa 9,32 gam muối. Mặt khác, hiđro hóa hoàn toàn 0,15 mol X thu được m gam triglixerit Y. Giá trị của m là
- A
129,30.
- B
130,20.
- C
133,50.
- D
128,40.
Đáp án: A
Phương pháp giải:
Sử dụng phương pháp ankan hóa
Lời giải chi tiết:
\(\mathop X\limits_{x\left( {mol} \right)} \xrightarrow{{ + {H_2}:a}}\mathop {X'}\limits_{x\left( {mol} \right)} \left( {CB\,no} \right)\)
H2 + ½ O2 → H2O
a → 0,5a → a
Đốt X' thì: nO2 = 0,77 + 0,5a (mol) và nH2O = 0,5 + a (mol)
Vì X' là chất béo no nên ta có: \({n_{X'}} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{2} \to {n_{C{O_2}}} = 2{n_{X'}} + {n_{{H_2}O}} = 2{\rm{x}} + 0,5 + a\left( {mol} \right)\)
Bảo toàn O → 6x + 2.(0,77 + 0,5a) = 2.(2x + 0,5 + a) + (0,5 + a) (1)
Mặt khác, \(X':x + KOH:3{\rm{x}} \to {{\rm{C}}_3}{H_5}{\left( {OH} \right)_3}:x + Muoi:\left( {9,32 + 2a} \right)g\)
Bảo toàn khối lượng ⟹ 44.(2x + 0,5 + a) + 18.(0,5 + a) - 32.(0,77 + 0,5a) + 3x.56 = 92x + 9,32 + 2a (2)
Giải hệ (1) (2) được x = 0,01 và a = 0,03
⟹ mX' = 92x + (9,32 + 2a) - 56.3x = 8,62 gam
Tỷ lệ:
0,01 mol X … 8,62 gam X'
0,15 mol → 129,3 gam
Đáp án A
15 bài tập vận dụng cao về chất béo đầy đủ các dạng có đáp án và lời giải chi tiết
20 bài tập vận dụng cao về chất béo đầy đủ các dạng từ trắc nghiệm đến tự luận có đáp án và lời giải chi tiết
40 bài tập vận dụng về phản ứng thủy phân chất béo đầy đủ các dạng từ dễ đến khó có đáp án và lời giải chi tiết.
40 câu hỏi mức độ thông hiểu về lý thuyết lipit, chất béo đầy đủ các dạng từ dễ đến khó có đáp án và lời giải chi tiết
40 câu hỏi lý thuyết mức độ nhận biết về lipit, chất béo có đáp án và lời giải chi tiết
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 15 bài toán cho từ từ axit vào muối cacbonat có lời giải
- 15 bài toán cho từ từ muối cacbonat vào axit có lời giải
- 50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có lời giải
- 20 bài tập CO2 tác dụng với dung dịch kiềm thổ có lời giải
- 15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có lời giải
- 50 câu hỏi lý thuyết mức độ vận dụng về ôn tập chương 6 có lời giải
- 50 câu hỏi lý thuyết mức độ thông hiểu về ôn tập chương 6 có lời giải
- 20 bài tập mức độ vận dụng cao nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 30 bài tập mức độ vận dụng nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 20 bài tập axit tác dụng với muối aluminat có lời giải









