15 bài tập vận dụng cao về chất béo có lời giải
Làm đề thiCâu hỏi 1 :
Đốt cháy hoàn toàn a mol X (là trieste của glixerol với các axit đơn chức, mạch hở), thu được b mol CO2 và c mol H2O (b – c = 5a). Hiđro hóa m1 gam X cần 6,72 lít H2 (đktc), thu được 89,00 gam Y (este no). Đun nóng m1 gam X với dung dịch chứa 0,45 mol NaOH, cô cạn dung dịch sau phản ứng, thu được m2 gam chất rắn. Giá trị của m2 là
- A 97,20.
- B 97,80.
- C 91,20.
- D 104,40.
Đáp án: A
Phương pháp giải:
Công thức trieste của glixerol và axit đơn chức ,mạch hở là CnH2n-4-2kO6 (k: là số liên kết pi gốc axit)
Bảo toàn khối lượng
Lời giải chi tiết:
Hướng dẫn giải
Công thức trieste của glixerol và axit đơn chức ,mạch hở là CnH2n-4-2kO6 (k: là số liên kết pi gốc axit)
CnH2n-4-2kO6 → nCO2 + (n -2 -k) H2O
x nx x(n - 2 - k) (mol)
nCO2−nH2O=5nX ⇒ nx - x (n – 2 – k) = 5x ⇒ k = 3
⇒ Công thức X là:CnH2n-10O6
CnH2n-10O6 + 3H2 → CnH2n-4O6
x 2x
Số mol H2: 3x = 0,3 ⇒ x = 0,1
Khối lượng X = mX' –mH2 = 89 – 2.0,3 = 88,4
(R-COO)3-C3H5 + 3NaOH → 3R-COONa + C3H5(OH)3
0,1 0,3mol 0,3 mol
Áp dụng định luật bảo toàn:
mchất rắn = mX + mNaOH - mC3H8O3 = 88,4 + 0,45.40 - 92.0,1 = 97,2
Đáp án A
Câu hỏi 2 :
E là trieste mạch hở, tạo bởi glixerol và ba axit cacboxylic đơn chức. Đốt cháy hoàn toàn x mol chất E thu được y mol CO2 và z mol H2O. Biết y = z + 5x và khi cho x mol chất E phản ứng vừa đủ với 72 gam Br2 trong nước, thu được 110,1 gam sản phẩm hữu cơ. Nếu cho x mol chất E phản ứng hết với dung dịch KOH, cô cạn dung dịch sau phản ứng, làm khô sản phẩm thu được m gam muối khan. Giá trị của m là
- A 24,75.
- B 8,25.
- C 9,90.
- D 49,50.
Đáp án: D
Phương pháp giải:
Sử dụng công thức tính : Đốt cháy hợp chất hữu cơ: CxHyOz có độ bất bão hòa k thì \({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}}\)
Từ mối quan hệ của CO2; H2O và nE => k =?
Viết PTHH , tính toán theo PTHH
Lời giải chi tiết:
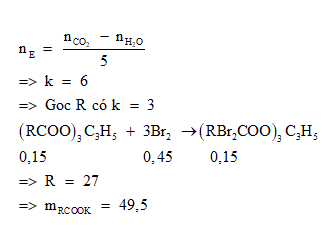
Đáp án D
Câu hỏi 3 :
Thủy phân hoàn toàn triglixerit X trong dung dịch NaOH, thu được glixerol, natri stearat và natri oleat. Đốt cháy hoàn toàn m gam X cần vừa đủ 3,22 mol O2, thu được H2O và 2,28 mol CO2. Mặt khác, m gam X tác dụng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
- A 0,20
- B 0,16
- C 0,04
- D 0,08.
Đáp án: D
Phương pháp giải:
Từ số C của muối => X có 57C
Gọi CTPT của X là: C57HxO6
nX = nCO2/57 = ? (mol)
C57HxO6 + ( 0,25x + 54)O2 → 57CO2 + 0,5xH2O
Theo PT: ( 0,25x + 54) → 57 (mol)
Theo đề bài: 3,22 → 2,28 (mol)
=> 2,28. ( 0,25x + 54) = 3,22.57
=> x = ?
=> CTCT của X là:? (mol)
=> nBr2 = số mol liên kết C=C có trong X
Lời giải chi tiết:
X + NaOH → C17H35COONa + C17H33COONa
Từ số C của muối => X có 57C
Gọi CTPT của X là: C57HxO6
nX = nCO2/57 = 2,28/57 = 0,04 (mol)
C57HxO6 + ( 0,25x + 54)O2 → 57CO2 + 0,5xH2O
Theo PT: ( 0,25x + 54) → 57 (mol)
Theo đề bài: 3,22 → 2,28 (mol)
=> 2,28. ( 0,25x + 54) = 3,22.57
=> x = 106
=> CTPT của X: C57H106O6
=> CTCT của X là: (C17H35COO)(C17H33COO)2C3H5: 0,04 (mol)
=> nBr2 = 2nX = 2.0,04 = 0,08 (mol)
Đáp án D
Câu hỏi 4 :
Hỗn hợp X gồm (CH3COO)3C3H5, CH3COOCH2CH(OOCCH3)CH2OH, CH3COOH, CH3COOCH2CH(OH)CH2OH, C3H5(OH)3 trong đó CH3COOH chiếm 10% tổng số mol hỗn hợp. Đun nóng m gam hỗn hợp X với dung dịch NaOH vừa đủ thu được dung dịch chứa 20,828 gam natri axetat và 0,6m gam glixerol. Để đốt cháy m gam hỗn hợp X cần V lít khí O2 đktc. Giá trị của V gần nhất với giá trị nào
- A 21,5376
- B 12,7456
- C 25,4912
- D 43,0752
Đáp án: C
Lời giải chi tiết:
nNaOH = nCH3COONa = 20,828 : 82 = 0,254 mol
Từ CTCT các chất nhận thấy: n hh = nCH3COOH + n glixerol => nhh = 0,1nhh + 0,6m/92
=> nhh = m/138 (mol)
=> nCH3COOH = 0,1m/138 (mol) => nH2O = nCH3COOH = 0,1m/138 (mol)
BTKL: m hh + mNaOH = m muối + m glixerol + mH2O
=> m + 0,254.40 = 20,828 + 0,6m + 18.(0,1m/138)
=> m = 27,569
=> nhh = 0,2 mol và nCH3COOH = 0,02 mol => n glixerol = 0,2 – 0,02 = 0,18 mol
Quy đổi hỗn hợp ban đầu thành:
CH3COOH: 0,254
C3H8O3: 0,18
H2O
Đốt cháy hỗn hợp là đốt cháy CH3COOH và C3H8O3 (vì H2O không cháy được)
C2H4O2 + 2O2 → 2CO2 + 2H2O
0,254 → 0,508
C3H8O3 + 3,5O2 → 3CO2 + 4H2O
0,18 → 0,63
=> VO2 = (0,508 + 0,63).22,4 = 25,4912 lít
Đáp án C
Câu hỏi 5 :
Đốt cháy hoàn toàn m gam hỗn hợp X gồm tripanmitin, triolein, axit stearic , axit panmitic (trong đó số mol các chất béo bằng nhau). Sau phản ứng thu được 83,776 lit khí CO2 (dktc) và 57,24g nước . Mặt khác, đun nóng m gam X với dung dịch NaOH dư đến khi các phản ứng xảy ra hoàn toàn thu được a gam glycerol. Giá trị của a là
- A 14,72
- B 13,80
- C 51,52
- D 22,2
Đáp án: A
Phương pháp giải:
Tính toán dựa vào phản ứng cháy :
CnH2n+2-2k + O2 →nCO2 + (n + 1 – k)H2O
=> nCO2 – nH2O = nchất(k – 1) [k là số liên kết pi]
Lời giải chi tiết:
Hỗn hợp X gồm : C51H98O6 (3 pi) ; C57H104O6 (6 pi) : x mol mỗi chất
C18H36O2 (1 pi) ; C16H32O2 (1 pi)
nCO2 = 83,776 : 22,4 = 3,74 ; nH2O = 57,24 : 18 = 3,18
Khi đốt cháy : nCO2 – nH2O = (3 – 1)x + (6 – 1)x = 7x = 3,74 – 3,18 = 0,56 mol
=> x = 0,08 mol
Khi X + NaOH :
(C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
(C17H33COO)3C3H5 + 3NaOH → 3C17H33COONa + C3H5(OH)3
nGlycerin = neste = 2x = 0,16 mol
=> mGlycerin= 14,72g
Đáp án A
Câu hỏi 6 :
Cho X, Y là hai axit cacboxylic đơn chức (MX < MY); T là este ba chức, mạch hở được tạo bởi X, Y với glixerol. Cho 23,06 gam hỗn hợp E gồm X, Y, T và glixerol (với số mol của X bằng 8 lần số mol của T) tác dụng vừa đủ với 200 ml dung dịch NaOH 2M, thu được hỗn hợp F gồm hai muối có tỉ lệ mol 1 : 3 và 3,68 gam glixerol. Đốt cháy hoàn toàn F cần vừa đủ 0,45 mol O2, thu được Na2CO3, H2O và 0,4 mol CO2. Phần trăm khối lượng của T trong E có giá trị gần nhất với giá trị nào sau đây?
- A 35
- B 26
- C 25
- D 29
Đáp án: B
Phương pháp giải:
\(E\left\{ \matrix{
X:8x \hfill \cr
Y:y \hfill \cr
Z:x \hfill \cr
glixerol:z \hfill \cr} \right.\buildrel { + 0,4molNaOH} \over
\longrightarrow \left\{ \matrix{
{R_1}{\rm{COONa}} \hfill \cr
{R_2}{\rm{COONa}} \hfill \cr
{\rm{glixerol:0,4}} \hfill \cr} \right.\)
Vì 2 muối có tỉ lệ 1 : 3 nên giả sử: R1COONa : 0,3 mol và R2COONa : 0,1 mol
Đốt muối có
Muối + 0,45 mol O2 → CO2 + H2O + Na2CO3
→ bảo toàn O có : 2nCOO- + 2nO2 = 2nCO2 + 3nNa2CO3 + nH2O => H2O = ? mol
Bảo toàn khối lượng: mmuối + mO2 = mCO2 + mNa2CO3 + mH2O => mmuối = ? (g)
Mặt khác: mmuối = 0,3(R1 + 67) + 0,1.(R2 + 67)
=> Mối quan hệ R1, R2
=> Chạy giá trị tìm được R1,R2
Bảo toàn khối lượng phản ứng tác dụng với NaOH có
mE + mNaOH = mmuối + mGlixerol + mH2O => nH2O = ?
→nX = ? mol và nY = ?
=> CTCT của Z. Từ đó tính được phần trăm =?
Lời giải chi tiết:
\(E\left\{ \matrix{
X:8x \hfill \cr
Y:y \hfill \cr
Z:x \hfill \cr
glixerol:z \hfill \cr} \right.\buildrel { + 0,4molNaOH} \over
\longrightarrow \left\{ \matrix{
{R_1}{\rm{COONa}} \hfill \cr
{R_2}{\rm{COONa}} \hfill \cr
{\rm{glixerol:0,4}} \hfill \cr} \right.\)
Vì 2 muối có tỉ lệ 1 : 3 nên giả sử: R1COONa : 0,3 mol và R2COONa : 0,1 mol
Đốt muối có
Muối + 0,45 mol O2 → CO2 + H2O + Na2CO3
BTNT “Na”: nNa2CO3 = 1/2n NaOH = 0,2 (mol)
→ bảo toàn O có : 2nCOO- + 2nO2 = 2nCO2 + 3nNa2CO3 + nH2O
=> H2O = 2.0,4 + 2.0,45 -2.0,4-3.0,2 = 0,3 mol
Bảo toàn khối lượng:
mmuối + mO2 = mCO2 + mNa2CO3 + mH2O
=> mmuối = 0,4.44 + 0,2.106 + 0,3.18 – 0,45.32 = 29,8 (g)
Bảo toàn khối lượng có mmuối = 29,8 g = 0,3(R1 + 67) + 0,1.(R2 + 67)
=> 3R1 + R2 = 30
=> R1 = 1 và R2 = 27 là nghiệm thỏa mãn
Bảo toàn khối lượng phản ứng tác dụng với NaOH có
mE + mNaOH = mmuối + mGlixerol + mH2O
=> 23,06 + 0,4.40 = 29,8 + 3,68 + mH2O
=> mH2O = 5,58 (g)
=> nH2O = 0,31mol → nZ = (0,4 - 0,31) : 3 = 0,03 mol
→nX = 0,24 mol và nY = 0,07
→ có nX + 2nZ = nR1COONa nên Z tạo từ 2X và 1 Y
Z là (HCOO)2-C3H5-OOC-C2H3 : 0,03
→%Z = 26,28% gần nhất với 26%
Đáp án B
Câu hỏi 7 :
Đốt a mol X là trieste của glixerol và các axit đơn chức mạch hở thu được b mol CO2 và c mol H2O, biết b – c = 4a. Hidro hóa hoàn toàn m gam X cần 6,72 lít H2 (đktc) thu được 133,5 gam Y. Nếu đun m gam X với dung dịch chứa 500 ml NaOH 1M đến phản ứng xảy ra hoàn toàn, cô cạn dung dịch sau phản ứng khối lượng chất rắn khan thu được là:
- A 112,7g
- B 139,1g
- C 140,3g
- D 138,3g
Đáp án: B
Phương pháp giải:
Xét phản ứng cháy: nCO2 – nH2O = (k – 1).nX (k là số liên kết pi)
Từ dữ kiện b – c = 4a => số liên kết pi trong X
=> tỉ lệ mol X + H2 => nX
Bảo toàn khối lượng: mX = mY – mH2
Bảo toàn khối lượng: mrắn = mX + mNaOH - mglixerol => mrắn
Lời giải chi tiết:
Xét phản ứng cháy: nCO2 – nH2O = (k – 1).nX (k là số liên kết pi)
Theo đề bài b – c = 4a => k = 5 => Trong X có 5 liên kết pi (3 pi ở gốc COO; 2 pi ở gốc hidrocacbon)
=> Để hidro hóa hoàn toàn 1 mol X cần 2 mol H2
X + 2H2 → Y
=> nX = ½ nH2 = ½ .6,72 : 22,4 = 0,15 mol
Bảo toàn khối lượng: mX = mY – mH2 = 133,5 – 0,3.2 = 132,9 gam
Khi phản ứng thủy phân: (RCOO)3C3H5 + NaOH → 3RCOONa + C3H5(OH)3
=> nGlixerol = nX = 0,15 mol
Bảo toàn khối lượng: mrắn = mX + mNaOH - mglixerol
=> mrắn = 132,9 + 0,5.40 – 0,15.92 = 139,1g
Đáp án B
Câu hỏi 8 :
Hỗn hợp A gồm axit panmitic, axit stearic và triglixerit X. Đốt cháy hoàn toàn m gam A cần dùng vừa đủ 9,21 mol O2, Thu được H2O và 6,42 mol CO2. Mặt khác, m gam A tác dụng vừa đủ với dung dịch chứa 0,36 mol NaOH, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối natri panmitat, natri sterat. Giá trị của a là?
- A 107,04.
- B 103,56.
- C 103,44.
- D 106,80.
Đáp án: D
Phương pháp giải:
- Do cho hỗn hợp A phản ứng với NaOH thu được hỗn hợp muối chứa natri panmitat, natri sterat nên chất béo được tạo nên từ axit panmitic, axit stearic → X là chất béo no
Đặt mol của axit và chất béo trong m gam A là x và y.
- Xét phản ứng cho m gam A tác dụng vừa đủ với NaOH:
RCOOH + NaOH → RCOONa + H2O
x → x → x
(R'COO)3C3H5 + 3NaOH → 3R'COONa + C3H5(OH)3
y → 3y → y
Từ mol NaOH → (1)
- Xét phản ứng đốt cháy m gam hỗn hợp A:
+ Đốt axit no, đơn chức, mạch hở có: nCO2(1) - nH2O(1) = 0
+ Đốt chất béo no, đơn chức, mạch hở có: nCO2(2) - nH2O(2) = 2.nchất béo
Cộng vế với vế ta được: ∑nCO2 - ∑nH2O = 2nX → nH2O theo y
Bảo toàn O → 2naxit + 6nchất béo + 2nO2 = 2nCO2 + nH2O → (2)
Giải (1) (2) được x, y
BTKL → mA = mCO2 + mH2O - mO2
- Xét phản ứng thủy phân trong NaOH:
BTKL → m muối = mA + mNaOH - mH2O - mC3H5(OH)3
Lời giải chi tiết:
- Do cho hỗn hợp A phản ứng với NaOH thu được hỗn hợp muối chứa natri panmitat, natri sterat nên chất béo được tạo nên từ axit panmitic, axit stearic → X là chất béo no
Đặt mol của axit và chất béo trong m gam A là x và y.
- Xét phản ứng cho m gam A tác dụng vừa đủ với NaOH:
RCOOH + NaOH → RCOONa + H2O
x → x → x
(R'COO)3C3H5 + 3NaOH → 3R'COONa + C3H5(OH)3
y → 3y → y
→ nNaOH = x + 3y = 0,36 (1)
- Xét phản ứng đốt cháy m gam hỗn hợp A:
+ Đốt axit no, đơn chức, mạch hở có: nCO2(1) - nH2O(1) = 0
+ Đốt chất béo no, đơn chức, mạch hở có: nCO2(2) - nH2O(2) = 2.nchất béo
Cộng vế với vế ta được: ∑nCO2 - ∑nH2O = 2nX
→ 6,42 - nH2O = 2y → nH2O = 6,42 - 2y (mol)
Bảo toàn O → 2naxit + 6nchất béo + 2nO2 = 2nCO2 + nH2O
→ 2x + 6y + 2.9,21 = 2.6,42 + 6,42 - 2y (2)
Giải (1) (2) được x = 0,18 và y = 0,06
BTKL → mA = mCO2 + mH2O - mO2 = 6,42.44 + 6,3.18 - 9,21.32 = 101,16 gam
- Xét phản ứng thủy phân trong NaOH:
BTKL: m muối = mA + mNaOH - mH2O - mC3H5(OH)3
= 101,16 + 0,36.40 - 0,18.18 - 0,06.92 = 106,8 gam
Đáp án D
Câu hỏi 9 :
Hỗn hợp X gồm CH3COOH, CH2=CHCOOC3H7, CH2=C(COOCH3)2, (C17H35COO)3C3H5 và CH3OOC-C≡C-COOH. Đốt cháy hoàn toàn a mol X cần dùng 1,89 mol O2, sản phẩm cháy gồm CO2 và H2O được dẫn qua bình đựng dung dịch H2SO4 đặc, dư thấy khối lượng bình tăng 22,32 gam. Hiđro hóa hoàn toàn a mol X cần dùng 0,25 mol H2 (Ni, t°). Giá trị của a là
- A 0,28
- B 0,25
- C 0,22
- D 0,27
Đáp án: C
Phương pháp giải:
X + H2 → X’ chứa C2H4O2; C6H12O2; C6H10O4; C5H8O4; C57H110O6
Ta thấy:
C2H4O2 = CH4 + CO2
C6H12O2 = C5H12 + CO2
C6H10O4 = C4H10 + 2CO2
C5H8O4 = C3H8 + 2CO2
C57H110O6 = C54H110 + 3CO2
Do vậy quy đổi X’ thành CnH2n+2 : a (mol) và CO2
Đốt X’ chính là đốt X và H2 ban đầu
Lời giải chi tiết:
X + H2 → X’ chứa C2H4O2; C6H12O2; C6H10O4; C5H8O4; C57H110O6
Ta thấy:
C2H4O2 = CH4 + CO2
C6H12O2 = C5H12 + CO2
C6H10O4 = C4H10 + 2CO2
C5H8O4 = C3H8 + 2CO2
C57H110O6 = C54H110 + 3CO2
Do vậy quy đổi X’ thành CnH2n+2 : a (mol) và CO2
Ta coi đốt X’chính là đốt X và H2: 0,25 (mol)
2H2 + O2 \(\xrightarrow{{{t^0}}}\) 2H2O
0,25→0,125 → 0,25 (mol)
Vậy lượng O2 cần đốt cháy X’ = 1,89 + 0,125 = 2,015 (mol)
Số mol H2O cháy tạo ra là: nH2O = 22,32/18 + 0,25 = 1,49 (mol)
PT cháy X’: CnH2n+2 + (3n+1)/2 O2 \(\xrightarrow{{{t^0}}}\) nCO2 + (n+1)H2O
Theo PTHH: \(\frac{{3n + 1}}{2}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\xrightarrow{{}}\,\,\,\,\,(n + 1)\) (mol)
Theo ĐB: 2,015 \(\xrightarrow{{}}\) 1,49 (mol)
\(\begin{array}{l}1,49.\frac{{3n + 1}}{2} = 2,015.(n + 1)\\ \to 2,235n + 0,745 = 2,015n + 2,015\\ \to 0,22n = 1,27\\ \to n = \frac{{127}}{{22}}\end{array}\)
Mặt khác: \({n_{{H_2}O}} = x(n + 1) = 1,49 \Rightarrow x(\frac{{127}}{{22}} + 1) = 1,49 \Rightarrow x = 0,22\)
Đáp án C
Câu hỏi 10 :
Cho X, Y là hai axit cacboxylic đơn chức (MX < MY); T là este ba chức, mạch hở tạo bởi X, Y với glixerol. Cho 23,06 gam hỗn hợp E gồm X, Y, T và glixerol (với số mol của X bằng 8 lần số mol của T) tác dụng vừa đủ với 200ml dung dịch NaOH 2M, thu được hỗn hợp F gồm hai muối có tỉ lệ mol 1 : 3 và 3,68 gam glixerol. Đốt cháy hoàn toàn F cần vừa đủ 0,45 mol O2, thu được Na2CO3, H2O và 0,4 mol CO2. Phần trăm khối lượng của T trong E có giá trị gần nhất với:
- A 25,22.
- B 26,22.
- C 29,22.
- D 35,22.
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 11 :
X, Y là hai axit cacboxylic đều đơn chức, mạch hở (trong đó Y không no chứa một liên kết C=C); Z là este tạo bởi X, Y và glixerol. Đun nóng 12,84 gam hỗn hợp E chứa X, Y, Z với 300 ml dung dịch NaOH 1M. Trung hòa lượng NaOH dư trong dung dịch sau phản ứng cần dùng 120 ml dung dịch HCl 0,5M. Cô cạn dung dịch sau khi trung hòa, thu được 20,87 gam muối khan. Mặt khác đốt cháy 12,84 gam E cần dùng 6,496 lít O2 (đktc). Thể tích dung dịch Br2 1M phản ứng tối đa với 0,3 mol E là
- A 360 ml.
- B 60 ml.
- C 320 ml.
- D 240 ml.
Đáp án: A
Lời giải chi tiết:
nNaOH(pư với HCl) = nHCl = 0,06 mol → nNaOH (pư với E) = 0,3 - 0,06 = 0,24 mol = nCOO(E)
*Xét phản ứng đốt 12,84g E:
nO(E) = 2nCOO(E) = 0,48 mol
Giải hệ: \(\left\{ \begin{array}{l}44{n_{C{O_2}}} + 18{n_{{H_2}O}} = 12,84 + 0,29.32\left( {BTKL} \right)\\2{n_{C{O_2}}} + {n_{{H_2}O}} = 0,48 + 0,29.2\left( {BT:O} \right)\end{array} \right. \to \left\{ \begin{array}{l}{n_{C{O_2}}} = 0,38\\{n_{{H_2}O}} = 0,3\end{array} \right.\)
*Quy đổi E thành:
\(E\left\{ \begin{array}{l}HCOOH:0,24\\C{H_2}:a\\{H_2}:b\left( {b < 0} \right)\\{C_3}{H_8}{O_3}:c\\{H_2}O: - 3c\end{array} \right. \to Muoi\left\{ \begin{array}{l}HCOON{\rm{a}}:0,24\\C{H_2}:a\\{H_2}:b\\NaCl:0,06\end{array} \right.\)
(1) mE = 0,24.46 + 14a + 2b + 92c + 18.(-3c) = 12,84
(2) mmuối = 0,24.68 + 14a + 2b + 0,06.58,5 = 20,87
(3) nCO2 = 0,24 + a + 3c = 0,38
Giải hệ được a = 0,08; b = -0,04; c = 0,02
+) nE = naxit + neste = (0,24 - 3c) + c = 0,2 mol
+) Số C trung bình của axit = (0,24 + a)/0,24 = 1,333
→ X là HCOOH
Mà nY = - nH2 = - b = 0,04 mol
→ nHCOOH = 0,24 - 0,04 = 0,2 mol
→ nBr2 = nHCOOH + nC=C = 0,2 + 0,04 = 0,24 mol
Tỷ lệ: 0,2 mol E phản ứng tối đa 0,24 mol Br2
→ 0,3 mol E ………………..0,36 mol Br2
Vậy Vdd Br2 = 360 ml
Đáp án A
Câu hỏi 12 :
Hỗn hợp X gồm triglixerit Y, a mol axit oleic và b mol axit stearic (a : b = 3 : 1). Đốt cháy hoàn toàn m gam X cần dùng vừa đủ 5,27 mol O2, thu được H2O và 3,72 mol CO2. Mặt khác, m gam hỗn hợp X tác dụng vừa đủ với dung dịch chứa 0,14 mol Br2. Nếu cho X tác dụng với dung dịch NaOH vừa đủ, sau phản ứng thu được hỗn hợp 2 muối. Phần trăm khối lượng của Y trong hỗn hợp X gần nhất với
- A 61%.
- B 50%.
- C 55%.
- D 52%.
Đáp án: A
Phương pháp giải:
Quy đổi X thành \(\left\{ \begin{array}{l}{C_{17}}{H_{35}}C{\rm{OOH:x(mol)}}\\{C_{17}}{H_{33}}{\rm{COOH: y(mol)}}\\{C_3}{H_5}{(OH)_3}:z(mol)\\{H_2}O: - 3{\rm{z}}\end{array} \right.\)
Khi X + Br2 ⟹ y (1)
Bảo toàn C cho pư cháy ⟹ (2)
Bảo toàn H tính được H2O theo x, y, z
Bảo toàn O cho pư cháy ⟹ (3)
Giải (1)(2)(3) có x, y, z ⟹ khối lượng của hỗn hợp X
Giả sử Y có công thức (C17H33COO)n(C17H35COO)3-nC3H5
a = 0,14 - 0,04n và b = 0,06 - 0,04.(3-n)
Mà theo đề bài a : b = 3 : 1 tìm được giá trị của n
Tính phần trăm khối lượng của Y trong X
Lời giải chi tiết:
Quy đổi X thành \(\left\{ \begin{array}{l}{C_{17}}{H_{35}}COOH:x\\{C_{17}}{H_{33}}COOH:y\\{C_3}{H_5}{(OH)_3}:z\\{H_2}O: - 3{\rm{z}}\end{array} \right.\)
Khi X + Br2 thì nBr2 = y = 0,14 mol (1)
Khi X + O2 thì bảo toàn C có nCO2 = 18x + 18y + 3z = 3,72 (2)
Bảo toàn H có nH2O thu dược = 18x + 17y + 4z - 3z = 18x + 17y + z
Bảo toàn O có nO(X) + 2nO2 = nH2O + 2nCO2 ⟹ 2x + 2y + 3z - 3z + 2.5,27 = 18x + 17y + z + 3,72.2
⟹ 16x + 15y + z = 3,1 (3)
Giải (1)(2)(3) có x = 0,06 mol và z = 0,04 mol
X quy đổi có \(\left\{ \begin{array}{l}{C_{17}}{H_{35}}COOH:0,06\\{C_{17}}{H_{33}}COOH:0,14\\{C_3}{H_5}{(OH)_3}:0,04\\{H_2}O: - 0,12\end{array} \right.\) ⟹ mX = 0,06.284 + 0,14.282 + 0,04.92 - 0,12.18 = 58,04 gam
Giả sử Y có công thức (C17H33COO)n(C17H35COO)3-nC3H5: 0,04 mol thì
a = 0,14 - 0,04n
b = 0,06 - 0,04.(3 - n)
Mà theo đề a : b = 3 : 1 nên 0,14 - 0,04n = 3.[0,06 - 0,04.(3-n)] ⟹ n = 2
Vậy Y là (C17H33COO)2(C17H35COO)C3H5 (0,04 mol)
\( \to \% {m_Y} = \frac{{0,04.886}}{{58,04}}.100\% = 61,06\% \) gần nhất với 61%
Đáp án A
Câu hỏi 13 :
Hỗn hợp X gồm metyl fomat, đimetyl oxalat, glixeryl triaxetat và phenyl axetat. Thủy phân hoàn toàn 4,73 gam X trong dung dịch NaOH dư, đun nóng, thu được m gam hỗn hợp muối và 1,56 gam hỗn hợp Y gồm các ancol. Cho Y tác dụng với Na dư, thu được 0,56 lít khí H2 (đktc). Mặt khác, đốt cháy hoàn toàn 4,73 gam X bằng oxi, thu được 9,24 gam CO2 và 2,61 gam H2O. Giá trị của m gần nhất với giá trị nào sau đây?
- A 5,3.
- B 5,5.
- C 5,9.
- D 5,8.
Đáp án: D
Phương pháp giải:
Đặt –COOR là gốc este của ancol và –COOC6H5 là gốc este của phenol
Khi cho Y tác dụng với Na dư thì: n-OH(trong ancol) = 2nH2 = ? (mol) = n-COOR
BTKL quá trình đốt cháy: mO(trong X) = mX – mC – mH = ? Từ đó tính được: n-COO = nO(trong X)/2 = ?
⟹ n-COOC6H5 = n-COO- – n-COOR = ? (mol)
⟹ nNaOH = n-COOR + 2n-COOC6H5 = ? (mol)
BTKL ta có: mX + mNaOH = mmuối + mancol + mH2O (Với nH2O = n-COOC6H5)
Lời giải chi tiết:
Cách 1:
Công thức cấu tạo của các chất lần lượt là:
HCOOCH3 ; (COOCH3)2 ; (CH3COO)3C3H5; CH3COOC6H5
Các ancol thu được là: CH3OH (x mol) và C3H5(OH)3 (y mol)
m ancol = 32x + 92y = 1,56 (1)
nH2 = 0,5nCH3OH + 1,5nC3H5(OH)3 = 0,5x + 1,5y = 0,025 (2)
Giải (1) (2) thu được x = 0,01; y = 0,02
Hỗn hợp đầu gồm: HCOOCH3 (a mol); (COOCH3)2 (b mol);(CH3COO)3C3H5 (0,1 mol); CH3COOC6H5 (c mol)
*m hh = 60x + 118y + 136z + 0,1.218 = 4,73 (3)
*nCH3OH = x + 2y = 0,02 (4)
*Đốt X: nCO2 = 0,21 mol; nH2O = 0,145 mol
mO(X) = mhh - mC - mH = 4,73 – 0,21.12 – 0,145.2 = 1,92 gam → nO(X) = 0,12 mol
BTNT “O”: nO(X) = 2x + 4y + 0,01.6 + 2z = 0,12 (5)
Giải (3) (4) (5) được a = 0,01; b = 0,005; c = 0,01
Xét phản ứng của X với NaOH:
nNaOH pư = a + 2b + 0,01.3 + 2c = 0,07 mol
nH2O = c = 0,01 mol
BTKL: m muối = m hh + mNaOH - m ancol - mH2O = 4,73 + 0,07.40 – 1,56 - 0,01.18 = 5,79 gam
Cách 2:
Tổng quát:
Đặt –COOR là gốc este của ancol và –COOC6H5 là gốc este của phenol
-COOR- + NaOH → -COONa + ROH
-COOC6H5 + 2NaOH → -COONa + C6H5ONa + H2O
Khi cho Y tác dụng với Na dư thì:
n-OH(trong ancol) = 2nH2 = 0,05 (mol) ⟹ n-COOR = n-OH(ancol) = 0,05 (mol)
Khi đốt cháy hh X thì: \({n_{O(trong\,X)}} = \frac{{{m_X} - 12{n_{C{O_2}}} - 2{n_{{H_2}O}}}}{{16}} = \frac{{4,73 - 12.0,21 - 2.0,145}}{{16}} = 0,12\,(mol)\)
⟹ n-COO- = no/2 = 0,06 (mol)
⟹ n-COOC6H5 = n-COO- – n-COOR = 0,06 – 0,05 = 0,01 (mol)
⟹ nNaOH = n-COOR + 2n-COOC6H5 = 0,05 + 2.0,01 = 0,07 (mol)
BTKL ta có: mX + mNaOH = mmuối + mancol + mH2O
⟹ m = 4,73 + 0,07.40 – 1,56 – 0,01.18
⟹m = 5,79 (g)
Vậy m gần nhất với 5,8 g
Đáp án D
Câu hỏi 14 :
Đốt cháy hoàn toàn m gam một triglixerit X cần vừa đủ 1,54 mol O2, thu được CO2 và 1 mol H2O. Nếu thủy phân hoàn toàn m gam X trong dung dịch KOH đun nóng thu được dung dịch chứa 18,64 gam muối. Để chuyển hóa a mol X thành chất béo no cần vừa đủ 0,06 mol H2. Giá trị của a là?
- A 0,06.
- B 0,02.
- C 0,01.
- D 0,03.
Đáp án: B
Phương pháp giải:
Đặt k là số liên kết π của triglixerit X và số mol của X trong m gam là x mol
⇒ Số liên kết π ngoài mạch cacbon là (k - 3) (vì có 3 liên kết π trong COO)
Áp dụng công thức khi đốt cháy chất hữu cơ X có độ bất bão hòa k ta có:
\({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \Rightarrow {n_{C{O_2}}} = ? (mol)\)
Bảo toàn O lập phương trình 1 giữa x và k
X +KOH
Có mX = mC + mH + mO
BTKL ta có: mX + mKOH = mMuối + mC3H5(OH)3 ⟹ phương trình (2)
⟹ tìm được x và k
Khi X phản ứng với dd H2 thì chỉ có liên kết π ở mạch cacbon mới tham gia phản ứng cộng
⇒ nH2 = (k - 3).a ⟹ a
Lời giải chi tiết:
Giả sử m (g) X tương đương với x mol
*m(g) X + KOH:
X + 3KOH → Muối + C3H5(OH)3
x → 3x → x (mol)
BTKL → mX = mmuối + mC3H5(OH)3 - mKOH = 18,64 + 92x - 56.3x = 18,64 - 76x (g)
*Đốt m(g) X:
Bảo toàn O → \({n_{C{O_2}}} = \frac{{6{n_X} + 2{n_{{O_2}}} - {n_{{H_2}O}}}}{2} = \frac{{6{\rm{x}} + 2.1,54 - 1}}{2} = 3{\rm{x + }}1,04\left( {mol} \right)\)
BTKL → mX + mO2 = mCO2 + mH2O → (18,64 - 76x) + 1,54.32 = 44.(3x + 1,04) + 18 → x = 0,02
→ nX = 0,02 mol; nCO2 = 1,1 mol
Công thức nhanh khi đốt cháy chất hữu cơ (chứa C, H, O) có độ bất bão hòa k:
\({n_X} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} \Leftrightarrow 0,02 = \frac{{1,1 - 1}}{{k - 1}} \Leftrightarrow k = 6\)
Ta thấy 3 nhóm COO có 3 π nên mạch cacbon có k - 3 = 3 liên kết π (lưu ý chỉ những liên kết π ngoài mạch C mới tham gia pư cộng)
*Hiđro hóa a mol X:
X + 3H2 → Chất béo no
0,02 ← 0,06 mol
Vậy a = 0,02 mol.
Đáp án B
Câu hỏi 15 :
Hỗn hợp X gồm axit oleic và triglixerit Y (tỉ lệ mol tương ứng 1 : 2). Đốt cháy hoàn toàn một lượng hỗn hợp X cần vừa đủ 1,785 mol O2, thu được 1,28 mol CO2 và 1,15 mol H2O. Mặt khác, cho 29,85 gam X trên tác dụng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
- A 0,130.
- B 0,180.
- C 0,090.
- D 0,135.
Đáp án: D
Phương pháp giải:
Khi đốt hợp chất hữu cơ bất kì (chứa C, H, O) có độ bất bão hòa k, ta luôn có:
nCO2 - nH2O = nhchc.(k-1)
Lời giải chi tiết:
BTKL → mX = mCO2 + mH2O - mO2 = 1,28.44 + 1,15.18 - 1,785.32 = 19,9 gam
Đặt số mol của axit oleic và triglixerit lần lượt là a và 2a mol
Bảo toàn O → 2.a + 6.2a + 2.1,785 = 2.1,28 + 1,15 → a = 0,01
→ naxit oleic = 0,01 mol; ntriglixerit = 0,02 mol
*Khi đốt hợp chất hữu cơ bất kì (chứa C, H, O) có độ bất bão hòa k, ta luôn có: nCO2 - nH2O = nhchc.(k-1)
- Đốt axit oleic (k = 2) thì: nCO2(do axit oleic) - nH2O(do axit oleic) = 0,01.(2 - 1) (*)
- Đốt triglixerit Y (k) thì: nCO2(do Y) - nH2O(do Y) = 0,02.(k - 1) (**)
Cộng vế với vế của (*) và (**) được:
∑nCO2 - ∑nH2O = 0,01 + 0,02.(k - 1)
→ 1,28 - 1,15 = 0,01 + 0,02.(k - 1)
→ k = 7
*Khi cho hỗn hợp tác dụng với Br2 thì:
nBr2 = naxit oleic + (7-3).ntriglixerit = 0,01 + 4.0,02 = 0,09 mol
Tỷ lệ: 19,9 gam hỗn hợp X tác dụng với tối đa 0,09 mol Br2
→ 29,85 gam ………………………………0,135 mol
Vậy x = 0,135
Đáp án D
30 bài tập về đốt cháy chất béo từ dễ đến khó, đầy đủ các dạng có đáp án và lời giải chi tiết
20 bài tập vận dụng cao về chất béo đầy đủ các dạng từ trắc nghiệm đến tự luận có đáp án và lời giải chi tiết
40 bài tập vận dụng về phản ứng thủy phân chất béo đầy đủ các dạng từ dễ đến khó có đáp án và lời giải chi tiết.
40 câu hỏi mức độ thông hiểu về lý thuyết lipit, chất béo đầy đủ các dạng từ dễ đến khó có đáp án và lời giải chi tiết
40 câu hỏi lý thuyết mức độ nhận biết về lipit, chất béo có đáp án và lời giải chi tiết
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 15 bài toán cho từ từ axit vào muối cacbonat có lời giải
- 15 bài toán cho từ từ muối cacbonat vào axit có lời giải
- 50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có lời giải
- 20 bài tập CO2 tác dụng với dung dịch kiềm thổ có lời giải
- 15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có lời giải
- 50 câu hỏi lý thuyết mức độ vận dụng về ôn tập chương 6 có lời giải
- 50 câu hỏi lý thuyết mức độ thông hiểu về ôn tập chương 6 có lời giải
- 20 bài tập mức độ vận dụng cao nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 30 bài tập mức độ vận dụng nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 20 bài tập axit tác dụng với muối aluminat có lời giải









