15 bài toán cho từ từ axit vào muối cacbonat có lời giải
Làm đề thiCâu hỏi 1 :
Cho từ từ dung dịch chứa a mol HCl vào dung dịch chứa b mol Na2CO3 đồng thời khuấy đều, thu được V lít khí (ở đktc) và dung dịch X. Khi cho dư nước vôi trong vào dung dịch X thấy có xuất hiện kết tủa. Biểu thức liên hệ giữa V với a, b là:
- A V = 11,2(a - b).
- B V = 22,4(a - b).
- C V = 22,4(a + b).
- D V = 11,2(a + b).
Đáp án: B
Phương pháp giải:
Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
+) Nhỏ từ từ muối cacbonat vào axit thì ban đầu H+ rất dư nên phản ứng là:
2H+ + CO32- →CO2 + H2O
HCO3- + H+ → CO2 + H2O
Lời giải chi tiết:
Do thu được khí CO2 ⟹ H+ dư so với CO32-:
Na2CO3 + HCl → NaHCO3 + NaCl
b mol → b mol → b mol
Do thêm nước vôi trong vào X thấy có kết tủa nên dd X có chứa HCO3- ⟹ HCO3- dư so với H+
NaHCO3 + HCl → NaCl + CO2 + H2O
(a-b) mol → (a-b) mol
Vậy V = 22,4(a - b)
Đáp án B
Câu hỏi 2 :
Nhỏ rất từ từ đến hết 200ml dung dịch X chứa đồng thời H2SO4 aM và HCl 0,15M vào 100ml dung dịch chứa đồng thời NaOH 0,5M và Na2CO3 0,4M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,448 lít khí (đktc). Giá trị của a là:
- A 0,4
- B 0,1
- C 0,3
- D 0,2
Đáp án: D
Phương pháp giải:
- Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
- Bảo toàn nguyên tố
Lời giải chi tiết:
Thứ tự phản ứng :
H+ + OH- -> H2O
H+ + CO32- -> HCO3-
H+ + HCO3- -> H2O + CO2
=> nH+ = 2nH2SO4 + nHCl = nOH + nCO3 + nCO2
=> 0,2.(2a + 0,15) = 0,05 + 0,04 + 0,02
=> a = 0,2M
Đáp án D
Câu hỏi 3 :
Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ 200ml dung dịch HCl 1M vào 100ml dung dịch X, sinh ra V lít khí (ở đktc). Giá trị của V là
- A 4,48.
- B 3,36.
- C 2,24.
- D 1,12.
Đáp án: D
Phương pháp giải:
Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
+) Nhỏ từ từ muối cacbonat vào axit thì ban đầu H+ rất dư nên phản ứng là:
2H+ + CO32- →CO2 + H2O
HCO3- + H+ → CO2 + H2O
Lời giải chi tiết:
nCO32- = 0,15 mol; nHCO3- = 0,1 mol; nH+ = 0,2 mol
Khi nhỏ từ từ HCl vào dung dịch muối thì ban đầu axit rất thiếu nên sẽ có phản ứng :
CO32- + H+ → HCO3-
0,15 → 0,15 dư 0,05 → 0,15 => nHCO3- = 0,1 + 0,15 = 0,25 mol
HCO3- + H+ → CO2 + H2O
0,05 ← 0,05 → 0,05
=>VCO2 = 1,12 lit
Đáp án D
Câu hỏi 4 :
Hấp thụ hoàn toàn 1,12 lit khí CO2 (dktc) vào 200 ml dung dịch NaOH 1M , thu được dung dịch Y. Cho từ từ dung dịch HCl 2,5M vào Y khi bắt đầu có khí sinh ra thì hết V ml . Giá trị của V là :
- A 80
- B 100
- C 60
- D 40
Đáp án: C
Lời giải chi tiết:
nCO2 = 0,05 ; nNaOH = 0,2 mol dư so với CO2
=> sau phản ứng có : 0,05 mol Na2CO3 và 0,1 mol NaOH
H+ + OH- -> H2O
CO32- + H+ -> HCO3-
HCO3- + H+ -> CO2 + H2O
=> nHCl = nCO3 + nOH = 0,15 mol
=> V = 0,06 lit = 60 ml
Đáp án C
Câu hỏi 5 :
Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 200ml dung dịch HCl 1M vào 100ml dung dịch X, sinh ra V lít khí CO2 (đktc).Giá trị của V là :
- A 2,24
- B 4,48
- C 3,36
- D 1,12
Đáp án: D
Phương pháp giải:
Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
+) Nhỏ từ từ muối cacbonat vào axit thì ban đầu H+ rất dư nên phản ứng là:
2H+ + CO32- →CO2 + H2O
HCO3- + H+ → CO2 + H2O
Lời giải chi tiết:
Vì lúc đầu HCl rất thiếu nên thứ tự phản ứng là :
H+ + CO32-→HCO3-
H+ + HCO3-→CO2 + H2O
Ban đầu : nHCO3 = 0,1 mol ; nCO3 = 0,15 mol ; nHCl = 0,2 mol
=> nCO2 = nHCl – nCO3 = 0,05 mol
=>V = 1,12 lit
Đáp án D
Câu hỏi 6 :
Cho từ từ 100 ml dung dịch HCl 0,2M và NaHSO4 0,6M vào 300 ml dung dịch NaHCO3 0,1M và K2CO3 0,2M thu được V lit CO2 (đktc) và dung dịch X. Cho 100ml dung dịch KOH 0,6M và BaCl2 1,5M vào dung dịch X, thu được m gam kết tủa. Giá trị V và m là
- A 1,0752 lít; 22,254 gam
- B 1,0752 lít; 23,43 gam
- C 0,448 lít ; 25,8 gam
- D 0,448 lít ; 11,82 gam
Đáp án: C
Phương pháp giải:
Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
+) Nhỏ từ từ muối cacbonat vào axit thì ban đầu H+ rất dư nên phản ứng là:
2H+ + CO32- →CO2 + H2O
HCO3- + H+ → CO2 + H2O
Lời giải chi tiết:
nH+= nHCl + NaHSO4 = 0,02 + 0,06 = 0,08 mol
nHCO3-= 0,03 mol
nCO32-= 0,06 mol
Đổ từ từ dung dịch axit vào hỗn hợp muối
CO32- + H+ → HCO3-
0,06 → 0,06 → 0,06 mol
HCO3- + H+ → CO2 + H2O
0,02 ← 0,02 → 0,02 mol => V = 0,448 l
Vậy dung dịch X chứa:
Na+: 0,06 + 0,03 = 0,09 mol
K+: 2.0,06 = 0,12 mol
Cl-: 0,02 mol
SO42-: 0,06 mol
HCO3-: 0,07 mol
HCO3- + OH- → CO32- + H2O
Bđ: 0,07 0,06
Pư: 0,06 ← 0,06 → 0,06 mol
nBa 2+ = 0,15 mol
nSO4 2-= 0,06 mol
nCO32- = 0,06 mol
Ba2+ dư so với SO42- và CO32- =>nBaSO4 = nSO42- = 0,06 mol và nBaCO3 = nCO32- = 0,06 mol
=> Vậy m = 0,06.233 + 0,06.197 = 25,8 gam
Đáp án C
Câu hỏi 7 :
Nhỏ từ từ từng giọt đến hết 20 ml dung dịch HCl 1,5M vào 100 ml dung dịch Na2CO3 0,1M và NaHCO3 0,2M, sau khi phản ứng thu được số mol CO2 là :
- A 0,015
- B 0,020
- C 0,010
- D 0,030
Đáp án: B
Phương pháp giải:
Muối Cacbonat , Hidrocacbonat + H+
- TH1 : Nếu Cho từ từ Muối (CO32- : x mol và HCO3- : y mol) vào dung dịch Axit
=> Do ban đầu H+ rất dư so với muối nên 2 muối đều phản ứng đồng thời
CO32- + 2H+ -> CO2 + H2O
HCO3- + H+ -> CO2 + H2O
=> nCO3 pứ : nHCO3 pứ = x : y
- TH2 : Nếu cho từ từ H+ vào dung dịch muối (CO32- : x mol và HCO3- : y mol)
=> Do ban đầu H+ thiếu nên phản ứng với CO32- trước :
CO32- + H+ -> HCO3-
HCO3- + H+ -> CO2 + H2O
- TH3 : Trộn nhanh 2 dung dịch axit và muối
=> Không biết chất nào phản ứng với chất nào trước
=> Xét cả 2 trường hợp TH1 và TH2 => và lấy giá trị trong khoảng.
Lời giải chi tiết:
nH+ = 0,03 mol
CO32- + H+ -> HCO3-
0,01 -> 0,01 -> 0,01 mol
HCO3- + H+ -> CO2 + H2O
0,03 0,02 -> 0,02 mol
Đáp án B
Câu hỏi 8 :
Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào 400ml dung dịch KOH x mol, thu được dung dịch X. Nhỏ từ từ đến hết 500 ml dung dịch HCl 1M vào dung dịch X, thu được dung dịch Y và thoát ra 2,24 lít khí (đktc). Cho dung dịch Y tác dụng với Ba(OH)2 dư thu được 39,4 gam kết tủa. Giá trị của x là:
- A 1,85
- B 1,25
- C 2,25
- D 1,75
Đáp án: D
Lời giải chi tiết:
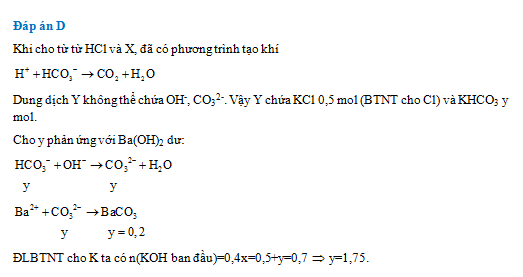
Câu hỏi 9 :
Cho rất từ từ 0,2 lít dung dịch HCl 1M vào 0,2 lít dung dịch hỗn hợp KOH 0,5M, K2CO3 0,4M đến phản ứng hoàn toàn, thu được x lít khí ở đktc. Giá trị của x là:
- A 1,12
- B 0,336
- C 0,448
- D 2,24.
Đáp án: C
Phương pháp giải:
B1: Tính nH+ ; nOH- ; nCO32-
B2: Viết phương trình ion rút gọn thứ tự các phản ứng xảy ra
H+ + OH - → H2O
H+ + CO32- → HCO3-
H+ + HCO3- → CO2 + H2O
B3: Tính toán theo phương trình với chú ý, chất nào phản ứng hết thì theo số mol của chất đó
Lời giải chi tiết:
nH+ = nHCl = 0,2 (mol);
nOH- = nKOH = 0,1 (mol) ; nCO32- = nK2CO3 = 0,08 (mol)
Thứ tự xảy ra phản ứng:
H+ + OH - → H2O
0,1← 0,1
H+ + CO32- → HCO3-
0,08 ← 0,08 → 0,08
H+ + HCO3- → CO2 + H2O
(0,2 – 0,1 – 0,08) → 0,02
nCO2 = 0,02 (mol) => VCO2 = 0,02.22,4 = 0,448 (l)
Đáp án C
Câu hỏi 10 :
Cho từ từ 200 ml dung dịch hỗn hợp HCl 1M và H2SO4 0,5M vào 300 ml dung dịch Na2CO3 1M thu được V lít khí (ở đktc). Giá trị của V là:
- A 2,24.
- B 4,48.
- C 3,36.
- D 1,68.
Đáp án: A
Phương pháp giải:
Cho từ từ H+ vào CO32- nên thứ tự phản ứng như sau:
H+ + CO32- →HCO3-
H+ + HCO3- → H2O + CO2
Đáp án A
Lời giải chi tiết:
\(\begin{array}{*{20}{l}}
{{n_{{H^ + }}} = {n_{HCl}} + 2{n_{{H_2}S{O_4}}} = 0,4{\text{ }}mol} \\
{{n_{C{O_3}^{2 - }}} = 0,3{\text{ }}mol}
\end{array}\)
Cho từ từ H+ vào CO32- nên thứ tự phản ứng như sau:
H+ + CO32- →HCO3-
0,3←0,3→ 0,3
H+ + HCO3- → H2O + CO2
0,1→0,1 → 0,1
V=0,1.22,4=2,24 lít
Đáp án A
Câu hỏi 11 :
Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào dung dịch chứa a mol NaOH và b mol Na2CO3, thu được dung dịch X. Chia X thành hai phần bằng nhau. Cho từ từ phần một vào 120 ml dung dịch HCl 1M, thu được 2,016 lít CO2 (đktc). Cho phần hai phản ứng hết với dung dịch Ba(OH)2 dư, thu được 29,55 gam kết tủa. Tỉ lệ a: b tương ứng là
- A 1:2.
- B 2: 3.
- C 2: 5.
- D 2: 1.
Đáp án: B
Phương pháp giải:
Bảo toàn nguyên tố C, Na
Bảo toàn điện tích
Lời giải chi tiết:
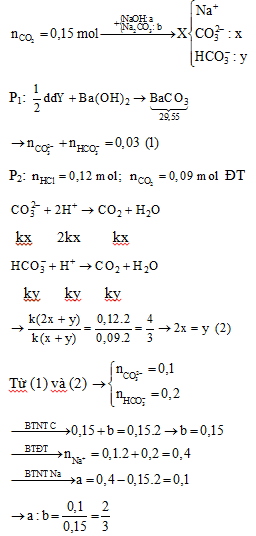
Đáp án B
Câu hỏi 12 :
Hòa tan m gam hỗn hợp Na2CO3 và KHCO3 vào nước để được 400 ml dung dịch X. Cho từ từ 100 ml dung dịch HCl 1,5M vào dung dịch X thu được dung dịch Y và 1,008 lít khí đktc. Cho Y tác dụng với Ba(OH)2 dư thu được 29,55 gam kết tủa. Cho từ từ dung dịch X vào bình đựng 100 ml dung dịch HCl 1,5M, thu được V lít khí đktc. Giá trị của m và V lần lượt là
- A 20,13 và 2,184
- B 20,13 và 2,688
- C 18,69 và 2,184
- D 18,69 và 2,688
Đáp án: A
Phương pháp giải:
Gọi số mol Na2CO3 và KHCO3 lần lượt là x và y.
Khi cho HCl vào thì CO32- phản ứng trước:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
Bảo toàn nguyên tố
Khi cho từ từ X vào dung dịch chứa HCl thì CO32- + 2H+ → CO2 + H2O
HCO3- + H+ → CO2 + H2O
2 phản ứng xảy ra đồng thời với \(\frac{{{n_{CO_3^{2 - }PU}}}}{{{n_{HCO_3^ - PU}}}} = \frac{x}{y}\)
Lời giải chi tiết:
Gọi số mol Na2CO3 và KHCO3 lần lượt là x và y.
Khi cho HCl vào thì CO32- phản ứng trước:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
Mặt khác khi cho Ba(OH)2 vào Y thì có kết tủa
⇒ HCO3- dư ⇒ H+ trước đó đã hết
⇒ Bảo toàn Cacbon ⇒ x+ y= nCO2+nBaCO3=0,195 mol
Và nHCl = nCO2 + x⇒ x = 0,105 mol ⇒ y = 0,09 mol
⇒ m = 20,13 g
Khi cho từ từ X vào dung dịch chứa HCl thì CO32- + 2H+ → CO2 + H2O
HCO3- + H+ → CO2 + H2O
2 phản ứng xảy ra đồng thời với \(\frac{{{n_{CO_3^{2 - }PU}}}}{{{n_{HCO_3^ - PU}}}} = \frac{x}{y} = \frac{7}{6}\)
Mà 2nCO3(PU) + nHCO3(PU) = 0,15 mol → nCO3 PU = 0,0525 mol và nHCO3 PU = 0,045 mol
→ nCO2 = 0,0975 mol → V = 2,184 lít
Đáp án A
Câu hỏi 13 :
Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M. Sau khi phản ứng kết thúc, thể tích khí CO2 thu được là
- A 224ml.
- B 336 ml.
- C 672ml.
- D 448ml.
Đáp án: A
Phương pháp giải:
Khi nhỏ từ từ H+ vào dd hỗn hợp CO32- và HCO3- xảy ra phản ứng:
H+ + CO32- → HCO3- (1)
H+ + HCO3- → CO2 + H2O (2)
=> nCO2(2) = ∑nH+ - nCO32- = ?
=> VCO2(thoát ra) = nCO2×22,4 = ?
Lời giải chi tiết:
nHCl = 0,03 (mol)
nNa2CO3 = 0,1.0,2 = 0,02 (mol) ; nNaHCO3 = 0,1.0,2 = 0,02 (mol)
Khi nhỏ từ từ H+ vào dd hỗn hợp CO32- và HCO3- xảy ra phản ứng:
H+ + CO32- → HCO3- (1)
H+ + HCO3- → CO2 + H2O (2)
=> nCO2(2) = ∑nH+ - nCO32- = 0,03 – 0,02 = 0,01 (mol)
=> VCO2(ddktc) = 0,01.22,4 = 0,224 (l) = 224 (ml)
Đáp án A
Câu hỏi 14 :
Dung dịch X gồm K2CO3 1M và Na2CO3 1M. Dung dịch Y gồm H2SO4 2M và HNO3 1M. Nhỏ từ từ 100ml dung dịch Y vào 200ml dung dịch X, thu được V lít khí CO2 (đktc) và dung dịch Z. Cho dung dịch Ba(OH)2 tới dư vào z, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m và V lần lượt là:
- A 59,1 và 1,12.
- B 105,7 và 1,12.
- C 59,1 và 2,24.
- D 105,7 và 2,24.
Đáp án: D
Câu hỏi 15 :
Nhỏ từ từ từng giọt đến hết 50 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,3M và NaHCO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, số mol CO2 thu được là
- A 0,040.
- B 0,020.
- C 0,025.
- D 0,035.
Đáp án: B
Phương pháp giải:
Cho từ từ dd HCl vào dd hỗn hợp Na2CO3 và NaHCO3 xảy ra phản ứng theo thứ tự sau:
PTHH: HCl + Na2CO3 → NaHCO3 + NaCl (1)
HCl + NaHCO3 → NaCl + CO2 + H2O (2)
Đổi số mol mối chất, PTHH (1) tính theo Na2CO3; PTHH (2) tính theo số mol HCl
Lời giải chi tiết:
100 ml = 0,1 (lít) ; 50 ml = 0,05 (lít)
nHCl = VHCl×CM HCl = 0,05×1 = 0,05 (mol)
nNa2CO3 = V.CM Na2CO3 = 0,1×0,3 = 0,03 (mol)
nNaHCO3 = V. CM NaHCO3 = 0,1×0,2 = 0,02 (mol)
Cho từ từ dd HCl vào dd hỗn hợp Na2CO3 và NaHCO3 xảy ra phản ứng theo thứ tự sau:
PTHH: HCl + Na2CO3 → NaHCO3 + NaCl (1)
(mol) 0,03Dư 0,02 ← 0,03 → 0,03
Kết thúc pư (1): nHCl dư = nHCl bđ – nHCl(1) = 0,05 – 0,03 = 0,02 (mol)
Tổng mol NaHCO3 = nNaHCO3 bđ + nNaHCO3 (1) = 0,02 + 0,03 = 0,05 (mol)
HCl + NaHCO3 → NaCl + CO2 + H2O (2)
bđ (mol) 0,02 0,05
pư (mol) 0,02 → 0,02 → 0,02
sau (mol) 0 0,03 0,02
Theo (2): nCO2 thu được = nHCl (2) = 0,02 (mol)
Đáp án B
15 bài toán cho từ từ muối cacbonat vào axit có đáp án và lời giải chi tiết
50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có đáp án và lời giải chi tiết
15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có đáp án và lời giải chi tiết
20 bài toán kim loại kiềm tác dụng với nước có đáp án và lời giải chi tiết
50 câu hỏi lý thuyết mức độ thông hiểu và vận dụng về kim loại kiềm có đáp án và lời giải chi tiết
50 câu hỏi lý thuyết mức độ nhận biết về kim loại kiềm có đáp án và lời giải chi tiết
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 15 bài toán cho từ từ axit vào muối cacbonat có lời giải
- 15 bài toán cho từ từ muối cacbonat vào axit có lời giải
- 50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có lời giải
- 20 bài tập CO2 tác dụng với dung dịch kiềm thổ có lời giải
- 15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có lời giải
- 50 câu hỏi lý thuyết mức độ vận dụng về ôn tập chương 6 có lời giải
- 50 câu hỏi lý thuyết mức độ thông hiểu về ôn tập chương 6 có lời giải
- 20 bài tập mức độ vận dụng cao nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 30 bài tập mức độ vận dụng nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 20 bài tập axit tác dụng với muối aluminat có lời giải









