Giải đề thi học kì II hóa 11 trường THPT Việt Đức - Hà Nội
Giải chi tiết đề thi kì 2 môn hoá lớp 11 năm 2019 - 2020 trường THPT Việt Đức với cách giải nhanh và chú ý quan trọng
Đề bài
I. PHẦN CHUNG
Câu 1 : Viết các phương trình hóa học thực hiện dãy chuyển hóa
CaC2 → C2H2 → CH3CHO → C2H5OH → C2H4
Câu 2: Viết PTHH của phản ứng trong các trường hợp sau; xác định sản phẩm chính (nếu có)
a, Butan -2- ol đun nóng với H2SO4 đặc 1700C
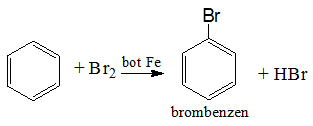
b, Cho benzen tác dụng với brom có bột Fe
Câu 3: Viết công thức cấu tạo và tên gọi các chất có công thức phân tử là C4H10
Câu 4: Kết quả thí nghiệm các chất X, Y, Z, T với thuốc thử được ghi vào bảng sau:
|
Dung dịch |
Thuốc thử |
Hiện tượng |
|
X |
Dung dịch AgNO3/NH3 |
Xuất hiện kết tủa màu vàng |
|
Y |
Cu(OH)2 |
Kết tủa tan, tạo dung dịch xanh lam |
|
Z |
Na |
Xuất hiện khí thoát ra |
|
T |
Dung dịch Brom |
Mất màu dung dịch brom |
X, Y, Z, T là những chất nào trong các chất sau: ancol etylic; pen -1- in; glixerol; pen-2-en?
Câu 5: Các nhận định sau là đúng hay sai:
- Khi oxi hóa hoàn toàn một ancol no, đơn chức, mạch hở thu được n CO2 > n H2O
- Ankan làm mất màu dung dịch nước brom
- Tất cả các ancol no, đơn chức đều có thể tham gia phản ứng tách nước tạo anken
- Phenol tan được trong dung dịch NaOH là đã phản ứng với NaOH tạo thành muối tan.
Câu 6: Đốt cháy hoàn toàn hỗn hợp gồm 2 hidrocacbon đồng đẳng kế tiếp thu được 1,568 lít CO2 (đktc) và 1,98 gam H2O. Tìm công thức và tính phần trăm thể tích mỗi hidrocacbon trên.
Câu 7: Cho m gam hỗn hợp X gồm phenol và etanol tác dụng với Na dư, thu được 6,72 lít khí (đktc). Nếu cho m gam hỗn hợp X trên tác dụng với dung dịch NaOH thì thấy có 200ml dung dịch NaOH 1M phản ứng. Tính giá trị của m
Câu 8. Hỗn hợp X gồm các hidrocacbon mạch hở (C2H6, C3H4, C2H2, C4H6) và H2. Cho 9,73 gam X vào dung dịch Br2 dư thì thấy có 0,43 mol Br2 tham gia phản ứng. Mặt khác đốt cháy hoàn toàn 14,56 lít hỗn hợp X cần V lít khí O2 (đktc) thu được 21,78 gam H2O. Tìm giá trị của V.
II. PHẦN RIÊNG (Học sinh chỉ được làm một trong 2 phần, phần A hoặc phần B)
A. Theo chương trình Chuẩn
Câu 9: Từ 336 gam ancol etylic pha được bao nhiêu ml cồn 70 độ, biết khố lượng riêng của C2H5OH là 0,8 g/ml?
Câu 10: Dẫn 1,12 lít anken X (đktc) vào dung dịch Br2 dư, thấy khối lượng bình brom tăng 2,8 gam
a, Xác định công thức phân tử của X
b, Viết CTCT của X biết cho X tác dụng với HCl thu được 1 sản phẩm duy nhất.
B. Theo chương trình Nâng cao
Câu 11: Tính khối lượng glucozo cần dùng để sản xuất 11,5 lít cồn 90 độ. Biết hiệu suất quá trình sản xuất là 90% và khối lượng riêng của C2H5OH là 0,8 g/ml
Câu 12: Cho V lít hỗn hợp khí X gồm andehit axetic và axetilen qua dung dịch AgNO3/NH3 dư, thu được 22,8 gam kết tủa. Nếu cho V lít hỗn hợp X trên tác dụng hết với hidro thấy có 3,36 lít khí hidro phản ứng. Tính giá trị của V (biết các thể tích khí đo ở đktc)
(Cho biết nguyên tử khối: H = 1; O =16; C = 12; Na = 23; K = 39; Ca = 40; Br = 80; Ag = 108)
Học sinh không được sử dụng bất kì tài liệu gì.
Lời giải chi tiết
I. PHẦN CHUNG
Câu 1:
Phương pháp
Xem lại phần tính chất hóa học điều chế axetilen, andehit, ancol, ..
Hướng dẫn giải
(1) CaC2 + H2O \(\to \)C2H2 + Ca(OH)2
(2) C2H2 + H2O \(\xrightarrow{{{t}^{0}},xt}\)CH3CHO
(3) CH3CHO + H2O \(\xrightarrow{{{t}^{0}},xt}\)C2H5OH
(4) C2H5OH \(\xrightarrow{{{170}^{0}},H+}\)C2H4 + H2O
Câu 2
Phương pháp
Xem lại phần tính chất hóa học của ancol và benzen và quy tắc tách Zaixep
Hướng dẫn giải
a, CH3-CH(OH)-CH2-CH3 \(\xrightarrow{{{t}^{0}},xt}\) CH2=CH-CH2-CH3 + H2O
CH3-CH=CH-CH3 (sp chính) + H2O
b,
Câu 3
Phương pháp
Xem lại cách viết đồng phân hidrocacbon có trong chương trình hóa học lớp 11
Hướng dẫn giải
C4H10 là 1 ankan, trong công thức cấu tạo chỉ có chứa liên kết đơn
Ta có:
CH3-CH2-CH2-CH3 : n- butan
CH3-CH(CH3)-CH3: 2-metyl propan hoặc iso butan
Câu 4:
Phương pháp giải:
Xem lại tổng hợp tính chất hóa học hidrocacbon và dẫn xuất hidrocacbon
Hướng dẫn giải
X tác dụng với AgNO3/NH3 thu được kết tủa vàng => X là ankin có chứa 1 liên kết 3 ở đầu mạch.
=> X là pen-1-in
Y tác dụng với Cu(OH)2 khiến kết tủa tan, tạo dung dịch xanh lam => Y là ancol đa chức, có ít nhất 2 nhóm –OH liền kề nhau trong mạch Cacbon
=> Y là glixerol
PTHH: C3H8O3 + Cu(OH)2 → (C3H7O3)2Cu + 2H2O
Z tác dụng với Na cho khí thoát ra => Z là ancol hoặc axit
> Z là ancol etylic
PTHH: C2H5OH + Na → C2H5ONa +1/2 H2
T tác dụng với dung dịch Brom khiến dung dịch brom bị mất màu => T có chứa liên kết pi trong CTPT
=> T là pen -2- en
PTHH:
CH3-CH=CH-CH2-CH3 + Br2 → CH3-CHBr-CHBr-CH2-CH3
Câu 5:
Phương pháp giải:
Xem lại phần tính chất hóa học chung của hidro cacbon và dẫn xuất hidrocacbon
Hướng dẫn giải
(1) Đúng vì ancol no, đơn chức mạch hở có CTTQ là CnH2n+2O (n>0)
Ta có PT: CnH2n+2O + 3n/2 O2 → n CO2 +(n +1) H2O
Theo tỉ lệ PTHH ta luôn có n CO2 < n H2O
(2) Sai vì ankan chỉ có chứa liên kết đơn trong CTPT mà không có chứa liên kết kém bền => không có phản ứng cộng => không làm mất màu được nước brom
(3) Đúng
(4) Đúng
Ta có phương trình:
C6H5OH + NaOH → C6H5ONa + H2O
Câu 6:
Phương pháp giải:
Tìm nCO2, nH2O => Nhận định xem 2 hidrocacbon này thuộc dãy đồng đẳng nào
=> Công thức phân tử trung bình
Mặt khác 2 ancol này thuộc dãy đồng đẳng liên tiếp
=> CTPT 2 hidrocacbon => phần trăm thể tích mỗi hidrocacbon.
Hướng dẫn giải:
nCO2 = 1,568 : 22,4 = 0,07 (mol)
nH2O = 1,98 : 18 = 0,11 (mol)
nH2O > nCO2
=> 2 hidro cacbon này thuộc dãy đồng đẳng của ankan
Gọi CTPT tổng quát của 2 hidrocacbon này là: CxH2x+2 (x>0)
Ta có phương trình hóa học:
CxH2x+2 + (3x+1)/2 O2 → xCO2 + (x+1)H2O
Vậy nCxH2x+2 = n H2O – n CO2 = 0,11 – 0,07 = 0,04 (mol)
=> Ta có x = n CO2/nCxH2x+2 = 0,07 : 0,04 = 1,75 (1)
2 hidrocacbon này thuộc dãy đồng đẳng liên tiếp
=> 2 hidro cacbon đó là CH4 và C2H6
Gọi nCH4 và nC2H6 lần lượt là a, b (mol)
Bảo toàn nguyên tố C ta có:
nCH4 + 2nC2H6 = nCO2 => a + 2b = 0,07 (3)
Bảo toàn nguyên tố H ta có
4nCH4 + 6nC2H6 = 2n H2O => 4a + 6b = 0,11 *2 (4)
Từ (3) và (4) => a = 0,01; b = 0,03
Vì tỉ lệ về thể tích cũng là tỉ lệ về số mol
=> %V CH4 = 0,01/(0,01 + 0,03) * 100% = 25%
%V C2H6 = 75%
Câu 7:
Phương pháp giải
- Xem lại tính chất hóa học của phenol và ancol.
- Dựa vào phương trình phản ứng để tính toán.
Hướng dẫn giải:
X (gồm phenol và etanol) tác dụng vừa đủ với 200ml NaOH 1M
Ta có:
C6H5OH + NaOH → C6H5ONa + H2O (1)
Từ (1) nNaOH = n C6H5OH = 0,2 * 1 = 0,2 (mol) (I)
X (gồm phenol và etanol) tác dụng với Na dư
nH2 = 6,72 : 22,4 = 0,3 (mol)
Ta có
C2H5OH + Na → C2H5ONa + ½ H2 (2)
C6H5OH + Na → C6H5ONa + ½ H2 (3)
Từ (3) => n H2 = ½ n C6H5OH = 0,1 (mol)
=> nH2(1) = 0,3 – nH2(3) = 0,3 – 0,1 = 0,2 (mol)
Từ (2) n C2H5OH = 2 nH2 = 2 * 0,2 = 0,4 (mol) (II)
Từ (I), (II) => m = mC2H5OH + m C6H5OH
= 0,2 * 94 + 0,4 * 46 = 37,2 (gam)
Câu 8:
Phương pháp giải:
Quy đổi hỗn hợp hidrocacbon trên thành: CH4, C2H2, H2
Gọi số mol của CH4, C2H2, H2 lần lượt là x, y,z
Áp dụng định luật bảo toàn khối lượng, bảo toàn nguyên tố => x, y, z
=> V O2
Hướng dẫn giải:
Quy đổi hỗn hợp trên thành: CH4, C2H2, H2
Xét 14,56 lít X
nX = 14,56 : 22,4 = 0,65 (mol)
=> x + y + z = 0,65 (I)
Khi đốt X thu được 1,21 mol H2O
Áp dụng định luật bảo toàn nguyên tố:
=> 2x + y + z = 1,21 (II)
Mặt khác, 9,73 gam X làm mất màu vừa đủ 0,43 mol Br2
=> Số liên kết pi trong 9,73 gam X là 0,43 mol
Mà số liên kết pi có trong 0,65 mol X bằng 2n C2H2 = 2y (mol)
Ta có tỉ lệ: (16x + 26y + 2z ) : 2y = 9,73 : 0,43 (III)
Từ (I), (II), (III) => x = 0,56; y = 0,43; z = - 0,34
Áp dụng định luật bảo toàn nguyên tố O ta có:
nO2 = nC + ¼ nH
= (0,56 + 0,43 * 2) + ¼ * ( 4 * 0,56 + 2 * 0,43 – 2 * 0,34) = 2,025 (mol)
V O2 = 2,025 * 22,4 = 45,36 (lít)
II. PHẦN RIÊNG
A. Theo chương trình Chuẩn
Câu 9:
Phương pháp giải
Từ khối lượng của rượu 70 độ => khối lượng của rượu và của nước => khối lượng của rượu
Hướng dẫn giải
V C2H5OH = m/D = 336 : 0,8 = 420 (ml)
Xét cồn 70 độ ta có:
100ml cồn 70 độ có chứa 70 ml rượu và 30 ml nước
=> x ml cồn 70 độ chứa 420 ml rượu
Vậy x = 420 : 70 * 100 = 600 ml
Vậy từ 336 gam ancol etylic thì ta thu được 600ml cồn 70 độ.
Câu 10:
Phương pháp giải:
Từ m Br2 dư => m anken => CTPT anken
Hướng dẫn giải:
Theo đề bài, khối lượng bình brom tăng lên 2,8 gam
=> manken = 2,8 gam => nanken = 1,12 : 22,4 = 0,05 (mol)
=> Manken = 2,8 : 0,05 = 56 (gam/mol)
Anken có dạng CnH2n
Vậy Manken = 14n = 56 => n = 4
Vậy anken cần tìm là C4H8
b, Các CTCT có thể có của X là:
CH2=CH-CH2-CH3 (1); CH3-CH=CH-CH3 (2); CH3-C(CH3)=CH2 (3)
Vì X tác dụng với HCl cho ra 1 sản phẩm duy nhất
=> chỉ có chất (2) thỏa mãn vì duy nhất chất đó đối xứng.
Vậy CTCT của X là CH3-CH=CH-CH3
B. Theo chướng trình Nâng cao
Câu 11:
Phương pháp giải:
Từ 11,5 lít cồn 90 độ => V cồn cần thu được (V cồn thực tế)
Từ H% => V cồn lý thuyết => m cồn lý thuyết => m glucozo
Hướng dẫn giải:
Xét 11,5 lít cồn 90 độ. => V cồn thực tế cần thu được là:
11,5 * 90 : 100 = 10,35 (l)
Khối lượng cồn thực tế cần thu được là:
m = V * D = 10,35 * 0,8 * 1000 = 8280 (gam)
Khối lượng cồn lý thuyết cần tạo ra là:
8280 : 90 * 100 = 9200 (gam)
Số mol cồn lý thuyết cần tạo ra là :
9200 : 46 = 200 (mol)
Ta có phương trình:
C6H12O6 \(\xrightarrow{{{t}^{0}},xt}\)2C2H5OH + 2CO2 (1)
nC6H12O6 = ½ C2H5OH = 100 (mol)
=> Khối lượng glucozo cần dùng là:
100 * 180 = 18000 gam = 18 kg
Câu 12:
Phương pháp giải:
Gọi số mol của CH3CHO; C2H2 lần lượt là x, y mol
Từ tỉ lệ của phương trình phản ứng => hệ phương trình 2 ẩn x, y => V
Hướng dẫn giải:
Gọi số mol của CH3CHO; C2H2 lần lượt là x, y mol
CH3CHO + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag + 2NH4NO3 (1)
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3 (2)
Từ (1) nAg = 2 nCH3CHO = 2x (mol)
(2) nC2Ag2 = nC2H2 = y (mol)
=> 108 * 2x + 240 * y = 22,8 (I)
CH3CHO + H2 \(\xrightarrow{{{t}^{0}},Ni}\)C2H5OH (3)
C2H2 +2H2 \(\xrightarrow{{{t}^{0}},Ni}\)C2H6 (4)
nH2 = 3,36 : 22,4 = 0,15 (mol)
Từ (3) nCH3CHO = nH2 = x (mol)
Từ (4) nC2H2 = 2 nH2 = 2y (mol)
=> x + 2y = 0,15 (II)
Từ (I) và (II) => x = y = 0,05 (mol)
Vậy V = (x + y) * 22,4 = 0,1 * 22,4 = 2,24 lít
Nguồn: Sưu tầm
Loigiaihay.com












Danh sách bình luận