10 bài tập vận dụng cao về amin có lời giải
Làm đề thiCâu hỏi 1 :
X, Y là hai amin no, hở; trong đó X đơn chức; Y hai chức; Z, T là hai ankan. Đốt cháy hoàn toàn 21,5g hỗn hợp H gồm X, T, Z, T (MZ < MX < MT < MY ; Z chiếm 36% về số mol hỗn hợp) trong oxi dư, thì thu được 31,86g H2O. Lấy cùng lượng H trên thì thấy tác dụng vừa đủ với 170 ml dung dịch HCl 2M. Biết X và T có số mol bằng nhau ; Y và Z có số nguyên tử cacbon bằng nhau. Tỉ lệ khối lượng của T so với Y có giá trị là
- A 1,051
- B 0,806
- C 0,595
- D 0,967
Đáp án: B
Phương pháp giải:
Qui đổi hỗn hợp H
$\left\{ \begin{gathered}
{M_Z} < {\text{ }}{M_X} < {\text{ }}{M_T} < {\text{ }}{M_Y} \hfill \\
{n_X} = {n_T} \hfill \\
Y,Z\,cung\,C \hfill \\
\end{gathered} \right. \Leftrightarrow \left\{ \begin{gathered}
Z:C{H_4}(M = 16):a \hfill \\
X:C{H_3}N{H_2}(M = 31):b \hfill \\
T:{C_3}{H_8}(M = 44):b \hfill \\
Y:C{H_2}{(N{H_2})_2}(M = 46):c \hfill \\
C{H_2}:d \hfill \\
\end{gathered} \right.$
$\left\{ \begin{gathered}
{m_H} = 16a + (31 + 44)b + 46c + 14d = 21,5 \hfill \\
{n_Z} = 0,36{n_H} = > a = 0,36(a + 2b + c) \hfill \\
{n_{{H_2}O}} = 2a + (2,5 + 4)b + 3c + d = 1,77 \hfill \\
{n_{HCl}} = b + 2c = 0,34 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
a = 0,18 \hfill \\
b = 0,1 \hfill \\
c = 0,12 \hfill \\
d = 0,4 \hfill \\
\end{gathered} \right.$
Tiến hành ghép CH2, tạo lại hỗn hợp H
$H\left\{ \begin{gathered}
Z:C{H_4}(M = 16):0,18 \hfill \\
X:C{H_3}N{H_2}(M = 31):0,1 \hfill \\
T:{C_3}{H_8}(M = 44):0,1 \hfill \\
Y:C{H_2}{(N{H_2})_2}(M = 46):0,12 \hfill \\
C{H_2}:0,4 = 0,18 + 0,1 + 0,12 \hfill \\
\end{gathered} \right. \Leftrightarrow \left\{ \begin{gathered}
Z:{C_2}{H_6}(M = 30):0,18 \hfill \\
X:C{H_3}N{H_2}(M = 31):0,1 \hfill \\
T:{C_4}{H_{10}}(M = 58):0,1 \hfill \\
Y:{C_2}{H_4}{(N{H_2})_2}(M = 60):0,12 \hfill \\
\end{gathered} \right. \to \frac{{{m_T}}}{{{m_Y}}} = 0,806$
Đáp án B
Câu hỏi 2 :
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hidrocacbon mạch hở có số liên kết pi nhỏ hơn 3. Trộn X và Y theo tỷ lệ mol nx:ny=1:5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17g hỗn hợp Z cần vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2,H2 và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của hidrocacbon có phân tử khối lớn hơn trong Y gần nhất với giá trị nào?
- A 71%
- B 79%
- C 57%
- D 50%
Đáp án: A
Phương pháp giải:
- BTKL=>mN2
- Gọi số mol CO2 và H2O. Dựa vào khối lượng bình tăng và BTNT O lập hệ và giải
- Tính Ctb và Htb suy ra 2 hiđrocacbon
Lời giải chi tiết:
nO2=0,3125 mol
BTKL=>mN2=3,17+0,3125.32-12,89=0,28 gam=>nN2=0,01 mol=>n amin=0,02 mol => n hiđrocacbon=0,1 mol
- Giả sử số mol CO2 và H2O lần lượt là x, y
44x+18y=12,89
0,3125.2=2x+y (BTNT: O)
=>x=0,205; y=0,215
Ctb=0,205/0,12=1,7 => CH4
Htb=0,215/0,12=1,8 => C2H2 (Do số liên kết pi nhỏ hơn 3)
Đặt:
C2H7N: a
C3H9N: 0,02-a
CH4: b
C2H2: 0,1-b
+ BTNT C: 2a+3(0,02-a)+b+2(0,1-b)=0,205
+ BTNT H: 7a+9(0,02-a)+4b+2(0,1-b)=0,215.2
=>a=0,015;b=0,04 => CH4 (0,04 mol) C2H2 (0,06 mol)
=>%mC2H2=0,06.26/(0,06.26+0,04.16)=71%
Đáp án A
Câu hỏi 3 :
Đun 7,36 gam ancol A với H2SO4, đặc ở 170oC thu được 2,688 lít olefin (đktc) với hiệu suất 75%. Cho 0,1 mol amin no B phản ứng tối đa với 0,2 mol HCl thu được 11,9 gam muối. Đốt cháy m gam hỗn hợp X gồm A và B bằng một lượng oxi vừa đủ rồi dẫn toàn bộ sản phẩm cháy vào bình chứa 100 gam dung dịch H2SO4 đặc 81,34%, sau khi hơi nước được hấp thụ hoàn toàn thấy nồng độ H2SO4 lúc bấy giờ là 70%. Biết CO2, N2 không bị nước hấp thụ. Giá trị m gần giá trị nào nhất sau đây
- A 14
- B 12
- C 13
- D 15
Đáp án: A
Phương pháp giải:
+ Tách nước A: n olefin = n ancol pư => n ancol bđ = n ancol pư/H% => M ancol => ancol
+ Amin B tác dụng với HCl: BTKL m amin = m muối – mHCl = > M amin
+ Ta thấy ancol và amin đều chứa 6H trong phân tử nên khi đốt đều cho 3H2O. Từ số mol H2O => số mol hỗn hợp
Mà M ancol = M amin => m
Lời giải chi tiết:
+ Tách nước A: n olefin = 0,12 mol => n ancol = 0,12.100/75 = 0,16 mol => M ancol = 7,36/0,16 = 46 (C2H6O)
+ Amin B tác dụng với HCl: BTKL m amin = m muối – mHCl = 11,9 – 0,2.36,5 = 4,6 => M amin = 4,6/0,1 = 46 (CH6N2)
+ Đốt cháy X (A và B) thu được x mol nước rồi dẫn vào H2SO4 đặc
nH2SO4 = 81,34 gam
Nồng độ dung dịch H2SO4 sau khi hấp thụ là: 81,34/(18x+100) = 70/100 => x = 0,9 mol
X (6H) → 3H2O
0,3 ← 0,9
Do MA = MB = 46 => mX = 0,3.46 = 13,8 gam
Đáp án A
Câu hỏi 4 :
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết (∏) nhỏ hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY = 1: 5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
- A 71%.
- B 70%.
- C 29%.
- D 30%
Đáp án: B
Phương pháp giải:
Gọi số mol của X và Y lần lượt là a và 5a (mol)
BTKL: mZ + mO2 = mCO2 + mH2O + mN2 (1)
mCO2 + mH2O = m bình NaOH tăng (2)
Từ (1) và (2) => mN2 = ? => nN2 = ? (mol)
BTNT N => nX = 2nN2 = ? (mol)
=> nZ = 6nX = ? (mol)
Gọi x và y lần lượt là số mol của CO2 và H2O
BTKL CO2 + H2O và BTNT O => tìm được x, y
Số C trung bình trong Z là: \(\overline C = \frac{{{n_{C{O_2}}}}}{{{n_Z}}} = ?\)
=> Y phải có CH4
TH1: Hidrocacbon còn lại trong Y không có liên kết pi
TH2: Hidrocacbon còn lại trong Y không có 1 liên kết pi
TH3: Hidrocacbon còn lại trong Y không có 2 liên kết pi
Trong mỗi trường hợp sử dụng mối quan hệ của H2O và CO2 để xem trường hợp nào thỏa mãn
Lời giải chi tiết:
nO2 = 7/22,4 = 0,3125 (mol)
Gọi số mol của X và Y lần lượt là a và 5a (mol)
BTKL: mZ + mO2 = mCO2 + mH2O + mN2
=> mCO2 + mH2O + mN2 = 3,17 + 0,3125.32 =13,17(g) (1)
Khối lượng dung dịch NaOH đặc tăng chính là khối lượng của CO2 và H2O
=> mCO2 + mH2O = 12,89 (g) (2)
Từ (1) và (2) => mN2 = 0,28 (g) => nN2 = 0,01 (mol)
BTNT N => nX = 2nN2 = 0,02 (mol)
=> nZ = 6nX = 0,12 (mol)
Gọi x và y lần lượt là số mol của CO2 và H2O
\(\left\{ \begin{gathered}
\sum {{m_{(C{O_2} + {H_2}O)}}} = 44x + 18y = 12,89 \hfill \\
\xrightarrow{{BTNT\,:\,O}}2x + y = 0,3125.2 \hfill \\
\end{gathered} \right. = > \left\{ \begin{gathered}
x = 0,205 \hfill \\
y = 0,215 \hfill \\
\end{gathered} \right.\)
Số C trung bình trong Z là: \(\overline C = \frac{{{n_{C{O_2}}}}}{{{n_Z}}} = \frac{{0,205}}{{0,12}} = 1,7\)
=> Y phải có CH4
TH1: Hidrocacbon còn lại trong Y không có liên kết pi
=> nH2O – nCO2 = 1,5namin + nY => ta thấy không thỏa mãn vì: 0,01 #0,08 => loại
TH2: Hidrocacbon còn lại trong Y không có 1 liên kết pi
=> nH2O – nCO2 = 1,5namin + nCH4 ( Vì đốt HC có 1 liên kết pi cho mol CO2 = H2O )
=> nCH4 = ( 0,215 – 0,205) – 1,5.0,02 = - 0,02 (mol) < 0 => loại
TH3: Hidrocacbon còn lại trong Y không có 2 liên kết pi
Gọi a và b lần lượt là số mol của CH4 và CmH2m-2 trong Y
\(\left\{ \begin{gathered}
\sum {{n_Y} = a + b = 0,1} \hfill \\
{n_{{H_2}O}} - {n_{C{O_2}}} = 1,5{n_{a\min }} + (a - b) \hfill \\
\end{gathered} \right. = > \left\{ \begin{gathered}
a + b = 0,1 \hfill \\
0,01 = 1,5.0,02 + (a - b) \hfill \\
\end{gathered} \right. = > \left\{ \begin{gathered}
a = 0,04 \hfill \\
b = 0,06 \hfill \\
\end{gathered} \right.\)
Gọi CTPT chung của 2 amin là:
\(\begin{gathered}
\left\{ \begin{gathered}
{C_{\overline n }}{H_{2\overline n + 3}}N:0,01\,mol \hfill \\
C{H_4}:0,04\,mol \hfill \\
{C_m}{H_{2m - 2}}:\,0,06\,mol \hfill \\
\end{gathered} \right.\xrightarrow{{BTNT:\,C}}{n_{C{O_2}}} = 0,01\overline n + 0,04 + 0,06m = 0,205 \hfill \\
= > 2 < \overline n = \frac{{0,165 - 0,06m}}{{0,02}} < 3 \hfill \\
= > 1,75 < m < 2,08 \hfill \\
= > m = 2 = > {C_2}{H_2} \hfill \\
= > \overline n = 2,25 \hfill \\
\end{gathered} \)
Gọi u và v lần lượt là số mol của C2H7N và C3H9N
\(\begin{gathered}
\left\{ \begin{gathered}
\sum {{n_X} = u + v = 0,02} \hfill \\
\overline n = \frac{{2u + 3v}}{{0,02}} = 2,25 \hfill \\
\end{gathered} \right. = > \left\{ \begin{gathered}
u = 0,015\,mol \hfill \\
v = 0,005\,mol \hfill \\
\end{gathered} \right. \hfill \\
= > \% {C_2}{H_7}N = \frac{{0,015.45}}{{0,015.45 + 0,005.59}}.100\% = 69,58\% \hfill \\
\end{gathered} \)
Gần nhất với 70%
Đáp án B
Câu hỏi 5 :
Người ta mô tả hiện tượng thu được ở một số thí nghiệm như sau:
(1) Nhỏ vài giọt dung dịch etylamin vào dung dịch hỗn hợp NaNO2 và HCl ở nhiệt độ thường thấy xuất hiện bọt khí.
(2) Đưa đũa thủy tinh vừa nhúng vào dung dịch HCl đậm đặc lên miệng lọ đựng dung dịch CH3NH2 đậm đặc thấy xung quanh đũa thủy tinh bay lên một làn khói trắng.
(3) Nhỏ vài giọt anilin vào nước, lắc kĩ thấy có vẩn đục. Nhỏ tiếp vài giọt dung dịch HCl đặc thấy vẩn đục tan, tạo dung dịch trong suốt.
(4) Nhỏ vài giọt nước brom vào ống nghiệm đựng sẵn vài giọt anilin, thấy trong ống nghiệm xuất hiện kết tủa màu vàng.
(5) Thêm vài giọt phenolphtalein vào dung dịch đimetylamin thấy xuất hiện màu xanh.
(6) Cho từ từ đến dư dung dịch CH3NH2 vào dung dịch FeCl3 thì lúc đầu có kết tủa màu nâu đỏ xuất hiện, sau đó kết tủa tan dần đến hết.
Số thí nghiệm mô tả đúng hiện tượng là
- A 6
- B 4
- C 5
- D 3
Đáp án: D
Lời giải chi tiết:
Trong số các mô tả đã cho, có thí nghiệm mô tả đúng hiện tượng: (1), (2), (3).
(1) đúng. C2H5NH2 + HNO2 → C2H5OH + N2 + H2O.
(2) đúng. Khí metylamin bay lên gặp hơi axit HCl đã xảy ra phản ứng tạo muối: CH3NH2 + HCl → CH3NH3Cl.
(3) đúng. Anilin hầu như không tan trong nước, nó tạo vẩn đục rồi lắng xuống đáy. Nhỏ HCl đặc vào ống nghiệm, anilin tan dần tạo dung dịch trong suốt do có phản ứng: C6H5NH2 + HCl → C6H5NH3Cl (tan tốt trong nước).
Chú ý: Nếu ta nhỏ tiếp NaOH, ta lại thấy dung dịch xuất hiện vẩn đục vì:
C6H5NH3Cl + NaOH → C6H5NH2 + NaCl
(4) sai. C6H5NH2 tác dụng với nước brom tạo kết tủa trắng.
(5) sai. Nhỏ vài giọt phenolphtalein vào dung dịch đimetylamin thấy xuất hiện màu hồng vì dd đimetylamin có môi trường bazơ.
(6) sai. Phản ứng giữa dung dịch CH3NH2 với FeCl3 có sinh ra kết tủa màu nâu đỏ Fe(OH)3 nhưng kết tủa này không bị tan trong dung dịch CH3NH2 dư.
Đáp án D
Câu hỏi 6 :
Cho 1,22 gam hỗn hợp X gồm hai amin bậc một (tỉ lệ mol là 1:2) tác dụng vừa đủ với 400 ml dung dịch HCl 0,1M thu được dung dịch Y. Mặt khác, khi đốt cháy hoàn toàn 0,09 mol hỗn hợp X thu được hỗn hợp khí và hơi. Dẫn toàn bộ hỗn hợp khí và hơi đó vào dung dịch Ba(OH)2 dư, lạnh thì thu được m gam kết tủa và thoát ra 1,344 lít (đktc) một khí duy nhất. Giá trị của m là
- A 23,64.
- B 78,8.
- C 11,82.
- D 39,40.
Đáp án: A
Lời giải chi tiết:
\(\begin{array}{l}T{N_1}:\,\,1,22\,gX + HCl:0,04\,mol \to \\ \Rightarrow {n_{N(hh1)}} = {n_{HCl}} = 0,04\,mol.\\T{N_2}:\,\,0,09\,mol\,X + {O_2} \to \left\{ \begin{array}{l}C{O_2}\\{H_2}O\\{N_2}\end{array} \right. + Ba{(OH)_2} \to \left\{ \begin{array}{l}m\,g \downarrow BaC{O_3}\\0,06\,mol\, \uparrow \end{array} \right.\\ \Rightarrow {n_{{N_2}}} = 0,06 \Rightarrow {n_{N{\kern 1pt} (hh2)}} = 0,12\,mol = 3{n_{N(hh1)}}\\ \Rightarrow {m_{X(T{N_2})}} = 3{m_{X(T{N_1})}} = 3,66\,gam.\end{array}\)
Ntb = 0,12/0,09 = 4/3 → X có chứa 1 amin đơn chức RNH2 (a mol); amin còn lại là amin đa chức R’(NH2)n (b mol) (Xét trong 3,66 gam X)
Tỉ lệ mol của 2 amin là 1: 2 → có 2 TH:
\(\begin{array}{l} + T{H_1}:\left\{ \begin{array}{l}a + b = 0,09\\b = 2a\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,03\\b = 0,06\end{array} \right.\\ \Rightarrow {n_N} = 0,12 = 0,03.1 + 0,06.n \Rightarrow n = 1,5\,(loai)\\ + T{H_2}:\left\{ \begin{array}{l}a + b = 0,09\\a = 2b\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,06\\b = 0,03\end{array} \right.\\ \Rightarrow \left\{ \begin{array}{l}{n_N} = 0,12 = 0,06.1 + 0,03.n\\0,06(R + 16) + 0,03(R' + 16n) = 3,66\end{array} \right. \Rightarrow \left\{ \begin{array}{l}n = 22\\R + R' = 58\end{array} \right.\\ \Rightarrow \left\{ \begin{array}{l}n = 2\\R = 15;R' = 28\end{array} \right.\\ \Rightarrow X\left\{ \begin{array}{l}C{H_3}N{H_2}:0,06\,mol\\{C_2}{H_4}{(N{H_2})_2}:0,03\,mol\end{array} \right. + {O_2} \to 0,12\,mol\,C{O_2} + Ba{(OH)_2} \to m\,g\,BaC{O_3}\\ \Rightarrow m = 0,12.197 = 23,64\,gam\end{array}\)
Đáp án A
Câu hỏi 7 :
Hỗn hợp X chứa etylamin và trimetylamin. Hỗn hợp Y chứa 2 hiđrocacbon mạch hở có số liên kết pi nhở hơn 3. Trộn X và Y theo tỉ lệ mol nX : nY = 1:5 thu được hỗn hợp Z. Đốt cháy hoàn toàn 3,17 gam hỗn hợp Z cần dùng vừa đủ 7,0 lít khí oxi (đktc), sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch NaOH đặc, dư thấy khối lượng dung dịch tăng 12,89 gam. Phần trăm khối lượng của etylamin trong X gần nhất với giá trị nào sau đây?
- A 21%.
- B 70%.
- C 79%.
- D 30%.
Đáp án: B
Phương pháp giải:
\(3,17\,g\,Z\left\{ \begin{array}{l}{C_n}{H_{2n + 3}}N:z\\{C_m}{H_{2m + 2 - 2\bar k}}:5z\end{array} \right. + {O_2}:0,3125\,mol \to \left\{ \begin{array}{l}C{O_2}:a\\{H_2}O:b\\{N_2}:0,5z\end{array} \right. + NaOH \to \Delta m = 12,89\,gam\)
+ Khối lượng dung dịch NaOH tăng lên = tổng khối lượng CO2 và H2O (N2 không bị hấp thụ nên thoát ra ngoài).
+ Biết số mol O2 và tổng khối lượng (CO2 + H2O) → kết hợp với BTNT oxi, ta tìm được số mol CO2, H2O.
+ BTKL (hoặc BTNT trong hỗn hợp Z) ta tìm được số mol N2 → tìm được z.
+ Xử lí tiếp bài toán theo các hướng như: tìm số nguyên tử C, H trung bình của Z; dựa vào hiệu số mol H2O và CO2; dựa vào số mol CO2, ….
Lời giải chi tiết:
\(\begin{array}{l}3,17\,g\,Z\left\{ \begin{array}{l}{C_n}{H_{2n + 3}}N:z\\{C_m}{H_{2m + 2 - 2\bar k}}:5z\end{array} \right. + {O_2}: + 0,3125\,mol \to \left\{ \begin{array}{l}C{O_2}:a\\{H_2}O:b\\{N_2}:0,5z\end{array} \right. + NaOH \to \Delta m = 12,89gam\\ \Rightarrow \left\{ \begin{array}{l}{m_{C{O_2}}} + {m_{{H_2}O}} = \Delta m = 12,892\\{n_{C{O_2}}} + {n_{{H_2}O}} = 2{n_{{O_2}}}(BTNT)\end{array} \right. \Rightarrow \left\{ \begin{array}{l}44a + 18b = 12,892\\a + b = 2.0,3125\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,205\\b = 0,215\end{array} \right.\\{m_Z} = {m_C} + {m_H} + {m_N} \Rightarrow {m_N} = 3,17 - (12.0,205 + 2.0,215) = 0,28gam\\ \Rightarrow {n_N} = 0,02\,mol \Rightarrow z = 0,02 \Rightarrow {n_Y} = 5z = 0,1\\{n_{{H_2}O}} - {n_{C{O_2}}} = 0,01 = 1,5z + 5z.(1 - \bar k) \Rightarrow \bar k = 1,2\\{n_Z} = 6z = 0,12\,mol \Rightarrow \bar C = \frac{{{n_{C{O_2}}}}}{{{n_Z}}} = 1,708;\,\bar H = \frac{{{n_H}}}{{{n_Z}}} = 3,583\end{array}\)
Vì X chứa 2 amin C2H7N và C3H9N, đều có số nguyên tử C > 1,708 và H > 3,583
→ Y chứa một hiđrocacbon có số nguyên tử C < 1,708 → Y chứa CH4.
Hai hiđrocacbon trong Y có số liên kết pi nhỏ hơn 3, mà CH4 (k=0) và = 1,2
→ hiđrocacbon còn lại Y2 có k = 2 và số nguyên tử H < 3,583 → Y2: C2H2
\(\begin{array}{l}\bar k = {\rm{ }}1,2 \Rightarrow PP\,duong\,cheo \Rightarrow \frac{{{n_{C{H_4}}}(k = 0)}}{{{n_{{Y_2}}}(k = 2)}} = \frac{{\left| {2 - 1,2} \right|}}{{\left| {0 - 1,2} \right|}} = \frac{2}{3}\\ \Rightarrow {n_{C{H_4}}} = 2z = 0,04;\,{n_{{Y_2}}} = 0,06\,mol\\{n_{C{O_2}}} = 0,205 = n.x + {n_{C{H_4}}} + 2{n_{{C_2}{H_2}}} \Rightarrow n = \frac{{0,205 - 0,04 - 2.0,06}}{{0,02}} = 2,25\\X\left\{ \begin{array}{l}{C_2}{H_7}N:x\\{C_3}{H_9}N:y\end{array} \right. \Rightarrow \left\{ \begin{array}{l}x + y = 0,02\\2x + 3y = 2,25.0,02 = {n_C}\end{array} \right. \Rightarrow \left\{ \begin{array}{l}x = 0,015\\y = 0,005\end{array} \right.\\ \Rightarrow \% {C_2}{H_7}N(X) = \frac{{0,015.45}}{{0,015.45 + 0,005.59}}.100\% = 69,59\% \end{array}\)
Đáp án B
Câu hỏi 8 :
Hợp chất hữu cơ X (C8H15O4N) tác dụng với dung dịch NaOH dư, đun nóng, thu được sản phẩm hữu cơ gồm muối đinatri glutamat và ancol. Số công thức cấu tạo của X là
- A 3
- B 6
- C 4
- D 5
Đáp án: B
Phương pháp giải:
Viết các đồng phân cấu tạo thỏa mãn các dữ kiện đề bài.
+ 2 chức este
+ 1 chức este và 1 chức axit
Lời giải chi tiết:
Các công thức cấu tạo thỏa mãn của X là:
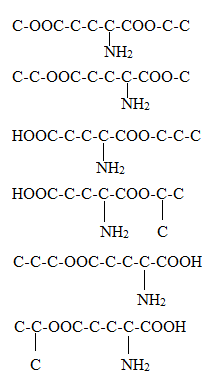
Đáp án B
Câu hỏi 9 :
Hỗn hợp X gồm glyxin, alanin, valin, metylamin và trimetylamin. Đốt cháy hoàn toàn 0,18 mol hỗn hợp X cần dùng vừa đủ 0,615 mol O2. Sản phẩm cháy gồm CO2, H2O và N2 (trong đó số mol CO2 là 0,40 mol). Cho lượng X trên vào dung dịch KOH dư thấy có a mol KOH tham gia phản ứng. Giá trị của a là:
- A 0,08.
- B 0,09.
- C 0,07.
- D 0,06.
Đáp án: A
Phương pháp giải:
Đặt số mol của amino axit, amin, H2O lần lượt là x, y, z
*nX => (1)
*BTNT “O”: 2n amino axit + 2nO2 = 2nCO2 + nH2O => (2)
*Peptit có dạng CnH2n+1O2N => n peptit = (nH2O – nCO2)/0,5
=> nH2O - nCO2 = 0,5 n peptit
Amin có dạng CmH2m+3N => n amin = (nH2O – nCO2)/1,5
=> nH2O – nCO2 = 1,5n amin
=> ∑nH2O – ∑nCO2 = 0,5 n peptit + 1,5n amin => (3)
Giải (1) (2) (3) thu được: x; y; z
Khi cho hỗn hợp tác dụng với KOH thì chỉ có amino axit phản ứng: nKOH = n amino axit = x
Lời giải chi tiết:
Đặt số mol của amino axit, amin, H2O lần lượt là x, y, z
*nX = x + y = 0,18 (1)
*BTNT “O”: 2n amino axit + 2nO2 = 2nCO2 + nH2O => 2x + 0,615.2 = 2.0,4 + z (2)
*Peptit có dạng CnH2n+1O2N => n peptit = (nH2O – nCO2)/0,5
=> nH2O - nCO2 = 0,5 n peptit
Amin có dạng CmH2m+3N => n amin = (nH2O – nCO2)/1,5
=> nH2O – nCO2 = 1,5n amin
=> ∑nH2O – ∑nCO2 = 0,5 n peptit + 1,5n amin => z – 0,4 = 0,5x + 1,5y (3)
Giải (1) (2) (3) thu được: x = 0,08; y = 0,1; z = 0,59
Khi cho hỗn hợp tác dụng với KOH thì chỉ có amino axit phản ứng: nKOH = n amino axit = x = 0,08 mol
Đáp án A
Câu hỏi 10 :
X, Y là hai amin no, đơn chức, mạch hở, cùng dãy đồng đẳng liên tiếp (MX < MY). Z, T là hai ankin có MT = MZ + 28. Đốt cháy hoàn toàn 16,24 gam hỗn hợp E gồm X, Y, Z, T thu được 36,96 gam CO2 và 20,16 gam H2O. Biết số mol Z lớn hơn số mol T; X và Y có tỉ lệ mol tương ứng 5 : 2. Dẫn 16,24 gam E qua lượng dư dung dịch AgNO3 trong NH3, đến khi các phản ứng kết thúc thu được m gam kết tủa. Giá trị lớn nhất của m là
- A 30,44.
- B 25,70.
- C 31,00.
- D 21,42.
Đáp án: D
Phương pháp giải:
+ mN = mE - mC - mH => nN = namin
+ n’H2O - n’CO2 = 1,5namin
n"H2O - n”CO2 = 1,5namin
Cộng 2 vế: nH2O - nCO2 = 1,5namin - nankin => nankin
+ Biện luận tìm amin và ankin
Lời giải chi tiết:
nCO2 = 0,84 mol; nH2O = 1,12 mol
nC = 0,84 mol; nH = 2,24 mol
=> mN = mE - mC - mH = 16,24 - 0,84.12 - 2,24 = 3,92g
=> nN = namin = 0,28 mol
=>nX = 0,2 mol; nY = 0,08 mol
n’H2O - n’CO2 = 1,5namin
n”H2O - n”CO2 = -nankin
Cộng 2 vế: nH2O - nCO2 = 1,5namin - nankin => 1,12 - 0,84 = 1,5.0,28 - nankin => nankin = 0,14 mol
nE = 0,28 + 0,14 = 0,42
Ctb = 0,84/0,42 = 2 => Amin: CH5N và C2H7N
CH5N: 0,2
C2H7N: 0,08
CnH2n-2: 0,14
16,24 = 31.0,2 + 45.0,08 + 0,14(14n - 2) => n = 3,4 (C3H4 và C5H8 hoặc C2H2 và C4H6)
nZ > nT => C3H4: x và C5H8: y
x + y = 0,14
3x + 5y = 0,84 - 0,2 - 0,08.2
=> x = 0,11; y = 0,03 (x > y thỏa mãn)
m = mC3H3Ag + mC5H7Ag = 0,11.147 + 0,03.175 = 21,42 gam
Đáp án D
30 bài tập tổng hợp về amin đầy đủ trắc nghiệm và tự luận có đáp án và lời giải chi tiết (phần 1)
40 bài tập vận dụng về amin tác dụng với dung dịch muối đầy đủ trắc nghiệm và tự luận có đáp án và lời giải chi tiết
30 bài tập về đốt cháy amin mức độ vận dụng đầy đủ trắc nghiệm và tự luận có đáp án và lời giải chi tiết
25 bài tập về đốt cháy amin mức độ vận dụng cơ bản cả trắc nghiệm và tự luận có đáp án và lời giải chi tiết
50 câu hỏi lý thuyết mức độ nhận biết về amin đầy đủ cả trắc nghiệm và tự luận có đáp án và lời giải chi tiết (phần 2)
50 câu hỏi lý thuyết mức độ nhận biết về amin từ dễ đến khó, đầy đủ trắc nghiệm và tự luận có đáp án và lời giải chi tiết (phần 1)
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 15 bài toán cho từ từ axit vào muối cacbonat có lời giải
- 15 bài toán cho từ từ muối cacbonat vào axit có lời giải
- 50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có lời giải
- 20 bài tập CO2 tác dụng với dung dịch kiềm thổ có lời giải
- 15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có lời giải
- 50 câu hỏi lý thuyết mức độ vận dụng về ôn tập chương 6 có lời giải
- 50 câu hỏi lý thuyết mức độ thông hiểu về ôn tập chương 6 có lời giải
- 20 bài tập mức độ vận dụng cao nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 30 bài tập mức độ vận dụng nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 20 bài tập axit tác dụng với muối aluminat có lời giải









