Đề tham khảo thi THPT môn Hóa - Đề số 3 (hay, chi tiết)
Khi thay thế nhóm …(1) ở nhóm …(2) của carboxylic acid bằng nhóm
Đề bài
Khi thay thế nhóm …(1) ở nhóm …(2) của carboxylic acid bằng nhóm …(3)… thì thu được ester. Nội dung phù hợp trong các ô trống (1), (2), (3) lần lượt là
-
A.
– COO - ; - OH; OR
-
B.
– OH; -COO-; OR
-
C.
– OR; - COOH; - OH
-
D.
– OH; - COOH; - OR
Thạch cao nung được dùng để đúc tương, bó bột khi hãy xương. Công thức hóa học của thạch cao nung là
-
A.
CaSO4
-
B.
CaSO4.2 H2O
-
C.
CaSO4.0,5H2O
-
D.
Ca3(PO4)2
Tơ nào sau đây thuộc loại tơ bán tổng hợp?
-
A.
Tơ nitron
-
B.
Tơ nylon – 6,6
-
C.
Tơ tằm
-
D.
Tơ cellulose acetate
Phức chất [Cu(H2O)6]2+ có dạng hình học là
-
A.
bát diện
-
B.
đường thẳng
-
C.
Tứ diện
-
D.
lục giác
Kim loại nào sau đây có thể điều chế bằng phương pháp thủy luyện?
-
A.
Na
-
B.
K
-
C.
Ag
-
D.
Mg
Nước chứa nhiều các ion nào sau đây có tính cứng toàn phần?
-
A.
Mg2+, Ca2+, HCO3- , SO42-.
-
B.
Na+, K+, SO42-, Cl-.
-
C.
Mg2+, Ca2+, HCO3-.
-
D.
Mg2+, Ca2+, SO42-, Cl-.
Có các thí nghiệm sau:
(a) Nhúng thanh sắt (iron) vào dung dịch H2SO4 loãng, nguội.
(b) Sục khí SO2 vào nước bromine.
(c) Cho dung dịch BaCl2 tác dụng với dung dịch H2SO4 loãng.
(d) Nhúng lá nhôm (aluminium) vào dung dịch H2SO4 đặc, nguội.
Số thí nghiệm xảy ra phản ứng hoá học là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Kim loại nào sau đây có tính khử mạnh nhất?
-
A.
K
-
B.
Mg
-
C.
Fe
-
D.
Na
Ethanol là một chất lỏng, có nhiệt độ sôi là 78,3oC và tan nhiều trong nước. Phương pháp tách riêng được ethanol từ hỗn hợp ethanol và nước là
-
A.
lọc.
-
B.
chiết.
-
C.
cô cạn.
-
D.
chưng cất.
Thủy phân C4H8O2 trong dung dịch NaOH thu được sodium acetate và alcohol X. Công thức X là
-
A.
CH3OH
-
B.
C2H5OH
-
C.
C3H7OH
-
D.
H2O
Dung dịch nào sau đây không làm quỳ tím hóa xanh?
-
A.
Phenylamine.
-
B.
Dimethylamine.
-
C.
Ethylamine.
-
D.
Methylamine.
Maltose có nhiều trong đường mạch nha. Công thức phân tử của maltose là
-
A.
C6H12O6
-
B.
C12(H2O)11
-
C.
(C6H10O5)n
-
D.
C6(H2O)n
Khi nấu món canh làm từ thịt cua, tôm, tép có nhiều mảng thịt đóng rắn lại. Hiện tượng trên gây ra bởi tính chất nào sau đây?
-
A.
Sự đông tụ protein bởi sự thay đổi pH.
-
B.
Sự đông tụ protein bởi nhiệt độ.
-
C.
Kết tủa carbonate của các chất khoáng có trong vỏ.
-
D.
Sự thuỷ phân protein bởi nhiệt độ.
Tên thông thường của acid CH3COOH là
-
A.
methanol
-
B.
acetic acid
-
C.
propanoic acid
-
D.
formic acid
Chất nào sau đây thuộc loại α – amino acid?
-
A.
CH2(NH2)COOH
-
B.
CH3NH2
-
C.
CH3COOH
-
D.
H2N – CH2 – CH2 – COOH
Insulin là hormon có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp có chứa các peptide: Glu- Gln-Cys, Gly-Ile-Val, Gln-Cys-Cys, Val-Glu-Gln. Nếu đánh số thứ tự amino acid đầu N là số 1 thì amino acid ở vị trí số 4 trong X là
-
A.
Gln.
-
B.
Val.
-
C.
Glu.
-
D.
Cys.
-
A.
Điện cực Zn là anode, điện cực Cu là cathode.
-
B.
Điện cực Zn là cathode, điện cực Cu là anode.
-
C.
Thế điện cực của điện cực Zn lớn hơn của điện cực Cu là 1,10 V.
-
D.
Tổng thế điện cực của hai điện cực là 1,10 V
Sức điện động chuẩn của các pin điện hóa: Zn – Cu là 1,1V; Cu – Ag là 0,46V. Biết thế điện cực chuẩn EoAg+/Ag= +0,8V. Thế điện cực chuẩn EoZn2+/Zn và EoCu2+/Cu có giá trị lần lượt là
-
A.
– 0,76V và + 0,34V.
-
B.
– 1,46V và – 0,34V.
-
C.
+ 1,56V và + 0,64V.
-
D.
– 1,56V và + 0,64V.
Thực hiện thí nghiệm sau (ở điều kiện thường)
- Rót dung dịch H2SO4 loãng và nước cất lần lượt vào hai cốc thủy tinh đánh số (1) và (2).
- Nhúng thanh đồng và thanh sắt vào mỗi cốc (chú ý không để thanh Cu và Fe chạm nhau)
- Dùng dây dẫn điện nối thanh sắt và thanh đồng ở mỗi cốc với đèn led.
a) Khi chưa nối dây dẫn, các thanh kim loại ở hai cốc không bị ăn mòn.
b) Khi nối dây dẫn, đèn led ở cốc (1) sáng, ở cốc (2) không sáng.
c) Khi nối dẫy dẫn, thanh Cu ở cốc (1) đóng vai trò anode và bị ăn mòn.
d) Khi nối dây dẫn, thanh Fe ở cốc (2) đóng vai trò anode và bị ăn mòn.
a) Lượng Al thu được trong một năm (365 ngày) cho 300 bể điện phân khoảng 293 nghìn tấn
b) Cryolite ngoài tạo hỗn hợp Na3AlF6-Al2O3 có nhiệt độ nóng chảy thấp hơn nhiều so với Al2O3 giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí.
c) Năng lượng điện tiêu thụ để sản xuất được 1 kg Al khoảng 15 kWh (làm tròn đến số nguyên gần nhất).
d) Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn Al2O3, 50 kg cryolite, 400 kg than cốc. Lượng Al2O3 tiêu thụ thực tế cao hơn so với lý thuyết do tạp chất trong Al2O3 và thất thoát trong quá trình vận chuyển và xử lý.
Nhiễm độc chì luôn luôn đáng lo ngại. Trong cơ thể con người, mức độ độc hại của chì có thể được giảm bớt bằng cách sử dụng phối tử EDTA4- để tạo phức [Pb(EDTA)]2- rất bền (hằng số bền β(Pb) = 1018,0) và được thận bài tiết. Phối tử EDTA4- được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2- tương đối kém bền (hằng số bền β(Ca) = 1010,7), sự trao đổi calcium với chì chủ yếu diễn ra trong mạch máu. Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.
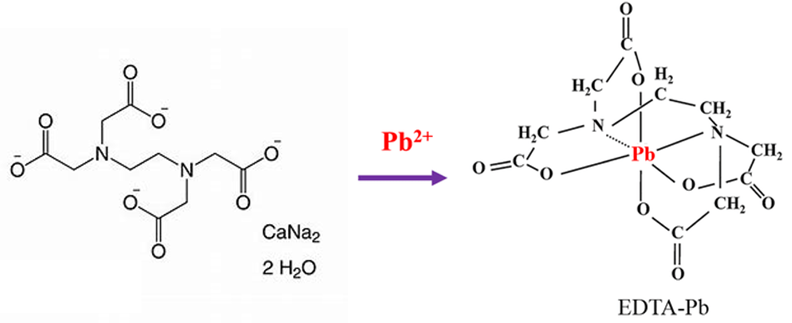
a) Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b) [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c) Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d) Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
Theo Tiêu chuẩn Việt Nam TCVN 7624: 2007, khi chế tạo gương, chiều dày lớp bạc phủ trên bề mặt tấm kính (quy ra tổng lượng bạc trên một đơn vị m kính) phải đạt tối thiểu 0,7g/m2. Một công ty cần sản xuất 20 000 m2 gương có độ dày lớp bạc phủ ở mức 0,75g/m2. Để tạo ra bạc, người ta tiến hành theo sơ đồ phản ứng như sau:
![]()
Biết hiệu suất cả quá trình là 80%.
a) Trong dung dịch A gồm có hai monosaccharide.
b) Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c) Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d) Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
Trong công nghiệp, kim loại sắt (Iron, Fe) được sản xuất bằng phương pháp nhiệt luyện quặng hemantite. Với hiệu suất chuyển hóa từ Fe2O3 thành Fe là 80%. Để sản xuất được 5,6 tấn Fe cần dùng bao nhiêu tấn nguyên liệu quặng hematite biết quặng có chưa 60% Fe2O3. (Làm tròn đến hàng phần mười)
Đáp án:
Có bao nhiêu đồng phân cấu tạo ester có cùng công thức phân tử C4H8O2?
Đáp án:
Quá trình quang hợp tạo ra lương thực, cân bằng lượng khí CO2 và O2 trong khí quyển. Giả thuyết quá trình quang hợp tạo ra tinh bột trong hạt gạo xảy ra theo hai giai đoạn sau với hiệu suất cả quá trình đạt 100%:
6CO2 + 6H2O → C6H12O6 + 6O2
nC6H12O6 → (C6H10O5)n + n H2O
Trên một thửa ruộng có diện tích 720 m2, mỗi vụ tạo ra 324 kg gạo (chứa 80% tinh bột), đồng thời đã hấp thụ V m3 khí CO2 (250C, 1 bar) để tạo ra lượng tinh bột trên. Giá trị của V là bao nhiêu? (Làm tròn kết quả đến phần nguyên).
Đáp án:
Ở một pH xác định, amino acid tồn tại dưới dạng ion lưỡng cực, khi đó nếu được đặt
trong một điện trường, amino acid không di chuyển về một điện cực nào. pH đó được gọi
điểm đẳng điện (the isoelectric point) và kí hiệu pHI. Đối với các amino acid có số nhóm
amino bằng số nhóm carboxyl, điểm đẳng điện được tính theo công thức:
\(p{H_1} = \frac{{p{K_{a1}} + p{K_{a2}}}}{2}\)
Trong đó, pKa1 và pKa2 lần lượt là hằng số phân li của nhóm -COOH và nhóm -N+H3.
Tính pHI của methionine biết pKa1 và pKa2 của nó lần lượt là 2,2 và 9,1. Làm tròn kết quả đến
chữ số hàng phần trăm.
Đáp án:
Trong các polymer sau: (1) poly(methyl methacrylate), (2) polystyrene, (3) nylon-7, poly(ethylene terephtalate) (4), (5) nylon-6,6, (6) poly(vinyl acetate).
Liệt kê các polymer là sản phẩm của phản ứng trùng ngưng theo số thứ tự tăng dần?
Đáp án:
Chỉ số ester hóa là số mg KOH dùng để xà phòng hóa hết lượng triglycerid có trong 1
gam mẫu chất béo. Một loại chất béo có chứa 65% triolein và 23% triliolein. Chỉ số ester hóa
của loại chất béo này có giá trị là bao nhiêu? (làm tròn tới chữ số hàng đơn vị)
Đáp án:
Lời giải và đáp án
Khi thay thế nhóm …(1) ở nhóm …(2) của carboxylic acid bằng nhóm …(3)… thì thu được ester. Nội dung phù hợp trong các ô trống (1), (2), (3) lần lượt là
-
A.
– COO - ; - OH; OR
-
B.
– OH; -COO-; OR
-
C.
– OR; - COOH; - OH
-
D.
– OH; - COOH; - OR
Đáp án : D
Dựa vào khái niệm của ester.
Khi thay thế nhóm – OH ở nhóm – COOH của carboxylic acid bằng nhóm – OR thì thu được ester.
Đáp án D
Thạch cao nung được dùng để đúc tương, bó bột khi hãy xương. Công thức hóa học của thạch cao nung là
-
A.
CaSO4
-
B.
CaSO4.2 H2O
-
C.
CaSO4.0,5H2O
-
D.
Ca3(PO4)2
Đáp án : C
Dựa vào một số hợp chất nhóm IIA thông dụng
Thạch cao nung có công thức hóa học là CaSO4.0,5H2O
Đáp án C
Tơ nào sau đây thuộc loại tơ bán tổng hợp?
-
A.
Tơ nitron
-
B.
Tơ nylon – 6,6
-
C.
Tơ tằm
-
D.
Tơ cellulose acetate
Đáp án : D
Dựa vào phân loại các loại tơ.
Tơ cellulose acetate thuộc loại tơ bán tổng hợp.
Đáp án D
Phức chất [Cu(H2O)6]2+ có dạng hình học là
-
A.
bát diện
-
B.
đường thẳng
-
C.
Tứ diện
-
D.
lục giác
Đáp án : A
Dựa vào một số hình dạng của phức chất.
Phức chất [Cu(H2O)6]2+ có hình bát diện.
Đáp án A
Kim loại nào sau đây có thể điều chế bằng phương pháp thủy luyện?
-
A.
Na
-
B.
K
-
C.
Ag
-
D.
Mg
Đáp án : C
Phương pháp thủy luyện dùng để điều chế các kim loại trung bình yếu.
Ag là kim loại yếu nên được điều chế bằng phương pháp thủy luyện.
Đáp án C
Nước chứa nhiều các ion nào sau đây có tính cứng toàn phần?
-
A.
Mg2+, Ca2+, HCO3- , SO42-.
-
B.
Na+, K+, SO42-, Cl-.
-
C.
Mg2+, Ca2+, HCO3-.
-
D.
Mg2+, Ca2+, SO42-, Cl-.
Đáp án : A
Nước cứng toàn phần chứa ion: Mg2+, Ca2+, SO42-, Cl-, HCO3-
Dung dịch chứa các ion Mg2+, Ca2+, HCO3- , SO42- là nước cứng toàn phần.
Đáp án A
Có các thí nghiệm sau:
(a) Nhúng thanh sắt (iron) vào dung dịch H2SO4 loãng, nguội.
(b) Sục khí SO2 vào nước bromine.
(c) Cho dung dịch BaCl2 tác dụng với dung dịch H2SO4 loãng.
(d) Nhúng lá nhôm (aluminium) vào dung dịch H2SO4 đặc, nguội.
Số thí nghiệm xảy ra phản ứng hoá học là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Đáp án : C
Dựa vào tính chất hóa học của kim loại.
(a) có phản ứng: Fe + H2SO4 → FeSO4 + H2
(b) có xảy ra phản ứng: SO2 + Br2 + 2H2O → 2HBr + H2SO4
(c) có xảy ra phản ứng: BaCl2 + H2SO4 → BaSO4 + 2HCl
(d) không xảy ra phản ứng
Đáp án C
Kim loại nào sau đây có tính khử mạnh nhất?
-
A.
K
-
B.
Mg
-
C.
Fe
-
D.
Na
Đáp án : A
Dựa vào ý nghĩa thế điện cực chuẩn của kim loại.
K là kim loại có tính khử mạnh nhất.
Đáp án A
Ethanol là một chất lỏng, có nhiệt độ sôi là 78,3oC và tan nhiều trong nước. Phương pháp tách riêng được ethanol từ hỗn hợp ethanol và nước là
-
A.
lọc.
-
B.
chiết.
-
C.
cô cạn.
-
D.
chưng cất.
Đáp án : D
Dựa vào các phương pháp tách chất.
Vì nhiệt độ sôi của ethanol và nước khác nhau nên có thể dùng phương pháp chưng cất để tách ethanol ra khỏi nước
Đáp án D
Thủy phân C4H8O2 trong dung dịch NaOH thu được sodium acetate và alcohol X. Công thức X là
-
A.
CH3OH
-
B.
C2H5OH
-
C.
C3H7OH
-
D.
H2O
Đáp án : B
Dựa vào tính chất hóa học của ester.
Vì thủy phân C4H8O2 thu được CH3COONa nên alcohol X là C2H5OH.
Đáp án B
Dung dịch nào sau đây không làm quỳ tím hóa xanh?
-
A.
Phenylamine.
-
B.
Dimethylamine.
-
C.
Ethylamine.
-
D.
Methylamine.
Đáp án : A
Dựa vào tính chất hóa học của amine.
Phenylamine là amine có tính base rất yếu nên không làm quỳ tím hóa xanh.
Đáp án A
Maltose có nhiều trong đường mạch nha. Công thức phân tử của maltose là
-
A.
C6H12O6
-
B.
C12(H2O)11
-
C.
(C6H10O5)n
-
D.
C6(H2O)n
Đáp án : B
Dựa vào cấu tạo của maltose.
Maltose có công thức phân tử C12H22O11.
Đáp án B
Khi nấu món canh làm từ thịt cua, tôm, tép có nhiều mảng thịt đóng rắn lại. Hiện tượng trên gây ra bởi tính chất nào sau đây?
-
A.
Sự đông tụ protein bởi sự thay đổi pH.
-
B.
Sự đông tụ protein bởi nhiệt độ.
-
C.
Kết tủa carbonate của các chất khoáng có trong vỏ.
-
D.
Sự thuỷ phân protein bởi nhiệt độ.
Đáp án : B
Dựa vào tính chất hóa học của protein.
Thịt cua, tôm, tép chứa nhiều protein. Khi nấu lên có hiện tượng đóng rắn lại là do protein bị đông tụ bởi nhiệt độ.
Đáp án B
Tên thông thường của acid CH3COOH là
-
A.
methanol
-
B.
acetic acid
-
C.
propanoic acid
-
D.
formic acid
Đáp án : B
Dựa vào tên gọi của carboxylic acid.
CH3COOH: acetic acid.
Đáp án B
Chất nào sau đây thuộc loại α – amino acid?
-
A.
CH2(NH2)COOH
-
B.
CH3NH2
-
C.
CH3COOH
-
D.
H2N – CH2 – CH2 – COOH
Đáp án : A
α – amino acid là các amino acid có nhóm – NH2 và – COOH cùng liên kết với nguyên tử carbon ở vị trí α.
CH2(NH2)COOH thuộc loại α – amino acid
Đáp án A
Insulin là hormon có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide X mạch hở. Khi thủy phân không hoàn toàn X, thu được hỗn hợp có chứa các peptide: Glu- Gln-Cys, Gly-Ile-Val, Gln-Cys-Cys, Val-Glu-Gln. Nếu đánh số thứ tự amino acid đầu N là số 1 thì amino acid ở vị trí số 4 trong X là
-
A.
Gln.
-
B.
Val.
-
C.
Glu.
-
D.
Cys.
Đáp án : C
Xác định được cấu tạo của X.
Khi thủy phân X thu được các peptide:
(1) Glu – Gln – Cys
(2) Gly – Ile – Val
(3) Gln – Cys – Cys
(4) Val – Glu – Gln
Ghép (1) và (3) ta được: Glu – Gln – Cys – Cys
Glép (2) và (2) ta được: Gly – Ile – Val – Glu – Gln
Vậy công thứ của X là: Gly – Ile – Val – Glu – Gln – Cys – Cys
Vậy amino acid ở vị trí số 4 là Glu.
Đáp án C
-
A.
Điện cực Zn là anode, điện cực Cu là cathode.
-
B.
Điện cực Zn là cathode, điện cực Cu là anode.
-
C.
Thế điện cực của điện cực Zn lớn hơn của điện cực Cu là 1,10 V.
-
D.
Tổng thế điện cực của hai điện cực là 1,10 V
Đáp án : A
Dựa vào nguyên tắc xảy ra ở pin điện.
A đúng, vì điện cực Zn tạo ra dòng electron nên là cực anode, điện cực Cu nhận electron nên là cathode.
Đáp án A
Sức điện động chuẩn của các pin điện hóa: Zn – Cu là 1,1V; Cu – Ag là 0,46V. Biết thế điện cực chuẩn EoAg+/Ag= +0,8V. Thế điện cực chuẩn EoZn2+/Zn và EoCu2+/Cu có giá trị lần lượt là
-
A.
– 0,76V và + 0,34V.
-
B.
– 1,46V và – 0,34V.
-
C.
+ 1,56V và + 0,64V.
-
D.
– 1,56V và + 0,64V.
Đáp án : A
Dựa vào công thức tính sức điện động của pin.
\(E_{pin(Cu - Ag)}^o = E_{A{g^ + }/Ag}^o - E_{C{u^{2 + }}/Cu}^o \to E_{C{u^{2 + }}/Cu}^o = 0,8 - 0,46 = 0,34V\)
\[E_{pin(Zn/Cu)}^o = E_{C{u^{2 + }}/Cu}^o - E_{Z{n^{2 + }}/Zn}^o \to E_{Z{n^{2 + }}/Zn}^o = 0,34 - 1,1 = - 0,76V\]
Đáp án A
Thực hiện thí nghiệm sau (ở điều kiện thường)
- Rót dung dịch H2SO4 loãng và nước cất lần lượt vào hai cốc thủy tinh đánh số (1) và (2).
- Nhúng thanh đồng và thanh sắt vào mỗi cốc (chú ý không để thanh Cu và Fe chạm nhau)
- Dùng dây dẫn điện nối thanh sắt và thanh đồng ở mỗi cốc với đèn led.
a) Khi chưa nối dây dẫn, các thanh kim loại ở hai cốc không bị ăn mòn.
b) Khi nối dây dẫn, đèn led ở cốc (1) sáng, ở cốc (2) không sáng.
c) Khi nối dẫy dẫn, thanh Cu ở cốc (1) đóng vai trò anode và bị ăn mòn.
d) Khi nối dây dẫn, thanh Fe ở cốc (2) đóng vai trò anode và bị ăn mòn.
a) Khi chưa nối dây dẫn, các thanh kim loại ở hai cốc không bị ăn mòn.
b) Khi nối dây dẫn, đèn led ở cốc (1) sáng, ở cốc (2) không sáng.
c) Khi nối dẫy dẫn, thanh Cu ở cốc (1) đóng vai trò anode và bị ăn mòn.
d) Khi nối dây dẫn, thanh Fe ở cốc (2) đóng vai trò anode và bị ăn mòn.
Dựa vào sự ăn mòn kim loại.
a) sai, ở cốc (2) xảy ra ăn mòn hóa học vì Fe phản ứng với H2SO4 loãng.
b) đúng
c) sai, thanh Cu ở cốc (1) đóng vai trò là cathode.
d) đúng
a) Lượng Al thu được trong một năm (365 ngày) cho 300 bể điện phân khoảng 293 nghìn tấn
b) Cryolite ngoài tạo hỗn hợp Na3AlF6-Al2O3 có nhiệt độ nóng chảy thấp hơn nhiều so với Al2O3 giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí.
c) Năng lượng điện tiêu thụ để sản xuất được 1 kg Al khoảng 15 kWh (làm tròn đến số nguyên gần nhất).
d) Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn Al2O3, 50 kg cryolite, 400 kg than cốc. Lượng Al2O3 tiêu thụ thực tế cao hơn so với lý thuyết do tạp chất trong Al2O3 và thất thoát trong quá trình vận chuyển và xử lý.
a) Lượng Al thu được trong một năm (365 ngày) cho 300 bể điện phân khoảng 293 nghìn tấn
b) Cryolite ngoài tạo hỗn hợp Na3AlF6-Al2O3 có nhiệt độ nóng chảy thấp hơn nhiều so với Al2O3 giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí.
c) Năng lượng điện tiêu thụ để sản xuất được 1 kg Al khoảng 15 kWh (làm tròn đến số nguyên gần nhất).
d) Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn Al2O3, 50 kg cryolite, 400 kg than cốc. Lượng Al2O3 tiêu thụ thực tế cao hơn so với lý thuyết do tạp chất trong Al2O3 và thất thoát trong quá trình vận chuyển và xử lý.
Nhiễm độc chì luôn luôn đáng lo ngại. Trong cơ thể con người, mức độ độc hại của chì có thể được giảm bớt bằng cách sử dụng phối tử EDTA4- để tạo phức [Pb(EDTA)]2- rất bền (hằng số bền β(Pb) = 1018,0) và được thận bài tiết. Phối tử EDTA4- được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2- tương đối kém bền (hằng số bền β(Ca) = 1010,7), sự trao đổi calcium với chì chủ yếu diễn ra trong mạch máu. Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.

a) Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b) [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c) Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d) Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
a) Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b) [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c) Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d) Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
a) đúng
Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.
Số mol chì = \(\frac{{0,828 \times {{10}^{ - 6}}}}{{207}}:{10^{ - 6}}\) = 4 ´ 10-3 (mmol)
Thể tích máu 1 mL = 10-3 L
Vậy nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b) sai qua 6 nhóm chức
c) đúng Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- do có hằng số bền cao hơn. Phản ứng ưu tiên xảy ra phản ứng thế Ca2+ trong phức [Ca(EDTA)]2- kém bền bằng Pb2+ tạo [Pb(EDTA)]2- bền hơn.
d) sai vì phức [Pb(EDTA)]2- có thể được thận bài tiết nên phải tan trong nước.
Theo Tiêu chuẩn Việt Nam TCVN 7624: 2007, khi chế tạo gương, chiều dày lớp bạc phủ trên bề mặt tấm kính (quy ra tổng lượng bạc trên một đơn vị m kính) phải đạt tối thiểu 0,7g/m2. Một công ty cần sản xuất 20 000 m2 gương có độ dày lớp bạc phủ ở mức 0,75g/m2. Để tạo ra bạc, người ta tiến hành theo sơ đồ phản ứng như sau:
![]()
Biết hiệu suất cả quá trình là 80%.
a) Trong dung dịch A gồm có hai monosaccharide.
b) Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c) Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d) Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
a) Trong dung dịch A gồm có hai monosaccharide.
b) Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c) Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d) Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
a) đúng A gồm glucose và fructose
b) sai không thể thay được xúc tác acid bằng base.
c) đúng. mAg = 0,75. 20 000 = 15000 gam = 15 kg
d) đúng. msaccharose =\(\frac{{15.342}}{{432}}:80\% = 14,84kg\)
Trong công nghiệp, kim loại sắt (Iron, Fe) được sản xuất bằng phương pháp nhiệt luyện quặng hemantite. Với hiệu suất chuyển hóa từ Fe2O3 thành Fe là 80%. Để sản xuất được 5,6 tấn Fe cần dùng bao nhiêu tấn nguyên liệu quặng hematite biết quặng có chưa 60% Fe2O3. (Làm tròn đến hàng phần mười)
Đáp án:
Đáp án:
Fe2O3 (s) + 3CO (g) → 2Fe (l) + 3CO2 (g)
nFe = 5600000 : 56 = 100000 mol → nFe2O3 = 50000 mol → nFe2O3 tt = 62500 mol
mquặng = (62500. 160):60% = 16666666,67g = 16,7 tấn
Có bao nhiêu đồng phân cấu tạo ester có cùng công thức phân tử C4H8O2?
Đáp án:
Đáp án:
Dựa vào cách vẽ đồng phân của ester.
HCOOCH2CH2CH3 (1)
HCOOCH(CH3)2 (2)
CH3COOC2H5
C2H5COOCH3
Đáp án 4
Quá trình quang hợp tạo ra lương thực, cân bằng lượng khí CO2 và O2 trong khí quyển. Giả thuyết quá trình quang hợp tạo ra tinh bột trong hạt gạo xảy ra theo hai giai đoạn sau với hiệu suất cả quá trình đạt 100%:
6CO2 + 6H2O → C6H12O6 + 6O2
nC6H12O6 → (C6H10O5)n + n H2O
Trên một thửa ruộng có diện tích 720 m2, mỗi vụ tạo ra 324 kg gạo (chứa 80% tinh bột), đồng thời đã hấp thụ V m3 khí CO2 (250C, 1 bar) để tạo ra lượng tinh bột trên. Giá trị của V là bao nhiêu? (Làm tròn kết quả đến phần nguyên).
Đáp án:
Đáp án:
Dựa vào tính chất của tinh bột.
Số mol tinh bột = số mol gốc glucose =\(\frac{{324000.0,8}}{{162}} = 1600mol\)
Số mol CO2= 1600.6 = 8640 (mol) → V=24,79.9600 = 237984 (lít) = 238 m3
Ở một pH xác định, amino acid tồn tại dưới dạng ion lưỡng cực, khi đó nếu được đặt
trong một điện trường, amino acid không di chuyển về một điện cực nào. pH đó được gọi
điểm đẳng điện (the isoelectric point) và kí hiệu pHI. Đối với các amino acid có số nhóm
amino bằng số nhóm carboxyl, điểm đẳng điện được tính theo công thức:
\(p{H_1} = \frac{{p{K_{a1}} + p{K_{a2}}}}{2}\)
Trong đó, pKa1 và pKa2 lần lượt là hằng số phân li của nhóm -COOH và nhóm -N+H3.
Tính pHI của methionine biết pKa1 và pKa2 của nó lần lượt là 2,2 và 9,1. Làm tròn kết quả đến
chữ số hàng phần trăm.
Đáp án:
Đáp án:
Dựa vào công thức điểm đẳng điện đề bài cung cấp.
\(p{H_1} = \frac{{p{K_{a1}} + p{K_{a2}}}}{2} = \frac{{2,2 + 9,1}}{2} = 5,65\)
Trong các polymer sau: (1) poly(methyl methacrylate), (2) polystyrene, (3) nylon-7, poly(ethylene terephtalate) (4), (5) nylon-6,6, (6) poly(vinyl acetate).
Liệt kê các polymer là sản phẩm của phản ứng trùng ngưng theo số thứ tự tăng dần?
Đáp án:
Đáp án:
Dựa vào phương pháp tổng hợp polymer.
(3) nylon-7, poly(ethylene terephtalate) (4), (5) nylon-6,6 được điều chế bằng phương pháp trùng ngưng.
Chỉ số ester hóa là số mg KOH dùng để xà phòng hóa hết lượng triglycerid có trong 1
gam mẫu chất béo. Một loại chất béo có chứa 65% triolein và 23% triliolein. Chỉ số ester hóa
của loại chất béo này có giá trị là bao nhiêu? (làm tròn tới chữ số hàng đơn vị)
Đáp án:
Đáp án:
Dựa vào tính chất hóa học của ester.
Trong 1 gam chất béo có 0,65g triolein (C17H33COO)3C3H5 và 0,23g triliolein (C17H31COO)3C3H5.
n triolein = 0,65 : 884 = \(\frac{1}{{1360}}mol \to {n_{K{\rm{O}}H}} = \frac{1}{{1360}}.3\)
n triliolein = 0,23 : 878 = \(\frac{{23}}{{87800}}mol \to {n_{K{\rm{O}}H}} = \frac{{23}}{{87800}}.3mol\)
m KOH cần dùng = \(\left( {\frac{3}{{1360}} + \frac{{69}}{{87800}}} \right){.56.10^3} = 168mg\)
Hợp chất nào sau đây là ester ?
Trong ăn mòn hóa học, phản ứng hóa học xảy ra là loại phản ứng nào sau đây?
Kim loại cứng nhất, thường được pha vào thép để tăng độ cứng và khả năng chống gỉ cho thép là
Phần I. Trắc nghiệm nhiều đáp án lựa chọn
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Be (Z = 4) là
Quá trình tạo thành ion Ca2+ nào sau đây là đúng?
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
Phức chất đơn giản thường có một
Cho phản ứng oxi hóa – khử:
Các bài khác cùng chuyên mục









Danh sách bình luận