Đề thi thử THPT môn Hóa lần 1 năm 2025 Sở GD Nghệ An
Để chuyển hóa dầu mỡ động thực vật thành xà phòng người ta thực hiện quá trình
Đề bài
Để chuyển hóa dầu mỡ động thực vật thành xà phòng người ta thực hiện quá trình
-
A.
xà phòng hóa dầu mỡ động thực vật.
-
B.
làm lạnh dầu mỡ động thực vật.
-
C.
oxi hóa dầu mỡ động thực vật ở nhiệt độ cao.
-
D.
hydrogen hóa dầu mỡ.
Ethylacetate là ester có mùi thơm đặc trưng, được sử dụng làm dung môi cho nước hoa, sơn móng tay... Công thức cấu tạo thu gọn của ester này là
-
A.
C3H7COOC2H5.
-
B.
C2H5COOC2H5.
-
C.
CH3COOC2H5.
-
D.
CH3COOCH3.
Glucose là chất rắn có vị ngọt, dễ tan trong nước. Saccharose có công thức phân tử là
-
A.
C3H6O3.
-
B.
C12H22O11.
-
C.
(C6H10O5)n.
-
D.
C6H12O6.
Trong sản xuất hợp kim, thêm manganese vào thép để tăng cường tính chất nào sau đây?
-
A.
Tính cứng.
-
B.
Tính dẫn điện.
-
C.
Tính chất từ.
-
D.
Tính dẫn nhiệt.
Quá trình điện phân dung dịch KCl bão hòa với điện cực trơ (graphite) thu được khí nào sau đây ở anode?
-
A.
O2.
-
B.
Cl2.
-
C.
HCl.
-
D.
H2.
Tên bán hệ thống của amino acid H2N-CH2-COOH là
-
A.
2-aminoethanoic acid.
-
B.
aminoacetic acid.
-
C.
glycine.
-
D.
aminoethanoic acid.
Phức chất cis-dichloro(ethylendiamine)platinium(II) có công thức cấu tạo sau:
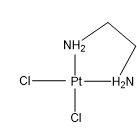
Số lượng phối tử có trong phức chất trên là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Arachidonic acid (AA hay ARA) được ứng dụng rộng rãi, đặc biệt là trong ngành sản xuất mỹ phẩm và chăm sóc sắc đẹp. Công thức của AA như sau:
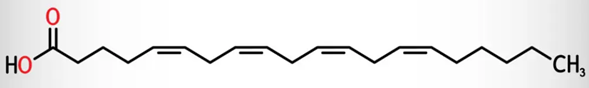
Cho các nhận định sau:
(a) Arachidonic acid có công thức phân tử là C20H32O2.
(b) Arachidonic acid thuộc nhóm acid béo omega-6.
(c) Arachidonic acid là một chất béo lỏng.
(d) Một phân tử Arachidonic acid tác dụng tối đa với năm phân tử hydrogen ở điều kiện thích hợpHH.
Các nhận định đúng là
-
A.
(b), (c), (d).
-
B.
(a), (b).
-
C.
(a), (b), (c).
-
D.
(a), (b), (d).
Nước cứng gây nhiều trở ngại cho đời sống thường ngày. Các nguồn nước ngầm hoặc nước ở các ao hồ, sông suối thường có độ cứng cao bởi quá trình hòa tan các ion Ca2+, Mg2+ có trong thành phần của lớp trầm tích đá vôi. Cho các phát biểu sau:
(a) Có thể dùng Na3PO4 để làm mềm nước có tính cứng vĩnh cửu.
(b) Nấu ăn bằng nước cứng làm thực phẩm lâu chín, giảm mùi vị.
(c) Nước tự nhiên có chứa ion Ca2+, Mg2+, Cl-, SO42- gọi là nước có tính cứng tạm thời.
(d) Nước không chứa hoặc chứa ít các ion Ca2+ và Mg2+ được gọi là nước mềm.
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
4
-
D.
3
Kim loại nhóm IA đều là kim loại nhẹ, có khối lượng riêng nhỏ là do
-
A.
có bán kính nguyên tử lớn và cấu trúc mạng tinh thể kém đặc khít.
-
B.
có độ âm điện lớn và thế điện cực chuẩn nhỏ.
-
C.
có bán kính nguyên tử nhỏ và cấu trúc mạng tinh thể đặc khít.
-
D.
có độ âm điện nhỏ và thế điện cực chuẩn nhỏ.
Dãy nào sau đây sắp xếp các kim loại Li, Na, K theo mức độ phản ứng với oxygen giảm dần?
-
A.
Li, Na, K.
-
B.
Na, K, Li.
-
C.
K, Na, Li.
-
D.
K, Li, Na.
Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trong đời sống. Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
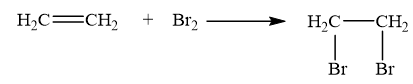
Cơ chế của phản ứng trên xảy ra qua 2 giai đoạn như sau:
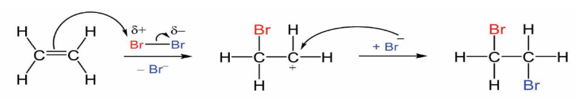
Nhận định nào sau đây không đúng?
-
A.
Hiện tượng của phản ứng là dung dịch bromine bị nhạt màu dần.
-
B.
Giai đoạn 2, có sự hình thành liên kết π.
-
C.
Giai đoạn 1, có sự phá vỡ liên kết π trong liên kết đôi C=C.
-
D.
Phản ứng trên thuộc loại phản ứng cộng.
Zinc blende (chứa ZnS) là loại quặng chứa kẽm trong tự nhiên. Trong công nghiệp, để tách kim loại Zn từ quặng zinc blende tiến hành theo sơ đồ sau:
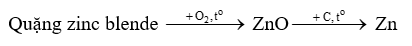
Phương pháp điều chế kim loại nào đã được sử dụng trong quá trình sản xuất Zn theo sơ đồ trên?
-
A.
Điện phân nóng chảy.
-
B.
Nhiệt luyện.
-
C.
Thuỷ luyện.
-
D.
Điện phân dung dịch.
Cho 1 số hiện tượng sau:
(a) Sáp nến chảy ra bị đông lại khi nguội.
(b) Sữa bị chua và vón cục khi để hở lâu trong không khí.
(c) Mật ong để lâu ngày thấy có hiện tượng kết tinh.
(d) Đậu phụ được làm từ sữa đậu nành.
Số hiện tượng không có sự đông tụ protein là
-
A.
4
-
B.
2
-
C.
3
-
D.
1
Trong quá trình hoạt động của pin Zn – Cu, quá trình xảy ra ở anode là
-
A.
Cu → Cu2+ + 2e.
-
B.
Cu2+ + 2e → Cu.
-
C.
Zn → Zn2+ + 2e.
-
D.
Zn2+ + 2e → Zn.
Trong công nghiệp, nguyên liệu thường dùng để sản xuất vôi sống, xi măng, vật liệu xây dựng là đá vôi. Thành phần chính của đá vôi là
-
A.
CaCO3.
-
B.
Ca3(PO4)2.
-
C.
CaSO4.
-
D.
Ca(H2PO4)2.
“... là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định”. Nội dung phù hợp trong dấu … là
-
A.
Kết tinh.
-
B.
Sắc ký.
-
C.
Chiết.
-
D.
Chưng cất.
Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:

Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 2 và số 4 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
-
A.
CH2=CH–Cl.
-
B.
CH2=CH–C6H5.
-
C.
CH2=CH–CH3.
-
D.
CH2=CH2.
a) Từ kết quả thí nghiệm, kết luận giả thuyết của nhóm học sinh trên là đúng.
b) Trong mẫu trắng đã có sẵn một lượng lactic acid đáng kể.
c) Nhiệt độ tối ưu cho quá trình lên men tạo acid lactic là 37°C.
d) Trong thí nghiệm trên, lượng acid lactic được tạo thành nhiều nhất trong một mẫu (200 mL) là 3,78 gam.
Lysine và cadaverine là hai hợp chất liên quan đến quá trình phân hủy protein. Lysine là một amino acid thiết yếu, còn cadaverine được hình thành từ sự khử carboxyl của Lysine dưới tác động của enzyme trong môi trường. Về cấu tạo, từ phân tử lysine, thay thế nhóm chức carboxyl bằng một nguyên tử hydrogen thì thu được phân tử cadaverine.
a) Công thức phân tử của cadaverine là C₅H₁₄N₂.
b) Lysine và cadaverine đều có hai nhóm amine trong phân tử.
c) Lysine thuộc loại α-amino acid, còn cadaverine không phải amino acid
d) Ở pH = 7, cả hai chất đều có thể tồn tại ở dạng ion lưỡng cực.
Một học sinh tiến hành thí nghiệm nghiên cứu sự tạo thành phức chất, phản ứng của phức chất iron(III), ghi lại hiện tượng quan sát được và đưa ra những nhận định như sau:
- Bước 1: Hòa tan iron(III) sulfate vào ống nghiệm chứa nước thu được dung dịch màu vàng nâu. Sau một thời gian, thấy có kết tủa màu nâu đỏ trong ống nghiệm.
- Bước 2: Lọc bỏ kết tủa, thêm KSCN (potassium thiocyanate) vào nước lọc thấy dung dịch chuyển sang màu đỏ máu của các phức chất bát diện chứa từ 1 đến 6 phối tử SCN-.
- Bước 3: Thêm tiếp dung dịch KF dư vào ống nghiệm thấy dung dịch nhạt màu dần và mất màu do tạo phức chất [FeF3]3-.
a) Các phức chất được tạo thành ở Bước 2 đều là phức chất trung tính, không mang điện tích.
b) Ở bước 1 đã xảy ra quá trình hình thành và thủy phân phức chất aqua của ion Fe³⁺.
c) Trong thí nghiệm trên, khi tạo phức với ion Fe³⁺, phối tử là anion tạo luôn ra phức chất có màu đậm hơn phối tử là phân tử trung hòa.
d) Ở Bước 2, xảy ra phản ứng thay thế phối tử H2O bằng phối tử SCN-.
Một nhóm học sinh nghiên cứu sự ăn mòn kim loại của một sợi kẽm với giả thuyết: “trong cùng điều kiện, tốc độ ăn mòn điện hóa nhanh hơn tốc độ ăn mòn hóa học”. Để kiểm tra giả thuyết của mình, nhóm học sinh trên đã chuẩn bị 2 sợi kẽm đã làm sạch bề mặt, có kích thước, khối lượng như nhau và tiến hành các thí nghiệm như sau:
- Thí nghiệm 1: Nhúng một sợi kẽm vào dung dịch H2SO4 0,5M (hình 1).
- Thí nghiệm 2: Nhúng sợi kẽm còn lại vào dung dịch H2SO4 0,5M cùng với một sợi đồng và nối chúng lại qua vôn kế (hình 2).
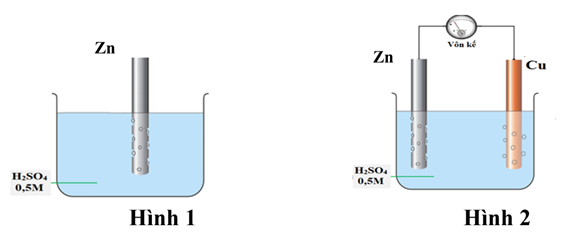
a) Nhóm học sinh trên quan sát thấy bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 1 nhanh hơn bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là sai.
b) Nếu thế điện cực chuẩn \({{\rm{E}}_{Z{n^{2 + }}/Zn}} = - 0,763{\rm{ V}}\), \({\rm{E}}_{2{H^{\rm{ + }}}{\rm{/}}{{\rm{H}}_2}}^0 = 0{\rm{ V}}\), \({\rm{E}}_{{\rm{C}}{{\rm{u}}^{2 + }}{\rm{/Cu}}}^0 = 0,340{\rm{ V}}\)thì vôn kế luôn chỉ giá trị cố định là 1,10 V.
c) Ở thí nghiệm 2, quan sát thấy có bọt khí thoát ra trên bề mặt sợi đồng, chứng tỏ sợi đồng bị ăn mòn điện hóa học.
d) Sau 3 phút, nhóm học sinh lấy 2 sợi kẽm ra cân lại, thấy khối lượng sợi kẽm ở thí nghiệm 1 lớn hơn khối lượng sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là đúng.
DEP (diethyl phthalatate) được dùng làm thuốc điều trị bệnh ghẻ và giảm triệu chứng sưng tấy ở vùng da bị côn trùng cắn. Có thể điều chế DEP từ o-xylene qua 2 giai đoạn được mô tả như sau:
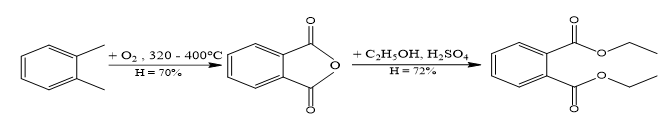
Một loại thuốc DEP thành phẩm trên thị trường (loại 10 g) có hàm lượng diethyl phthalatate là 96% (về khối lượng). Hãy tính số lọ thuốc loại này sản xuất được từ 12 kg o-xylene? (làm tròn đến hàng đơn vị).
Trong công nghiệp, sản xuất nước Javel xảy ra qua hai giai đoạn chính sau:
- Giai đoạn 1: điện phân dung dịch NaCl bão hòa không có màng ngăn điện cực:
2NaCl(aq) + 2H2O(l) → 2NaOH(aq) + H2(g) + Cl2(g)
- Giai đoạn 2: khí Cl2 phản ứng với dung dịch NaOH tạo ra nước Javel:
Cl2(g) + 2NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l)
Một loại nước Javel (có khối lượng riêng 1,15 g/cm3) được bán trên thị trường với can dung tích 5,0 L có nồng độ NaClO, NaCl và NaOH lần lượt là 10%; 8% và 0,8%. Để sản xuất 500 can nước Javel ở trên cần bao nhiêu kg dung dịch NaCl 18,5% (làm tròn kết đến hàng đơn vị)?
Cho thế điện cực chuẩn của các cặp oxi hoá - khử như bảng sau:
|
Cặp oxi hóa – khử |
Al3+/Al |
Pb2+/Pb |
Sn2+/Sn |
Fe3+/Fe2+ |
Fe2+/Fe |
Hg2+/Hg |
Ag+/Ag |
|
Thế điện cực chuẩn (V) |
–1,676 |
–0,126 |
–0,137 |
0,771 |
–0,440 |
0,853 |
0,799 |
Trong số các kim loại: Al, Pb, Sn, Fe, Hg và Ag, ở điều kiện chuẩn có bao nhiêu kim loại tác dụng được với dung dịch Fe(NO3)3?
Một nhà máy nhiệt điện khí có sản lượng điện 106 kWh/ngày (1 kWh = 3600 kJ) sử dụng khí thiên nhiên hóa lỏng LNG làm nhiên liệu đã giảm được a% khí thải CO2 so với nhà máy nhiệt điện than (sử dụng than đá làm nhiên liệu) có cùng sản lượng điện. Biết rằng:
- Khí thiên nhiên hóa lỏng LNG chứa 95% CH4 và 5% C2H6 về thể tích. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 mol CH4 là 890 kJ; 1 mol C2H6 là 1560 kJ và có 64% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn LNG được chuyển hóa thành điện năng.
- Than đá chứa 78% carbon về khối lượng, còn lại là các tạp chất không chứa carbon. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 tấn than đá là 3.107 kJ và chỉ có 50% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn than đá được chuyển hóa thành điện năng.
Tính giá trị của a (làm tròn đến hàng đơn vị).
Cho các hydrocarbon sau: propane, buta-1,3-diene, ethane, ethene, styrene, propene. Có bao nhiêu chất có thể trùng hợp tạo polymer?
Ở điều kiện thường, hợp chất hữu cơ X tồn tại ở trạng thái lỏng. Khi phân tích thành phần nguyên tố của hợp chất hữu cơ X thu được kết quả %C; %H;, %O (theo khối lượng) lần lượt là 60.00%; 13.33%; 26.67%. Cho các nhận định sau về X:
(1) Công thức phân tử của X là C3H8O.
(2) X tạo được liên kết hydrogen với nước.
(3) Oxi hóa X bằng CuO luôn cho sản phẩm có phản ứng với thuốc thử Tollens.
(4) X là alcohol.
Hãy sắp xếp các nhận định đúng theo thứ tự tăng dần.
Lời giải và đáp án
Để chuyển hóa dầu mỡ động thực vật thành xà phòng người ta thực hiện quá trình
-
A.
xà phòng hóa dầu mỡ động thực vật.
-
B.
làm lạnh dầu mỡ động thực vật.
-
C.
oxi hóa dầu mỡ động thực vật ở nhiệt độ cao.
-
D.
hydrogen hóa dầu mỡ.
Đáp án : A
Dựa vào tính chất hoá học của chất béo.
Để chuyển hoá dầu mỡ động thực vật thành xà phòng người ta thực hiện quá trình xà phòng hoá dầu mỡ động thực vật.
Đáp án A
Ethylacetate là ester có mùi thơm đặc trưng, được sử dụng làm dung môi cho nước hoa, sơn móng tay... Công thức cấu tạo thu gọn của ester này là
-
A.
C3H7COOC2H5.
-
B.
C2H5COOC2H5.
-
C.
CH3COOC2H5.
-
D.
CH3COOCH3.
Đáp án : C
Dựa vào danh pháp của ester.
Ethylacetate có công thức cấu tạo là CH3COOC2H5.
Đáp án C
Glucose là chất rắn có vị ngọt, dễ tan trong nước. Saccharose có công thức phân tử là
-
A.
C3H6O3.
-
B.
C12H22O11.
-
C.
(C6H10O5)n.
-
D.
C6H12O6.
Đáp án : B
Dựa vào công thức phân tử của glucose.
Saccharose có công thức phân tử là: C12H22O11.
Đáp án B
Trong sản xuất hợp kim, thêm manganese vào thép để tăng cường tính chất nào sau đây?
-
A.
Tính cứng.
-
B.
Tính dẫn điện.
-
C.
Tính chất từ.
-
D.
Tính dẫn nhiệt.
Đáp án : A
Dựa vào tính chất của hợp kim.
Khi thêm Mn vào thép để tăng cường tính cứng của hợp kim.
Đáp án A
Quá trình điện phân dung dịch KCl bão hòa với điện cực trơ (graphite) thu được khí nào sau đây ở anode?
-
A.
O2.
-
B.
Cl2.
-
C.
HCl.
-
D.
H2.
Đáp án : B
Dựa vào phương pháp điện phân dung dịch KCl.
Tại anode thu được khí Cl2.
Đáp án B
Tên bán hệ thống của amino acid H2N-CH2-COOH là
-
A.
2-aminoethanoic acid.
-
B.
aminoacetic acid.
-
C.
glycine.
-
D.
aminoethanoic acid.
Đáp án : B
Dựa vào tên gọi của amino acid.
Tên bán hệ thống của amino acid H2N-CH2-COOH là aminoacetic acid.
Đáp án B
Phức chất cis-dichloro(ethylendiamine)platinium(II) có công thức cấu tạo sau:

Số lượng phối tử có trong phức chất trên là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Đáp án : B
Dựa vào cấu tạo của phức chất.
Phức chất cis – dichlori(Ethylendiamine)platinium(II) có 3 phối tử.
Đáp án B
Arachidonic acid (AA hay ARA) được ứng dụng rộng rãi, đặc biệt là trong ngành sản xuất mỹ phẩm và chăm sóc sắc đẹp. Công thức của AA như sau:

Cho các nhận định sau:
(a) Arachidonic acid có công thức phân tử là C20H32O2.
(b) Arachidonic acid thuộc nhóm acid béo omega-6.
(c) Arachidonic acid là một chất béo lỏng.
(d) Một phân tử Arachidonic acid tác dụng tối đa với năm phân tử hydrogen ở điều kiện thích hợpHH.
Các nhận định đúng là
-
A.
(b), (c), (d).
-
B.
(a), (b).
-
C.
(a), (b), (c).
-
D.
(a), (b), (d).
Đáp án : B
Dựa vào cấu tạo của arachidonic acid.
a) đúng
b) đúng
c) sai vì đây là acid không no chứ không phải chất béo.
d) sai, AA phản ứng cộng với 4 mol H2.
Đáp án B
Nước cứng gây nhiều trở ngại cho đời sống thường ngày. Các nguồn nước ngầm hoặc nước ở các ao hồ, sông suối thường có độ cứng cao bởi quá trình hòa tan các ion Ca2+, Mg2+ có trong thành phần của lớp trầm tích đá vôi. Cho các phát biểu sau:
(a) Có thể dùng Na3PO4 để làm mềm nước có tính cứng vĩnh cửu.
(b) Nấu ăn bằng nước cứng làm thực phẩm lâu chín, giảm mùi vị.
(c) Nước tự nhiên có chứa ion Ca2+, Mg2+, Cl-, SO42- gọi là nước có tính cứng tạm thời.
(d) Nước không chứa hoặc chứa ít các ion Ca2+ và Mg2+ được gọi là nước mềm.
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
4
-
D.
3
Đáp án : D
Dựa vào thành phần của nước cứng.
a) Đúng
b) Đúng
c) Sai, nước có tính cứng vĩnh cửu
d) đúng
đáp án D
Kim loại nhóm IA đều là kim loại nhẹ, có khối lượng riêng nhỏ là do
-
A.
có bán kính nguyên tử lớn và cấu trúc mạng tinh thể kém đặc khít.
-
B.
có độ âm điện lớn và thế điện cực chuẩn nhỏ.
-
C.
có bán kính nguyên tử nhỏ và cấu trúc mạng tinh thể đặc khít.
-
D.
có độ âm điện nhỏ và thế điện cực chuẩn nhỏ.
Đáp án : A
Dựa vào tính chất vật lí của kim loại nhóm IA.
Kim loại nhóm IA có khối lượng riêng nhỏ là do có bán kính nguyên tử lớn và cấu trúc mạng tinh thể kém đặc khít.
Đáp án A
Dãy nào sau đây sắp xếp các kim loại Li, Na, K theo mức độ phản ứng với oxygen giảm dần?
-
A.
Li, Na, K.
-
B.
Na, K, Li.
-
C.
K, Na, Li.
-
D.
K, Li, Na.
Đáp án : C
Dựa vào tính chất hoá học của nhóm IA.
K, Na, Li giảm dần tính khử.
Đáp án C
Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trong đời sống. Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
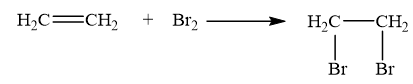
Cơ chế của phản ứng trên xảy ra qua 2 giai đoạn như sau:

Nhận định nào sau đây không đúng?
-
A.
Hiện tượng của phản ứng là dung dịch bromine bị nhạt màu dần.
-
B.
Giai đoạn 2, có sự hình thành liên kết π.
-
C.
Giai đoạn 1, có sự phá vỡ liên kết π trong liên kết đôi C=C.
-
D.
Phản ứng trên thuộc loại phản ứng cộng.
Đáp án : B
Dựa vào cơ chế của phản ứng.
B sai do giai đoạn 2 có sự phá vỡ liên kết π.
Đáp án B
Zinc blende (chứa ZnS) là loại quặng chứa kẽm trong tự nhiên. Trong công nghiệp, để tách kim loại Zn từ quặng zinc blende tiến hành theo sơ đồ sau:
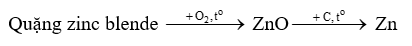
Phương pháp điều chế kim loại nào đã được sử dụng trong quá trình sản xuất Zn theo sơ đồ trên?
-
A.
Điện phân nóng chảy.
-
B.
Nhiệt luyện.
-
C.
Thuỷ luyện.
-
D.
Điện phân dung dịch.
Đáp án : B
Dựa vào các phương pháp tách chất.
Phương pháp điều chế Zn trên là phương pháp nhiệt luyện.
Đáp án B
Cho 1 số hiện tượng sau:
(a) Sáp nến chảy ra bị đông lại khi nguội.
(b) Sữa bị chua và vón cục khi để hở lâu trong không khí.
(c) Mật ong để lâu ngày thấy có hiện tượng kết tinh.
(d) Đậu phụ được làm từ sữa đậu nành.
Số hiện tượng không có sự đông tụ protein là
-
A.
4
-
B.
2
-
C.
3
-
D.
1
Đáp án : B
Dựa vào tính chất hoá học của protein.
(a) sai, vì sáp nến không chứa protein.
(c) sai, vì không có sự đông tụ protein.
Đáp án B
Trong quá trình hoạt động của pin Zn – Cu, quá trình xảy ra ở anode là
-
A.
Cu → Cu2+ + 2e.
-
B.
Cu2+ + 2e → Cu.
-
C.
Zn → Zn2+ + 2e.
-
D.
Zn2+ + 2e → Zn.
Đáp án : C
Dựa vào nguyên tắc xảy ra trong pin điện hoá.
ở anode xảy ra quá trình oxi hoá Zn: Zn → Zn2+ + 2e.
Đáp án C
Trong công nghiệp, nguyên liệu thường dùng để sản xuất vôi sống, xi măng, vật liệu xây dựng là đá vôi. Thành phần chính của đá vôi là
-
A.
CaCO3.
-
B.
Ca3(PO4)2.
-
C.
CaSO4.
-
D.
Ca(H2PO4)2.
Đáp án : A
Dựa vào hợp chất nhóm IIA.
Đá vôi có thành phần chính là CaCO3.
Đáp án A
“... là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định”. Nội dung phù hợp trong dấu … là
-
A.
Kết tinh.
-
B.
Sắc ký.
-
C.
Chiết.
-
D.
Chưng cất.
Đáp án : D
Dựa vào phương pháp tinh chế hợp chất hữu cơ.
Chưng cất là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất trong hỗn hợp ở áp suất nhất định.
Đáp án D
Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:

Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 2 và số 4 được điều chế bằng phản ứng trùng hợp monomer nào dưới đây?
-
A.
CH2=CH–Cl.
-
B.
CH2=CH–C6H5.
-
C.
CH2=CH–CH3.
-
D.
CH2=CH2.
Đáp án : D
Dựa vào cấu tạo của polymer.
Polymer (2) và (4) được điều chế từ ethylene
Đáp án D
a) Từ kết quả thí nghiệm, kết luận giả thuyết của nhóm học sinh trên là đúng.
b) Trong mẫu trắng đã có sẵn một lượng lactic acid đáng kể.
c) Nhiệt độ tối ưu cho quá trình lên men tạo acid lactic là 37°C.
d) Trong thí nghiệm trên, lượng acid lactic được tạo thành nhiều nhất trong một mẫu (200 mL) là 3,78 gam.
a) Từ kết quả thí nghiệm, kết luận giả thuyết của nhóm học sinh trên là đúng.
b) Trong mẫu trắng đã có sẵn một lượng lactic acid đáng kể.
c) Nhiệt độ tối ưu cho quá trình lên men tạo acid lactic là 37°C.
d) Trong thí nghiệm trên, lượng acid lactic được tạo thành nhiều nhất trong một mẫu (200 mL) là 3,78 gam.
Dựa vào các yếu tố ảnh hưởng đến tốc độ phản ứng.
a) sai, vì trong thí nghiệm có ảnh hưởng của chất xúc tác.
b) sai, mẫu trắng có chứa CH3COOH.
c) đúng
d) đúng
Lysine và cadaverine là hai hợp chất liên quan đến quá trình phân hủy protein. Lysine là một amino acid thiết yếu, còn cadaverine được hình thành từ sự khử carboxyl của Lysine dưới tác động của enzyme trong môi trường. Về cấu tạo, từ phân tử lysine, thay thế nhóm chức carboxyl bằng một nguyên tử hydrogen thì thu được phân tử cadaverine.
a) Công thức phân tử của cadaverine là C₅H₁₄N₂.
b) Lysine và cadaverine đều có hai nhóm amine trong phân tử.
c) Lysine thuộc loại α-amino acid, còn cadaverine không phải amino acid
d) Ở pH = 7, cả hai chất đều có thể tồn tại ở dạng ion lưỡng cực.
a) Công thức phân tử của cadaverine là C₅H₁₄N₂.
b) Lysine và cadaverine đều có hai nhóm amine trong phân tử.
c) Lysine thuộc loại α-amino acid, còn cadaverine không phải amino acid
d) Ở pH = 7, cả hai chất đều có thể tồn tại ở dạng ion lưỡng cực.
Dựa vào tính điện di của amino acid.
a) đúng
b) đúng
c) đúng
d) sai, ở pH = 7, chỉ có lysine tồn tại ở dạng ion lưỡng cực.
Một học sinh tiến hành thí nghiệm nghiên cứu sự tạo thành phức chất, phản ứng của phức chất iron(III), ghi lại hiện tượng quan sát được và đưa ra những nhận định như sau:
- Bước 1: Hòa tan iron(III) sulfate vào ống nghiệm chứa nước thu được dung dịch màu vàng nâu. Sau một thời gian, thấy có kết tủa màu nâu đỏ trong ống nghiệm.
- Bước 2: Lọc bỏ kết tủa, thêm KSCN (potassium thiocyanate) vào nước lọc thấy dung dịch chuyển sang màu đỏ máu của các phức chất bát diện chứa từ 1 đến 6 phối tử SCN-.
- Bước 3: Thêm tiếp dung dịch KF dư vào ống nghiệm thấy dung dịch nhạt màu dần và mất màu do tạo phức chất [FeF3]3-.
a) Các phức chất được tạo thành ở Bước 2 đều là phức chất trung tính, không mang điện tích.
b) Ở bước 1 đã xảy ra quá trình hình thành và thủy phân phức chất aqua của ion Fe³⁺.
c) Trong thí nghiệm trên, khi tạo phức với ion Fe³⁺, phối tử là anion tạo luôn ra phức chất có màu đậm hơn phối tử là phân tử trung hòa.
d) Ở Bước 2, xảy ra phản ứng thay thế phối tử H2O bằng phối tử SCN-.
a) Các phức chất được tạo thành ở Bước 2 đều là phức chất trung tính, không mang điện tích.
b) Ở bước 1 đã xảy ra quá trình hình thành và thủy phân phức chất aqua của ion Fe³⁺.
c) Trong thí nghiệm trên, khi tạo phức với ion Fe³⁺, phối tử là anion tạo luôn ra phức chất có màu đậm hơn phối tử là phân tử trung hòa.
d) Ở Bước 2, xảy ra phản ứng thay thế phối tử H2O bằng phối tử SCN-.
Dựa vào tính chất của phức chất.
a) sai, phức chất [FeF3]3- có mang điện tích.
b) đúng
c) sai, phối tử F- có màu nhạt hơn phối tử trung hoà.
d) đúng
Một nhóm học sinh nghiên cứu sự ăn mòn kim loại của một sợi kẽm với giả thuyết: “trong cùng điều kiện, tốc độ ăn mòn điện hóa nhanh hơn tốc độ ăn mòn hóa học”. Để kiểm tra giả thuyết của mình, nhóm học sinh trên đã chuẩn bị 2 sợi kẽm đã làm sạch bề mặt, có kích thước, khối lượng như nhau và tiến hành các thí nghiệm như sau:
- Thí nghiệm 1: Nhúng một sợi kẽm vào dung dịch H2SO4 0,5M (hình 1).
- Thí nghiệm 2: Nhúng sợi kẽm còn lại vào dung dịch H2SO4 0,5M cùng với một sợi đồng và nối chúng lại qua vôn kế (hình 2).

a) Nhóm học sinh trên quan sát thấy bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 1 nhanh hơn bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là sai.
b) Nếu thế điện cực chuẩn \({{\rm{E}}_{Z{n^{2 + }}/Zn}} = - 0,763{\rm{ V}}\), \({\rm{E}}_{2{H^{\rm{ + }}}{\rm{/}}{{\rm{H}}_2}}^0 = 0{\rm{ V}}\), \({\rm{E}}_{{\rm{C}}{{\rm{u}}^{2 + }}{\rm{/Cu}}}^0 = 0,340{\rm{ V}}\)thì vôn kế luôn chỉ giá trị cố định là 1,10 V.
c) Ở thí nghiệm 2, quan sát thấy có bọt khí thoát ra trên bề mặt sợi đồng, chứng tỏ sợi đồng bị ăn mòn điện hóa học.
d) Sau 3 phút, nhóm học sinh lấy 2 sợi kẽm ra cân lại, thấy khối lượng sợi kẽm ở thí nghiệm 1 lớn hơn khối lượng sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là đúng.
a) Nhóm học sinh trên quan sát thấy bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 1 nhanh hơn bọt khí thoát ra trên bề mặt sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là sai.
b) Nếu thế điện cực chuẩn \({{\rm{E}}_{Z{n^{2 + }}/Zn}} = - 0,763{\rm{ V}}\), \({\rm{E}}_{2{H^{\rm{ + }}}{\rm{/}}{{\rm{H}}_2}}^0 = 0{\rm{ V}}\), \({\rm{E}}_{{\rm{C}}{{\rm{u}}^{2 + }}{\rm{/Cu}}}^0 = 0,340{\rm{ V}}\)thì vôn kế luôn chỉ giá trị cố định là 1,10 V.
c) Ở thí nghiệm 2, quan sát thấy có bọt khí thoát ra trên bề mặt sợi đồng, chứng tỏ sợi đồng bị ăn mòn điện hóa học.
d) Sau 3 phút, nhóm học sinh lấy 2 sợi kẽm ra cân lại, thấy khối lượng sợi kẽm ở thí nghiệm 1 lớn hơn khối lượng sợi kẽm ở thí nghiệm 2, chứng tỏ giả thuyết trên là đúng.
Dựa vào cấu tạo của pin điện
a) sai, bọt khí thoát ra ở thí nghiệm 2 nhanh hơn thí nghiệm 1.
b) sai, không được đo ở điều kkiện chuẩn.
c) sai, Zn bị ăn mòn điện hoá.
d) đúng
DEP (diethyl phthalatate) được dùng làm thuốc điều trị bệnh ghẻ và giảm triệu chứng sưng tấy ở vùng da bị côn trùng cắn. Có thể điều chế DEP từ o-xylene qua 2 giai đoạn được mô tả như sau:

Một loại thuốc DEP thành phẩm trên thị trường (loại 10 g) có hàm lượng diethyl phthalatate là 96% (về khối lượng). Hãy tính số lọ thuốc loại này sản xuất được từ 12 kg o-xylene? (làm tròn đến hàng đơn vị).
Tính số mol o – xylene từ sơ đồ phản ứng tính được DEP.
n o – xylene = 12 : 106 = \(\frac{6}{{53}}k.mol\)
n DEF = \(\frac{6}{{53}}k.mol\)
m DEF = \(\frac{6}{{53}}.222 = \frac{{1332}}{{53}}kg\)
m thuốc = \(\frac{{1332}}{{53}}.1000:96\% .50,4\% = 13194\)g
Số lọ thuốc sản xuất được là: 13194 : 10 = 1319 lọ
Đáp án 1319
Trong công nghiệp, sản xuất nước Javel xảy ra qua hai giai đoạn chính sau:
- Giai đoạn 1: điện phân dung dịch NaCl bão hòa không có màng ngăn điện cực:
2NaCl(aq) + 2H2O(l) → 2NaOH(aq) + H2(g) + Cl2(g)
- Giai đoạn 2: khí Cl2 phản ứng với dung dịch NaOH tạo ra nước Javel:
Cl2(g) + 2NaOH(aq) → NaCl(aq) + NaClO(aq) + H2O(l)
Một loại nước Javel (có khối lượng riêng 1,15 g/cm3) được bán trên thị trường với can dung tích 5,0 L có nồng độ NaClO, NaCl và NaOH lần lượt là 10%; 8% và 0,8%. Để sản xuất 500 can nước Javel ở trên cần bao nhiêu kg dung dịch NaCl 18,5% (làm tròn kết đến hàng đơn vị)?
Tính khối lượng NaClO, NaCl, NaOH.
Khối lượng nước Javel trong 500 can là: 5000.1,15= 5750 kg
Khối lượng NaClO là: 10% . 5750 = 575kg
Khối lượng NaCl là: 8%.5750 = 460kg
Khối lượng NaOH là: 0,8%.5750 = 46kg
n NaClO = \(\frac{{575}}{{74,5}}kmol\)
n NaCl = \(\frac{{460}}{{58,5}}kmol\)
n NaOH =\(\frac{{46}}{{40}}kmol\)
Bảo toàn nguyên tố Na: n NaCl = \(\frac{{575}}{{74,5}}kmol\)+\(\frac{{460}}{{58,5}}kmol\)+\(\frac{{46}}{{40}}kmol\)=16,731 kmol
m dd NaCl = 5290kg => Số chai cần dùng = 5290.500.10-3 = 2645 chai
Cho thế điện cực chuẩn của các cặp oxi hoá - khử như bảng sau:
|
Cặp oxi hóa – khử |
Al3+/Al |
Pb2+/Pb |
Sn2+/Sn |
Fe3+/Fe2+ |
Fe2+/Fe |
Hg2+/Hg |
Ag+/Ag |
|
Thế điện cực chuẩn (V) |
–1,676 |
–0,126 |
–0,137 |
0,771 |
–0,440 |
0,853 |
0,799 |
Trong số các kim loại: Al, Pb, Sn, Fe, Hg và Ag, ở điều kiện chuẩn có bao nhiêu kim loại tác dụng được với dung dịch Fe(NO3)3?
Dựa vào cấu tạo của pin điện.
Al, Pb, Sn, Fe có tác dụng với Fe(NO3)3.
Đáp án 4
Một nhà máy nhiệt điện khí có sản lượng điện 106 kWh/ngày (1 kWh = 3600 kJ) sử dụng khí thiên nhiên hóa lỏng LNG làm nhiên liệu đã giảm được a% khí thải CO2 so với nhà máy nhiệt điện than (sử dụng than đá làm nhiên liệu) có cùng sản lượng điện. Biết rằng:
- Khí thiên nhiên hóa lỏng LNG chứa 95% CH4 và 5% C2H6 về thể tích. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 mol CH4 là 890 kJ; 1 mol C2H6 là 1560 kJ và có 64% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn LNG được chuyển hóa thành điện năng.
- Than đá chứa 78% carbon về khối lượng, còn lại là các tạp chất không chứa carbon. Năng lượng tỏa ra khi đốt cháy hoàn toàn 1 tấn than đá là 3.107 kJ và chỉ có 50% nhiệt lượng tỏa ra của quá trình đốt cháy hoàn toàn than đá được chuyển hóa thành điện năng.
Tính giá trị của a (làm tròn đến hàng đơn vị).
Tính nhiệt lượng của khí thiên nhiên hoá lỏng và than đá.
Lượng nhiệt toả ra khi đốt cháy than đá: \(3,{6.10^9}.50\% = 1,{8.10^9}kJ\)→ m than đá: \(\frac{{1,{{8.10}^9}}}{{{{3.10}^7}}} = 60\)
→m C = 78%.240 = 46,8 tấn
n CO2 = n C = \(\frac{{46,8}}{{12}} = 3,{9.10^6}mol\)
Gọi số mol của CH4 và C2H6 lần lượt là 0,95a và 0,05a
Lượng nhiệt toả ra khi đốt cháy LNG = \({\bf{3}},{\bf{6}}.{\bf{1}}{{\bf{0}}^{\bf{9}}}.\frac{{100}}{{64}} = 5,{625.10^9}kJ\)
→ 0,95a.890 + 0,05a.1560 = 5,625.109 → a = 6,09.106
Bảo toàn nguyên tố C: n CO2 = 0,95a + 0,05.2.a =6394500 mol
Vậy n CO2 giảm = \(\frac{{3,{{9.10}^6} - 6394500}}{{3,{{9.10}^6}}}.100\% = \)59%
Cho các hydrocarbon sau: propane, buta-1,3-diene, ethane, ethene, styrene, propene. Có bao nhiêu chất có thể trùng hợp tạo polymer?
Dựa vào phương pháp điều chế polymer.
Buta – 1,3 – diene, ethene, styrene, propene có thể trùng hợp tạo polymer.
Đáp án 4.
Ở điều kiện thường, hợp chất hữu cơ X tồn tại ở trạng thái lỏng. Khi phân tích thành phần nguyên tố của hợp chất hữu cơ X thu được kết quả %C; %H;, %O (theo khối lượng) lần lượt là 60.00%; 13.33%; 26.67%. Cho các nhận định sau về X:
(1) Công thức phân tử của X là C3H8O.
(2) X tạo được liên kết hydrogen với nước.
(3) Oxi hóa X bằng CuO luôn cho sản phẩm có phản ứng với thuốc thử Tollens.
(4) X là alcohol.
Hãy sắp xếp các nhận định đúng theo thứ tự tăng dần.
Tìm công thức của hợp chất hữu cơ X.
\(C:H:O = \frac{{60}}{{12}}:\frac{{13,33}}{1}:\frac{{26,67}}{{16}} = 5:13,33:1,666875 = 3:8:1\)
CTPT X: C3H8O
(1) đúng
(2) đúng
(3) sai, vì oxi hoá alcohol bậc 2 thu được ketone.
(4) đúng
Đáp án 124
Vào mùa hè, trong một số khách sạn hay nhà hàng
I. Trắc nghiệm
Cho dung dịch glucose vào ống ng̣hiệm chứa copper
Cho ba dung dịch có cùng nồng độ mol sau:
Thức uống chứa cồn như rượu, bia, nước trái cây lên men
Cho biết số hiệu nguyên tử của sodium là 11. Vị trí của sodium trong bảng tuần hoàn là
Điện phân dung dịch CuSO4 với anode
Chuẩn độ dung dịch NaOH chưa biết chính xác nồng độ
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau
Chất nào sau đây thuộc loại disaccharide?
Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu
Tro thực vật được sử dụng như một loại phân bón
Cho khối lượng riêng của các chất như bảng sau:
Cho biết nguyên tử khối: H = 1; C = 12; N = 14; O = 16; Na = 23; Al = 27; S = 32; Fe = 56
Tinh bột chứa hỗn hợp chất nào sau đây?
Đề thi thử THPT môn Hóa lần 1 năm 2025 Trường THPT Chuyên KHTN Hà Nội
Cấu trúc mạch vòng của carbohydrate nào sau đây không có nhóm -OH hemiacetal hoặc hemiketal?
Trong nước, thế điện cực chuẩn của kim loại Mn+/M
Chất X có công thức cấu tạo là CH3CH2COOCH3. Tên gọi của X là
Các bài khác cùng chuyên mục









Danh sách bình luận