Đề thi thử THPT môn Hóa lần 1 năm 2025 Sở GD Thanh Hóa
Tro thực vật được sử dụng như một loại phân bón
Đề bài
Tro thực vật được sử dụng như một loại phân bón cung cấp nguyên tố potassium cho cây trồng do có chứa loại muối nào sau đây?
-
A.
\({{\rm{K}}_2}{\rm{C}}{{\rm{O}}_3}\).
-
B.
KCl.
-
C.
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\).
-
D.
\({{\rm{K}}_2}{\rm{S}}{{\rm{O}}_4}\).
Đồ thị dưới đây biểu thị sự thay đổi nhiệt độ sôi theo số nguyên tử carbon trong phân tử alkane không phân nhánh:
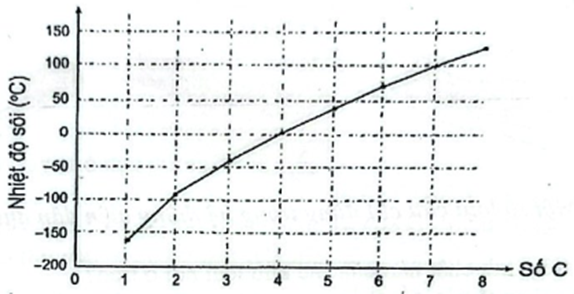
Dựa vào đồ thị, hãy cho biết có bao nhiêu alkane không phân nhánh ở thể khí trong điều kiện thường (25oC, 1 bar)?
-
A.
4
-
B.
3
-
C.
2
-
D.
5
Một thí nghiệm được mô tả như hình bên dưới:

Giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại được gọi là điểm đẳng điện (kí hiệu là pI). Mỗi amino acid có điểm đẳng điện khác nhau: Alanine ( \({\rm{pI}} = 6,0\) ), Lysine ( \({\rm{pI}} = 9,74\) ) và glutamic acid ( \({\rm{pI}} = 3,08\) ). Khi \({\rm{pH}} < {\rm{pI}}\) thì amino acid đó tồn tại chủ yếu ở dạng cation, còn khi \({\rm{pH}} > {\rm{pI}}\) thì amino acid đó tồn tại chủ yếu ở dạng anion.
Cho các nhận định sau:
(a) Thí nghiệm trên biểu diễn tính điện li của amino acid.
(b) Ion tồn tại chủ yếu đối với Lys là cation, sẽ di chuyển về cực âm của nguồn điện nên vệt (1) là cation của Lys.
(c) Ion tồn tại chủ yếu đối với Ala là ion lưỡng cực, không di chuyển nên vệt (2) là Ala.
(d) Ion tồn tại chủ yếu đối với Glu là anion, sẽ di chuyển về cực dương của nguồn điện nên vệt (3) là anion của Glu.
Các nhận định đúng là:
-
A.
(a), (b), (d).
-
B.
(b), (c), (d).
-
C.
(a), (c), (d).
-
D.
(a), (b), (c).
Trong khái niệm về liên kết kim loại: " Liên kết kim loại là liên kết được hình thành do lực hút tĩnh điện giữa các electron...(1)... với các ion...(2)... kim loại ở các nút mạng."
Các từ cần điền vào vị trí (1), (2) lần lượt là:
-
A.
ngoài cùng, âm.
-
B.
hóa trị tự do, dương.
-
C.
hóa trị, lưỡng cực.
-
D.
hóa trị tự do, âm.
Nhận xét nào sau đây đúng về quá trình điện phân ở hai điện cực?
-
A.
Anion nhận electron ở anode.
-
B.
Sự khử anion xảy ra ở cathode.
-
C.
Cation nhường electron ở cathode.
-
D.
Sự oxi hoá xảy ra ở anode.
Dây cầu chì thường được làm từ các kim loại như Thiếc (Sn), Chì (Pb) và Cadmium (Cd). Khi dòng điện vượt quá mức cho phép, dây chì sẽ nóng chảy và ngắt mạch, ngăn dòng điện tiếp tục lưu thông và tránh nguy cơ cháy nổ.

Hình: Một số loại cầu chì dùng trong hệ thống điện dân dụng và công nghiệp
Ứng dụng này dựa trên tính chất nào của các kim loại nói ở trên?
-
A.
Có nhiệt độ nóng chảy tương đối thấp.
-
B.
Có tính dẻo cao.
-
C.
Có độ dẫn điện cao.
-
D.
Có độ cứng tương đối thấp.
Trên hộp xốp cách nhiệt, hộp đựng thức ăn mang về, cốc, chén đĩa dùng một lần,... thường được in kí hiệu như hình dưới đây.

Polymer dùng làm các đồ dùng đó được tổng hợp từ monomer nào sau đây?
-
A.
\({\rm{C}}{{\rm{H}}_2} = {\rm{C}}{{\rm{H}}_2}\).
-
B.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CHCl}}\).
-
C.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CH}} - {{\rm{C}}_6}{{\rm{H}}_5}\).
-
D.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CHC}}{{\rm{H}}_3}\).
"Amino acid là hợp chất hữu cơ tạp chức, trong phân tự chứa đồng thời nhóm chức..(1)... và nhóm chức.. (2)..". Nội dung phư hợp trong ô trống (1), (2) lần lượt là:
-
A.
carboxyl ( -COOH ), amino (\( - {\rm{N}}{{\rm{H}}_2}\)).
-
B.
hydroxyl ( -OH ), amino \(\left( { - {\rm{N}}{{\rm{H}}_2}} \right)\).
-
C.
carboxyl ( -COOH ), hydroxyl ( -OH ).
-
D.
carbonyl (-CO-), carboxyl (-COOH).
Phát biểu nào sau đây đúng?
-
A.
Cao su lưu hóa có tính đàn hồi kém hơn cao su chưa lưu hóa.
-
B.
Tơ polyamide rất bền trong môi trường acid.
-
C.
Tơ cellulose acetate thuộc loại tơ bán tổng hợp.
-
D.
Polyethylene được điều chế bằng phản ứng trùng ngưng ethylene.
Cho các phát biểu sau:
(a) Ở điều kiện thường, methylamine là chất khí mùi khai khó chịu, độc, dễ tan trong nước.
(b) Ở điều kiện thường, alanine là chất lỏng ít tan trong nước.
(c) Dung dịch aniline làm đổi màu phenolphtalein.
(d) Khi nấu canh cua, hiện tượng riêu cua nổi lên trên là do sự đông tụ protein.
(e) Tripeptide Ala-Val-Gly có phản ứng màu biure.
(f) Các alkylamine đều tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng khí nitrogen.
(g) Các arylamine được điều chế từ ammonia và dẫn xuất halogen.
Số phát biểu đúng là:
-
A.
2
-
B.
5
-
C.
4
-
D.
3
Chất nào sau đây thuộc loại polysaccharide?
-
A.
Tinh bột.
-
B.
Maltose.
-
C.
Glucose.
-
D.
Saccharose.
Cặp chất nào sau đây không phải là đồng phân của nhau?
-
A.
Maltose và saccharose.
-
B.
Methyl formate và acetic acid.
-
C.
Fructose và glucose.
-
D.
Tinh bột và cellulose.
Để khám phá khoa học, một học sinh chế tạo ra một pin quả chanh gồm một lá Cu và một lá Zn ghim vào một quả chanh và nối với vôn kế như hình dưới. Vôn kế quay đồng nghĩa với sự xuất hiện dòng điện.
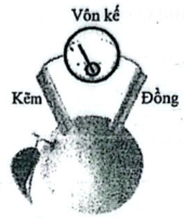
Bán phản ứng nào sau đây xảy ra ở cực dương?
-
A.
\({\rm{Zn}}({\rm{s}}) \to {\rm{Z}}{{\rm{n}}^{2 + }}({\rm{aq}}) + 2{\rm{e}}\).
-
B.
\({\rm{C}}{{\rm{u}}^{2 + }}({\rm{aq}}) + 2{\rm{e}} \to {\rm{Cu}}({\rm{s}})\).
-
C.
\(2{{\rm{H}}^ + }({\rm{aq}}) + 2{\rm{e}} \to {{\rm{H}}_2}(\;{\rm{g}})\).
-
D.
\({\rm{Cu}}({\rm{s}}) \to {\rm{C}}{{\rm{u}}^{2 + }}({\rm{aq}}) + 2{\rm{e}}\).
Công thức cấu tạo thu gọn của ethylmethylamine là
-
A.
\({\rm{C}}{{\rm{H}}_3} - {\rm{C}}{{\rm{H}}_2} - {\rm{N}}{{\rm{H}}_2}\).
-
B.
\({\rm{C}}{{\rm{H}}_3} - {\rm{N}}{{\rm{H}}_2}\).
-
C.
\({\rm{C}}{{\rm{H}}_3} - {\rm{NH}} - {\rm{C}}{{\rm{H}}_3}\).
-
D.
\({\rm{C}}{{\rm{H}}_3} - {\rm{NH}} - {\rm{C}}{{\rm{H}}_2} - {\rm{C}}{{\rm{H}}_3}\).
-
A.
Benzyl acetate.
-
B.
Propyl acetate.
-
C.
Isopropyl acetate.
-
D.
Isoamyl acetate.
Bơ thực vật (chất béo no, ở dạng rắn) có thể được tạo ra từ dầu thực vật (chất béo không no, ở dạng lỏng) bằng phản ứng hóa học nào sau đây?
-
A.
Hydrogen hoá.
-
B.
Thuẏ phân.
-
C.
Hydrate hoá.
-
D.
Xà phòng hoá.
Hiện tượng nổ nào sau đây có phản ứng hóa học?
-
A.
Bóng bay bị nổ do bơm quá căng.
-
B.
Pháo hoa được bắn trong các dịp lễ hội.
-
C.
Nổ nồi hơi khi đang sử dụng.
-
D.
Nổ lốp xe khi đang di chuyển trên đường.
Phát biểu nào sau đây đúng?
-
A.
Poly(vinyl chloride) được điều chế bằng phản ứng cộng HCl vào ethylene.
-
B.
Amylose có cấu trúc mạch phân nhánh.
-
C.
Polybuta-1,3-diene được dùng để sản xuất cao su buna.
-
D.
Polyacrylonitrile được điều chế bằng phản ứng trùng ngưng.
Tại một nhà máy sản xuất rượu, cứ 10 tấn tinh bột (chứa 6,85% tạp chất trơ) sẽ sản xuất được \(7,21\;{{\rm{m}}^3}\) dung dịch ethanol 40 độ (cho khối lượng riêng của ethanol nguyên chất là \(0,789\;{\rm{g}}/{\rm{c}}{{\rm{m}}^3}\)). Tinh bột là một polysaccharide gồm nhiều gốc \(\alpha \)-glucose liên kết với nhau tạo ra hai dạng mạch amylose và amylopectin. Dưới đây là một đoạn cấu tạo của tinh bột:
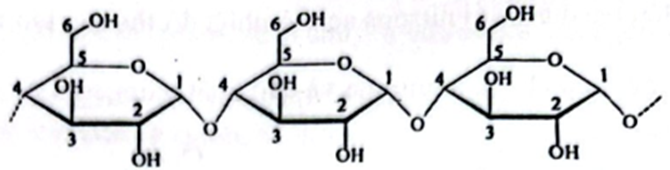
a) Hiệu suất của quá trình sản xuất ethanol ở trên đạt 40% (kết quả cuối cùng được làm tròn đến hàng đơn vị).
b) Đoạn mạch trên có các gốc \(\alpha \)-glucose được liên kết với nhau bằng liên kết \(\alpha \)-1,4-glycoside.
c) Tinh bột bị thủy phân hoàn toàn trong môi trường acid tạo thành glucose.
d) Amylopectin có các gốc \(\alpha \)-glucose liên kết với nhau bởi liên kết \(\alpha - 1,4\)-glycoside và \(\alpha - 1,6\)-glycoside.
Quá trình điện phân để mạ đồng (Cu) lên một chiếc chìa khoá được làm từ thép không gỉ, được mô tả ở hình vẽ (cathode là chìa khóa, anode là đồng thô, dung dịch điện phân là \({\rm{CuS}}{{\rm{O}}_4}\)). Biết cường độ dòng điện không đổi là 10 A, thời gian điện phân là 16 phút 5 giây, Cu có khối lượng riêng là ; nguyên tử khối của Cu là ; hiệu su\(8,9{\rm{gam}}/{\rm{c}}{{\rm{m}}^3}\)t điện phân 100%.
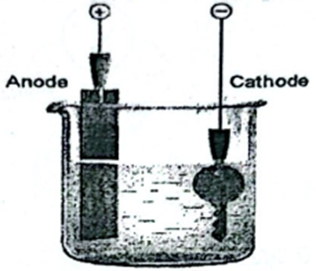
a) Trong quá trình điện phân, điện cực anode tan dần.
b) Trong quá trình điện phân, số mol muối \({\rm{CuS}}{{\rm{O}}_4}\) không thay đổi.
c) Anode xảy ra quá trình khử ion \({\rm{C}}{{\rm{u}}^{2 + }}\).
d) Nếu chiếc chìa khóa có tổng diện tích cần mạ là \(20\;{\rm{c}}{{\rm{m}}^2}\) thì bề dày lớp đồng bám đều trên chiếc chìa khóa là \(0,006\;{\rm{cm}}\) (làm tròn đến hàng phần nghìn).
Acid béo là thành phần quan trọng trong một chế độ ăn uống lành mạnh. Cho acid béo oleic acid và linoleic acid với công thức, kèm theo nhiệt độ nóng chảy tnc
|
Oleic acid \(\left( {t_{nc}^0 = {{13}^o}{\rm{C}}} \right)\) : |
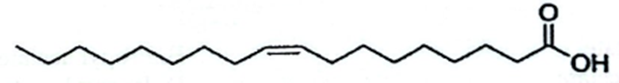 |
|
Linoleic acid (ts=15oC) |
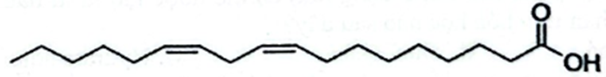 |
a) Oleic acid và linoleic acid đều ở dạng đồng phân cis.
b) Oleic acid và linoleic acid đều có khả năng làm mất màu dung dịch bromine.
c) Oleic acid và linoleic acid đều là các acid béo omega-6.
d) Một loại mỡ động vật chứa 50% triolein, 30% tripalmitin và 20% tristearin về khối lượng. Khối lượng muối RCOONa điều chế từ 100 kg loại mỡ trên là 110,25 kg. (Cho hiệu suất phản ứng là 100%, kết quả làm tròn, lấy đến hàng phần trăm)
Trong phòng thí nghiệm, một nhóm học sinh xác định thành phần của chiếc đinh sắt (đinh sắt được làm từ hợp kim của sắt với carbon và một số nguyên tố khác) đã bị oxi hóa một phần thành gỉ sắt \(\left( {{\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3}.{\rm{n}}{{\rm{H}}_2}{\rm{O}}} \right)\) theo các bước sau:
Bước 1: Hòa tan hoàn toàn đinh sắt vào dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) loãng, nóng (dùng gấp đôi lượng phản ứng), thu được 200 mL dung dịch X và \(0,2225\;{\rm{mol}}{{\rm{H}}_2}\),
Bước 2: Cho dung dịch \({\rm{Ba}}{({\rm{OH}})_2}\) dư vào 20 mL dung dịch X thu được \(14,4\;{\rm{g}}\) kết tủa.
Bước 3: Nhỏ từ từ dung dịch \({\rm{KMn}}{{\rm{O}}_4}0,1{\rm{M}}\) vào 20 mL dung dịch X đến khi phản ứng vừa đủ thì hết 46 mL.
Giả thiết toàn bộ gỉ sắt tạo ra bám trên đinh sắt; carbon và một số nguyên tố khác trong đinh sắt là những chất không tham gia phản ứng trong các bước.
a) Sau bước 1, trong dung dịch X chỉ chứa hai muối tan.
b) Phần trăm khối lượng sắt đã bị oxi hóa thành gi sắt là 20% (làm tròn đến hàng đơn vị).
c) Ở bước 1 và bước 3 đều xảy ra phản ứng oxi - hóa khứ.
d) Đinh sắt bị gỉ chủ yếu do sự ăn mòn điện hóa học.
Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 2,0 kg than đá. Giả thiết loại than đá này chứa 90% carbon và 1,2% sulfur về khối lượng, còn lại là các tạp chất trơ không cháy.
Cho các phản ứng:
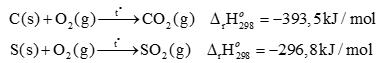
hiệu suất sử dụng nhiệt là 37,5%. Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện? (Biết cứ 1 số điện =1 kWh=3600 kJ)? (Kết quả làm tròn đến hàng đơn vị).
Đáp án:
Đun nóng một loại mỡ động vật với dung dịch NaOH, sản phẩm thu được có chứa muối sodium stearate. Phân tử khối của sodium stearate là bao nhiêu?
Đáp án:
Khi thủy phân không hoàn toàn pentapeptide A có công thức Val-Ala-Gly-Ala-Gly thì dung dịch thu được có tối đa bao nhiêu peptide có thể tham gia phản ứng màu biuret?
Đáp án:
Đề tìm hiểu về sự ăn mòn kim loại. Một nhóm học sinh đã thực hiện 5 thí nghiệm sau
- Thí nghiệm 1: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
- Thí nghiệm 2: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M nhỏ thêm vài giọt dung dịch CuSO4.
- Thí nghiệm 3: Cho một dây bạc sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
- Thí nghiệm 4: Cho một dây Cu được quấn bởi dây Zinc(Zn) vào ống nghiệm chứa 2 mL dung dịch HCl 0,2M.
- Thí nghiệm 5: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch CuSO4 0,2M.
Liệt kê các thí nghiệm xuất hiện ăn mòn điện hóa theo thứ tự tăng dần? (Ví dụ 123,1234, ...)
Đáp án:
Quy trình công nghệ̣ sản xuất phèn aluminium \(\left( {{\rm{KAl}}{{\left( {{\rm{S}}{{\rm{O}}_4}} \right)}_2} \cdot 12{{\rm{H}}_2}{\rm{O}}} \right)\) từ cao lanh (thành phần khoáng chính là kaolinit \(\left( {{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}.{\rm{Si}}{{\rm{O}}_2}} \right)\) được tiến hành như sau:
- Bước 1: Cao lanh đã tuyển được hoạt hóa ở chế độ nung 700C {\rm{C}}\) trong 1 giờ.
- Bước 2: Sau đó được nghiền nhỏ và hòa tan trong \(117,6\;{\rm{kg}}\) dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}25\% \) ở nhiệt độ \({95^o}{\rm{C}}\). Lượng acid được tính theo tỷ lượng vừa đủ. Sau khi phản ứng, dung dịch muối aluminium sulfate được lọc tách khỏi bã silicon.
- Bước 3: Thêm tiếp 87 kg dung dịch \({{\rm{K}}_2}{\rm{S}}{{\rm{O}}_4}20\% \) vừa đủ vào dung dịch sau phản ứng rồi đun nóng để nước bay hơi cho đến khi khối lượng dung dịch giảm đi 30% so với ban đầu.
- Bước 4: Hạ nhiệt độ dung dịch về \({20^o}{\rm{C}}\) để phèn chua tách ra.
Biết các phản ứng xảy ra hoàn toàn và 100 gam nước ở \({20^o}{\rm{C}}\) hòa tan được tối đa 11,2 gam \({\rm{KAl}}{\left( {{\rm{S}}{{\rm{O}}_4}} \right)_2}\). Sau khi kết thúc các bước trên thu được m kg phèn chua. Tính m ? (kết quả làm tròn đến hàng phần mười)
Đáp án:
Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
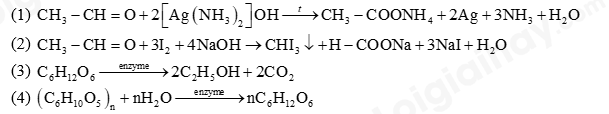
Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi; Phản ứng với thuốc thử Tollens, phản ứng lên men rượu, phản ứng tạo iodoform, phản ứng thủy phân và sắp xếp theo trình tự thành dãy bốn số. (ví dụ: 1234, 4321, .. ).
Đáp án:
Lời giải và đáp án
Tro thực vật được sử dụng như một loại phân bón cung cấp nguyên tố potassium cho cây trồng do có chứa loại muối nào sau đây?
-
A.
\({{\rm{K}}_2}{\rm{C}}{{\rm{O}}_3}\).
-
B.
KCl.
-
C.
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\).
-
D.
\({{\rm{K}}_2}{\rm{S}}{{\rm{O}}_4}\).
Đáp án : A
Dựa vào kiến thức về phân bón hóa học.
Trong tro thực vật có chứa muối K2CO3 có thể làm phân bón cung cấp nguyên tố K cho cây trồng.
Đáp án A
Đồ thị dưới đây biểu thị sự thay đổi nhiệt độ sôi theo số nguyên tử carbon trong phân tử alkane không phân nhánh:

Dựa vào đồ thị, hãy cho biết có bao nhiêu alkane không phân nhánh ở thể khí trong điều kiện thường (25oC, 1 bar)?
-
A.
4
-
B.
3
-
C.
2
-
D.
5
Đáp án : A
Các alkane có nhiệt độ sôi thấp hơn 0 thường ở thể khí.
Có 4 alkane ở thể khí trong điều kiện thường.
Đáp án A
Một thí nghiệm được mô tả như hình bên dưới:

Giá trị pH mà khi đó amino acid có nồng độ ion lưỡng cực là cực đại được gọi là điểm đẳng điện (kí hiệu là pI). Mỗi amino acid có điểm đẳng điện khác nhau: Alanine ( \({\rm{pI}} = 6,0\) ), Lysine ( \({\rm{pI}} = 9,74\) ) và glutamic acid ( \({\rm{pI}} = 3,08\) ). Khi \({\rm{pH}} < {\rm{pI}}\) thì amino acid đó tồn tại chủ yếu ở dạng cation, còn khi \({\rm{pH}} > {\rm{pI}}\) thì amino acid đó tồn tại chủ yếu ở dạng anion.
Cho các nhận định sau:
(a) Thí nghiệm trên biểu diễn tính điện li của amino acid.
(b) Ion tồn tại chủ yếu đối với Lys là cation, sẽ di chuyển về cực âm của nguồn điện nên vệt (1) là cation của Lys.
(c) Ion tồn tại chủ yếu đối với Ala là ion lưỡng cực, không di chuyển nên vệt (2) là Ala.
(d) Ion tồn tại chủ yếu đối với Glu là anion, sẽ di chuyển về cực dương của nguồn điện nên vệt (3) là anion của Glu.
Các nhận định đúng là:
-
A.
(a), (b), (d).
-
B.
(b), (c), (d).
-
C.
(a), (c), (d).
-
D.
(a), (b), (c).
Đáp án : B
Dựa vào tính điện di của amino acid.
(a) sai, thí nghiệm trên biểu diễn tính điện di của amino acid.
(b) đúng
(c) đúng
(d) đúng
Đáp án B
Trong khái niệm về liên kết kim loại: " Liên kết kim loại là liên kết được hình thành do lực hút tĩnh điện giữa các electron...(1)... với các ion...(2)... kim loại ở các nút mạng."
Các từ cần điền vào vị trí (1), (2) lần lượt là:
-
A.
ngoài cùng, âm.
-
B.
hóa trị tự do, dương.
-
C.
hóa trị, lưỡng cực.
-
D.
hóa trị tự do, âm.
Đáp án : B
Dựa vào khái niệm liên kết kim loại.
Liên kết kim loại là liên kết được hình thành do lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Đáp án B
Nhận xét nào sau đây đúng về quá trình điện phân ở hai điện cực?
-
A.
Anion nhận electron ở anode.
-
B.
Sự khử anion xảy ra ở cathode.
-
C.
Cation nhường electron ở cathode.
-
D.
Sự oxi hoá xảy ra ở anode.
Đáp án : D
Dựa vào nguyên tắc điện phân.
Khi điện phân: Tại cathode xảy ra quá trình khử, tại anode xảy ra quá trình oxi hóa.
Đáp án D
Dây cầu chì thường được làm từ các kim loại như Thiếc (Sn), Chì (Pb) và Cadmium (Cd). Khi dòng điện vượt quá mức cho phép, dây chì sẽ nóng chảy và ngắt mạch, ngăn dòng điện tiếp tục lưu thông và tránh nguy cơ cháy nổ.

Hình: Một số loại cầu chì dùng trong hệ thống điện dân dụng và công nghiệp
Ứng dụng này dựa trên tính chất nào của các kim loại nói ở trên?
-
A.
Có nhiệt độ nóng chảy tương đối thấp.
-
B.
Có tính dẻo cao.
-
C.
Có độ dẫn điện cao.
-
D.
Có độ cứng tương đối thấp.
Đáp án : A
Dựa vào tính chất vật lí của kim loại.
Ứng dụng trên dựa vào nhiệt độ nóng chảy tương đối thấp của kim loại, điều này ngăn cho dòng điện vượt mức tiếp tục vượt quá tránh tình trạng cháy nổ.
Đáp án A
Trên hộp xốp cách nhiệt, hộp đựng thức ăn mang về, cốc, chén đĩa dùng một lần,... thường được in kí hiệu như hình dưới đây.

Polymer dùng làm các đồ dùng đó được tổng hợp từ monomer nào sau đây?
-
A.
\({\rm{C}}{{\rm{H}}_2} = {\rm{C}}{{\rm{H}}_2}\).
-
B.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CHCl}}\).
-
C.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CH}} - {{\rm{C}}_6}{{\rm{H}}_5}\).
-
D.
\({\rm{C}}{{\rm{H}}_2} = {\rm{CHC}}{{\rm{H}}_3}\).
Đáp án : C
Dựa vào kí hiệu trên polymer.
Trên hình xốp có kí hiệu PS là viết tắt của polystryrene nên monomer tương ứng là\({\rm{C}}{{\rm{H}}_2} = {\rm{CH}} - {{\rm{C}}_6}{{\rm{H}}_5}\)
Đáp án C
"Amino acid là hợp chất hữu cơ tạp chức, trong phân tự chứa đồng thời nhóm chức..(1)... và nhóm chức.. (2)..". Nội dung phư hợp trong ô trống (1), (2) lần lượt là:
-
A.
carboxyl ( -COOH ), amino (\( - {\rm{N}}{{\rm{H}}_2}\)).
-
B.
hydroxyl ( -OH ), amino \(\left( { - {\rm{N}}{{\rm{H}}_2}} \right)\).
-
C.
carboxyl ( -COOH ), hydroxyl ( -OH ).
-
D.
carbonyl (-CO-), carboxyl (-COOH).
Đáp án : A
Dựa vào khái niệm về amino acid.
(1) carboxyl ( -COOH ), (2) amino (\( - {\rm{N}}{{\rm{H}}_2}\)).
Đáp án A
Phát biểu nào sau đây đúng?
-
A.
Cao su lưu hóa có tính đàn hồi kém hơn cao su chưa lưu hóa.
-
B.
Tơ polyamide rất bền trong môi trường acid.
-
C.
Tơ cellulose acetate thuộc loại tơ bán tổng hợp.
-
D.
Polyethylene được điều chế bằng phản ứng trùng ngưng ethylene.
Đáp án : C
Dựa vào tính chất của polymer.
A. sai, cao su lưu hóa có tính đàn hồi cao hơn.
B sai, tơ polyamide kém bền trong môi trường acid hoặc base.
C đúng
D sai, PE được điều chế từ phản ứng trùng hợp ethylene.
Đáp án C
Cho các phát biểu sau:
(a) Ở điều kiện thường, methylamine là chất khí mùi khai khó chịu, độc, dễ tan trong nước.
(b) Ở điều kiện thường, alanine là chất lỏng ít tan trong nước.
(c) Dung dịch aniline làm đổi màu phenolphtalein.
(d) Khi nấu canh cua, hiện tượng riêu cua nổi lên trên là do sự đông tụ protein.
(e) Tripeptide Ala-Val-Gly có phản ứng màu biure.
(f) Các alkylamine đều tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng khí nitrogen.
(g) Các arylamine được điều chế từ ammonia và dẫn xuất halogen.
Số phát biểu đúng là:
-
A.
2
-
B.
5
-
C.
4
-
D.
3
Đáp án : D
Dựa vào tính chất vật lí của peptide.
(a) đúng
(b) sai, ở điều kiện thường alanine tồn tại ở thể rắn dễ tan trong nước.
(c) sai, dung dịch aniline không làm đổi màu quỳ tím và phenolphtalein.
(d) đúng
(e) đúng
(f) sai, có thể sinh ra muối diazonium
g) sai vì các arylamine thường được điều chế bằng cách khử hợp chất nitrobenzene (hoặc dẫn xuất nitro tương ứng) bởi một số kim loại (Zn, Fe,...) trong dung dịch HCl.
Đáp án D
Chất nào sau đây thuộc loại polysaccharide?
-
A.
Tinh bột.
-
B.
Maltose.
-
C.
Glucose.
-
D.
Saccharose.
Đáp án : A
Dựa vào phân loại carbohydrate.
Tinh bột thuộc polysaccharide.
Đáp án A
Cặp chất nào sau đây không phải là đồng phân của nhau?
-
A.
Maltose và saccharose.
-
B.
Methyl formate và acetic acid.
-
C.
Fructose và glucose.
-
D.
Tinh bột và cellulose.
Đáp án : D
Dựa vào phân loại carbohydrate.
Tinh bột và cellulose không phải đồng phân của nhau cho hệ số n khác nhau.
Đáp án D
Để khám phá khoa học, một học sinh chế tạo ra một pin quả chanh gồm một lá Cu và một lá Zn ghim vào một quả chanh và nối với vôn kế như hình dưới. Vôn kế quay đồng nghĩa với sự xuất hiện dòng điện.

Bán phản ứng nào sau đây xảy ra ở cực dương?
-
A.
\({\rm{Zn}}({\rm{s}}) \to {\rm{Z}}{{\rm{n}}^{2 + }}({\rm{aq}}) + 2{\rm{e}}\).
-
B.
\({\rm{C}}{{\rm{u}}^{2 + }}({\rm{aq}}) + 2{\rm{e}} \to {\rm{Cu}}({\rm{s}})\).
-
C.
\(2{{\rm{H}}^ + }({\rm{aq}}) + 2{\rm{e}} \to {{\rm{H}}_2}(\;{\rm{g}})\).
-
D.
\({\rm{Cu}}({\rm{s}}) \to {\rm{C}}{{\rm{u}}^{2 + }}({\rm{aq}}) + 2{\rm{e}}\).
Đáp án : B
Dựa vào nguyên tắc hoạt động của pin Galvani.
Tại điện cực dương xảy ra quá trình khử: \({\rm{C}}{{\rm{u}}^{2 + }}({\rm{aq}}) + 2{\rm{e}} \to {\rm{Cu}}({\rm{s}})\)
Đáp án B
Công thức cấu tạo thu gọn của ethylmethylamine là
-
A.
\({\rm{C}}{{\rm{H}}_3} - {\rm{C}}{{\rm{H}}_2} - {\rm{N}}{{\rm{H}}_2}\).
-
B.
\({\rm{C}}{{\rm{H}}_3} - {\rm{N}}{{\rm{H}}_2}\).
-
C.
\({\rm{C}}{{\rm{H}}_3} - {\rm{NH}} - {\rm{C}}{{\rm{H}}_3}\).
-
D.
\({\rm{C}}{{\rm{H}}_3} - {\rm{NH}} - {\rm{C}}{{\rm{H}}_2} - {\rm{C}}{{\rm{H}}_3}\).
Đáp án : D
Dựa vào tên gọi amine suy luận ra công thức cấu tạo.
Ethylmethylamine có công thức là: \({\rm{C}}{{\rm{H}}_3} - {\rm{NH}} - {\rm{C}}{{\rm{H}}_2} - {\rm{C}}{{\rm{H}}_3}\)
Đáp án D
-
A.
Benzyl acetate.
-
B.
Propyl acetate.
-
C.
Isopropyl acetate.
-
D.
Isoamyl acetate.
Đáp án : D
Dựa vào một số ester có mùi thơm đặc biệt.
Isoamyl acetate có mùi thơm của chuối chín.
Đáp án D
Bơ thực vật (chất béo no, ở dạng rắn) có thể được tạo ra từ dầu thực vật (chất béo không no, ở dạng lỏng) bằng phản ứng hóa học nào sau đây?
-
A.
Hydrogen hoá.
-
B.
Thuẏ phân.
-
C.
Hydrate hoá.
-
D.
Xà phòng hoá.
Đáp án : A
Dựa vào tính chất của chất béo.
Có thể chuyển hóa chất béo no, ở dạng rắn thành dầu thực vật qua phản ứng hydrogen hóa.
Đáp án A
Hiện tượng nổ nào sau đây có phản ứng hóa học?
-
A.
Bóng bay bị nổ do bơm quá căng.
-
B.
Pháo hoa được bắn trong các dịp lễ hội.
-
C.
Nổ nồi hơi khi đang sử dụng.
-
D.
Nổ lốp xe khi đang di chuyển trên đường.
Đáp án : B
Dựa vào dấu hiện nhận biết phản ứng hóa học.
Pháo hoa được bắn trong các dịp lễ hội có phản ứng hóa học do các hợp chất được đốt cháy trong không khí.
Đáp án B
Phát biểu nào sau đây đúng?
-
A.
Poly(vinyl chloride) được điều chế bằng phản ứng cộng HCl vào ethylene.
-
B.
Amylose có cấu trúc mạch phân nhánh.
-
C.
Polybuta-1,3-diene được dùng để sản xuất cao su buna.
-
D.
Polyacrylonitrile được điều chế bằng phản ứng trùng ngưng.
Đáp án : C
Dựa vào tính chất hóa học của polymer
A sai, PVC được điều chế từ phản ứng trùng hợp vinyl chloride.
B sai, amylose có cấu trúc mạch không phân nhánh.
C đúng
D sai, polyacrylonitrile được điều chế bằng phản ứng trùng hợp.
Tại một nhà máy sản xuất rượu, cứ 10 tấn tinh bột (chứa 6,85% tạp chất trơ) sẽ sản xuất được \(7,21\;{{\rm{m}}^3}\) dung dịch ethanol 40 độ (cho khối lượng riêng của ethanol nguyên chất là \(0,789\;{\rm{g}}/{\rm{c}}{{\rm{m}}^3}\)). Tinh bột là một polysaccharide gồm nhiều gốc \(\alpha \)-glucose liên kết với nhau tạo ra hai dạng mạch amylose và amylopectin. Dưới đây là một đoạn cấu tạo của tinh bột:

a) Hiệu suất của quá trình sản xuất ethanol ở trên đạt 40% (kết quả cuối cùng được làm tròn đến hàng đơn vị).
b) Đoạn mạch trên có các gốc \(\alpha \)-glucose được liên kết với nhau bằng liên kết \(\alpha \)-1,4-glycoside.
c) Tinh bột bị thủy phân hoàn toàn trong môi trường acid tạo thành glucose.
d) Amylopectin có các gốc \(\alpha \)-glucose liên kết với nhau bởi liên kết \(\alpha - 1,4\)-glycoside và \(\alpha - 1,6\)-glycoside.
a) Hiệu suất của quá trình sản xuất ethanol ở trên đạt 40% (kết quả cuối cùng được làm tròn đến hàng đơn vị).
b) Đoạn mạch trên có các gốc \(\alpha \)-glucose được liên kết với nhau bằng liên kết \(\alpha \)-1,4-glycoside.
c) Tinh bột bị thủy phân hoàn toàn trong môi trường acid tạo thành glucose.
d) Amylopectin có các gốc \(\alpha \)-glucose liên kết với nhau bởi liên kết \(\alpha - 1,4\)-glycoside và \(\alpha - 1,6\)-glycoside.
Dựa vào cấu tạo của tinh bột.
a) Sai vì
khối lượng tinh bột = 10.93,15% = 9,315 tấn
Thể tích C2H5OH nguyên chất là: = 7,21.40% = 2,884 m3 = 2,884.106 cm3.
m C2H5OH = 2,884.106.0,789 = 2,275476.106 g = 2,275476 tấn.
(C6H10O5)n → 2 C2H5OH
162 92
← 2,275476
H% = \(\frac{{2,275476}}{{46}}:2.162:9,315.100\% = 43\% \)
b) đúng
c) đúng
d) đúng
Quá trình điện phân để mạ đồng (Cu) lên một chiếc chìa khoá được làm từ thép không gỉ, được mô tả ở hình vẽ (cathode là chìa khóa, anode là đồng thô, dung dịch điện phân là \({\rm{CuS}}{{\rm{O}}_4}\)). Biết cường độ dòng điện không đổi là 10 A, thời gian điện phân là 16 phút 5 giây, Cu có khối lượng riêng là ; nguyên tử khối của Cu là ; hiệu su\(8,9{\rm{gam}}/{\rm{c}}{{\rm{m}}^3}\)t điện phân 100%.

a) Trong quá trình điện phân, điện cực anode tan dần.
b) Trong quá trình điện phân, số mol muối \({\rm{CuS}}{{\rm{O}}_4}\) không thay đổi.
c) Anode xảy ra quá trình khử ion \({\rm{C}}{{\rm{u}}^{2 + }}\).
d) Nếu chiếc chìa khóa có tổng diện tích cần mạ là \(20\;{\rm{c}}{{\rm{m}}^2}\) thì bề dày lớp đồng bám đều trên chiếc chìa khóa là \(0,006\;{\rm{cm}}\) (làm tròn đến hàng phần nghìn).
a) Trong quá trình điện phân, điện cực anode tan dần.
b) Trong quá trình điện phân, số mol muối \({\rm{CuS}}{{\rm{O}}_4}\) không thay đổi.
c) Anode xảy ra quá trình khử ion \({\rm{C}}{{\rm{u}}^{2 + }}\).
d) Nếu chiếc chìa khóa có tổng diện tích cần mạ là \(20\;{\rm{c}}{{\rm{m}}^2}\) thì bề dày lớp đồng bám đều trên chiếc chìa khóa là \(0,006\;{\rm{cm}}\) (làm tròn đến hàng phần nghìn).
Dựa vào nguyên tắc điện phân
a) đúng
b) đúng
c) sai, tại anode xảy ra quá trình oxi hóa Cu.
d) sai vì
ne trao đổi = \(\frac{{I.t}}{F} = \frac{{10.965}}{{96500}} = 0,1mol\)
n Cu = 0,1 : 2 = 0,05 mol
Thể tích Cu cần mạ là: 0,05.64:8,9 = 0,356cm3 => Bề dạy lớp đồng bám trên chiếc chìa khóa là: 0,356 : 20 = 0,0178 cm
Acid béo là thành phần quan trọng trong một chế độ ăn uống lành mạnh. Cho acid béo oleic acid và linoleic acid với công thức, kèm theo nhiệt độ nóng chảy tnc
|
Oleic acid \(\left( {t_{nc}^0 = {{13}^o}{\rm{C}}} \right)\) : |
 |
|
Linoleic acid (ts=15oC) |
 |
a) Oleic acid và linoleic acid đều ở dạng đồng phân cis.
b) Oleic acid và linoleic acid đều có khả năng làm mất màu dung dịch bromine.
c) Oleic acid và linoleic acid đều là các acid béo omega-6.
d) Một loại mỡ động vật chứa 50% triolein, 30% tripalmitin và 20% tristearin về khối lượng. Khối lượng muối RCOONa điều chế từ 100 kg loại mỡ trên là 110,25 kg. (Cho hiệu suất phản ứng là 100%, kết quả làm tròn, lấy đến hàng phần trăm)
a) Oleic acid và linoleic acid đều ở dạng đồng phân cis.
b) Oleic acid và linoleic acid đều có khả năng làm mất màu dung dịch bromine.
c) Oleic acid và linoleic acid đều là các acid béo omega-6.
d) Một loại mỡ động vật chứa 50% triolein, 30% tripalmitin và 20% tristearin về khối lượng. Khối lượng muối RCOONa điều chế từ 100 kg loại mỡ trên là 110,25 kg. (Cho hiệu suất phản ứng là 100%, kết quả làm tròn, lấy đến hàng phần trăm)
Dựa vào cấu tạo của acid béo.
a) đúng
b) đúng
c) sai, oleic acid là acid béo omega – 9.
d) sai vì
khối lượng triolein trong mỡ là: 50%.100 = 50kg → n triolein = 50 : 884 = \(\frac{{25}}{{442}}k.mol\)
khối lượng tripalmitin là: 100.30% = 30kg → n tripalmitin = \(\frac{{30}}{{806}}k.mol\)
khối lượng tristrearin là: 100.20% = 20 kg → n tristrearin = \(\frac{{20}}{{887}}k.mol\)
n NaOH = (\(\frac{{25}}{{442}}k.mol\)+ \(\frac{{30}}{{806}}k.mol\)+\(\frac{{20}}{{887}}k.mol\)).3
n C3H5(OH)3 = (\(\frac{{25}}{{442}}k.mol\)+ \(\frac{{30}}{{806}}k.mol\)+\(\frac{{20}}{{887}}k.mol\)).
Bảo toàn khối lượng: m RCOONa = 100 + (\(\frac{{25}}{{442}}k.mol\)+ \(\frac{{30}}{{806}}k.mol\)+\(\frac{{20}}{{887}}k.mol\)).3.40 - (\(\frac{{25}}{{442}}k.mol\)+ \(\frac{{30}}{{806}}k.mol\)+\(\frac{{20}}{{887}}k.mol\)).92 = 103,26kg.
Trong phòng thí nghiệm, một nhóm học sinh xác định thành phần của chiếc đinh sắt (đinh sắt được làm từ hợp kim của sắt với carbon và một số nguyên tố khác) đã bị oxi hóa một phần thành gỉ sắt \(\left( {{\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3}.{\rm{n}}{{\rm{H}}_2}{\rm{O}}} \right)\) theo các bước sau:
Bước 1: Hòa tan hoàn toàn đinh sắt vào dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) loãng, nóng (dùng gấp đôi lượng phản ứng), thu được 200 mL dung dịch X và \(0,2225\;{\rm{mol}}{{\rm{H}}_2}\),
Bước 2: Cho dung dịch \({\rm{Ba}}{({\rm{OH}})_2}\) dư vào 20 mL dung dịch X thu được \(14,4\;{\rm{g}}\) kết tủa.
Bước 3: Nhỏ từ từ dung dịch \({\rm{KMn}}{{\rm{O}}_4}0,1{\rm{M}}\) vào 20 mL dung dịch X đến khi phản ứng vừa đủ thì hết 46 mL.
Giả thiết toàn bộ gỉ sắt tạo ra bám trên đinh sắt; carbon và một số nguyên tố khác trong đinh sắt là những chất không tham gia phản ứng trong các bước.
a) Sau bước 1, trong dung dịch X chỉ chứa hai muối tan.
b) Phần trăm khối lượng sắt đã bị oxi hóa thành gi sắt là 20% (làm tròn đến hàng đơn vị).
c) Ở bước 1 và bước 3 đều xảy ra phản ứng oxi - hóa khứ.
d) Đinh sắt bị gỉ chủ yếu do sự ăn mòn điện hóa học.
a) Sau bước 1, trong dung dịch X chỉ chứa hai muối tan.
b) Phần trăm khối lượng sắt đã bị oxi hóa thành gi sắt là 20% (làm tròn đến hàng đơn vị).
c) Ở bước 1 và bước 3 đều xảy ra phản ứng oxi - hóa khứ.
d) Đinh sắt bị gỉ chủ yếu do sự ăn mòn điện hóa học.
Dựa vào sự ăn mòn kim loại.
a) Sai, sau bước 1 X chứa 2 muối và acid dư.
b) sai, trong 20ml X chứa FeSO4 (a) và Fe2(SO4)3 (b) và H2SO4 dư (a + 3b)
khi tác dụng với Ba(OH)2
m kết tủa = m BaSO4 + m Fe(OH)2 + m Fe(OH)3 = 233(2a + 6b) + 90a + 107.2b = 14,4g
Khi tác dụng với KMnO4: n Fe2+ = a = 0,046.0,1.5 = 0,023 mol => b = 0,01
Trong 200ml X chứa FeSO4 (0,23), Fe2(SO4)3 (0,01) và H2SO4 dư
n H2SO4 phản ứng = 0,23 + 0,01.3 = n H2 + n H2O => n O = n H2O = 0,035 => n Fe2O3 = 0,0125 mol
=> %Fe bị oxi hóa = 0,0125.2:0,25.100 = 10%
c) đúng
d) đúng, do đinh sắt là hợp kim Fe – C nên ăn mòn điện hóa học là chủ yếu
Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 2,0 kg than đá. Giả thiết loại than đá này chứa 90% carbon và 1,2% sulfur về khối lượng, còn lại là các tạp chất trơ không cháy.
Cho các phản ứng:
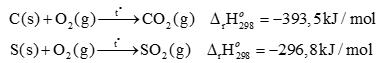
hiệu suất sử dụng nhiệt là 37,5%. Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện? (Biết cứ 1 số điện =1 kWh=3600 kJ)? (Kết quả làm tròn đến hàng đơn vị).
Đáp án:
Đáp án:
tính số mol C và S có trong than đá từ đó tính tổng lượng nhiệt tỏa ra từ phản ứng đốt cháy.
Khối lượng C là: 2.90% = 1,8kg => n C= \(\frac{{1,8}}{{12}} = 0,15k.mol\)=150 mol
Khối lượng S là: 2.1,2% = 0,024kg → n S = \(\frac{{0,024}}{{32}} = 0,00075k.mol = 0,75mol\)
Lượng nhiệt tỏa ra khi đốt cháy 2kg than đá là: 150.393,5 + 0,75.296,8 = 59247,6 kJ
Lượng nhiệt cung cấp cho hộ gia đình là: 59247,6.37,5% = 22217,85 kJ.
Số điện tương đương là: 22217,85 : 3600 = 6 số
Đun nóng một loại mỡ động vật với dung dịch NaOH, sản phẩm thu được có chứa muối sodium stearate. Phân tử khối của sodium stearate là bao nhiêu?
Đáp án:
Đáp án:
Dựa vào công thức cấu tạo của chất béo.
Muối sodium stearate có công thức: C17H35COONa. Phân tử khối là: 306
Đáp án 306
Khi thủy phân không hoàn toàn pentapeptide A có công thức Val-Ala-Gly-Ala-Gly thì dung dịch thu được có tối đa bao nhiêu peptide có thể tham gia phản ứng màu biuret?
Đáp án:
Đáp án:
Từ tripeptide có phản ứng màu biuret.
Val – Ala – Gly; Ala – Gly – Ala; Gly – Ala – Gly; Val – Ala – Gly – Ala; Ala – Gly – Ala – Gly; Val – Ala – Gly – Ala – Gly
Vậy có tối đa 6
Đề tìm hiểu về sự ăn mòn kim loại. Một nhóm học sinh đã thực hiện 5 thí nghiệm sau
- Thí nghiệm 1: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
- Thí nghiệm 2: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M nhỏ thêm vài giọt dung dịch CuSO4.
- Thí nghiệm 3: Cho một dây bạc sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
- Thí nghiệm 4: Cho một dây Cu được quấn bởi dây Zinc(Zn) vào ống nghiệm chứa 2 mL dung dịch HCl 0,2M.
- Thí nghiệm 5: Cho một dây Zinc(Zn) sạch vào ống nghiệm chứa 2 mL dung dịch CuSO4 0,2M.
Liệt kê các thí nghiệm xuất hiện ăn mòn điện hóa theo thứ tự tăng dần? (Ví dụ 123,1234, ...)
Đáp án:
Đáp án:
Dựa vào nguyên tắc ăn mòn điện hóa.
TN1: chỉ xảy ra ăn mòn hóa học do không đủ 2 điện cực.
TN2: Có xảy ra ăn mòn điện hóa.
TN3: chỉ xảy ra ăn mòn hóa học
TN4: có xảy ra ăn mòn điện hóa.
TN5: có xảy ra ăn mòn hóa học
Thứ tự tăng dần là: 245
Quy trình công nghệ̣ sản xuất phèn aluminium \(\left( {{\rm{KAl}}{{\left( {{\rm{S}}{{\rm{O}}_4}} \right)}_2} \cdot 12{{\rm{H}}_2}{\rm{O}}} \right)\) từ cao lanh (thành phần khoáng chính là kaolinit \(\left( {{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}.{\rm{Si}}{{\rm{O}}_2}} \right)\) được tiến hành như sau:
- Bước 1: Cao lanh đã tuyển được hoạt hóa ở chế độ nung 700C {\rm{C}}\) trong 1 giờ.
- Bước 2: Sau đó được nghiền nhỏ và hòa tan trong \(117,6\;{\rm{kg}}\) dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}25\% \) ở nhiệt độ \({95^o}{\rm{C}}\). Lượng acid được tính theo tỷ lượng vừa đủ. Sau khi phản ứng, dung dịch muối aluminium sulfate được lọc tách khỏi bã silicon.
- Bước 3: Thêm tiếp 87 kg dung dịch \({{\rm{K}}_2}{\rm{S}}{{\rm{O}}_4}20\% \) vừa đủ vào dung dịch sau phản ứng rồi đun nóng để nước bay hơi cho đến khi khối lượng dung dịch giảm đi 30% so với ban đầu.
- Bước 4: Hạ nhiệt độ dung dịch về \({20^o}{\rm{C}}\) để phèn chua tách ra.
Biết các phản ứng xảy ra hoàn toàn và 100 gam nước ở \({20^o}{\rm{C}}\) hòa tan được tối đa 11,2 gam \({\rm{KAl}}{\left( {{\rm{S}}{{\rm{O}}_4}} \right)_2}\). Sau khi kết thúc các bước trên thu được m kg phèn chua. Tính m ? (kết quả làm tròn đến hàng phần mười)
Đáp án:
Đáp án:
Dựa vào các bước sản xuất phèn nhôm.
n H2SO4 = 177,6.25% : 98 = 0,3 k.mol
Al2O3 +3 H2SO4 → Al2(SO4)3 + 3H2O
m dung dịch Al2(SO4)3 = m Al2O3 + m dd H2SO4 = 0,1.102 + 117,6 = 127,8kg
n Al2(SO4)3 = 0,1 k.mol
n K2SO4 = 87.20% : 174 = 0,1 k.mol
m dung dịch sau pha trộn = 127,8 + 87 = 214,8 kg
Khối lượng dung dịch còn lại sau bay hơi: 214,8 – 214,8.30% = 150,36kg
n KAl(SO4)2 ban đầu = 0,2 k.mol
Đặ n Kal(SO4)2.12H2O thu được = x
C% KAl(SO4)2 bão hòa còn lại = \(\frac{{258.(0,2 - x)}}{{150,36 - 474{\rm{x}}}}.100 = \frac{{11,2}}{{11,2 + 100}} = > x = 0,17338k.mol\)
=> m KAl(SO4)2.12H2O = 0,17338.447 = 82,2Kg
Cho phương trình hóa học của các phản ứng được đánh số thứ tự từ 1 tới 4 dưới đây:
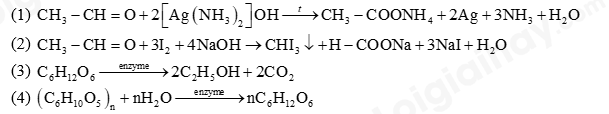
Gán số thứ tự phương trình hoá học của các phản ứng theo tên gọi; Phản ứng với thuốc thử Tollens, phản ứng lên men rượu, phản ứng tạo iodoform, phản ứng thủy phân và sắp xếp theo trình tự thành dãy bốn số. (ví dụ: 1234, 4321, .. ).
Đáp án:
Đáp án:
Dựa vào tính chất hóa học của tinh bột.
(1) phản ứng với thuốc thử Tollens
(2) phản ứng tạo iodoform
(3) phản ứng lên men rượu
(4) phản ứng thủy phân.
Sắp xếp: 1324
Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu
Chất nào sau đây thuộc loại disaccharide?
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau
Chuẩn độ dung dịch NaOH chưa biết chính xác nồng độ
Điện phân dung dịch CuSO4 với anode
Cho biết số hiệu nguyên tử của sodium là 11. Vị trí của sodium trong bảng tuần hoàn là
Thức uống chứa cồn như rượu, bia, nước trái cây lên men
Cho ba dung dịch có cùng nồng độ mol sau:
Để chuyển hóa dầu mỡ động thực vật thành xà phòng người ta thực hiện quá trình
Vào mùa hè, trong một số khách sạn hay nhà hàng
I. Trắc nghiệm
Cho dung dịch glucose vào ống ng̣hiệm chứa copper
Cho khối lượng riêng của các chất như bảng sau:
Cho biết nguyên tử khối: H = 1; C = 12; N = 14; O = 16; Na = 23; Al = 27; S = 32; Fe = 56
Tinh bột chứa hỗn hợp chất nào sau đây?
Đề thi thử THPT môn Hóa lần 1 năm 2025 Trường THPT Chuyên KHTN Hà Nội
Cấu trúc mạch vòng của carbohydrate nào sau đây không có nhóm -OH hemiacetal hoặc hemiketal?
Trong nước, thế điện cực chuẩn của kim loại Mn+/M
Chất X có công thức cấu tạo là CH3CH2COOCH3. Tên gọi của X là
Các bài khác cùng chuyên mục










Danh sách bình luận