Đề tham khảo thi THPT môn Hóa - Đề số 10 (hay, chi tiết)
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
Đề bài
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
-
A.
W.
-
B.
Cr.
-
C.
Hg.
-
D.
Pb.
Trong các mẫu nước cứng sau đây, nước cứng tạm thời là
-
A.
dung dịch Ca(HCO3)2
-
B.
dung dịch MgSO4
-
C.
dung dịch CaCl2
-
D.
dung dịch Mg(NO3)2
Polymer nào sau đây có chứa nguyên tố chlorine?
-
A.
Poly(methyl methacrylate).
-
B.
Polyethylene.
-
C.
Polybutadien.
-
D.
Poly(vinyl chloride).
Duralumin là hợp kim của nhôm có thành phần chính là
-
A.
nhôm và đồng.
-
B.
nhôm và sắt.
-
C.
nhôm và carbon.
-
D.
nhôm và thuỷ ngân.
-
A.
Các ion Na+ và ion Cl– góp chung cặp electron hình thành liên kết.
-
B.
Các nguyên tử Na và Cl góp chung cặp e hình thành liên kết.
-
C.
Các nguyên tử Na và Cl hút nhau bằng lực hút tĩnh điện.
-
D.
Các ion ion Na+ và ion Cl – hút nhau bằng lực hút tĩnh điện.
Thực hiện bốn phản ứng hoá học theo sơ đồ:
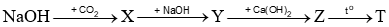
Biết X, Y, Z, T là các hợp chất của kim loại. Công thức hoá học của T là
-
A.
NaOH.
-
B.
CaCO3.
-
C.
Na2CO3.
-
D.
CaO.
Hợp chất X có công thức C8H14O4. Từ X thực hiện các phản ứng (theo đúng tỉ lệ mol):
(a) X + 2NaOH → X1 + X2 + H2O
(b) X1 + H2SO4 → X3 + Na2SO4
(c) nX3 + nX4 → nylon-6,6 + 2nH2O
(d) 2X2 + X3 → X5 + 2H2O
Phân tử khối của X5 là
-
A.
174.
-
B.
216.
-
C.
202.
-
D.
198.
Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện theo sơ đồ phản ứng: H2S + SO2 → S + H2O.
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1 000 m3 khí thiên nhiên (đkc) (chứa 5 mg H2S/m3) là
-
A.
10,0 g.
-
B.
5,0 g.
-
C.
7,06 g.
-
D.
100,0 g.
Trên phổ hồng ngoại của hợp chất hữu cơ X chỉ có hấp thụ đặc trưng ở 1715 cm-1. Chất X có thể là chất nào trong các chất dưới đây?
-
A.
CH3COCH3.
-
B.
CH3CH2OH.
-
C.
CH3CH2CHO.
-
D.
C6H5CH2OH.
Tên gọi của ester CH3COOC2H5 là
-
A.
Ethyl formate.
-
B.
Ethyl acetate.
-
C.
Methyl acetate.
-
D.
Methyl formate.
Cho dãy các chất: H2, H2NCH2COOH, C6H5NH2, C2H5NH2, CH3COOH. Số chất trong dãy phản ứng với NaOH trong dung dịch là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Ở điều kiện thường, chất nào sau đây dễ tan trong nước?
-
A.
Tristearin.
-
B.
Cellulose.
-
C.
Glucose.
-
D.
Tinh bột.
Ở điều kiện thích hợp (nhiệt độ, áp suất, chất xúc tác), benzene tác dụng được với tất cả các chất trong dãy nào dưới đây?
-
A.
HCl, HNO3, Cl2, H2.
-
B.
HNO3, H2, Cl2, H2O.
-
C.
HNO3, Cl2, KMnO4, Br2.
-
D.
HNO3, H2, Cl2, O2.
Công thức nào sau đây có thể là công thức của chất béo?
-
A.
CH3COOCH2C6H5.
-
B.
C15H31COOCH3.
-
C.
(C17H33COO)2C2H4.
-
D.
(C17H35COO)3C3H5.
Chất nào sau đây là amine bậc 2?
-
A.
H2N-CH2-NH2.
-
B.
(CH3)2CH-NH2.
-
C.
CH3-NH-CH2C(CH3)2
-
D.
(CH3)3N.
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với các thuốc thử được ghi lại dưới bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Dung dịch I2 |
Có màu xanh tím |
|
Y |
Cu(OH)2 trong môi trường kiềm |
Có màu tím |
|
Z |
Dung dịch AgNO3 trong môi trường NH3 đun nóng |
Kết tủa Ag trắng sáng |
|
T |
Nước Br2 |
Kết tủa trắng |
Dung dịch X, Y, Z, T lần lượt là
-
A.
Lòng trắng trứng, hồ tinh bột, glucose, aniline.
-
B.
Hồ tinh bột, aniline, lòng trắng trứng, glucose.
-
C.
Hồ tinh bột, lòng trắng trứng, glucose, aniline.
-
D.
Hồ tinh bột; lòng trắng trứng; aniline; glucose.
Cho phương trình hóa học của phản ứng: 2Cr + 3Sn2+ → 2Cr3+ + 3Sn.
Nhận xét nào sau đây về phản ứng trên là đúng?
-
A.
Sn2+ là chất khử, Cr3+ là chất oxi hóa.
-
B.
Sn2+ là chất khử, Cr3+ là chất oxi hóa.
-
C.
Cr là chất khử, Sn2+ là chất oxi hóa.
-
D.
Cr3+ là chất khử, Sn2+ là chất oxi hóa.
Trong công nghiệp, phương pháp điện phân dung dịch được sử dụng để sản xuất một lượng đáng kể kim loại nào sau đây?
-
A.
Zn.
-
B.
Al.
-
C.
Fe.
-
D.
Mg.
Xét quá trình hoạt động của một pin điện hoá Cu – Ag được thiết lập ở các điều kiện như hình vẽ bên. Cho thế điện cực chuẩn của các cặp Cu2+/Cu và Ag+/Ag lần lượt là +0,340 V vả +0,799 V.
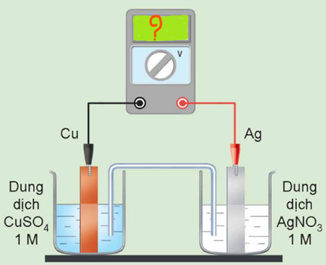
a. Giá trị sức điện động chuẩn của pin điện hoá trên là 0,459 V.
b. Ở anode xảy ra quá trình oxi hoá Cu, ở cathode xảy ra quá trình khử Ag+.
c. Điện cực Cu tăng khối lượng, điện cực Ag giảm khối lượng.
d. Phản ứng hoá học xảy ra trong pin: Cu + 2Ag+ --> Cu2+ + 2Ag.
Theo Tiêu chuẩn Việt Nam TCVN 7624: 2007, khi chế tạo gương, chiều dày lớp bạc phủ trên bề mặt tấm kính (quy ra tổng lượng bạc trên một đơn vị m kính) phải đạt tối thiểu 0,7g/m2. Một công ty cần sản xuất 20 000 m2 gương có độ dày lớp bạc phủ ở mức 0,75g/m2. Để tạo ra bạc, người ta tiến hành theo sơ đồ phản ứng như sau:
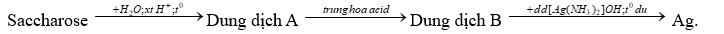
Biết hiệu suất cả quá trình là 80%.
a. Trong dung dịch A gồm có hai monosaccharide.
b. Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c. Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d. Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
Poly(butylene terephthalate) (PBT) là một polymer kị nước được sử dụng rộng rãi trong hệ thống đánh lửa của động cơ ô tô. Polymer này có công thức cấu tạo như sau:
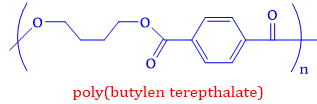
a. PBT hầu như không tan trong nước, có khả năng chống chịu tốt khi tiếp xúc với nhiệt trong thời gian dài và nhiệt độ ngắn hạn.
c. PBT thuộc loại polyester được điều chế từ phản ứng trùng ngưng các monomer tương ứng.
d. Phần trăm khối lượng nguyên tố carbon trong một mắt xích của PBT chưa đến 65%.
Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
|
Lần chuẩn độ |
1 |
2 |
3 |
|
Thể tích dung dịch KMnO4 (mL) |
16,0 |
16,1 |
16,0 |
a. Dung dịch H2SO4 được thêm vào dung dịch chuẩn độ để tạo thành môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
b. Có thể thay dung dịch H2SO4 bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
c. Trong mỗi lần chuẩn độ, dung dịch KMnO4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO4 cuối cùng nhỏ vào dung dịch Y không mất màu.
d. Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87 độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị gần nhất với 98,45.
Tiến hành các thí nghiệm sau:
(1) Điện phân MgCl2 nóng chảy.
(2) Cho CO qua Fe2O3 đun nóng
(3) Nhiệt phân hoàn toàn CaCO3.
(4) Cho kim loại Na vào dung dịch CuSO4 dư.
(5) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, các thí nghiệm thu được kim loại được sắp xếp theo trình tự từ nhỏ đến lớn là bao nhiêu?
Thủy phân 129,76 gam saccharose thu được dung dịch X, sau đó cho X tác dụng với AgNO3 trong NH3 dư. Toàn bộ lượng bạc thu được đem tráng một loại gương soi có diện tích bề mặt là 104 cm2 với độ dày lớp bạc được tráng lên là 10-5 cm. Biết hiệu suất phản ứng thủy phân và tráng bạc lần lượt là 80% và 75%, khối lượng riêng của bạc là 10,49 g/cm3. Số gương soi tối đa được tráng bạc là bao nhiêu?
Đáp án:
Cho các chất: saccharose, glucose, fructose, ethyl formate, formic acid và acetic aldehyde. Trong các chất trên, số chất vừa có khả năng tham gia phản ứng tráng bạc vừa có khả năng phản ứng với Cu(OH)2 ở điều kiện thường là
Đáp án:
Cho các chất sau:
H2N-CH2-CO-NH-CH(CH3)-COOH (1)
H2N-CH(CH2-C6H5)-CO-NH-CH2-COOH (2)
H2N-CH2-CH2-CO-NH-CH2-COOOH (3)
H2N-CH2-COOH (4)
H2N-CH(CH3)-CO-NH-CH2-COOH (5)
H2N-CH2-CO-NH-CH2-COOH (6)
Số chất thuộc peptide là bao nhiêu?
Đáp án:
Một nhà máy sản xuất tấm nhựa dẻo trải bàn cần sản xuất tấm nhựa PVC hình chữ nhật có kích thước là 90cm x 120cm, bề dày của tấm nhựa dẻo là 2mm. Biết hiệu suất phản ứng trùng hợp vinylchloride để điều chế PVC là 60%, quá trình chuyển PVC thành tấm nhựa dẻo có hiệu suất là 95% và biết khối lượng riêng của nhựa PVC là 1,45 g/cm3. Tính khối lượng nguyên liệu vinylchloride (tấn) dùng để sản xuất đơn hàng 5.000 tấm nhựa dẻo trải bàn trên?
(Làm tròn kết quả đến hàng phần chục).
Đáp án:
Một công ty sản xuất thép với công nghệ là lò luyện thép Martin (phản ứng luyện thép trong lò là: FexOy + C ---> Fe + CO2). Nguyên liệu công ty trên sử dụng để luyện thép gồm sắt phế liệu (chứa 50% Fe3O4; 49% Fe; 1% C theo khối lượng) và gang (với 4% khối lượng C). Với giá thành nguyên liệu và chi phí (nhân công, điện, hao mòn thiết bị) cho theo bảng sau:
|
|
Sắt phế liệu |
Gang (4% C) |
Thép thành phẩm (1% C) |
Chi phí/1kg thép |
|
Giá (vnđ/1kg) |
8000 |
13000 |
16000 |
1600 |
Một mẻ luyện thép vừa đủ cần 5 tấn gang và m tấn sắt phế liệu. Số tiền công ty lãi là x triệu. Tính x?(Kết quả chỉ lấy phần nguyên)
Đáp án:
Lời giải và đáp án
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
-
A.
W.
-
B.
Cr.
-
C.
Hg.
-
D.
Pb.
Đáp án : C
Dựa vào ứng dụng của kim loại.
Hg là kim loại ở thể lỏng được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác.
Đáp án C
Trong các mẫu nước cứng sau đây, nước cứng tạm thời là
-
A.
dung dịch Ca(HCO3)2
-
B.
dung dịch MgSO4
-
C.
dung dịch CaCl2
-
D.
dung dịch Mg(NO3)2
Đáp án : A
Dựa vào phân loại nước cứng.
Nước cứng tạm thời chứa ion Ca2+, Mg2+ và HCO3-
Đáp án A
Polymer nào sau đây có chứa nguyên tố chlorine?
-
A.
Poly(methyl methacrylate).
-
B.
Polyethylene.
-
C.
Polybutadien.
-
D.
Poly(vinyl chloride).
Đáp án : D
Dựa vào thành phần của polymer.
Poly(vinyl chloride) chứa nguyên tố chlorine.
Đáp án D
Duralumin là hợp kim của nhôm có thành phần chính là
-
A.
nhôm và đồng.
-
B.
nhôm và sắt.
-
C.
nhôm và carbon.
-
D.
nhôm và thuỷ ngân.
Đáp án : D
Dựa vào thành phần của hợp kim.
Duralumin là hợp kim của nhôm có thành phần chính là nhôm và đồng.
Đáp án D
-
A.
Các ion Na+ và ion Cl– góp chung cặp electron hình thành liên kết.
-
B.
Các nguyên tử Na và Cl góp chung cặp e hình thành liên kết.
-
C.
Các nguyên tử Na và Cl hút nhau bằng lực hút tĩnh điện.
-
D.
Các ion ion Na+ và ion Cl – hút nhau bằng lực hút tĩnh điện.
Đáp án : D
Dựa vào cấu trúc tinh thể NaCl.
A, B, C sai, liên kết trong tinh thể NaCl là liên kết ion.
D đúng.
Đáp án D
Thực hiện bốn phản ứng hoá học theo sơ đồ:
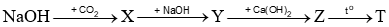
Biết X, Y, Z, T là các hợp chất của kim loại. Công thức hoá học của T là
-
A.
NaOH.
-
B.
CaCO3.
-
C.
Na2CO3.
-
D.
CaO.
Đáp án : D
Dựa vào tính chất hoá học của hợp chất IIA, IA.
X là NaHCO3; Y là Na2CO3, Z là CaCO3, T là CaO
Hợp chất X có công thức C8H14O4. Từ X thực hiện các phản ứng (theo đúng tỉ lệ mol):
(a) X + 2NaOH → X1 + X2 + H2O
(b) X1 + H2SO4 → X3 + Na2SO4
(c) nX3 + nX4 → nylon-6,6 + 2nH2O
(d) 2X2 + X3 → X5 + 2H2O
Phân tử khối của X5 là
-
A.
174.
-
B.
216.
-
C.
202.
-
D.
198.
Đáp án : C
Dựa vào tính chất hoá học của ester.
Từ (b) ⇒ X3 là acid tạo nylon – 6,6 ⇒ X3 là C4H8(COOH)2 ; X1 : C4H8(COONa)2
X có CT C8H14O4 tạo X1 ⇒ X: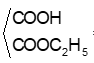 ⇒ X2: C2H5OH ⇒X5:
⇒ X2: C2H5OH ⇒X5: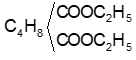 = 202
= 202
Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện theo sơ đồ phản ứng: H2S + SO2 → S + H2O.
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1 000 m3 khí thiên nhiên (đkc) (chứa 5 mg H2S/m3) là
-
A.
10,0 g.
-
B.
5,0 g.
-
C.
7,06 g.
-
D.
100,0 g.
Đáp án : C
Tính khối lượng H2S có trong khí thiên nhiên.
\(\begin{array}{l}2{H_2}S\;\;\; + \;\;\;S{O_2}\;\;\; \to \;\;\;3S\;\;\; + \;\;\;2{H_2}O\\\frac{{1\;000.0,005}}{{34}}.3\; = \;\frac{m}{{32}}.2\; \Leftrightarrow \;m\; = \;7,06\;gam\end{array}\)
Trên phổ hồng ngoại của hợp chất hữu cơ X chỉ có hấp thụ đặc trưng ở 1715 cm-1. Chất X có thể là chất nào trong các chất dưới đây?
-
A.
CH3COCH3.
-
B.
CH3CH2OH.
-
C.
CH3CH2CHO.
-
D.
C6H5CH2OH.
Đáp án : A
Dựa vào đặc trưng tín hiệu của nhóm chức.
Vì hợp chất X có tín hiệu đặc trưng ở 1715 cm-1 nên X có thể chứa nhóm chức – CO –
Đáp án A
Tên gọi của ester CH3COOC2H5 là
-
A.
Ethyl formate.
-
B.
Ethyl acetate.
-
C.
Methyl acetate.
-
D.
Methyl formate.
Đáp án : B
Dựa vào cách gọi tên của ester.
CH3COOC2H5 có tên là ethyl acetate.
Đáp án B
Cho dãy các chất: H2, H2NCH2COOH, C6H5NH2, C2H5NH2, CH3COOH. Số chất trong dãy phản ứng với NaOH trong dung dịch là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Đáp án : A
Các chất có nhóm – COOH có phản ứng với NaOH.
H2NCH2COOH, CH3COOH có phản ứng với dung dịch NaOH.
Đáp án A
Ở điều kiện thường, chất nào sau đây dễ tan trong nước?
-
A.
Tristearin.
-
B.
Cellulose.
-
C.
Glucose.
-
D.
Tinh bột.
Đáp án : C
Dựa vào tính chất vật lí của polysaccharide.
Ở điều kiện thường, glucose dễ tan trong nước.
Đáp án C
Ở điều kiện thích hợp (nhiệt độ, áp suất, chất xúc tác), benzene tác dụng được với tất cả các chất trong dãy nào dưới đây?
-
A.
HCl, HNO3, Cl2, H2.
-
B.
HNO3, H2, Cl2, H2O.
-
C.
HNO3, Cl2, KMnO4, Br2.
-
D.
HNO3, H2, Cl2, O2.
Đáp án : D
Dựa vào tính chất hoá học của benzene.
A loại HCl; B loại H2O; C loại KMnO4
Đáp án D
Công thức nào sau đây có thể là công thức của chất béo?
-
A.
CH3COOCH2C6H5.
-
B.
C15H31COOCH3.
-
C.
(C17H33COO)2C2H4.
-
D.
(C17H35COO)3C3H5.
Đáp án : D
Dựa vào cấu tạo của chất béo.
(C17H35COO)3C3H5 là công thức của chất béo.
Đáp án D
Chất nào sau đây là amine bậc 2?
-
A.
H2N-CH2-NH2.
-
B.
(CH3)2CH-NH2.
-
C.
CH3-NH-CH2C(CH3)2
-
D.
(CH3)3N.
Đáp án : C
Amine bậc 2 có dạng RNHR.
CH3-NH-CH2C(CH3)2 là amine bậc 2.
Đáp án C
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với các thuốc thử được ghi lại dưới bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Dung dịch I2 |
Có màu xanh tím |
|
Y |
Cu(OH)2 trong môi trường kiềm |
Có màu tím |
|
Z |
Dung dịch AgNO3 trong môi trường NH3 đun nóng |
Kết tủa Ag trắng sáng |
|
T |
Nước Br2 |
Kết tủa trắng |
Dung dịch X, Y, Z, T lần lượt là
-
A.
Lòng trắng trứng, hồ tinh bột, glucose, aniline.
-
B.
Hồ tinh bột, aniline, lòng trắng trứng, glucose.
-
C.
Hồ tinh bột, lòng trắng trứng, glucose, aniline.
-
D.
Hồ tinh bột; lòng trắng trứng; aniline; glucose.
Đáp án : C
Dựa vào hiện tượng phản ứng với các thuốc thử đặc trưng.
T tạo kết tủa trắng với nước bromine ⇒ loại B, D
X phản ứng màu với I2 ⇒ X là hồ tinh bột ⇒ Chọn C
Cho phương trình hóa học của phản ứng: 2Cr + 3Sn2+ → 2Cr3+ + 3Sn.
Nhận xét nào sau đây về phản ứng trên là đúng?
-
A.
Sn2+ là chất khử, Cr3+ là chất oxi hóa.
-
B.
Sn2+ là chất khử, Cr3+ là chất oxi hóa.
-
C.
Cr là chất khử, Sn2+ là chất oxi hóa.
-
D.
Cr3+ là chất khử, Sn2+ là chất oxi hóa.
Đáp án : C
Dựa vào sự thay đổi số oxi hoá của phản ứng.
Cr là chất khử, Sn2+ là chất oxi hóa
Đáp án C
Trong công nghiệp, phương pháp điện phân dung dịch được sử dụng để sản xuất một lượng đáng kể kim loại nào sau đây?
-
A.
Zn.
-
B.
Al.
-
C.
Fe.
-
D.
Mg.
Đáp án : A
Phương pháp điện phân dung dịch để điều chế kim loại trung bình, yếu.
Zn là kim loại trung bình nên được điều chế bằng phương pháp điện phân dung dịch.
Đáp án A
Xét quá trình hoạt động của một pin điện hoá Cu – Ag được thiết lập ở các điều kiện như hình vẽ bên. Cho thế điện cực chuẩn của các cặp Cu2+/Cu và Ag+/Ag lần lượt là +0,340 V vả +0,799 V.

a. Giá trị sức điện động chuẩn của pin điện hoá trên là 0,459 V.
b. Ở anode xảy ra quá trình oxi hoá Cu, ở cathode xảy ra quá trình khử Ag+.
c. Điện cực Cu tăng khối lượng, điện cực Ag giảm khối lượng.
d. Phản ứng hoá học xảy ra trong pin: Cu + 2Ag+ --> Cu2+ + 2Ag.
a. Giá trị sức điện động chuẩn của pin điện hoá trên là 0,459 V.
b. Ở anode xảy ra quá trình oxi hoá Cu, ở cathode xảy ra quá trình khử Ag+.
c. Điện cực Cu tăng khối lượng, điện cực Ag giảm khối lượng.
d. Phản ứng hoá học xảy ra trong pin: Cu + 2Ag+ --> Cu2+ + 2Ag.
Dựa vào nguyên tắc hoạt động của pin.
a. Đúng.
b. Đúng.
c. Sai vì điện cực Cu giảm khối lượng, điện cực Ag tăng khối lượng.
d. Đúng.
Theo Tiêu chuẩn Việt Nam TCVN 7624: 2007, khi chế tạo gương, chiều dày lớp bạc phủ trên bề mặt tấm kính (quy ra tổng lượng bạc trên một đơn vị m kính) phải đạt tối thiểu 0,7g/m2. Một công ty cần sản xuất 20 000 m2 gương có độ dày lớp bạc phủ ở mức 0,75g/m2. Để tạo ra bạc, người ta tiến hành theo sơ đồ phản ứng như sau:
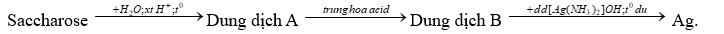
Biết hiệu suất cả quá trình là 80%.
a. Trong dung dịch A gồm có hai monosaccharide.
b. Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c. Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d. Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
a. Trong dung dịch A gồm có hai monosaccharide.
b. Trong quá trình thủy phân saccharose có thể thay xúc tác acid bằng xúc tác base.
c. Lượng bạc được tráng lên 20 000 m2 gương với độ dày lớp bạc phủ ở mức 0,75 g/m2 là 15 kg.
d. Công ty yêu cầu dùng 15 kg saccharose là đảm bảo để sản xuất lượng gương với độ phủ bạc như trên.
Dựa vào quy trình sản xuất tráng bạc.
a) đúng A gồm glucose và fructose
b) sai không thể thay được xúc tác acid bằng base.
c) đúng. mAg = 0,75*20 000 = 15000 gam = 15 kg
d) đúng. msaccharose = \(\frac{{15*342}}{{432}}*\frac{{100}}{{80}}\)= 14,84 kg
Poly(butylene terephthalate) (PBT) là một polymer kị nước được sử dụng rộng rãi trong hệ thống đánh lửa của động cơ ô tô. Polymer này có công thức cấu tạo như sau:

a. PBT hầu như không tan trong nước, có khả năng chống chịu tốt khi tiếp xúc với nhiệt trong thời gian dài và nhiệt độ ngắn hạn.
c. PBT thuộc loại polyester được điều chế từ phản ứng trùng ngưng các monomer tương ứng.
d. Phần trăm khối lượng nguyên tố carbon trong một mắt xích của PBT chưa đến 65%.
a. PBT hầu như không tan trong nước, có khả năng chống chịu tốt khi tiếp xúc với nhiệt trong thời gian dài và nhiệt độ ngắn hạn.
c. PBT thuộc loại polyester được điều chế từ phản ứng trùng ngưng các monomer tương ứng.
d. Phần trăm khối lượng nguyên tố carbon trong một mắt xích của PBT chưa đến 65%.
a. Đúng vì PBT là polymer kị nước nên hầu như không tan trong nước, có khả năng chống chịu tốt khi tiếp xúc với nhiệt trong thời gian dài và nhiệt độ ngắn hạn nên có thể coi như là một chất chống cháy bởi vì vật liệu đạt được chỉ số nhiệt độ cao và nhiệt độ lệch nhiệt cao.
b. Sai vì hai monomer dùng để điều chế PBT là p-HOOC-C6H4-COOH (-C6H4- chứa vòng benzene) và HO-[CH2]4-OH.
c. Đúng.
d. Sai vì polymer PBT có công thức (C12H12O4)n nên phần trăm khối lượng carbon trong một mắt xích = 12.12/220 = 65,45% > 65%.
Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
|
Lần chuẩn độ |
1 |
2 |
3 |
|
Thể tích dung dịch KMnO4 (mL) |
16,0 |
16,1 |
16,0 |
a. Dung dịch H2SO4 được thêm vào dung dịch chuẩn độ để tạo thành môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
b. Có thể thay dung dịch H2SO4 bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
c. Trong mỗi lần chuẩn độ, dung dịch KMnO4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO4 cuối cùng nhỏ vào dung dịch Y không mất màu.
d. Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87 độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị gần nhất với 98,45.
a. Dung dịch H2SO4 được thêm vào dung dịch chuẩn độ để tạo thành môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành Mn2+.
b. Có thể thay dung dịch H2SO4 bằng dung dịch acid mạnh như HCl, HNO3 nhưng phải đảm bảo lượng H+ dư sau phản ứng.
c. Trong mỗi lần chuẩn độ, dung dịch KMnO4 được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch KMnO4 cuối cùng nhỏ vào dung dịch Y không mất màu.
d. Theo kết quả chuẩn độ ở trên, trong số các giá trị: 93,32; 98,45; 97,36; 99,87 độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị gần nhất với 98,45.
a. Đúng \(MnO_4^ - \)bị khử thành Mn2+ (không màu) trong môi trường acid giúp người chuẩn độ nhận biết điểm dừng.
b. Sai, nếu thay bằng HCl thì Cl- khử \(MnO_4^ - /{H^ + }\) nếu thay bằng HNO3 thì \(NO_3^ - /{H^ + }\)oxi hóa Fe2+ làm ảnh hưởng đến kết quả chuẩn độ.
c. Đúng, giọt dung dịch KMnO4 cuối cùng không bị mất màu chứng tỏ Fe2+ trong dung dịch đã hết.
d. Sai, độ tinh khiết gần nhất với 99,87%.
\({V_{tb}} = \frac{{16 + 16,1 + 16}}{3} = 10,0333mL \to {n_{KMnO4}} = 3,{6877.10^{ - 4}}mol\)
Phản ứng chuẩn độ:
5Fe2+ + 8H+ \( + MnO_4^ - \)→5Fe3+ + Mn2+ + 4H2O
=> nFe2+ = \(5.{n_{Mn{O_4} - }}\)= 1,8439.10-3
=> %(NH4)2Fe(SO4)2.6H2O = (10.1,8439.10-3.392): 7,237 = 99,8769%
Tiến hành các thí nghiệm sau:
(1) Điện phân MgCl2 nóng chảy.
(2) Cho CO qua Fe2O3 đun nóng
(3) Nhiệt phân hoàn toàn CaCO3.
(4) Cho kim loại Na vào dung dịch CuSO4 dư.
(5) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, các thí nghiệm thu được kim loại được sắp xếp theo trình tự từ nhỏ đến lớn là bao nhiêu?
Dựa vào tính chất hoá học của kim loại

Thủy phân 129,76 gam saccharose thu được dung dịch X, sau đó cho X tác dụng với AgNO3 trong NH3 dư. Toàn bộ lượng bạc thu được đem tráng một loại gương soi có diện tích bề mặt là 104 cm2 với độ dày lớp bạc được tráng lên là 10-5 cm. Biết hiệu suất phản ứng thủy phân và tráng bạc lần lượt là 80% và 75%, khối lượng riêng của bạc là 10,49 g/cm3. Số gương soi tối đa được tráng bạc là bao nhiêu?
Đáp án:
Đáp án:
mAg = 108.4. \(\frac{{129,76}}{{342}}\).75%%.80% = 98,34442 gam
mAg (1 gương) = 104.10-5.10,49 = 1,049 gam \( \Rightarrow \) Số gương soi = \(\frac{{98,34442}}{{1,049}}\)= 93,75 cái.
Đáp số: 93
Cho các chất: saccharose, glucose, fructose, ethyl formate, formic acid và acetic aldehyde. Trong các chất trên, số chất vừa có khả năng tham gia phản ứng tráng bạc vừa có khả năng phản ứng với Cu(OH)2 ở điều kiện thường là
Đáp án:
Đáp án:
Dựa vào tính chất hoá học của glucose.
Đáp số: 3 (glucose, fructose, formic acid).
Cho các chất sau:
H2N-CH2-CO-NH-CH(CH3)-COOH (1)
H2N-CH(CH2-C6H5)-CO-NH-CH2-COOH (2)
H2N-CH2-CH2-CO-NH-CH2-COOOH (3)
H2N-CH2-COOH (4)
H2N-CH(CH3)-CO-NH-CH2-COOH (5)
H2N-CH2-CO-NH-CH2-COOH (6)
Số chất thuộc peptide là bao nhiêu?
Đáp án:
Đáp án:
Các chất thuộc loại peptide bao gồm: (1), (2), (5) và (6).
(3) không phải peptide vì amino acic đầu N không phải là α-amino acid
(4) là amino acid
Đáp án. 4
Một nhà máy sản xuất tấm nhựa dẻo trải bàn cần sản xuất tấm nhựa PVC hình chữ nhật có kích thước là 90cm x 120cm, bề dày của tấm nhựa dẻo là 2mm. Biết hiệu suất phản ứng trùng hợp vinylchloride để điều chế PVC là 60%, quá trình chuyển PVC thành tấm nhựa dẻo có hiệu suất là 95% và biết khối lượng riêng của nhựa PVC là 1,45 g/cm3. Tính khối lượng nguyên liệu vinylchloride (tấn) dùng để sản xuất đơn hàng 5.000 tấm nhựa dẻo trải bàn trên?
(Làm tròn kết quả đến hàng phần chục).
Đáp án:
Đáp án:
Diện tích của 1 tấm nhựa là: 90x120 = 10800 (cm2)
Thể tích của tấm nhựa là: 10800x0,2 = 2160 (cm3)
=> khối lượng PVC của 1 tấm nhựa = 2160 (cm3) x 1,45 (g/cm3) = 3132 (gam)
=> khối lượng 5.000 tấm nhựa = 3132 x 5.000 = 15.660.000 (gam) = 15,66 tấn
Gọi khối lượng vinylchloride cần lấy là m (tấn)
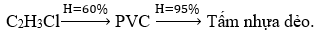
=> m.60%.95% = 15,66
=> m = 27,4736 tấn
Đáp số: 27,5
Một công ty sản xuất thép với công nghệ là lò luyện thép Martin (phản ứng luyện thép trong lò là: FexOy + C ---> Fe + CO2). Nguyên liệu công ty trên sử dụng để luyện thép gồm sắt phế liệu (chứa 50% Fe3O4; 49% Fe; 1% C theo khối lượng) và gang (với 4% khối lượng C). Với giá thành nguyên liệu và chi phí (nhân công, điện, hao mòn thiết bị) cho theo bảng sau:
|
|
Sắt phế liệu |
Gang (4% C) |
Thép thành phẩm (1% C) |
Chi phí/1kg thép |
|
Giá (vnđ/1kg) |
8000 |
13000 |
16000 |
1600 |
Một mẻ luyện thép vừa đủ cần 5 tấn gang và m tấn sắt phế liệu. Số tiền công ty lãi là x triệu. Tính x?(Kết quả chỉ lấy phần nguyên)
Đáp án:
Đáp án:
Trong 5 tấn gang chứa \(\left\{ \begin{array}{l}{m_{Fe}} = 4,8\\{m_C} = 0,2\end{array} \right.\) và trong m tấn sắt phế liệu chứa \(\left\{ \begin{array}{l}{m_{F{e_3}{O_4}}} = 0,5m\\{m_{Fe}} = 0,49m\\{m_C} = 0,01m\end{array} \right.\)
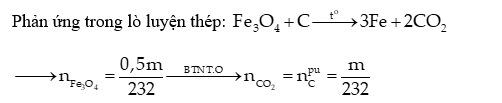
Thép thành phẩm chứa \(\left\{ \begin{array}{l}{m_{Fe}} = 4,8 + 0,49m + \frac{{0,5m}}{{232}}.3.56\\{m_C} = 0,2 + 0,01m - \frac{m}{{232}}.12\end{array} \right. \to \frac{{{m_C}}}{{{m_{Fe}}}} = \frac{1}{{99}} \to m \approx 3\) (tấn)
→ Khối lượng của thép = 7,43 (tấn)
→ Số tiền lãi \( = 7,43.1000.16000 - (3.1000.8000 + 5.1000.13000 + 7,43.1000.1600) = 17.992.000\) (triệu) = 17,99 triệu
Quá trình tạo thành ion Ca2+ nào sau đây là đúng?
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Be (Z = 4) là
Phần I. Trắc nghiệm nhiều đáp án lựa chọn
Kim loại cứng nhất, thường được pha vào thép để tăng độ cứng và khả năng chống gỉ cho thép là
Trong ăn mòn hóa học, phản ứng hóa học xảy ra là loại phản ứng nào sau đây?
Hợp chất nào sau đây là ester ?
Khi thay thế nhóm …(1) ở nhóm …(2) của carboxylic acid bằng nhóm
Phức chất đơn giản thường có một
Cho phản ứng oxi hóa – khử:
Các bài khác cùng chuyên mục









Danh sách bình luận