50 câu hỏi lý thuyết mức độ nhận biết về kim loại kiềm thổ và hợp chất có lời giải
Làm đề thiCâu hỏi 1 :
Chất nào sau đây không bị phân huỷ khi nung nóng ?
- A Mg(NO3)2
- B CaCO3
- C CaSO4
- D Mg(OH)2
Đáp án: C
Lời giải chi tiết:
2Mg(NO3)2 → 4NO2 + 4O2 + 2MgO
CaCO3 → CaO + CO2
Mg(OH)2 → MgO + H2O
Đáp án C
Câu hỏi 2 :
Điều chế kim loại Mg bằng cách điện phân MgCl2 nóng chảy, quá trình nào xảy ra ở catot (cực âm) ?
- A Mg → Mg2+ + 2e
- B Mg2+ + 2e→ Mg
- C 2Cl- → Cl2 + 2e
- D Cl2 + 2e → 2Cl-
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 3 :
Xếp các kim loại kiềm thổ theo chiều tăng dần của điện tích hạt nhân, thì
- A bán kính nguyên tử giảm dần
- B năng lượng ion hoá giảm dần
- C tính khử giảm dần
- D khả năng tác dụng với nước giảm dần
Đáp án: B
Lời giải chi tiết:
A. Bán kính nguyên tử tăng
C. Tính khử tăng
D. Tính bazo tăng => khả năng tác dụng với nước tăng
Đáp án B
Câu hỏi 4 :
Cách nào sau đây thường được dùng để điều chế kim loại Ca ?
- A Điện phân dung dịch CaCl2 có màng ngăn
- B Điện phân CaCl2 nóng chảy
- C Dùng Ba để đẩy Ca ra khỏi dung dịch CaCl2
- D Dùng Al để khử CaO ở nhiệt độ cao
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 5 :
Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
- A thạch cao khan.
- B thạch cao sống.
- C đá vôi.
- D thạch cao nung.
Đáp án: B
Lời giải chi tiết:
+ CaSO4.2H2O : thạch cao sống
+ CaSO4.H2O hoặc CaSO4.0,5H2O : thạch cao nung
+ CaSO4: thạch cao khan
Đáp án B
Câu hỏi 6 :
Canxi cacbonat (CaCO3) phản ứng được với dung dịch
- A KNO3.
- B HCl.
- C NaNO3.
- D KCl.
Đáp án: B
Lời giải chi tiết:
2HCl + CaCO3 → CaCl2 + H2O + CO2
Đáp án B
Câu hỏi 7 :
Thực hiện các thí nghiệm sau:
1. Cho dung dịch NaCl vào dung dịch Ba(OH)2.
2. Cho dung dịch Na2CO3 vào dung dịch Ca(OH)2.
3. Điện phân dung dịch NaCl với điện cực trơ, có màng ngăn.
4. Cho Cu(OH)2 vào dung dịch Na2SO4.
5. Cho từ từ dung dịch HCl vào dung dịch Na2CO3.
Số thí nghiệm đều tạo ra được NaOH là:
- A 3
- B 4
- C 1
- D 2
Đáp án: D
Lời giải chi tiết:
Các thí nghiệm : 2 ; 3
Đáp án D
Câu hỏi 8 :
Có thể dùng CaO mới nung để làm khô các chất khí
- A NH3, SO2, CO, Cl2.
- B N2, NO2, CO2, CH4, H2.
- C NH3, O2, N2, H2, C2H4.
- D N2, Cl2, O2 , H2.
Đáp án: C
Lời giải chi tiết:
Nguyên tắc làm khô là chất làm khô không phản ứng với chất được làm khô
Đáp án C
Câu hỏi 9 :
Thạch cao nung được dùng để đúc tượng, bó bột khi gãy xương. Công thức phân tử của thạch cao nung là
- A CaSO4.2H2O.
- B CaSO4.5H2O.
- C CaSO4.H2O.
- D CaSO4.
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 10 :
Trước khi thi đấu các môn thể thao, các vận động viên thường xoa một ít chất X dưới dạng bột màu trắng làm tăng ma sát và hút ẩm. X là
- A MgCO3
- B CaOCl2
- C CaO
- D Tinh bột
Đáp án: A
Câu hỏi 11 :
Trong số các phương pháp làm mềm nước cứng, phương pháp nào chỉ khử được nước cứng tạm thời :
- A Phương pháp cất nước
- B Phương pháp trao đổi ion
- C Phương pháp hóa học
- D Phương pháp đun sôi nước
Đáp án: D
Lời giải chi tiết:
Đáp án D
Câu hỏi 12 :
Dung dịch nào sau đây tác dụng với dung dịch Ba(HCO3)2, vừa thu được kết tủa, vừa có khí thoát ra?
- A Ca(OH)2
- B NaOH
- C H2SO4
- D HCl
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 13 :
Nhỏ dung dịch Ba(OH)2 vào dung dịch nào sau đây không có hiện tượng hóa học xảy ra?
- A Dung dịch Na2CrO4.
- B Dung dịch AlCl3.
- C Dung dịch NaAlO2.
- D Dung dịch NaHCO3.
Đáp án: C
Lời giải chi tiết:
A. Ba(OH)2 + Na2CrO4 → 2KOH + BaCrO4↓ => hiện tượng: xuất hiện kết tủa trắng
B. 3Ba(OH)2 + 2AlCl3 → 2Al(OH)3↓ + 3BaCl2
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
=> hiện tương: xuất hiện kết tủa trắng keo, sau đó kết tủa tan dần
C. không có hiện tượng
D. Ba(OH)2 + 2NaHCO3 → Na2CO3 + BaCO3↓ + 2H2O => hiện tượng: xuất hiện kết tủa trắng
Đáp án C
Câu hỏi 14 :
Canxi hiđroxit còn gọi là vôi tôi có công thức hóa học là
- A Ca(OH)2.
- B Ca(HCO3)2.
- C CaCO3.
- D CaO.
Đáp án: A
Lời giải chi tiết:
A. Vôi tôi
B. Canxi hidrocacbonat
C. đá vôi
D. vôi sống
Đáp án A
Câu hỏi 15 :
Muối (NH4)2CO3 không tạo kết tủa khi phản ứng với dung dịch của hóa chất nào sau đây ?
- A Ca(OH)2
- B MgCl2
- C FeSO4
- D NaOH
Đáp án: D
Lời giải chi tiết:
Đáp án D
Câu hỏi 16 :
Nguyên nhân chính khiến cho tính chất vật lí của các kim loại kiềm thổ không biến đổi theo một quy luật nhất định là các kim loại kiềm thổ:
- A có bán kính nguyên tử lớn
- B có ít electron hóa trị
- C có điện tích hạt nhân nhỏ
- D có kiểu mạng tinh thể không giống nhau
Đáp án: D
Phương pháp giải:
Be, Mg có kiểu mạng lục phương; Ca, Sr có kiểu mạng tinh thể lập phương tâm diện; còn Ba có kiểu mạng tinh thể lập phương tâm khối.
Lời giải chi tiết:
Be, Mg có kiểu mạng lục phương; Ca, Sr có kiểu mạng tinh thể lập phương tâm diện; còn Ba có kiểu mạng tinh thể lập phương tâm khối.
Do có kiểu mạng tinh thể không giống nhau như vậy nên tính chất vật lí của các kim loại kiềm thổ không biến đổi theo một quy luật nhất định.
Đáp án D
Câu hỏi 17 :
Nhận xét nào sau đây không đúng?
- A Các kim loại kiềm thổ có tính khử mạnh
- B Tính khử của các kim loại kiềm thổ tăng dần từ Be đến Ba
- C Tính khử của các kim loại kiềm thổ yếu hơn kim loại kiềm trong cùng chu kì
- D Be, Mg, Ca, Sr, Ba đều phản ứng với nước ở nhiệt độ thường nên gọi là kim loại kiềm thổ
Đáp án: D
Phương pháp giải:
Ghi nhớ: Be, Mg không phản ứng với nước ở nhiệt độ thường.
Lời giải chi tiết:
D sai vì trong nhóm các kim loại kiềm thổ chỉ có Ca, Sr, Ba phản ứng được với nước còn Be và Mg không phản ứng với H2O ở nhiệt độ thường.
R + 2H2O →R(OH)2+ H2↑
Đáp án D
Câu hỏi 18 :
Nguyên tắc chung để điều chế kim loại kiềm thổ là?
- A Điện phân muối halogenua hoặc oxit nóng chảy.
- B Điện phân dung dịch muối halogenua có màng ngăn giữa hai điện cực.
- C Dùng kim loại mạnh hơn để đẩy kim loại yếu hơn ra khỏi dung dịch muối.
- D Điện phân dung dịch muối halogenua không có màng ngăn giữa hai điện cực.
Đáp án: A
Phương pháp giải:
Các kim loại kiềm thổ là các kim loại có tính khử mạnh nên phương pháp điều chế kim loại kiềm thổ là điện phân nóng chảy.
Lời giải chi tiết:
Kim loại kiềm thổ có tính khử mạnh nên dùng phương pháp điện phân muối halogenua nóng chảy.
RCl2 \(\xrightarrow{{dpnc}}\) R +Cl2
Với Mg thường điện phân oxit nóng chảy:
2MgO \(\xrightarrow{{dpnc}}\) 2Mg + O2
Đáp án A
Câu hỏi 19 :
Phản ứng nào sau đây giải thích cho hiện tượng “Nước chảy, đá mòn” :
- A CaCO3 + CO2 + H2O → Ca(HCO3)2
- B Ca(HCO3)2 → CaCO3 + CO2 + H2O
- C CaO + CO2 → CaCO3
- D CaO + H2O → Ca(OH)2
Đáp án: A
Phương pháp giải:
Lý thuyết về tính chất hóa học của hợp chất cacbonat
Lời giải chi tiết:
“Nước chảy, đá mòn” là hiện tượng “ăn mòn” đá vôi dưới tác động của dòng nước có hòa tan CO2 theo phản ứng sau :
CaCO3 + CO2 + H2O → Ca(HCO3)2
(Không tan) (tan)
Đáp án A
Câu hỏi 20 :
Ở nhiệt độ thường, dung dịch Ba(HCO3)2 loãng tác dụng được với dung dịch nào sau đây?
- A NaCl.
- B KCl.
- C Na2CO3.
- D KNO3.
Đáp án: C
Phương pháp giải:
Ba(HCO3)2 là muối axit => tính chất hóa học là: tác dụng được với axit; tác dụng được với dd muối (đk tạo chất kết tủa hoặc bay hơi); dễ bị nhiệt phân hủy
Lời giải chi tiết:
Ba(HCO3)2 tác dụng được với dd Na2CO3
Ba(HCO3)2 + Na2CO3 → BaCO3↓ + 2NaHCO3
Đáp án C
Câu hỏi 21 :
Sự thiếu hụt nguyên tố (ở dạng hợp chất) nào sau đây gây ra bệnh loãng xương?
- A Photpho.
- B Sắt
- C Kẽm.
- D Canxi.
Đáp án: D
Phương pháp giải:
Tính chất của các nguyên tố kim loại.
Lời giải chi tiết:
Sự thiếu hụt nguyên tố Canxi (ở dạng hợp chất) gây ra bệnh loãng xương
Đáp án D
Câu hỏi 22 :
Phân biệt BaCl2 người ta không dùng dung dịch
- A Na2CO3
- B AgNO3.
- C H2SO4.
- D HCl
Đáp án: D
Phương pháp giải:
Tính chất hóa học hợp chất của kim loại kiềm
Lời giải chi tiết:
Không dùng HCl vì HCl không phản ứng với BaCl2 để tạo ra kết tủa (hoặc khí)
Đáp án D
Câu hỏi 23 :
Chất nào sau đây tác dụng với dung dịch Ba(OH)2 tạo ra kết tủa ?
- A NaCl
- B KCl
- C KNO3
- D Ca(HCO3)2
Đáp án: D
Phương pháp giải:
Dựa vào tính chất hóa học của Ba(OH)2
+ làm quỳ tím chuyển sang màu xanh, dd phenolphtalein chuyển sang màu đỏ
+ tác dụng với axit
+ tác dụng với dd muối (đk tạo thành chất kết tủa hoặc bay hơi)
Lời giải chi tiết:
Chất tạo kết tủa với Ba(OH)2 là Ca(HCO3)2
Ba(OH)2 + Ca(HCO3)2 → BaCO3 + CaCO3 + 2H2O
Đáp án D
Câu hỏi 24 :
Chất X là một bazơ mạnh, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất clorua vôi (CaOCl2), vật liệu xây dựng. Ngoài ra chất X còn dùng để xử lí chất thải. Công thức của X là
- A Ca(OH)2.
- B NaOH.
- C Ba(OH)2.
- D KOH.
Đáp án: A
Phương pháp giải:
Ứng dụng các hợp chất của canxi
Lời giải chi tiết:
Ca(OH)2 là một bazơ mạnh, được sử dụng rộng rãi trong nhiều ngành công nghiệp như sản xuất clorua vôi (CaOCl2), vật liệu xây dựng. Ngoài ra chất X còn dùng để xử lí chất thải.
Đáp án A
Câu hỏi 25 :
Công thức chung của oxit kim loại nhóm IIA là:
- A R2O
- B RO2
- C R2O3
- D RO
Đáp án: D
Lời giải chi tiết:
Công thức chung của oxit kim loại nhóm IIA là RO
Đáp án D
Câu hỏi 26 :
Phát biểu nào sau đây là sai ?
- A Có thể dùng lượng dư dung dịch NaOH để làm mềm nước cứng có tính cứng toàn phần
- B NaHCO3 được dùng để pha chế thuốc giảm đau dạ dày do chứng thừa axit
- C NaOH là chất rắn, hút ẩm mạnh, tan nhiều trong nước, khi hòa tan tỏa nhiệt mạnh
- D CaCO3 tan rất ít trong nước, phản ứng với dung dịch HCl giải phóng khí CO2
Đáp án: A
Phương pháp giải:
Phương pháp làm mềm nước cứng:
- Với nước cứng tạm thời:
+ Đun sôi.
+ Thêm Ca(OH)2 vừa đủ.
+ Thêm các dung dịch kiềm khác, dung dịch muối CO32-, dung dịch PO43-.
- Với nước cứng vĩnh cửu:
Thêm các dung dịch muối CO32-, dung dịch PO43-.
Lời giải chi tiết:
A sai. Vì nước cứng toàn phần bao hàm cả nước cứng vĩnh cửu và tạm thời
=> Phải dùng phương pháp có thể làm mềm được cả 2 loại nước cứng. Mà NaOH chỉ làm mềm nước cứng tạm thời => không thỏa mãn
B, C, D đúng
Đáp án A
Câu hỏi 27 :
Ở trạng thái cơ bản, nguyên tử kim loại kiềm thổ có số electron hoá trị là
- A 1e.
- B 2e.
- C 3e.
- D 4e.
Đáp án: B
Phương pháp giải:
Dựa vào lý thuyết về các kim loại kiềm thổ.
Lời giải chi tiết:
Ở trạng thái cơ bản, nguyên tử kim loại kiềm thổ có số electron hóa trị là 2 electron.
Đáp án B
Câu hỏi 28 :
Sục khí nào sau đây vào dung dịch Ca(OH)2 dư thấy xuất hiện kết tủa màu trắng?
- A O2
- B HCl
- C CO2
- D H2
Đáp án: C
Lời giải chi tiết:
Sục CO2 vào dd Ca(OH)2 dư thấy xuất hiện kết tủa trắng do có phản ứng:
CO2 + Ca(OH)2 → CaCO3 ↓ trắng + H2O
Đáp án C
Câu hỏi 29 :
Thuốc Trimafort có chứa Aluminium Hydroxide Gel, Magnesium Hydroxide và Simethicon, có tác dụng điều trị các bệnh lý về dạ dày như đầy hơi, ợ chua, ăn không tiêu, đau bụng, khó chịu ở dạ dày. Công thức hóa học của Magnesium Hydroxide (Magie hiđroxit) là
- A NaHCO3.
- B Al(OH)3.
- C NaCl.
- D Mg(OH)2.
Đáp án: D
Lời giải chi tiết:
CTHH của Magie hiđroxit là Mg(OH)2
Đáp án D
Câu hỏi 30 :
Câu nào sau đây là không đúng?
- A Nước cứng là nước chứa nhiều ion Ca2+, Mg2+.
- B Dùng Na2CO3 (hoặc Na3PO4) để làm mất tính cứng tạm thời và tính cứng vĩnh cửu.
- C Dùng phương pháp trao đổi ion để làm giảm tính cứng tạm thời và tính cứng vĩnh cửu.
- D Đun sôi nước có thể làm mất tính cứng vĩnh cửu.
Đáp án: D
Phương pháp giải:
Dựa vào lý thuyết về nước cứng để chọn phát biểu không đúng.
Lời giải chi tiết:
Phát biểu D không đúng vì nước cứng vĩnh cửu có chứa Ca2+, Mg2+, Cl-, SO42- nên khi đun sôi không thể làm mất tính cứng được.
Đáp án D
Câu hỏi 31 :
Ở nhiệt độ thường, kim loại nào sau đây tan hết trong nước dư?
- A Ba.
- B Al.
- C Fe.
- D Cu.
Đáp án: A
Phương pháp giải:
Các kim loại kiềm và kim loại kiềm thổ (trừ Be, Mg) tan được hết trong nước dư ở đk thường.
Lời giải chi tiết:
Ba tan được hết trong nước dư ở đk thường
PTHH minh họa: Ba + 2H2O → Ba(OH)2 + H2↑
Đáp án A
Câu hỏi 32 :
Các bể đựng nước vôi trong để lâu ngày thường có một lớp màng cứng rất mỏng trên bề mặt, chạm nhẹ tay vào đó, lớp màng sẽ vỡ ra. Thành phần chính của lớp màng cứng này là
- A Ca(OH)2.
- B CaO.
- C CaCO3.
- D CaCl2.
Đáp án: C
Phương pháp giải:
Khi để nước vôi trong tiếp xúc với không khí thì nó sẽ tiếp xúc với các thành phần như O2, N2, CO2… hay gặp trong không khí ⟹ lựa chọn chất để tạo thành kết tủa phù hợp
Lời giải chi tiết:
Do không khí có chứa CO2 nên khi tiếp xúc với dd Ca(OH)2 xảy ra phản ứng:
Ca(OH)2 + CO2 → CaCO3 ↓ + H2O
⟹ CaCO3 là chất rắn tạo lớp màng mỏng phủ phía trên
Đáp án C
Câu hỏi 33 :
Không nên dùng xà phòng để giặt cửa trong nước chứa nhiều ion
- A NH4+.
- B Na+.
- C Cl-.
- D Ca2+.
Đáp án: D
Lời giải chi tiết:
Không nên dùng xà phòng để giặt cửa trong nước chứa nhiều ion Ca2+ vì thành phần chính của xà phòng là muối natri hoặc kali của axit béo, khi phản ứng với ion Ca2+ tạo kết tủa làm mất khả năng giặt rửa của xà phòng:
Minh họa: 2RCOONa + Ca2+ → (RCOO)2Ca ↓ + 2Na+
Đáp án D
Câu hỏi 34 :
Canxi hiđroxit là một bazơ mạnh, lại rẻ tiền nên được sử dụng rộng rãi trong nhiều ngành công nghiệp: sản xuất amoniac (NH3), clorua vôi (CaOCl2), vật liệu xây dựng,… Công thức của canxi hiđroxit là
- A Ca(HCO3)2.
- B CaCO3.
- C Ca(OH)2.
- D CaO.
Đáp án: C
Phương pháp giải:
Xem lại các hợp chất quan trọng của KL kiềm thổ
Lời giải chi tiết:
Công thức của canxi hiđroxit là Ca(OH)2.
Đáp án C
Câu hỏi 35 :
Các bể đựng nước vôi trong để lâu ngày thường có một lớp màng cứng rất mỏng trên bề mặt, chạm nhẹ tay vào đó, lớp màng sẽ vỡ ra. Thành phần chính của lớp màng cứng này là
- A CaCl2.
- B CaCO3.
- C Ca(OH)2.
- D CaO.
Đáp án: B
Lời giải chi tiết:
Khi để trong không khí lâu ngày, dung dịch nước vôi trong tiếp xúc và phản ứng với các chất trong không khí.
Trong đó, chủ yếu là tác dụng với CO2 tạo kết tủa CaCO3 trên bề mặt: CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Vậy thành phần chính của lớp màng cứng trên bề mặt nước vôi trong là CaCO3.
Đáp án B
Câu hỏi 36 :
Chỉ dùng nước và dung dịch HCl hãy trình bày cách nhận biết 4 chất rắn (đựng trong 4 lọ riêng biệt): Na2CO3, CaCO3, Na2SO4, CaSO4.2H2O.
Phương pháp giải:
Hòa tan 4 chất rắn vào nước, chia nhóm chất tan và nhóm chất không tan
Sau đó cho dung dịch HCl tác dụng với các chất trong mỗi nhóm.
Lời giải chi tiết:
Hoà vào nước ta được hai nhóm chất:
(1) Tan trong nước là Na2CO3 và Na2SO4. Phân biệt 2 chất này bằng dung dịch HCl. Tác dụng với dung dịch HCl là Na2CO3 (sủi bọt khí); không tác dụng với dung dịch HCl là Na2SO4.
(2) Không tan trong nước là CaCO3 và CaSO4.2H2O. Dùng dung dịch HCl để nhận ra CaCO3 (có sủi bọt khí) còn lại là CaSO4.2H2O.
Câu hỏi 37 :
Chất nào sau đây có thể hòa tan được BaCO3 tạo dung dịch trong suốt?
- A dd H2SO4.
- B dd HCl.
- C dd Ba(OH)2.
- D dd NaCl.
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 38 :
Thạch cao nung được dùng để đúc tượng vì khi trộn với nước thì giãn nở về thể tích, nên rất ăn khuân. Công thức của thạch cao nung là
- A CaSO4.
- B CaSO4. H2O.
- C CaCO3.
- D CaSO4. 2H2O.
Đáp án: B
Phương pháp giải:
Dựa vào kiến thức học trong chương kim loại kiềm thổ và hợp chất quan trọng của chúng trong sgk hóa 12
Lời giải chi tiết:
Công thức của thạch cao nung là CaSO4. H2O.
Đáp án B
Câu hỏi 39 :
Trong nước tự nhiên thường có lẫn một lượng nhỏ các muối Ca(NO3)2, Mg(NO3)2, Ca(HCO3)2, Mg(HCO3)2. Có thể dùng dung dịch nào sau đây để loại đồng thời các cation trong các muối trên ra khỏi nước ?
- A Dung dịch NaOH
- B Dung dịch K2SO4
- C Dung dịch Na2CO3
- D Dung dịch NaNO3
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 40 :
Có 3 lọ, mỗi lọ đựng một dung dịch sau: BaCl2, Ba(NO3)2, Ba(HCO3)2. Chỉ dùng thuốc thử nào sau đây có thể nhận biết được các dung dịch trên ?
- A Quỳ tím
- B Phenolphtalein
- C Na2CO3
- D AgNO3
Đáp án: D
Lời giải chi tiết:
- Đun nóng các dung dịch, có kết tủa xuất hiện là dung dịch Ba(HCO3)2:
Ba(HCO3)2 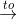 BaCO3↓+CO2↑+H2O
BaCO3↓+CO2↑+H2O
- Cho AgNO3 vào 2dung dịch còn lại, có kết tủa là dung dịch BaCl2; còn lại không có hiên tượng gì là
Ba(NO3)22AgNO3+BaCl2→2AgCl↓+Ba(NO3)2
Đáp án D
Câu hỏi 41 :
Cho các phát biểu sau:
(1) Các kim loại Na, Ba, K đều có cấu trúc mạng tinh thể lập phương tâm khối.
(2) Từ Li đến Cs (nhóm IA) khả năng P/ứ với nước mạnh dần.
(3) Từ Be đến Ba(nhóm IIA) nhiệt độ nóng chảy tăng dần.
(4) NaHCO3 là chất lưỡng tính.
(5) Thạch cao nung có công thức CaSO4.2H2O được ứng dụng bó bột, đắp tượng, đúc khuôn,...
(6) Liti là kim loại nhẹ nhất.
Các phát biểu đúng là:
- A 1;4;5;6
- B 1;2;3;6
- C 1;2;4;6
- D 2;3;4;5
Đáp án: C
Lời giải chi tiết:
(3) Sai. nhóm IIA có nhiệt độ nóng chảy không theo qui luật
(5) Sai.Thạch cao nung là CaSO4.H2O
Đáp án C
Câu hỏi 42 :
Lần lượt cho một mẫu Ba và các dung dịch K2SO4, NaHCO3, HNO3, NH4Cl. Có bao nhiêu trường hợp xuất hiện kết tủa?
- A 3
- B 4
- C 2
- D 1
Đáp án: C
Lời giải chi tiết:
K2SO4, NaHCO3
Đáp án C
Câu hỏi 43 :
Chỉ dùng CO2 và H2O nhận biết được bao chất bột trắng (trong các lọ không nhãn) trong số các chất sau: NaCl , Na2CO3, Na2SO4, BaCO3 , BaSO4
- A 2
- B 4
- C 5
- D 3
Đáp án: C
Lời giải chi tiết:
Dùng nước :
+) Nhóm Không tan : BaCO3 ; BaSO4
=> Sục CO2 vào => kết tủa tan là BaCO3 , còn lại là BaSO4
+) Nhóm tan : NaCl ; Na2CO3 ; Na2SO4
- Cho Ba(HCO3)2 lần lượt vào các dụng dịch NaCl; Na2CO3; Na2SO4
+ Nếu không có hiện tượng gì là: NaCl
+ Xuất hiện kết tủa trắng là: Na2CO3 và Na2SO4
PTHH: Ba(HCO3)2 + Na2CO3 → BaCO3↓ + 2NaHCO3
Ba(HCO3)2 + Na2SO4 → BaSO4↓ + 2NaHCO3
- Lọc kết tủa tương ứng ta thu được 2 kết tủa là BaCO3 và BaSO4
- Sục CO2 đến dư lần lượt vào từng kết tủa trên
+ Nếu kết tủa tan dần là BaCO3 → dung dịch tạo kết tủa này ban đầu là Na2CO3
PTHH: CO2 + H2O + BaCO3↓ → Ba(HCO3)2
+ Nếu kết tủa không tan là BaSO4 → dung dịch tạo kết tủa này ban đầu là Na2SO4
Đáp án C
Câu hỏi 44 :
Trong các dung dịch : HNO3, NaCl, K2SO4, Ca(OH)2, NaHSO4, Mg(NO3)2. Dãy gồm các chất đều tác dụng được với dung dịch Ba(HCO3)2 là :
- A HNO3, Ca(OH)2, NaHSO4, Mg(NO3)2
- B HNO3, NaCl, K2SO4
- C HNO3, Ca(OH)2, NaHSO4, K2SO4
- D NaCl, K2SO4, Ca(OH)2
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 45 :
Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch NaHSO4, Ca(OH)2, H2SO4, Ca(NO3)2, NaHCO3, Na2CO3, CH3COOH. Số trường hợp có xảy ra phản ứng là?
- A 6
- B 5
- C 4
- D 3
Đáp án: B
Lời giải chi tiết:
Gồm các chất: NaHSO4, Ca(OH)2, H2SO4, Na2CO3, CH3COOH.
Đáp án B
Câu hỏi 46 :
Cho các phản ứng hóa học sau:
(1) (NH4)2SO4 + BaCl2 → (2) CuSO4 + Ba(NO3)2 →
(3) Na2SO4 + BaCl2 → (4) H2SO4 + BaCO3 →
(5) (NH4)2SO4 + Ba(OH)2 → (6) Al2(SO4)3 + Ba(NO3)2 →
Các phản ứng đều có cùng một phương trình ion rút gọn là:
- A (1), (2), (3), (6).
- B (1), (2), (5), (6).
- C (2), (3), (4), (6).
- D (3), (4), (5), (6).
Đáp án: A
Lời giải chi tiết:
(1), (2), (3), (6) cùng có phương trình ion rút gọn là:
Ba2+ + SO42- → BaSO4↓
Đáp án A
Câu hỏi 47 :
Cho các phát biểu sau đây về độ cứng của nước:
(1) Khi đun sôi ta có thể loại bỏ được độ cứng tạm thời của nước.
(2) Có thể dùng Na2CO3 để lọa bỏ cả độ cứng tạm thời và độ cứng vĩnh cửu của nước.
(3) Có thể dùng HCl để làm mềm nước cứng.
(4) Có thể dùng Ca(OH)2 với lượng vừa đủ để loại độ cứng của nước.
Số phát biểu đúng là
- A 1
- B 2
- C 3
- D 4
Đáp án: C
Lời giải chi tiết:
(1) Đ
(2) Đ
(3) S
(4) Đ
Đáp án C
Câu hỏi 48 :
Cho các chất: H2O (t0); CO2 (t0); SiO2 (to); HNO3 đặc nguội; dung dịch AlCl3. Số chất mà Mg có thể phản ứng là:
- A 2
- B 3
- C 4
- D 5
Đáp án: D
Phương pháp giải:
Dựa vào tính chất hóa học của Mg.
Lời giải chi tiết:
Mg có thể phản ứng với: H2O (t0); CO2 (t0); SiO2 (to); HNO3 đặc nguội; dung dịch AlCl3 (5 chất).
Phương trình phản ứng:
Mg + H2O \(\xrightarrow{{{t^o}}}\) MgO + H2
2Mg + CO2 \(\xrightarrow{{{t^o}}}\) 2MgO + C
2Mg + SiO2 \(\xrightarrow{{{t^o}}}\) 2MgO + Si
Mg + 10HNO3 → 4Mg(NO3)2+ 3H2O + NH4NO3 (có thể tạo sản phẩm khử khác như NO, NO2, N2O, N2).
3Mg + 2AlCl3 → 3MgCl2+ 2Al
Đáp án D
Câu hỏi 49 :
Thực hiện các phản ứng sau:
(1) X + CO2 → Y
(2) 2X + CO2 → Z + H2O
(3) Y + T → Q + X + H2O
(4) 2 Y + T→ Q + Z + 2H2O
Hai chất X, T tương ứng là:
- A Ca(OH)2, NaOH
- B Ca(OH)2, Na2CO3
- C NaOH, NaHCO3
- D NaOH, Ca(OH)2
Đáp án: D
Phương pháp giải:
Dựa vào tính chất hóa học của kim loại kiềm, hợp chất của kim loại kiềm, kim loại kiềm thổ, hợp chất của kim loại kiềm thổ.
Lời giải chi tiết:
(1) NaOH + CO2 → NaHCO3
(2) 2NaOH + CO2 → Na2CO3+ H2O
(3) NaHCO3 + Ca(OH)2 → CaCO3 + NaOH+ H2O
(4) 2 NaHCO3 + Ca(OH)2→ CaCO3 + Na2CO3 + 2H2O
Vậy X là NaOH, Y là NaHCO3, Z là Na2CO3, T là Ca(OH)2, Q là CaCO3
Đáp án D
Câu hỏi 50 :
Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch sau: HNO3, Na2SO4, Ba(OH)2, NaHSO4. Số trường hợp có phản ứng xảy ra là:
- A 3
- B 2
- C 1
- D 4
Đáp án: D
Lời giải chi tiết:
Ba(HCO3)2 + 2HNO3 → Ba(NO3)2+ 2CO2+ 2H2O
Ba(HCO3)2+ Na2SO4 → BaSO4+ 2NaHCO3
Ba(HCO3)2+ Ba(OH)2→ 2BaCO3+ 2H2O
Ba(HCO3)2+ 2NaHSO4 → BaSO4+ Na2SO4+ 2CO2+2 H2O
Vậy có 4 phản ứng xảy ra.
Đáp án D
20 bài tập vận dụng cao về kim loại kiềm thổ và hợp chất có đáp án và lời giải chi tiết
30 bài tập CO2 tác dụng với Ca(OH)2; Ba(OH)2 có đáp án và lời giải
30 bài tập vận dụng về kim loại kiềm thổ và hợp chất có đáp án và lời giải chi tiết
20 câu hỏi lý thuyết về nước cứng có đáp án và lời giải chi tiết
15 bài tập về nước cứng có đáp án và lời giải chi tiết
20 bài tập CO2 tác dụng với dung dịch kiềm thổ có đáp án và lời giải chi tiết
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 15 bài toán cho từ từ axit vào muối cacbonat có lời giải
- 15 bài toán cho từ từ muối cacbonat vào axit có lời giải
- 50 bài tập CO2 tác dụng với dung dịch kiềm và muối cacbonat có lời giải
- 20 bài tập CO2 tác dụng với dung dịch kiềm thổ có lời giải
- 15 bài toán CO2 tác dụng với dung dịch kiềm, muối cacbonat có lời giải
- 50 câu hỏi lý thuyết mức độ vận dụng về ôn tập chương 6 có lời giải
- 50 câu hỏi lý thuyết mức độ thông hiểu về ôn tập chương 6 có lời giải
- 20 bài tập mức độ vận dụng cao nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 30 bài tập mức độ vận dụng nhôm, kim loại kiềm và hợp chất tác dụng với nước có lời giải
- 20 bài tập axit tác dụng với muối aluminat có lời giải









