Đề số 3 - Đề kiểm tra giữa học kì II - Hóa học 9 có đáp án và lời giải chi tiết
Đề số 3 - Đề kiểm tra giữa học kì II - Hóa học 9 có đáp án và lời giải chi tiết
Đề bài
I. TRẮC NGHIỆM (3 điểm)
Câu 1 : Hiđrocacbon có liên kết ba trong công thức cấu tạo là
A. benzen.
B. axetilen.
C. etilen.
D. metan.
Câu 2 : Tính chất vật lí chung của các hiđrocacbon (metan, etilen, axetilen) là
A. đều là chất khí ở điều kiện thường.
B. đều là chất lỏng ở điều kiện thường.
C. tan nhiều trong nước.
D. đều có mùi khai.
Câu 3 : Cho 7 (g) hỗn hợp X gồm hai anken đồng đẳng kế tiếp phản ứng với dung dịch Br2 dư thấy có 32 (g) brom phản ứng. Công thức phân tử của hai anken trong X là
A. C3H6 và C4H8.
B. CH4 và C2H4.
C. C2H4 và C3H6.
D. C2H2 và C3H4.
Câu 4 : Benzen có thể phản ứng với dãy gồm các chất nào dưới đây (điều kiện thích hợp)?
A. Dung dịch HCl, H2O, khí O2.
B. Dung dịch Br2, dung dịch NaOH, khí Cl2.
C. Dung dịch KMnO4, dung dịch Br2, dung dịch HNO3.
D. Brom khan, khí H2, khí O2.
Câu 5 : Cho 2,24 (l) khí metan phản ứng hoàn toàn với V (l) khí clo ở đktc, thu được một sản phẩm hữu cơ duy nhất X trong đó clo chiếm 92,21% về khối lượng. Công thức phân tử của X là
A. CCl4.
B. CHCl3.
C. CH2Cl2.
D. CH3Cl.
Câu 6 : Hợp chất hữu cơ được chia thành hai loại là
A. hiđrocacbon no và hiđrocacbon không no.
B. hiđrocacbon no và hiđrocacbon thơm.
C. hiđrocacbon và ancol.
D. hiđrocacbon và dẫn xuất hiđrocacbon.
II. TỰ LUẬN (7 điểm)
Câu 7 : (2 điểm) Viết tất cả các công thức cấu tạo có thể có của các hiđrocacbon mạch hở, có công thức phân tử: C5H12 và C4H6.
Câu 8 : (2 điểm) Hợp chất hữu cơ A có khối lượng phân tử gấp 1,5 lần khối lượng phân tử của axit axetic (CH3COOH). Trong hợp chất A có tỉ lệ khối lượng các nguyên tố C; H; N; S lần lượt là 12 : 3 : 14 : 16. Xác định công thức phân tử của A.
Câu 9 : (3 điểm) Đun nóng 8,8 g hỗn hợp X gồm C2H2, C2H4, H2 (trong đó số mol etilen gấp đôi số mol axetilen) với chất xúc tác thích hợp thu được hỗn hợp Y. Đốt cháy hoàn toàn hỗn hợp Y, rồi dẫn toàn bộ sản phẩm cháy lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 đựng Ca(OH)2 dư, thấy khối lượng bình 1 tăng 14,4g và bình 2 tăng m gam.
a) Xác định thành phần phần trăm về khối lượng mỗi hợp chất trong A.
b) Tính m?
Lời giải chi tiết
|
1.B |
2.A |
3.C |
4.D |
5.A |
6.D |
Câu 1
Axetilen có công thức cấu tạo là CH≡CH (có liên kết ba).
Đáp án B
Câu 2
Tính chất vật lí chung của các hiđrocacbon (metan, etilen, axetilen) là đều là chất khí ở điều kiện thường.
Đáp án A
Câu 3
Công thức trung bình của 2 anken trong X là \({{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}\)
\({{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}+B{{r}_{2}}\to {{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}B{{r}_{2}}\)
Theo PTHH ⟹ \({{n}_{{{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}}}={{n}_{B{{r}_{2}}}}=32/160=0,2(mol)\)
Ta có: \({{M}_{{{C}_{{\bar{n}}}}{{H}_{2\bar{n}}}}}=m/n=14\bar{n}=35\Rightarrow \bar{n}=2,5\)
Vậy 2 anken đồng đẳng liên tiếp trong hỗn hợp X là C2H4 và C3H6.
Đáp án C
Câu 4
Benzen có thể phản ứng thế với brom khan, phản ứng cộng với khí hiđro và phản ứng đốt cháy với khí oxi.
Đáp án D
Câu 5
PTHH: CH4 + xCl2 \(\xrightarrow{a/s}\) CH4-xClx + xHCl
\(%{{m}_{Cl(X)}}=\frac{{{m}_{Cl}}}{{{m}_{X}}}.100%=\frac{35,5x.100%}{12+4-x+35,5x}=92,21%\Rightarrow x=4\)
Vậy CTPT của X là CCl4.
Đáp án A
Câu 6
Hợp chất hữu cơ được chia thành hai loại là hiđrocacbon và dẫn xuất hiđrocacbon.
Đáp án D
Câu 7
Hướng dẫn giải:
a) CTCT của C5H12 là
b) CTCT của C4H6 là
CH ≡ C – CH2 – CH3
CH3 – C≡ C – CH3
CH2 = CH – CH = CH2
CH2 = C = CH – CH3
Câu 8
Gọi CTĐGN của A là CxHyNzSt
⟹ \(x:y:z:t=\frac{12}{12}:\frac{3}{1}:\frac{14}{14}:\frac{16}{32}=2:6:2:1\)
⟹ CTĐGN của A là C2H6N2S ⟹ CTPT của A là (C2H6N2S)n
Ta có: MA = 90n = 90 ⟹ n = 1.
Vậy CTPT của A là C2H6N2S.
Câu 9
a)
Gọi số mol C2H2, C2H4 và H2 trong X lần lượt là x, 2x và y (mol)
⟹ mX = 26x + 28.2x + 2y = 8,8 ⟹ 82x + 2y = 8,8 (1)
* Đốt cháy X
2C2H2 + 5O2 \(\xrightarrow{{{t}^{0}}}\) 4CO2 + 2H2O
C2H4 + 3O2 \(\xrightarrow{{{t}^{0}}}\) 2CO2 + 2H2O
2H2 + O2 \(\xrightarrow{{{t}^{0}}}\) 2H2O
Theo PTHH ⟹ \({{n}_{C{{O}_{2}}}}=2{{n}_{{{C}_{2}}{{H}_{2}}}}+2{{n}_{{{C}_{2}}{{H}_{4}}}}=2x+2.2x=6x(mol)\)
Theo PTHH ⟹ \({{n}_{{{H}_{2}}O}}={{n}_{{{C}_{2}}{{H}_{2}}}}+2{{n}_{{{C}_{2}}{{H}_{4}}}}+{{n}_{{{H}_{2}}}}=x+2.2x+y=5x+y(mol)\)
* mbình 1 tăng = mH2O = 14,4 (g)
⟹ \({{n}_{{{H}_{2}}O}}={{n}_{{{C}_{2}}{{H}_{2}}}}+2{{n}_{{{C}_{2}}{{H}_{4}}}}+{{n}_{{{H}_{2}}}}=5x+y=0,8\) (2)
Từ (1)(2) ⟹ x = 0,1 và y = 0,3
Vậy
b)
Theo PTHH (đốt cháy X) ⟹ \({{n}_{C{{O}_{2}}}}=2{{n}_{{{C}_{2}}{{H}_{2}}}}+2{{n}_{{{C}_{2}}{{H}_{4}}}}=0,6(mol)\)
Ta có: m = mbình 2 tăng = mCO2 = 0,6.44 = 26,4 (g).
Loigiaihay.com
- Đề số 4 - Đề kiểm tra giữa học kì II - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 5 - Đề kiểm tra giữa kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 2 - Đề kiểm tra giữa học kì II - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 1 - Đề kiểm tra giữa học kì II - Hóa học 9 có đáp án và lời giải chi tiết
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu





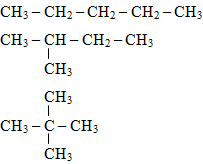
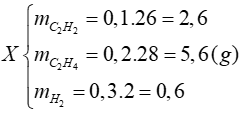








Danh sách bình luận