 Giải bài tập hóa học 9, Hóa 9 - Để học tốt hóa học 9
Giải bài tập hóa học 9, Hóa 9 - Để học tốt hóa học 9
 ĐỀ KIỂM TRA HỌC KÌ 2 (ĐỀ THI HỌC KÌ 2) - HÓA HỌC 9
ĐỀ KIỂM TRA HỌC KÌ 2 (ĐỀ THI HỌC KÌ 2) - HÓA HỌC 9
Đề số 5 - Đề kiểm tra học kì 2 – Hóa học 9
Đáp án và lời giải chi tiết Đề số 5 - Đề kiểm tra học kì 2 (Đề thi học kì 2) – Hóa học 9
Đề bài
I. TRẮC NGHIỆM : ( 3 điểm) Chọn ý trả lời đúng nhất trong các ý sau:
Câu 1: Dãy chất gồm hiđrocacbon
A. C6H12O6, C6H6, C5H10
B. C2H4, C3H6, CH3Cl
C. C2H2, CH4, C2H6O.
D. C2H4, CH4, C6H6.
Câu 2: Để thu được CH4 tinh khiết từ hỗn hợp CH4 và CO2, ta dẫn hỗn hợp khí qua
A. dung dịch H2SO4 đặc dư.
B. dung dịch Ca(OH)2 dư.
C. dung dịch nước brom dư.
D. dung dịch muối ăn dư.
Câu 3: Chất vừa tham gia phản ứng thế, vừa tham gia phản ứng cộng
A. CH4. B. C2H4.
C. C2H2. D. C6H6.
Câu 4: Công thức hóa học viết sai
A. CH2=CH-CH3. B. CH3-CH3
C. CH2-CH2. D. CH2=CH2.
Câu 5: Dãy chất đều tham gia phản ứng thủy phân
A. chất béo, saccarozơ, tinh bột
B. tinh bột, xenlulozơ, glucozơ.
C. tinh bột, glucozơ, protein.
D. glucozơ, saccarozơ, xenlulozơ.
Câu 6: Trên vỏ lon bia Tiger 330 ml có ghi độ cồn ( độ rượu) là 4,60. Vậy thể tích rượu etylic có trong 330 ml bia trên là
A. 14,12 ml. B. 15,18 ml
C. 13,18ml. D. 11,35 ml.
Câu 7: Đốt cháy hợp chất hữu cơ X trong khí oxi, sản phẩm thu được gồm: CO2, H2O và N2. Vậy X là:
A. tinh bột. B. glucozơ.
C. xenlulozơ. D. protein.
Câu 8: Một hợp chất A là chất lỏng không màu, tan vô hạn trong nước, tác dụng với natri giải phóng khí H2. A tham gia phản ứng este hóa nhưng không tác dụng với Na2CO3.
A. C2H5OH. B. CH3-O-CH3.
C. CH3COOH. D. CH3COOC2H5.
Câu 9: Có sơ đồ phản ứng sau: \(Etilen\xrightarrow{+{{H}_{2}}O}A\xrightarrow{+{{O}_{2}}}B\xrightarrow{+{{C}_{2}}{{H}_{5}}OH}C\).
Các chất A, B, C lần lượt là
A. axit axetic, rượu etylic, etyl axetat.
B. etyl axetat, rượu etylic, axit axetic.
C. rượu etylic, axit axetic, etyl axetat
D. axetilen, rượu etylic, etyl axetat.
Câu 10: Khi thủy phân chất béo trong môi trường axit ta thu được
A. glixerol và axit béo.
B. glixerol và muối của axit béo.
C. glixerol và hỗn hợp muối của axit béo.
D. glixerol và hỗn hợp các axit béo.
Câu 11: Dãy muối cacbonat bị thủy phân ở nhiệt độ cao
A. Na2CO3, Ca(HCO3)2.
B. K2CO3, KHCO3.
C. CaCO3, Ca(HCO3)2.
D. MgCO3, K2CO3.
Câu 12: Trong một chu kì, khi đi từ đầu đến cuối chu kì theo chiều tăng dần của điện tích hạt nhân
A. tính phi kim của các nguyên tố giảm dần.
B. tính kim loại của các nguyên tố tăng lên.
C. tính chất các nguyên tố không thay đổi.
D. tính kim loại của các nguyên tố giảm dần.
II. TỰ LUẬN
Câu 1: Viết phương trình hóa học thực hiện chuỗi phản ứng sau, ghi rõ điều kiện ( nếu có):
Câu 2: Bằng phương pháp hóa học, hãy nhận biết các chất lỏng không màu đựng trong các lọ riêng biệt mất nhãn sau: dung dịch glucozơ, axit axetic, rượu etylic.(Viết phương trình hóa học xảy ra nếu có).
Câu 3: Nêu hiện tượng và viết phương trình hóa học của phản ứng (nếu có) khi:
a. Cho dung dịch CH3COOH vào ống nghiệm có chứa dung dịch Na2CO3.
b. Cho dung dịch CH3COOH vào ống nghiệm có chứa một ít kim loại đồng.
Câu 4: Đốt cháy hoàn toàn 23 gam hợp chất hữu cơ X chứa C, H, O thu được 44 gam CO2, 27 gam H2O. Xác định công thức phân tử của X, biết khối lượng mol phân tử của X là 46 gam/mol.
Câu 5: Thực hiện phản ứng este hóa hoàn toàn 28,75 ml rượu etylic 800 với axit axetic.
a. Tính khối lượng etyl axetat thu được, biết hiệu suất của phản ứng este hóa là 75%
b. Để có được lượng rượu etylic thực hiện phản ứng trên, người ta đã lên men rượu bao nhiêu gam glucozơ?
Biết hiệu suất của phản ứng lên men rượu là 80%.
Lời giải chi tiết
HƯỚNG DẪN GIẢI CHI TIẾT
Câu 1:
Ghi nhớ: Hidrocacbon chỉ chứa nguyên tố C và H trong phân tử
Đáp án D
Câu 2:
Phương pháp:
Để thu được CH4 từ hỗn hợp CH4 và CO2 ta phải chọn thuốc thử nào phản ứng với CO2 nhưng không phản ứng với CH4.
Hướng dẫn giải:
Ca(OH)2 phản ứng với CO2, nhưng không phản ứng với CH4 => CH4 thoát ra ngoài, ta thu CH4 sẽ được tinh khiết.
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Đáp án B
Câu 3:
Hướng dẫn giải:
C6H6 vừa tham gia phản ứng thế, vừa tham gia phản ứng cộng.
+ Phản ứng thế:
C6H6 + Br2 \(\xrightarrow{{{t}^{0}}}\) C6H5Br + HBr
+ phản ứng cộng
C6H6 + 3H2 \(\xrightarrow{Ni,{{t}^{0}}}\) C6H12
Đáp án D
Câu 4:
Hướng dẫn giải:
CH2-CH2 => viết sai vì C không đủ hóa trị IV trong hợp chất này.
Đáp án C
Câu 5:
Hướng dẫn giải:
Glucozo là chất không tham gia phản ứng thủy phân => loại B, C,D
Đáp án A
Câu 6:
Hướng dẫn giải:
Công thức tính độ rượu:
Đáp án B
Câu 7:
Hướng dẫn giải:
Từ sản phẩm thu được là CO2, H2O và N2 => ta suy ra chất ban đầu chắc chắn phải có nguyên tố C, H, N có thể có nguyên tố O
=> loại tinh bột, glucozo và xenlulozo vì không chứa N trong phân tử
=> chọn protein
Đáp án D
Câu 8:
Hướng dẫn giải:
chất A là chất lỏng không màu, tan vô hạn trong nước, tác dụng với natri giải phóng khí H2. A tham gia phản ứng este hóa => A có thể là C2H5OH hoặc CH3COOH
A không tác dụng với Na2CO3 => loại CH3COOH
Đáp án A
Câu 9:
Hướng dẫn giải:
CH2=CH2 + H2O \(\xrightarrow{{{H}^{+}},{{t}^{0}}}\) C2H5OH
C2H5OH + O2 \(\xrightarrow{men\,giam}\)CH3COOH + H2O
CH3COOH + C2H5OH \(\underset{{}}{\overset{{{H}_{2}}S{{O}_{4}}\,dac\,,{{t}^{0}}}{\longleftrightarrow}}\) CH3COOC2H5 + H2O
Đáp án C
Câu 10:
Hướng dẫn giải:
Chất béo có dang: (RCOO)3C3H5 bị thủy phân trong môi trường axit có phản ứng:
(RCOO)3C3H5 + 3H2O \(\underset{{}}{\overset{{{H}^{+}}\,,{{t}^{0}}}{\longleftrightarrow}}\) 3RCOOH + C3H5(OH)3 => thu được glixerol và hỗn hợp các axit béo
Đáp án D
Câu 11:
Hướng dẫn giải:
Ghi nhớ: Na2CO3 và K2CO3 không bị nhiệt phân hủy
=> loại A, B, D => chọn C
CaCO3 \(\xrightarrow{{{t}^{0}}}\) CaO + CO2↑
Ca(HCO3)2 \(\xrightarrow{{{t}^{0}}}\) CaCO3 + CO2 + H2O
Đáp án C
Câu 12:
Hướng dẫn giải:
Khi đi từ đầu đến cuối chu kì theo chiều tăng dần của điện tích hạt nhân số lớp e như nhau, điện tích hạt nhân tăng dần => khả năng hút e của hạt nhân tăng mạnh hơn => tính kim loại giảm dần, tính phi kim tăng dần do điện tích hạt nhân tăng.
Đáp án D
II. TỰ LUẬN
Câu 13:
Hướng dẫn giải:
Câu 14:
Phương pháp:
Sử dụng quỳ tím và kim loại Na để phân biệt 3 chất.
Hướng dẫn giải:
Lấy mỗi chất 1 ít cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng:
- Cho quỳ tím lầ lượt vào từng ống nghiệm:
+ Qùy tím chuyển sang màu đỏ là: axit axetic
+ Qùy tím không chuyển màu là: dd glucozo và rượu etylic. ( dãy I)
- Cho mẩu Na lần lượt vào các ống nghiệm ở dãy (I)
+ ống nào thấy có sủi bọt khí thoát ra là: rượu etylic
2C2H5OH + 2Na → 2C2H5ONa + H2↑
+ ống nào không có hiện tượng gì là: dd glucozo
Câu 15:
Phương pháp:
Hiện tượng quan sát được: có khí thoát ra hay không, có kết tủa hay không? Dung dịch thu được có màu gì?
=> quan sát được gì, nêu hiện tượng đó.
Hướng dẫn giải:
a. Hiện tượng: có bọt khí thoát ra ngoài
2CH3COOH + Na2CO3 → 2CH3COONa + CO2↑ + H2O
b. Hiện tượng: bột đồng tan dần đến hết, dd thu được có màu xanh lam
2CH3COOH + Cu (đỏ) → (CH3COO)2Cu ( màu xanh lam) + H2O
Câu 16:
Phương pháp:
Tính nCO2 => nC = nCO2 => mC = ?
Tính nH2O => mH = 2nH2O => mH = ?
Khối lượng O trong X:
mO = 2,3 – mC – mH = ? => nO = ?
Gọi công thức của X có dạng: CxHyOz (x, y, z € N*)
Ta có: x : y : z = nC : nH : nO
=> Công thức đơn giản nhất
Có PTK của X = 46 => CTPT của X =?
Hướng dẫn giải:
Khối lượng O trong X là:
mO = 23 – mC – mH = 23 – 12 -3 = 8(g)
Gọi công thức của X có dạng: CxHyOz (x, y, z € N*)
Ta có: x : y : z = nC : nH : nO
= 1 : 3 : 0,5
= 2: 6 : 1
=> công thức đơn giản nhất của X là: (C2H6O)n
Vì phân tử khối của X = 46 (g/mol)
=> ( 12.2 + 6 + 16)n = 46
=> 46n = 46
=> n = 1
=> CTPT của X là C2H6O.
Câu 17:
Phương pháp:
Dr = 0,8 (g/ml) => m rượu = Vrượu . Dr = ?
PTHH: C2H5OH + CH3COOH \(\underset{{}}{\overset{{{H}_{2}}S{{O}_{4\,}}\,d,{{t}^{0}}}{\longleftrightarrow}}\) CH3COOC2H5 + H2O
Tính được khối lượng este lí thuyết thu được theo phương trình:
Vì H = 75% nên lượng este thực tế thu được là:
\({{m}_{C{{H}_{3}}COO{{C}_{2}}{{H}_{5}}\,\,TT}}=\frac{{{m}_{C{{H}_{3}}COO{{C}_{2}}{{H}_{5}}\,\,LT}}}{100%}.H%=?\,\,(g)\)
b. PTHH: C6H12O6 \(\xrightarrow{men\,ruou}\) 2C2H5OH + 2CO2
Tính được khối lượng glucozo cần lấy theo lí thuyết ( theo phương trình)
Vì H = 80% nên lượng glucozo thực tế cần phải lấy là:
\({{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6\,}}\,TT}}=\frac{{{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6\,}}\,LT}}}{H%}.100%=?(g)\)
Hướng dẫn giải:
Dr = 0,8 (g/ml)
=> m rượu = Vrượu . Dr = 23. 0,8 = 18,4 (g)
PTHH:
C2H5OH + CH3COOH \(\underset{{}}{\overset{{{H}_{2}}S{{O}_{4\,}}\,d,{{t}^{0}}}{\longleftrightarrow}}\) CH3COOC2H5 + H2O
Theo PTHH: nCH3COOOH = nC2H5OH = 0,4 (mol)
Khối lượng lí thuyết este thu được là:
mCH3COOH LT = 0,4. 88 = 35,2 (g)
Vì H = 75% nên lượng este thực tế thu được là:
\({{m}_{C{{H}_{3}}COO{{C}_{2}}{{H}_{5}}\,\,TT}}=\frac{{{m}_{C{{H}_{3}}COO{{C}_{2}}{{H}_{5}}\,\,LT}}}{100%}.H%=\frac{35,2}{100%}.75%=26,4\,\,(g)\)
b. C6H12O6 \(\xrightarrow{men\,ruou}\) 2C2H5OH + 2CO2
Theo PTHH:
nC6H12O6 = ½ nC2H5OH = ½. 0,4 = 0,2 (mol)
Khối lượng glucozo cần lấy theo lí thuyết là:
mC6H12O6 LT = 0,2. 180 = 36 (g)
Vì H = 80% nên lượng glucozo thực tế cần phải lấy là:
\({{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6\,}}\,TT}}=\frac{{{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6\,}}\,LT}}}{H%}.100%=\frac{36}{80%}.100%=45\,(g)\) = 45g
Nguồn: Sưu tầm
Loigiaihay.com
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu





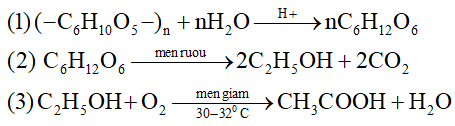
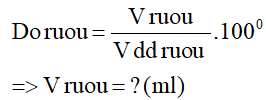
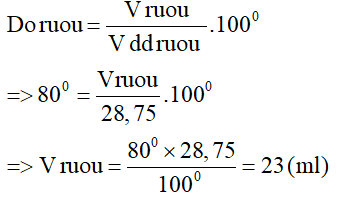








Danh sách bình luận