Đề cương ôn tập học kỳ I môn hóa lớp 12
Tổng hợp kiến thức cần nắm vững, các dạng bài tập và câu hỏi có khả năng xuất hiện trong đề thi HK1 Hóa học 12 sắp tới
ÔN TẬP HỌC KÌ I
CHƯƠNG 1: ETSE - LIPIT
A. ESTE
I. ĐỊNH NGHĨA
- Khi thay thế nhóm OH ở nhóm COOH của axit bằng gốc OR ta thu được este
* Công thức tổng quát
+ Este được tạo bởi axit cacboxylic no, đơn chức mạch hở và ancol no, đơn chức, mạch hở (este no, đơn chức, mạch hở): CmH2m+1COOCm’H2m’+1 hay CnH2nO2 (m ≥ 0; m’ ≥ 1; n ≥ 2 ).
+ Este đa chức được tạo bởi axit cacboxylic đa chức và ancol đơn chức: R(COOR’)n
+ Este đa chức được tạo bởi axit cacboxylic đơn chức và ancol đa chức: (RCOO)nR’
+ Este đa chức được tạo bởi axit cacboxylic đa chức và ancol đa chức (cùng có n nhóm chức): R(COO)nR’
+ Tóm lại, có thể đặt CTTQ của este : CxHyOz (x, z ≥ 2; y là số chẵn, y ≤ 2x)
II. DANH PHÁP
Tên gốc hiđrocacbon R’ + tên anion gốc axit (đuôi “at”)
HCOOC2H5: etyl fomat
CH3COOCH=CH2: vinyl axetat
III. TÍNH CHẤT VẬT LÝ:
- Nhiệt độ sôi thấp hơn axit, ancol vì không tạo liên kết hiđro
- Thường: lỏng, nhẹ hơn nước, ít tan trong nước
- Hòa tan nhiều hợp chất hữu cơ
- Thường có mùi thơm dễ chịu: isoamyl axetat: mùi chuối chín; etyl butirat: mùi dứa, etyl isovalerat: mùi táo
IV. TÍNH CHẤT HÓA HỌC
1. Thủy phân môi trường axit (thuận nghịch)
R-COO-R’ + H-OH \(\overset{{{H}_{2}}S{{O}_{4}},{{t}^{{}^\circ }}}{\mathop{\leftrightarrows }}\,\)R-COOH + R’-OH
2. Thủy phân môi trường kiềm ( phản ứng xà phòng hóa)
R-COO-R’ + NaOH \(\xrightarrow{{{H}_{2}}O,{{t}^{{}^\circ }}}\)R-COONa + R’-OH
a) Tạo ancol:
CH3COOCH3 + NaOH → CH3COONa + CH3OH
b) Tạo anđehit:
RCOOCH=CH-R’ + NaOH → RCOONa + R’-CH2CH=O
c) Tạo xeton :
RCOOC(R’)=CH-R” + NaOH → RCOONa + R’-CO-CH2R”
d) Tạo phenolat:
RCOOC6H4R’ + 2NaOH → RCOONa + R’-C6H5ONa + H2O
3. Phản ứng tráng bạc của HCOOR
HCOOR + 2AgNO3 + 3NH3 + H2O → ROCOONH4 + 2Ag↓ + 2NH4NO3
V. ĐIỀU CHẾ:
1. Este của ancol (phản ứng este hóa)
\(C{{H}_{3}}COOH+{{(C{{H}_{3}})}_{2}}CHC{{H}_{2}}C{{H}_{2}}OH\overset{{{H}_{2}}S{{O}_{4}},{{t}^{o}}}{\mathop{\leftrightarrows }}\,C{{H}_{3}}COOC{{H}_{2}}C{{H}_{2}}CH{{(C{{H}_{3}})}_{2}}+{{H}_{2}}O\) Ancol isoamylic Isoamyl axetat
VI. ỨNG DỤNG:
- Dung môi hữu cơ
- Trùng hợp vinyl axetat: chất dẻo hoặc thủy phân tạo poli(vinyl ancol)
- Trùng hợp metyl acrylat; metyl metacrylat: Thủy tinh hữu cơ
- Este có mùi thơm: Công nghiệp thực phẩm, mĩ phẩm
B. LIPIT
I. ĐỊNH NGHĨA
Lipit: Hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi hữu cơ không phân cực như ete, xăng dầu…
Chất béo (triglixerit hay triaxyl glixerol) là trieste của glixerol với axit béo
Axit béo: axit monoaxitcacboxylic có số C chẵn từ 12C ÷ 24C, không phân nhánh
+ No: axit panmitic (C15H31COOH; k = 1);
axit stearic (C17H35COOH; k = 1)
+ Không no: axit oleic (C17H33COOH; k = 2);
axit linoleic (C17H31COOH; k = 3)
II. TÍNH CHẤT VẬT LÝ
- Triglixerit chứa chủ yếu gốc axit béo no: rắn như mỡ động vật
- Triglixerit chứa chủ yếu gốc axit béo không no (dầu) : lỏng
- Chất béo: Nhẹ hơn nước, không tan trong nước, tan trong các dung môi hữu cơ như benzen, xăng, ete
III. TÍNH CHẤT HÓA HỌC
a. Thủy phân trong môi trường axit
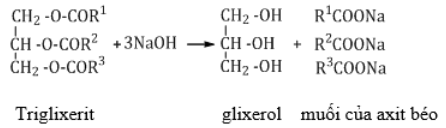
b. Thủy phân trong môi trường kiềm (phản ứng xà phòng hóa)
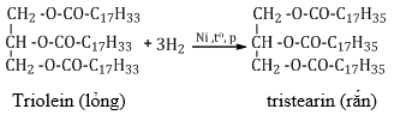
c. Phản ứng hiđro hóa
* Phương pháp giải
- BTKL: m xà phòng+ m glixerol = m chất béo + m NaOH
- Số trieste tối đa tạo bởi glixerol và n gốc axit béo: \(\frac{{{n}^{2}}(n+1)}{2}\)
- Xà phòng hóa chất béo bằng NaOH (KOH):
nchất béo = nglixerol = 1/3.nNaOH
- Hiệu suất \(H%=\frac{{{m}_{thuc.te}}}{{{m}_{lythuyet}}}.100%\)
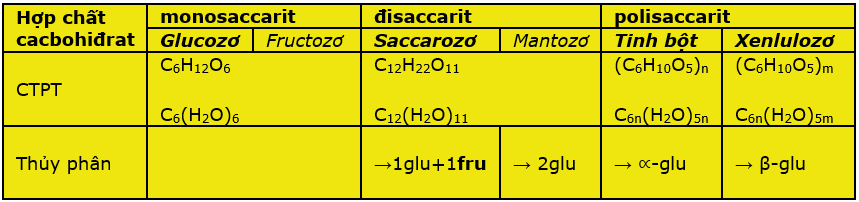
CHƯƠNG 2: CACBOHIDRAT
* Cacbohiđrat là những hợp chất hữu cơ tạp chức và thường có công thức chung là Cn(H2O)m
I. GLUCOZƠ : C6H12O6
1. Tính chất vật lý và trạng thái tự nhiên:
- Glucozơ là chất rắn, kết tinh không màu, dễ tan trong nước và có vị ngọt.
- Glucozơ có trong hầu hết các bộ phận của cây: lá, hoa, rễ, quả,… có trong cơ thể người và động vật (trong máu người chiếm 0,1%).
2. Cấu tạo phân tử:
* Cơ sở thực nghiệm xác định CTPT Glucozơ :
- Glucozơ + dd AgNO3/NH3 và dd Brom => Glucozơ có chứa nhóm CH=O.
- Glucozơ + Cu(OH)2 => Glucozơ có chứa nhiều nhóm –OH liền kề nhau.
- Glucozơ tạo este chứa 5 gốc axetat => Glucozơ chứa 5 nhóm –OH
- Khử hoàn toàn Glucozơ cho hexan => Glucozơ chứa mạch 6C không phân nhánh.
* Kết luận: Glucozơ là hợp chất tạp chức, mạch hở, ptử có chứa một nhóm CH=O và 5 nhóm OH liền kề nhau
\(\overset{6}{\mathop{C}}\,{{H}_{2}}OH-\overset{5}{\mathop{C}}\,HOH-\overset{4}{\mathop{C}}\,HOH-\overset{3}{\mathop{C}}\,HOH-\overset{2}{\mathop{C}}\,HOH-\overset{1}{\mathop{C}}\,H=O\) hay CH2OH[CHOH]4CH=O
3. Tính chất hóa học:
a. Tính chất của ancol đa chức:
- Tác dụng với Cu(OH)2:
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2H2O
dd xanh lam (phức)
- Phản ứng tạo este:
Glucozơ + (CH3CO)2O → este chứa 5 gốc axit axetic
b. Tính chất của anđehit :
- Oxi hóa glucozơ bằng dd AgNO3/NH3:
HOCH2[CHOH]4CH=O + 2AgNO3 + 3NH3 + H2O → HOCH2[CHOH]4COONH4 +2Ag↓ + 2NH4NO3
- Oxi hóa glucozơ bằng Cu(OH)2, to.
HOCH2[CHOH]4CH=O + 2Cu(OH)2 + NaOH \(\xrightarrow{{{t}^{o}}}\) HOCH2[CHOH]4COONa + Cu2O↓(đỏ gạch) + 3H2O
- Tác dụng với dung dịch Br2
HOCH2[CHOH]4CH=O + Br2 + H2O → HOCH2[CHOH]4COOH + HBr
- Khử glucozơ bằng hiđro:
HOCH2[CHOH]4CH=O + H2 \(\xrightarrow{Ni,{{t}^{o}}}\) HOCH2[CHOH]4CH2OH (sobitol)
c. Phản ứng lên men
C6H12O6 \(\xrightarrow{enzim,30-{{35}^{o}}C}\) 2C2H5OH + 2CO2
* Glucozơ là hợp chất vừa thể hiện tính chất của ancol đa chức và vừa thể hiện tính chất của andehit.
4. Điều chế và ứng dụng:
a. Điều chế: Thủy phân tinh bột.
(C6H10O5)n + nH2O \(\xrightarrow{{{H}^{+}},{{t}^{o}}}\) nC6H12O6
b. Ứng dụng: làm thức ăn quan trọng của con người, dùng cho phản ứng tráng gương và điều chế ancol etylic.
II. FRUCTOZƠ : C6H12O6
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH
- Lý tính: chất kết tinh, dễ tan trong nước, có vị ngọt,...
- Hóa tính:
+ td với Cu(OH)2 (tạo dd phức màu xanh lam)
+ cộng H2 (tạo poliancol)
+ Trong môi trường bazơ fructozơ chuyển thành glucozơ, nên fructozơ cũng cho được pứ với AgNO3/NH3 hay Cu(OH)2, to.
Fructozơ \(\overset{O{{H}^{-}}}{\mathop{\leftrightarrows }}\,\) Glucozơ
* Để phân biệt giữa glucozơ và fructozơ ta dùng dd brom vì glucozơ làm mất màu dd brom
III. SACCAROZƠ : C12H22O11
- Là loại đường phổ biến nhất, có trong nhiều loài thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt.
1. Tính chất vật lý: Là chất rắn kết tinh, không màu, không mùi, có vị ngọt, tan tốt trong nước.
2. Cấu trúc phân tử
- Saccarozơ là một đisaccarit được cấu tạo từ một gốc ∝-glucozơ và một gốc β-fructozơ LK với nhau qua nguyên tử oxi.
- Trong ptử saccarozơ có nhiều nhóm OH và không có nhóm chức CHO.
3. Tính chất hóa học:
- Có tính chất của ancol đa chức và có phản ứng thủy phân.
- Phân tử không có nhóm –CHO nên không có tính chất của anđehit
a. Phản ứng với Cu(OH)2 → dd màu xanh (to thường)
b. Phản ứng thủy phân: (môi trường axit, xt enzim)
C12H22O11 + H2O \(\xrightarrow{{{H}^{+}},{{t}^{o}}}\) C6H12O6 + C6H12O6.
Saccarozơ glucozơ fructozơ
4. Sản xuất và ứng dụng.
a. Sản xuất: Từ cây mía, củ cải đường, hoa thốt nốt.
(quy trình sản xuất: lưu ý SO2 dùng để tẩy trắng đường).
b. Ứng dụng:
- Làm đường ăn, làm nguyên liệu quan trọng trong công nghiệp thực phẩm, ...
- Dùng để pha chế một số thuốc trong dược phẩm.
* MANTOZƠ: đồng phân của saccarozơ. (đọc thêm)
Cấu tạo của mantozơ gồm 2 gốc α–glucozơ. Trong ptử có nhiều nhóm OH và có chứa chức CHO nên mantozơ có tính chất tương tự glucozơ, nhưng có thêm phản ứng thủy phân.
IV. TINH BỘT: (C6H10O5)n
1. Tính chất vật lý:
- Là chất rắn dạng bột vô định hình, không tan trong nước lạnh.
- Dung dịch tinh bột gọi là hồ tinh bột.
2. Cấu trúc phân tử:
- CTPT (C6H10O5)n gồm nhiều mắc xích ∝–glucozơ liên kết với nhau tạo thành 2 dạng: amilozơ (không nhánh) và amilopectin (có nhánh).
- TB được tạo thành trong cây xanh nhờ quá trình quang hợp.
6nCO2 + 5nH2O \(\xrightarrow{{{H}_{2}}O,as,clorophin}\) (C6H10O5)n + 6nO2
3. Tính chất hóa học
a. Phản ứng thủy phân:
(C6H10O5)n + nH2O \(\xrightarrow{{{H}^{+}},{{t}^{o}}}\) nC6H12O6
b. Phản ứng tạo màu với iot:
TB + iot → hợp chất màu xanh tím (nhận biết)
V. XENLULOZƠ: (C6H10O5)n
1. Tính chất vật lý, trạng thái tự nhiên
- Là chất rắn dạng sợi, màu trắng, không có mùi vị và không tan trong nước.
- Là thành phần chính tạo nên màng tế bào thực vật.
2. Cấu trúc phân tử
CTPT (C6H10O5)n hay [C6H7O2(OH)3]n gồm nhiều mắc xích β–glucozơ liên kết với nhau tạo thành mạch không phân nhánh có khối lượng phân tử rất lớn.
3. Tính chất hóa học
a. Phản ứng thủy phân:
(C6H10O5)n + nH2O \(\xrightarrow{{{H}^{+}},{{t}^{o}}}\) nC6H12O6
b. Phản ứng với axit nitric:
[C6H7O2(OH)3]n +3nHNO3 (đặc) \(\xrightarrow{{{H}_{2}}S{{O}_{4}},{{t}^{o}}}\) [C6H7O2(ONO2)3]n + 3nH2O
thuốc súng không khói
4. Ứng dụng: Kéo sợi dệt vải, giấy, tơ nhân tạo tơ visco, tơ axetat.
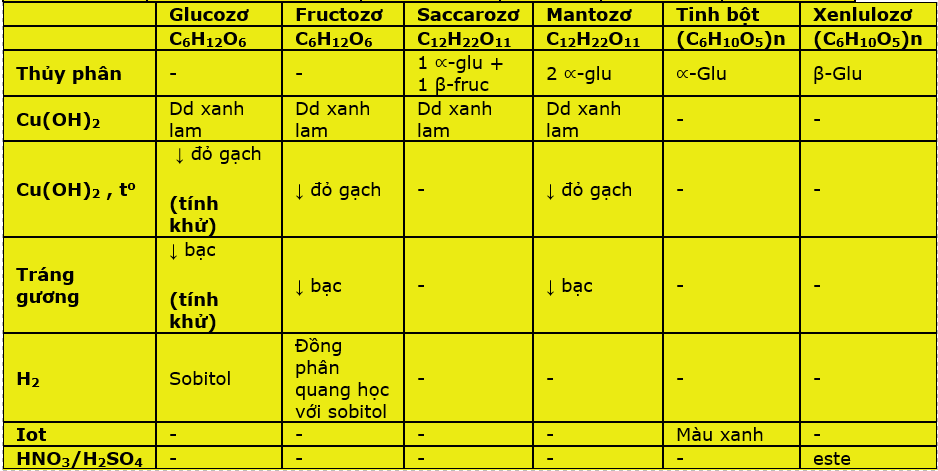
TỔNG KẾT
A. AMINCHƯƠNG 3: AMIN – AMINOAXIT – PEPTIT
I. KHÁI NIỆM, CÔNG THỨC, PHÂN LOẠI, ĐỒNG PHÂN VÀ DANH PHÁP
1. Khái niệm: Khi thay thế nguyên tử hidro trong phân tử NH3 bằng gốc hiđrocacbon ta được hợp chất amin. Ví dụ: CH3-NH2; CH3- NH-CH3
2. Công thức
a. Amin: CxHyNt điều kiện: 0 < y < 2x + 2 + t và y, t cùng chẳn hoặc cùng lẻ
b. Amin đơn chức: CxHyN điều kiện: 0 < y < 2x + 3
c. Amin no đơn chức, mạch hở : CnH2n+3N ( n ≥ 1)
3. Phân loại
a. Theo gốc hidrocacbon
* amin béo: CH3-NH2
* amin thơm: C6H5-NH2 (anilin)
b. Theo bậc amin:
* amin bậc I: R – NH2
* amin bậc II: R – NH – R’
* amin bậc III:
4. Đồng phân: Amin có đồng phân về mạch cacbon, vị trí nhóm chức, bậc amin. (C2H7N, C3H9N)
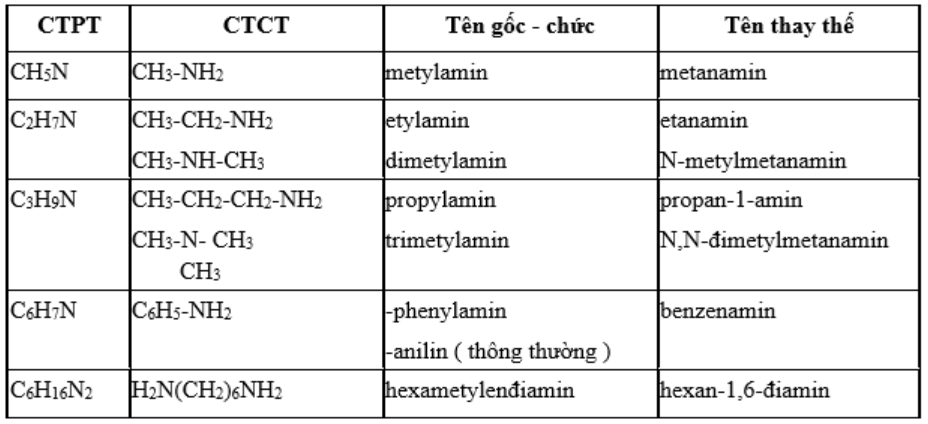
5. Danh pháp:
II. TÍNH CHẤT VẬT LÍ:
- Các amin CH3-NH2, (CH3)2-NH, (CH3)3N, C2H5-NH2 là các chất khí, mùi khai, tan nhiều trong nước.
- Anilin C6H5NH2 là chất lỏng, không mùi, ít tan trong nước, nặng hơn nước.
- Các amin đều rất độc
III. TÍNH CHẤT HÓA HỌC: Amin có tính bazơ tương tự NH3
1. Tính bazơ
a. Phản ứng với nước: CH3-NH2 + H2O → [CH3NH3]+ + OH-
* Các amin béo làm quỳ tím hóa xanh (nhận biết amin)
* C6H5NH2 (anilin) không làm đổi màu quỳ tím (do có tính bazơ rất yếu)
b. Phản ứng với axit: CH3-NH2(đặc) + HCl(đặc)→ [CH3NH3]+Cl- ( metyl amoni clorua)
C6H5NH2 HCl → [C6H5NH3]+Cl- ( phenyl amoni clorua)
c. So sánh tính bazơ của các amin:
(Rthơm)3N < (R thơm)2NH < RthơmNH2 < NH3 < Rno NH2 < (Rno)2NH < (Rno)3N
Chú ý: với gốc Rno càng cồng kềnh thì ảnh hưởng không gian của nó càng lớn làm cản trở quá trình H+ tiến lại gần nguyên tử N nên (Rno)2NH < (Rno)3N sẽ không còn đúng nữa.
2. Phản ứng thế ở nhân thơm của anilin (nhận biết anilin)
C6H5-NH2 + 3B2 → C6H2Br3NH2 (↓ trắng) + 3HBr
B. AMINO AXIT
I. KHÁI NIỆM
1. Amino axit là hợp chất hữu cơ tạp chức phân tử có chứa đồng thời nhóm amino (-NH2) và nhóm cacboxyl (-COOH)
2. Công thức: amino axit: R(NH2)n(COOH)m hoặc CxHyOzNt
3. Đồng phân: (C2H5O2N và C3H7O2N)
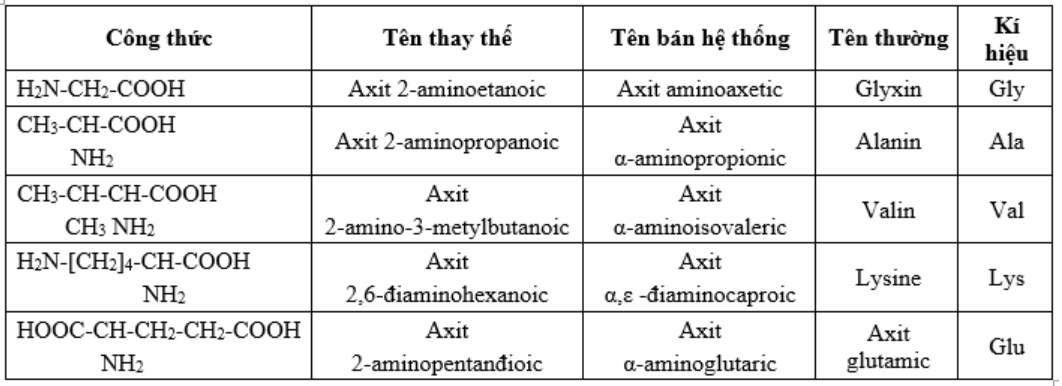
4. Danh pháp:
II. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT VẬT LÍ
- Phân tử có nhóm –COOH thể hiện tính axit
- Phân tử có nhóm –NH2 thể hiện tính bazơ
- Có sự tương tác tạo ra ion lưỡng cực:
H2N-R-COOH ↔ H3N+- R – COO-
- Amino axit là những hợp chất ion, ở điều kiện thường là chất rắn kết tinh, dễ tan trong nước.
III. TÍNH CHẤT HÓA HỌC
1. Tính chất lưỡng tính: Phản ứng với axit vô cơ mạnh và bazơ mạnh
HOOC-CH2-NH2 + HCl → HOOC-CH2-NH3Cl
H2N-CH2–COOH + NaOH → H2N–CH2–COONa + H2O
2. Tính axit, bazơ của dung dịch amino axit: R(NH2)n(COOH)m
+ Đối với hợp chất có dạng (NH2)xR(COOH)y
+ nếu x < y → dung dịch có môi trường axit→ quỳ chuyển đỏ
+ nếu x > y → dung dịch có môi trường bazơ→ quỳ chuyển xanh
+ nếu x = y → dung dịch có môi trường trung tính→ không đổi màu quỳ
+ Đối với hợp chất dạng: R(NH3Cl)x(COOH)y(NH2)z(COONa)t
+ Nếu x + y > z + t môi trường axit => quì sang đỏ
+ Nếu x + y < z + t môi trường bazo => quì sang xanh
+ Nếu x + y = z + t môi trường trung tính => không đổi màu quì
3. Phản ứng riêng của nhóm –COOH: phản ứng este hóa
NH2–CH2–COOH + C2H5OH ↔ H2N–CH2–COO-C2H5 + H2O
4. Phản ứng trùng ngưng:
nH2N-[CH2]5–COOH → -(-NH–[CH2]5–CO-)n- + nH2O
axit-ε-aminocaproic policaproamit (tơ capron)
C. PEPTIT VÀ PROTEIN
I. PEPTIT
1. Khái niệm
- Peptit: là loại hợp chất chứa từ 2 đến 50 gốc α-amino axit liên kết với nhau bởi các liên kết peptit
- Liên kết peptit: là liên kết -CO – NH- giữa hai đơn vị α- amino axit
- Nhóm –CO – NH-: được gọi là nhóm peptit
* Phân tử peptit chứa 2 gốc α-amino axit gọi là đipeptit (có 1 liên kết peptit)
* Phân tử peptit chứa 3 gốc α-amino axit gọi là tripeptit (có 2 liên kết peptit)
* Phân tử peptit chứa trên 10 gốc α-amino axit gọi là poli peptit
2. Tính chất hóa học
Phản ứng thủy phân (xt axit hay bazơ) → các α - amino axit.
Phản ứng màu: peptit + Cu(OH)2/NaOH → hợp chất màu tím (phức chất của đồng)
II. PROTEIN
1. Khái niệm: Protein là những polipeptit cao phân tử có phân tử khối từ vài chục nghìn đến vài triệu.
2. Phân loại: 2 loại
Protein đơn giản: khi thủy phân cho hỗn hợp các - amino axit
Protein phức tạp: là loại protein được tạo thành từ prtein đơn giản và phi protein.
3. Tính chất:
Tính chất đông tụ: các protein hình cầu tan được trong nước tạo thành dung dịch keo và đông tụ khi đun nóng.
Vd: Sự đông tụ của lòng trắng trứng khi đun nóng
Phản ứng thủy phân: (xt axit hay bazơ) tạo thành α-amino axit
Protein \(\xrightarrow{xt}\) các chuỗi peptit \(\xrightarrow{xt}\) các α-amino axit
Phản ứng màu với Cu(OH)2/NaOH tạo màu tím đặc trưng để phân biệt protein.
Protein + Cu(OH)2 \(\xrightarrow{O{{H}^{-}}}\) hợp chất màu tím => Phản ứng nhận biết lòng trắng trứng
CHƯƠNG 4: POLIME
I. ĐẠI CƯƠNG POLIME
1. Khái niệm: Polime là hợp chất có phân tử khối lớn do nhiều đơn vị cơ sở gọi là mắt xích liên kết với nhau tạo nên.
Ví dụ: (–CH2-CH2–)n , (–NH[CH2]5–CO–)n
Polietilen Nilon-6
Với: + n là hệ số polime hóa hay độ polime hóa.
+ Các phân tử CH2=CH2, H2N[CH2]5COOH, ... phản ứng với nhau tạo nên polime thì gọi là monome.
+ Tên của polime = poli + tên của monome.
2. Phân loại:
- Polime thiên nhiên: tinh bột, xenlulozơ, cao su, ...
- Polime tổng hợp (được trùng hợp, trùng ngưng): polietilen, cao su buna, 6,6, ...
- Polime bán tổng hợp: tơ visco, tơ axetat, ...
3. Đặc điểm cấu trúc: Polime là những chất phân tử khối cao
- Mạch không nhánh: PE, PVC, xenlulozơ, amilozơ.
- Mạch có nhánh: amilopectin, glicogen, …
- Mạch mạng không gian: CS lưu hóa, nhựa bakelit.
4. Tính chất vật lý: Không bay hơi, không có nhiệt độ nóng chảy cố định, khó hòa tan, cách điện, cách nhiệt, một số có tính dẻo, tính đàn hồi, …
5. Tính chất hóa học: (đọc thêm)
Polime có những pứ phân cắt mạch, giữ nguyên mạch và phát triển mạch cacbon.
6. Phương pháp điều chế:
a. Phản ứng trùng hợp: là quá trình kết hợp nhiều phân tử nhỏ (momome) giống nhau hay tương tự nhau thành ptử lớn (polime).
* Điều kiện: Cấu tạo monome phải có liên kết bội hoặc vòng kém bền.
b. Phản ứng trùng ngưng: là quá trình kết hợp nhiều ptử nhỏ (momome) giống nhau hay tương tự nhau thành ptử lớn (polime) đồng thời giải phóng những ptử nhỏ khác (H2O, HCl, ...).
* Điều kiện: Cấu tạo monome phải có ít nhất 2 nhóm chức có khả năng pứ.
Ví dụ: HOOC-C6H4-COOH; OH-CH2-CH2–OH
II. VẬT LIỆU POLIME
1. Chất dẻo: là những vật liệu polime có tính dẻo (PE, PVC, thủy tinh hữu cơ, PPF)
a) Polietilen. (PE): (-CH2 - CH2-)n
nCH2=CH2 \(\xrightarrow{xt}\) ( CH2 - CH2 )n.
b) Polivinyl clorua. (PVC): (-CH2 – CHCl-)n
c) Poli(metyl metacrylat): thủy tinh hữu cơ plexiglas
d) Poli(phenol-fomanđehit) (PPF)
2. Tơ: Tơ là những vật liệu polime hình sợi dài, bền, có mạch không phân nhánh.
Phân loại:
- Tơ thiên nhiên: bông, sợi, len, lông cừu, tơ tằm, …
- Tơ hóa học: + Tơ tổng hợp: nilon-6,6, capron, nitron hay olon, ...
* Nilon-6,6:
NH2-[CH2]5-NH2 + HOOC-[CH2]4-COOH → (-NH-[CH2]5-NH-OC-[CH2]4-CO-)n + 2nH2O
Hexametylenđiamin axit ađipic (thuộc loại tơ poliamit)
* Nilon-7: tơ enang.
NH2-[CH2]6-COOH → (-NH-[CH2]6 –CO-)n + H2O
* Tơ nitron hay tơ olon:
nCH2=CHCN \(\xrightarrow{ROOR,{{t}^{0}}}\) ( CH2 - CHCN )n
acrilonitrin poli(acrilonitrin)
+ Tơ bán tổng hợp: visco, xenlulozơ axetat, ...
3. Cao su: Cao su là loại vật liệu polime có tính đàn hồi.
Phân loại:
- Cao su thiên nhiên: (C5H8)n có tên poliisopren
- Cao su tổng hợp: Cao su buna, cao su buna-S, cao su buna-N
4. Vật liệu compozit: là vật liệu hỗn hợp gồm ít nhất hai thành phần phân tán vào nhau mà không tan vào nhau.
5. Keo dán tổng hợp (đọc thêm): Keo dán là loại vật liệu có khả năng kết dính mà không làm biến đổi bản chất hóa học. Vd: Nhựa vá săm, keo dán epoxi, keo dán ure-fomanđehit.
CHƯƠNG 5: ĐẠI CƯƠNG KIM LOẠI
1. Tính chất vật lý
- Khối lượng riêng: Os lớn nhất, Li nhỏ nhất
- Nhiệt độ nóng chảy: W lớn nhất, Hg nhỏ nhất
- Tính cứng: Cr cứng nhất, Cs nhỏ nhất
Tính chất hóa học: Tính khử:
- Tác dụng với phi kim:
|
3Fe + 2O2 \(\xrightarrow{{{t}^{{}^\circ }}}\) Fe3O4 (FeO.Fe2O3) |
|
|
2Fe + 3Cl2 \(\xrightarrow{{{t}^{{}^\circ }}}\) 2FeCl3 2Fe + 3Br2 \(\xrightarrow{{{t}^{{}^\circ }}}\) 2FeBr3 |
|
- Tác dụng với axit:
+) H2SO4 loãng, HCl + kim loại trước H → H2↑ + muối (kim loại có hóa trị thấp)
+) H2SO4 đặc nóng, HNO3 + hầu hết các kim loại ( trừ Au,Pt) tạo muối (kim loại có hóa trị cao) + sản phẩm khử + H2O
3Cu + 8HNO3 (l) \(\xrightarrow{{}}\)3Cu(NO3)2 + 2NO↑ + 4H2O
\(2\overset{0}{\mathop{Fe}}\,+6{{H}_{2}}S{{O}_{4}}\xrightarrow{{{t}^{{}^\circ }}}\overset{+3}{\mathop{Fe}}\,{{}_{2}}{{(S{{O}_{4}})}_{3}}+3S{{O}_{2}}+6{{H}_{2}}O\)
* Fe, Al, Cr thụ động (không phản ứng) với HNO3 đặc nguội, H2SO4 đặc nguội
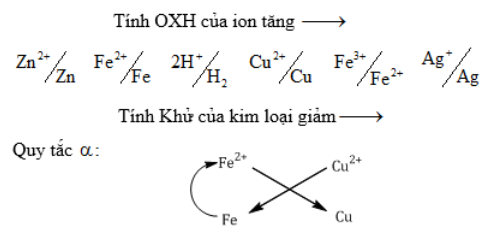
2. Dãy điện hóa:
* Tác dụng với\(\overset{+1}{\mathop{H}}\,{{}_{2}}O\): Kim loại kiềm, Ca, Ba, Sr (t0 thường)
Na + H2O \(\xrightarrow{{}}\) NaOH + H2↑
Ba + 2H2O \(\xrightarrow{{}}\) Ba(OH)2 + H2↑
Điều chế kim loại:
\(\underbrace{K,Na,Ca,Mg}_{(1)},\underbrace{Al}_{(2)},\underbrace{Zn,Fe,Ni,Sn,Pb,H,Cu,Hg,Ag,Pt,Au}_{(3)}\)
(1): Điện phân nóng chảy: \(MC{{l}_{n}}\xrightarrow{dpnc}M+\frac{n}{2}C{{l}_{2}}\)
(2): Điện phân nóng chảy: \(2A{{l}_{2}}{{O}_{3}}\xrightarrow[N{{a}_{3}}Al{{F}_{6}}]{dpnc}4Al+3{{O}_{2}}\)
(3): Điện phân dung dịch, thủy luyện, nhiệt luyện
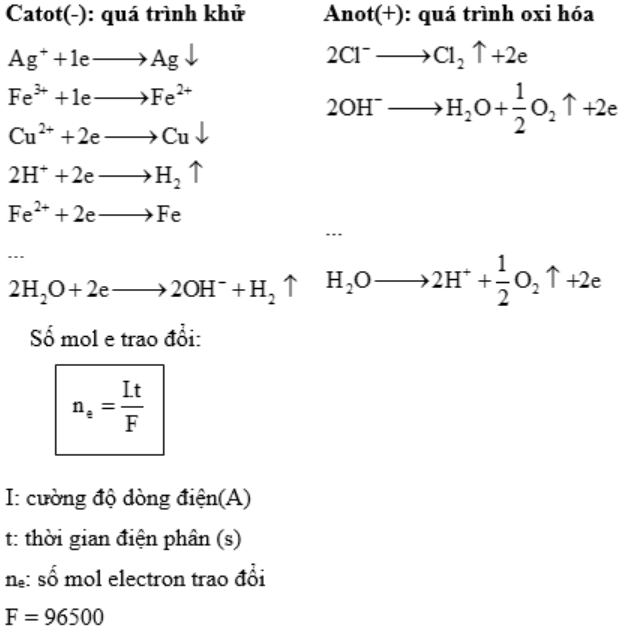
Điện phân dung dịch:
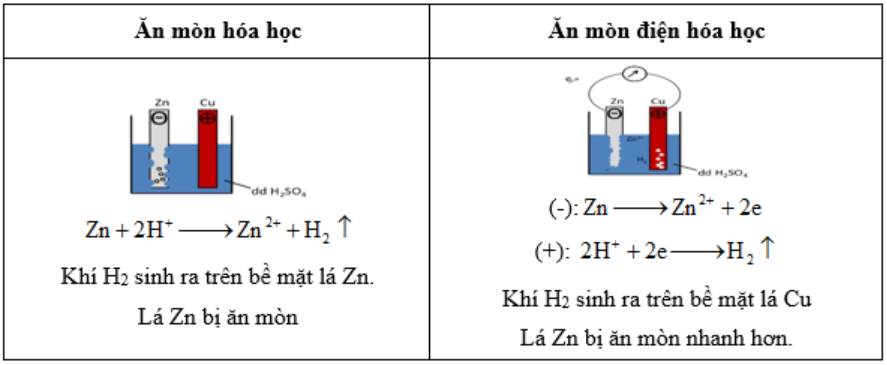
Ăn mòn kim loại:
Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường (quá trình OXH – Khử)
Điều kiện xảy ra ăn mòn điện hóa học:
- Các điện cực khác nhau về bản chất.
- Các điện cực tiếp xúc trực tiếp hoặc gián tiếp.
- Các điện cực cùng tiếp xúc với dung dịch điện ly.
Bảo vệ kim loại:
- Phương pháp bảo vệ bề mặt: sơn, mạ, bôi dầu mỡ…
- Phương pháp điện hóa: dùng kim loại mạnh hơn làm vật hi sinh ví dụ: dùng Zn bảo vệ Fe.
Loigiaihay.com
Các bài khác cùng chuyên mục
- Đề số 10 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết





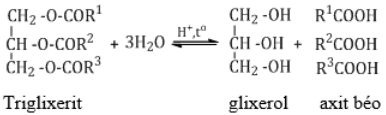
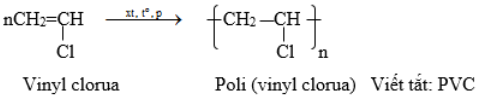
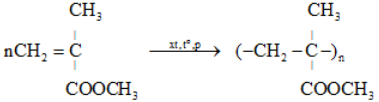
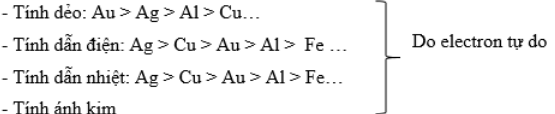
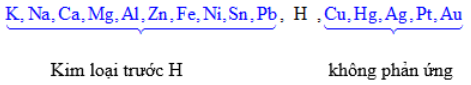
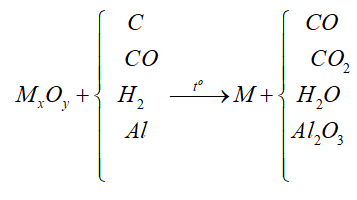








Danh sách bình luận