 Giải bài tập hóa học 12, Hóa 12 - Để học tốt hóa học 12
Giải bài tập hóa học 12, Hóa 12 - Để học tốt hóa học 12
 Bài 12. Luyện tập: Cấu tạo và tính chất của amin, amino..
Bài 12. Luyện tập: Cấu tạo và tính chất của amin, amino..
Lý thuyết cấu tạo và tính chất của amin, amino axit và protein.
Kiến thức trọng tâm
A. AMIN
I. KHÁI NIỆM, CÔNG THỨC, PHÂN LOẠI, ĐỒNG PHÂN VÀ DANH PHÁP
1. Khái niệm: Khi thay thế nguyên tử hidro trong phân tử NH3 bằng gốc hiđrocacbon ta được hợp chất amin. Ví dụ: CH3-NH2; CH3- NH-CH3
2. Công thức
a. Amin: CxHyNt điều kiện: 0 < y < 2x + 2 + t và y, t cùng chẳn hoặc cùng lẻ
b. Amin đơn chức: CxHyN điều kiện: 0 < y < 2x + 3
c. Amin no đơn chức, mạch hở : CnH2n+3N ( n ≥ 1)
3. Phân loại
a. Theo gốc hidrocacbon
* amin béo: CH3-NH2
* amin thơm: C6H5-NH2 (anilin)
b. Theo bậc amin:
* amin bậc I: R – NH2
* amin bậc II: R – NH – R’
* amin bậc III: $\begin{array}{*{35}{l}} R-\underset{|}{\mathop{N}}\,-{{R}^{'}} \\ ~\,\,\,\,\,\,\,\,\,\,{{R}^{''}} \\\end{array}$
4. Đồng phân: Amin có đồng phân về mạch cacbon, vị trí nhóm chức, bậc amin. (C2H7N, C3H9N)
5. Danh pháp:
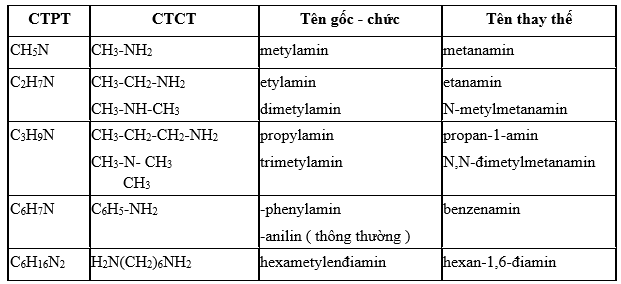
II. TÍNH CHẤT VẬT LÍ:
- Các amin CH3-NH2, (CH3)2-NH, (CH3)3N, C2H5-NH2 là các chất khí, mùi khai, tan nhiều trong nước.
- Anilin C6H5NH2 là chất lỏng, không mùi, ít tan trong nước, nặng hơn nước.
- Các amin đều rất độc
III. TÍNH CHẤT HÓA HỌC: Amin có tính bazơ tương tự NH3
1. Tính bazơ
a. Phản ứng với nước: CH3-NH2 + H2O $\underset{{}}{\overset{{}}{\longleftrightarrow}}$ [CH3NH3]+ + OH-
* Các amin béo làm quỳ tím hóa xanh (nhận biết amin)
* C6H5NH2 (anilin) không làm đổi màu quỳ tím (do có tính bazơ rất yếu)
b. Phản ứng với axit: CH3-NH2 + HCl → [CH3NH3]+Cl- ( metyl amoni clorua)
đặc đặc khói trắng => nhận biết
C6H5NH2 HCl → [C6H5NH3]+Cl- ( phenyl amoni clorua)
c. So sánh tính bazơ của các amin:
(Rthơm)3N < (R thơm)2NH < RthơmNH2 < NH3 < Rno NH2 < (Rno)2NH < (Rno)3N
Chú ý: với gốc Rno càng cồng kềnh thì ảnh hưởng không gian của nó càng lớn làm cản trở quá trình H+ tiến lại gần nguyên tử N nên (Rno)2NH < (Rno)3N sẽ không còn đúng nữa.
2. Phản ứng thế ở nhân thơm của anilin (nhận biết anilin)
C6H5-NH2 + 3B2 → C6H2Br3NH2 (↓ trắng) + 3HBr
B. AMINO AXIT
I. KHÁI NIỆM
1. Amino axit là hợp chất hữu cơ tạp chức phân tử có chứa đồng thời nhóm amino (-NH2) và nhóm cacboxyl (-COOH)
2. Công thức: amino axit: R(NH2)n(COOH)m hoặc CxHyOzNt
3. Đồng phân: (C2H5O2N và C3H7O2N)
4. Danh pháp:
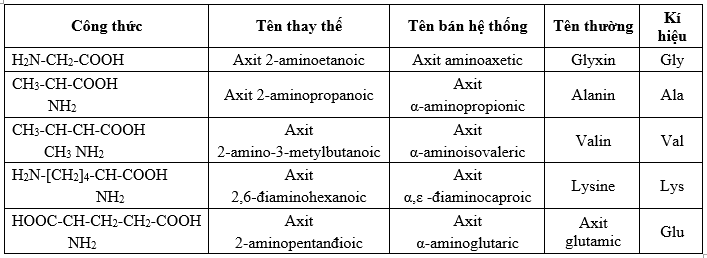
II. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT VẬT LÍ
- Phân tử có nhóm –COOH thể hiện tính axit
- Phân tử có nhóm –NH2 thể hiện tính bazơ
- Có sự tương tác tạo ra ion lưỡng cực: H2N-R-COOH $\underset{{}}{\overset{{}}{\longleftrightarrow}}$ H3N+- R – COO-
- Amino axit là những hợp chất ion, ở điều kiện thường là chất rắn kết tinh, dễ tan trong nước.
III. TÍNH CHẤT HÓA HỌC
1. Tính chất lưỡng tính: Phản ứng với axit vô cơ mạnh và bazơ mạnh
HOOC-CH2-NH2 + HCl → HOOC-CH2-NH3Cl
H2N-CH2–COOH + NaOH → H2N–CH2–COONa + H2O
2. Tính axit, bazơ của dung dịch amino axit: R(NH2)n(COOH)m
+ Đối với hợp chất có dạng (NH2)xR(COOH)y
+ nếu x < y → dung dịch có môi trường axit→ quỳ chuyển đỏ
+ nếu x > y → dung dịch có môi trường bazơ→ quỳ chuyển xanh
+ nếu x = y → dung dịch có môi trường trung tính→ không đổi màu quỳ
+ Đối với hợp chất dạng: R(NH3Cl)x(COOH)y(NH2)z(COONa)t
+ Nếu x + y > z + t môi trường axit => quì sang đỏ
+ Nếu x + y < z + t môi trường bazo => quì sang xanh
+ Nếu x + y = z + t môi trường trung tính => không đổi màu quì
3. Phản ứng riêng của nhóm –COOH: phản ứng este hóa
NH2–CH2–COOH + C2H5OH $\underset{{}}{\overset{{}}{\longleftrightarrow}}$ H2N–CH2–COO-C2H5 + H2O
4. Phản ứng trùng ngưng:
nH2N-[CH2]5–COOH → -(-NH–[CH2]5–CO-)n- + nH2O
axit-ε-aminocaproic policaproamit (tơ capron)
C. PEPTIT VÀ PROTEIN
I. PEPTIT
1. Khái niệm
- Peptit: là loại hợp chất chứa từ 2 đến 50 gốc α-amino axit liên kết với nhau bởi các liên kết peptit
- Liên kết peptit: là liên kết -CO – NH- giữa hai đơn vị α- amino axit
- Nhóm –CO – NH-: được gọi là nhóm peptit
* Phân tử peptit chứa 2 gốc α-amino axit gọi là đipeptit (có 1 liên kết peptit)
* Phân tử peptit chứa 3 gốc α-amino axit gọi là tripeptit (có 2 liên kết peptit)
* Phân tử peptit chứa trên 10 gốc α-amino axit gọi là poli peptit
2. Tính chất hóa học
Phản ứng thủy phân (xt axit hay bazơ) → các α - amino axit.
Phản ứng màu: peptit + Cu(OH)2/NaOH → hợp chất màu tím (phức chất của đồng)
II. PROTEIN
1. Khái niệm: Protein là những polipeptit cao phân tử có phân tử khối từ vài chục nghìn đến vài triệu.
2. Phân loại: 2 loại
Protein đơn giản: khi thủy phân cho hỗn hợp các - amino axit
Protein phức tạp: là loại protein được tạo thành từ prtein đơn giản và phi protein.
3. Tính chất:
Tính chất đông tụ: các protein hình cầu tan được trong nước tạo thành dung dịch keo và đông tụ khi đun nóng.
Vd: Sự đông tụ của lòng trắng trứng khi đun nóng
Phản ứng thủy phân: (xt axit hay bazơ) tạo thành α-amino axit
Protein $\xrightarrow{xt}$ các chuỗi peptit $\xrightarrow{xt}$ các α-amino axit
Phản ứng màu với Cu(OH)2/NaOH tạo màu tím đặc trưng để phân biệt protein.
Protein + Cu(OH)2 $\xrightarrow{O{{H}^{-}}}$hợp chất màu tím => Phản ứng nhận biết lòng trắng trứng
Các bài khác cùng chuyên mục
- Đề số 10 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 12 có đáp án và lời giải chi tiết












Danh sách bình luận