Lý thuyết Một số bazơ quan trọng
Natri hiđroxit là chất rắn không màu...
A. NATRI HIĐROXIT (NaOH)
I. Tính chất vật lí
- Natri hiđroxit là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt.
- Dung dịch NaOH có tính nhờn, làm bục vải giấy và ăn mòn da. Khi sử dụng NaOH phải hết sức cẩn thận.
II. Tính chất hóa học
Natri hiđroxit có đầy đủ tính chất của một bazơ tan (kiềm).
1. Làm đổi màu chất chỉ thị.
- Dung dịch NaOH làm đổi màu qùy tím thành xanh.
- Dung dịch phenolphatalein không màu thành màu đỏ.
2. Tác dụng với axit → muối + nước (phản ứng trung hòa)
Thí dụ:
NaOH + HCl → NaCl + H2O
2NaOH + H2SO4 → Na2SO4 + H2O
3. Tác dụng với oxit axit → muối + nước
Thí dụ:
2NaOH + CO2 → Na2CO3 + H2O
2NaOH + SO2 → Na2SO3 + H2O
(khi NaOH tác dụng với \(CO_2, SO_2\) còn có thể tạo ra muối axit NaHCO3, NaHSO3)
4. Tác dụng với dung dịch muối.
Thí dụ:
2NaOH + CuSO4 → Na2SO4 + Cu(OH)2↓
III. Ứng dụng
Natri hiđroxit có nhiều ứng dụng trong đời sống và trong sản xuất. Nó được dùng trong:
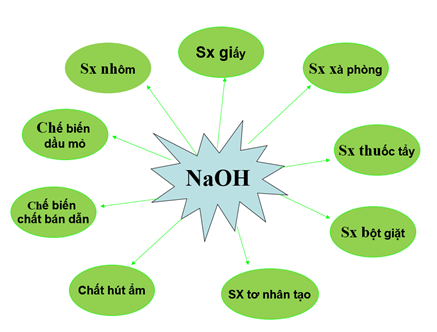
IV. Sản xuất Natri hiđroxit
- Trong công nghiệp, NaOH được điều chế bằng cách điện phân dung dịch NaCl
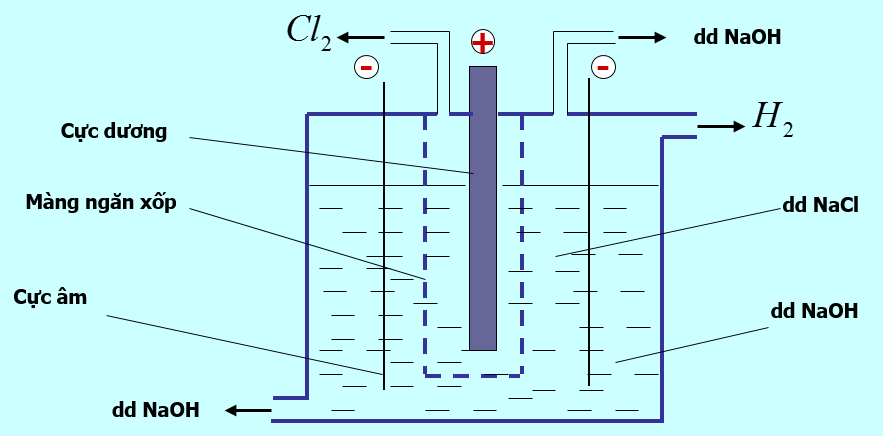
- Phương trình điện phân:
2NaCl + 2H2O $\xrightarrow[mang\,\,ngan\,\,xop]{đpdd}$ 2NaOH + H2 + Cl2
- Tác dụng của màng ngăn xốp: không cho khí clo thoát ra tác dụng với dung dịch NaOH vì xảy ra phản ứng:
Cl2 + 2NaOH → NaCl + NaClO + H2O
B. CANXI HIĐROXIT Ca(OH)2
I. Tính chất hóa học Ca(OH)2
- Ca(OH)2 có tính chất hóa học của một bazơ tan.
1. Làm đổi màu chất chỉ thị
- Làm đổi màu qùy tím thành xanh.
- Dung dịch phenolphatalein không màu thành màu đỏ.
2. Ca(OH)2 + axit → muối + nước (phản ứng trung hòa)
Phương trình hóa học :
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Ca(OH)2 + H2SO4 → CaSO4 + H2O
3. Dung dịch Ca(OH)2 + oxit axit → muối + nước
Phương trình hóa học
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Ca(OH)2 + SO2 → CaSO3↓ + H2O
4. Ca(OH)2 + dung dịch muối → muối mới + bazo mới
Phương trình hóa học
Ca(OH)2 + FeCl2 → Fe(OH)2↓ + CaCl2
II. Ứng dụng
- Làm vật liệu trong xây dựng.
- Khử chua đất trồng trọt.
- Khử độc các chất thải công nghiệp, diệt trùng chất thải sinh hoạt và xác chết động vật…
III. Thang PH
- pH = 7: Dung dịch là trung tính Thí dụ : nước cất có pH = 7
- pH < 7: Dung dịch có tính axit, pH càng nhỏ độ axit càng lớn.
- pH > 7: Dung dịch có tính bazơ, pH càng lớn độ bazơ càng lớn.
Sơ đồ tư duy: Một số bazo quan trọng
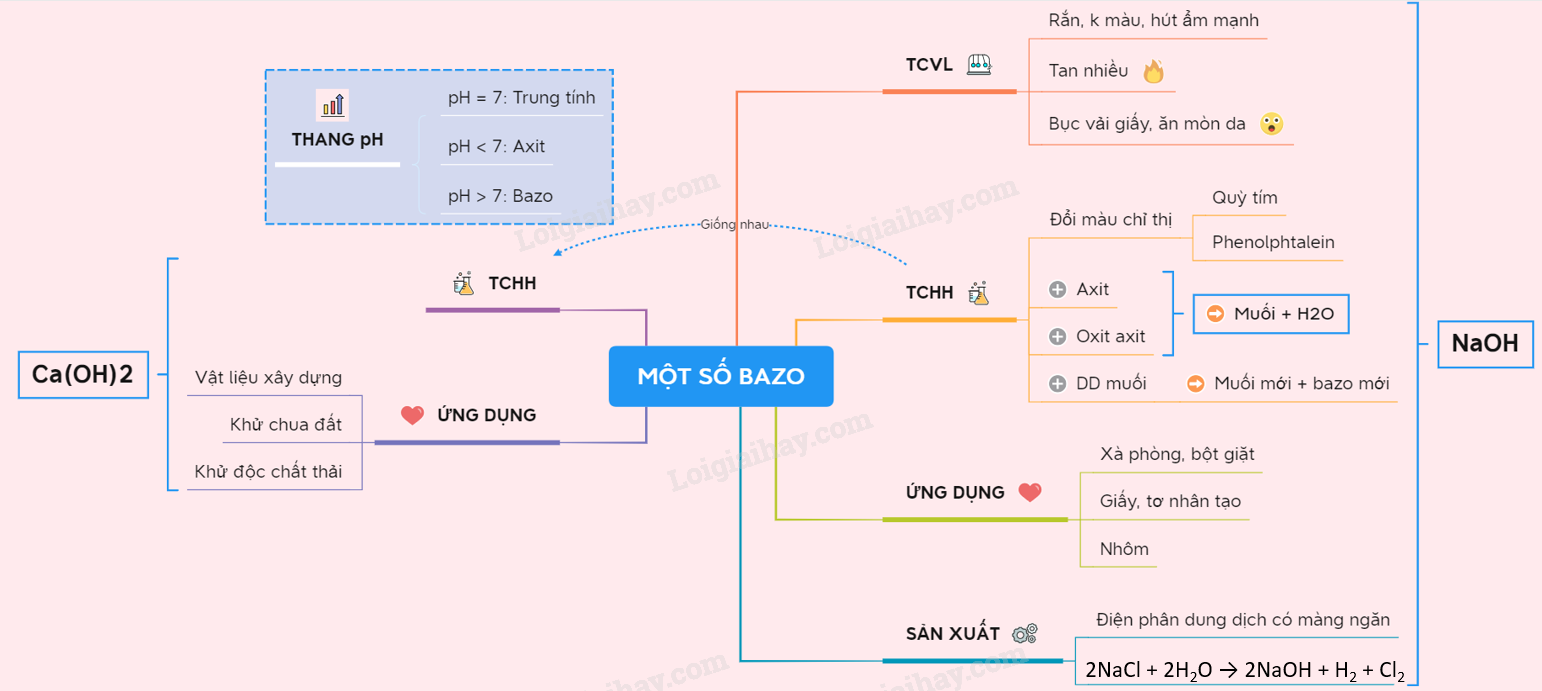
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu













Danh sách bình luận