Giải đề thi hết học kì II năm học 2017 - 2018 phòng giáo dục thành phố Cao Bằng
Đề thi hết học kì II năm học 2017 - 2018 phòng giáo dục thành phố Cao Bằng có đáp án và lời giải chi tiết
Đề bài
Câu 1 : Nếu hiện tượng và viết phương trình hóa học cho các thí nghiệm sau:
a) Dẫn khí axetilen qua ống thủy tinh đầu vuốt nhọn rồi đốt cháy khí axetilen thoát ra.
b) Dẫn khí etilen qua dung dịch brom màu da cam.
Câu 2 : Viết phương trình hóa học biểu diễn các chuyển đổi sau (Ghi rõ điều kiện của các phản ứng nếu có)
\({{C}_{6}}{{H}_{12}}{{O}_{6}}\xrightarrow{(1)}{{C}_{2}}{{H}_{5}}OH\xrightarrow{(2)}C{{H}_{3}}COO{{C}_{2}}{{H}_{5}}\xrightarrow{(4)}C{{H}_{3}}COONa\)
Câu 3 : Khi xác định công thức của các chất hữu cơ A và B, người ta thấy công thức phân tử A là C2H6O, còn công thức phân tử của B là C2H4O2. Để chứng minh A là rượu etylic, B là axit axetic cần phải làm thêm những thí nghiệm nào? Viết các phương trình phản ứng hóa học minh họa (nếu có).
Câu 4 : Theo kinh nghiệm dân gian truyền lại: Khi côn trùng (ong, kiến...) đốt, ta thường lấy nước vôi bôi vào vết đốt thì vết thương sẽ mau lành và giảm cảm giác ngứa rát. Em hãy giải thích vì sao khi bôi nước vôi vào chỗ côn trùng đốt sẽ đỡ đau? Viết phương trình phản ứng hóa học minh họa (nếu có)
Câu 5 : Đốt cháy 6 gam chất hữu cơ A, thu được 8,96 lít CO2 (ở đktc) và 10,8 gam H2O.
a) Trong chất hữu cơ A có những nguyên tố nào?
b) Biết tỉ khối của A so với hidro là 15. Tìm công thức phân tử và gọi tên chất hữu cơ A.
c) Viết công thức cấu tạo của A và cho biết A có làm mất màu dung dịch brom không? Vì sao?
d) Viết phương trình hóa học của A với clo khi có ánh sáng
(Cho: H = 1; C = 12; O =16)
-------------HẾT--------------
Lời giải chi tiết
Câu 1:
Phương pháp:
Dựa vào kiến thức được học về axetilen và etilen trong sgk hóa 9
Hướng dẫn giải:
a) Hiện tượng: Axetilen cháy trong khí với ngọn lửa sáng, tỏa nhiều nhiệt.
PTHH: 2C2H2(k) + 5O2(k) \(\xrightarrow{{{t}^{0}}}\) 4CO2 (k) + 2H2O (h)
b) Hiện tượng: Dung dịch brom bị mất màu da cam
PTHH: CH ≡ CH (k) + Br2 (dd) → CHBr2 − CH2Br (l)
màu da cam không màu
Câu 2:
Phương pháp:
Dựa vào kiến thức được học về chương 5: dẫn xuất của hidrocacbon - polime
Hướng dẫn giải:
Phương trình hóa học xảy ra các phản ứng là:
Câu 3:
Phương pháp:
Chứng minh A là ancol etylic, lấy chất phản ứng với A để chứng minh có nhóm -OH
Chứng minh B là axit axetic,lấy chất phản ứng với B để chứng minh có nhóm -COOH
Hướng dẫn giải:
Cho A tác dụng với natri nếu có sủi bọt khí ta chứng minh được A có nhóm OH, vậy A là rượu etylic:
PTHH: 2C2H5OH + 2Na → 2C2H5ONa + H2↑
Để chứng minh B là axit axetic, ta cho mẩu quỳ tím vào chất B, nếu quỳ tím chuyển sang màu đỏ → B là axit axetic.
Chú ý: Để chứng minh B là axit axetic ta có thể dùng kim loại Mg, Zn...hoặc muối cacbonat hoặc hòa tan oxit kim loại. Sau đó viết PTHH xảy ra
Câu 4:
Phương pháp:
Dựa vào kiến thức hiểu biết thực tế
Hướng dẫn giải:
Do trong nọc ong, kiến và một số côn trùng khác có axit fomic. Nước vôi là bazơ, nên trung hòa axit làm ta đỡ đau.
PTHH: 2HCOOH + Ca(OH)2 → (HCOO)2Ca + 2H2O
Câu 5:
Phương pháp:
a) Dựa vào số mol CO2 tính được khối lượng C trong A
Dựa vào khối lượng H2O tính được khối lượng H trong A
Nếu mA = mC + mH thì A chỉ chứa nguyên tố C và H
Nếu mA > mC + mH thì A chứa các nguyên tố là C, H và O
b) Tìm công thức đơn giản nhất của A, sau đó có tỉ khối của A với H2 tìm được phân tử khối của A
có phân tử khối suy ra được CTPT của A
c) Viết CTCT của A, nếu A có chứa liên kết đôi, ba thì sẽ làm mất màu dd nước brom, còn nếu A chỉ chứa liên kết đơn thì sẽ không làm mất màu dd nước Br2
d) Dựa vào phản ứng thế của metan với Cl2 viết tương tự
Hướng dẫn giải:
Số mol của CO2 ở đktc là:
\({n_{C{O_2}}}(dktc) = \frac{{8,96}}{{22,4}} = 0,4\,(mol)\)
Số mol của H2O là:
\({n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,(mol)\)
Khối lượng C có trong A là:
mC = 12×nCO2 = 12×0,4 = 4,8 (g)
Khối lượng H có trong A là:
mH = 2 ×nH2O = 2×0,6 = 1,2 (g)
Ta thấy mC + mH = 4,8 + 1,2 = 6 = mA
Vậy công thức phân tử của hidrocacbon A chỉ chứa nguyên tố C và H
b) Gọi công thức phân tử của A là CxHy (x,y € N*)
Ta có tỉ lệ:
\(x:y = \frac{{{m_C}}}{{{M_C}}}:\frac{{{m_H}}}{{{M_H}}} = \frac{{4,8}}{{12}}:\frac{{1,2}}{1} = 1:3\)
=> công thức tổng quát của A là: (CH3)n (n € N*)
Biết dA/H2 = 15 => MA = 15×MH2 = 15×2 = 30 (g/mol)
=> 15n = 30 => n = 2
Vậy, công thức phân tử của hidrocacbon A là C2H6 (etan)
c) Công thức cấu tạo của A: CH3-CH3
Chất A không làm mất màu dung dịch brom vì A chỉ có liên kết đơn trong phân tử
d) Phương trình hóa học:
C2H6 + Cl2 .\(\xrightarrow{as}\) C2H5Cl + HCl
Loigiaihay.com
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu





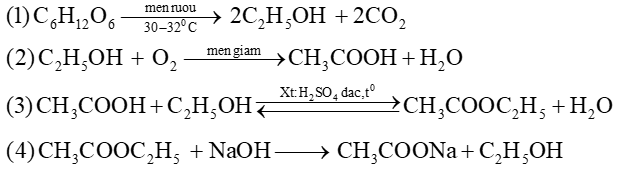







Danh sách bình luận