Đề thi giữa kì 1 Hóa 11 Cánh diều - Đề số 8
Cân bằng hóa học liên quan đến loại phản ứng
Đề bài
Cân bằng hóa học liên quan đến loại phản ứng
-
A.
không thuận nghịch.
-
B.
thuận nghịch.
-
C.
một chiều.
-
D.
oxi hóa – khử.
Điền vào khoảng trống trong câu sau bằng cụm từ thích hợp: “Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận... tốc độ phản ứng nghịch”.
-
A.
lớn hơn
-
B.
bằng
-
C.
nhỏ hơn
-
D.
Khác
Khi phản ứng thuận nghịch ở trạng thái cân bằng thì nó
-
A.
không xảy ra nữa.
-
B.
vẫn tiếp tục xảy ra.
-
C.
chỉ xảy ra theo chiều thuận.
-
D.
chỉ xảy ra theo chiều nghịch.
Chất nào sau đây là chất điện li?
-
A.
C6H6.
-
B.
NaCl.
-
C.
C2H5OH.
-
D.
C6H12O6.
Dung dịch chất nào sau đây có khả năng dẫn điện?
-
A.
C12H22O11.
-
B.
AlCl3
-
C.
C2H5OH.
-
D.
C6H12O6.
Chất nào sau đây là chất điện li mạnh?
-
A.
HCl.
-
B.
Fe(OH)2.
-
C.
H3PO4.
-
D.
H2S.
Phân tử Nitrogen có cấu tạo
-
A.
N≡N.
-
B.
N=N.
-
C.
N-N.
-
D.
N→N.
Trong hợp chất Nitrogen có các mức oxi hóa nào sau đây?
-
A.
-3, +3, +5.
-
B.
-3, 0, +3, +5.
-
C.
3, +1, +2, +3, +4, +5.
-
D.
-3, 0, +1, +2, +3, +4, +5.
Trong phân tử Nitrogen các nguyên tử liên kết với nhau bằng
-
A.
liên kết cộng hoá trị phân cực.
-
B.
liên kết ba kém bền vững.
-
C.
liên kết cho- nhận.
-
D.
liên kết cộng hoá trị không phân cực.
Tính base của NH3 do
-
A.
trên N còn cặp e tự do.
-
B.
phân tử có 3 liên kết cộng hóa trị phân cực.
-
C.
NH3 tan được nhiều trong nước.
-
D.
NH3 tác dụng với nước tạo NH4OH.
Muối có trong bột khai sử dụng làm bánh là
-
A.
NH4HCO3.
-
B.
Na2CO3.
-
C.
NH4HSO3.
-
D.
NH4Cl.
H2SO4 loãng tác dụng chất nào sau đây thuộc phản ứng oxi hóa khử:
-
A.
Fe.
-
B.
BaCl2
-
C.
Fe2O3
-
D.
Fe3O4
Trong các oxide của nitrogen thì oxide được điều chế trực tiếp từ phản ứng của nitrogen với oxygen là:
-
A.
NO2
-
B.
NO
-
C.
N2O
-
D.
N2O5
N2 phản ứng với O2 tạo thành NO ở điều kiện nào dưới đây?
-
A.
Điều kiện thường
-
B.
Nhiệt độ cao khoảng 1000oC
-
C.
Nhiệt độ cao khoảng 10000oC
-
D.
Nhiệt độ khoảng 3000oC
Nước cường toan là hỗn hợp của dung dịch HNO3 đậm đặc với :
-
A.
Dung dịch HCl đậm đặc.
-
B.
Sulfuric acid đặc.
-
C.
Xút đậm đặc.
-
D.
Hỗn hợp HCl và H2SO4.
Nguyên tố sulfur có số hiệu nguyên tử là 16, trong bảng tuần hoàn, sulfur thuộc nhóm nào?
-
A.
nhóm IIA.
-
B.
nhóm IVA.
-
C.
nhóm VIA.
-
D.
nhóm VIIA.
Sulfur là chất rắn có màu
-
A.
đỏ.
-
B.
vàng.
-
C.
không màu.
-
D.
xanh.
Trong phản ứng: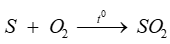 . Sulfur đóng vai trò là
. Sulfur đóng vai trò là
-
A.
chất khử.
-
B.
chất oxi hóa.
-
C.
chất bị khử.
-
D.
kim loại.
Chọn nhận định về muối ammonium ?
Muối ammonium bền với nhiệt.
Các muối ammonium đều là chất điện li mạnh.
Tất cả các muối ammonium đều tan trong nước.
Các muối ammonium đều không bị thủy phân trong nước.
Trong những hiện tượng sau: Những hiện tượng sinh ra sulfur dioxide vào môi trường
Hiện tượng cháy rừng.
Nhà máy điện sử dụng nguồn năng lượng hóa thạch.
Các phương tiện giao thông vận tải.
Quá trình quang hợp của cây xanh.
Chọn nhận định trong các phát biểu sau:
Sulfur dioxide là chất oxi hoá khi tác dụng với halogen, potassium permanganate…
Sulfur dioxide là chất oxi hóa khi tác dụng với H2S, Mg…
Sulfur dioxide có thể đóng vai trò là chất oxi hóa hoặc chất khử.
Sulfur dioxide là chất khí sinh ra từ quá trình quang hợp của cây xanh.
Học sinh A tiến hành thí nghiệm đốt cháy sulfur với bột sắt như sau:
Bước 1: lấy thìa nhỏ bột sắt và thìa nhỏ bột sulfur, trộn đều và cho vào ống nghiệm. Nút ống nghiệm bằng bông.
Bước 2: Đun nóng ống nghiệm có chứa hỗn hợp trên ngọn lửa đèn cồn đến khi có đốm sáng xuất hiện trong ống nghiệm thì ngừng đun, tắt đèn cồn.
Sau bước 1, phản ứng đã xảy ra nhưng chậm.
Sau bước 2, thấy hỗn hợp cháy sáng, kết thúc phản ứng hỗn hợp chuyển thành chất bột màu đen.
Sản phẩm tạo thành sau bước 2 là muối iron (III) sulfide.
Phương trình phản ứng xảy ra ở bước 2 là:
Lời giải và đáp án
Cân bằng hóa học liên quan đến loại phản ứng
-
A.
không thuận nghịch.
-
B.
thuận nghịch.
-
C.
một chiều.
-
D.
oxi hóa – khử.
Đáp án : B
Dựa vào khái niệm cân bằng hóa học
Cân bằng hóa học liên quan đến phản ứng thuận nghịch.
Đáp án B
Điền vào khoảng trống trong câu sau bằng cụm từ thích hợp: “Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận... tốc độ phản ứng nghịch”.
-
A.
lớn hơn
-
B.
bằng
-
C.
nhỏ hơn
-
D.
Khác
Đáp án : B
Dựa vào khái niệm cân bằng hóa học.
Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Đáp án B
Khi phản ứng thuận nghịch ở trạng thái cân bằng thì nó
-
A.
không xảy ra nữa.
-
B.
vẫn tiếp tục xảy ra.
-
C.
chỉ xảy ra theo chiều thuận.
-
D.
chỉ xảy ra theo chiều nghịch.
Đáp án : B
Dựa vào trạng thái cân bằng.
Khi phản ứng thuận nghịch ở trạng thái cân bằng thì nó vẫn tiếp tục xảy ra.
Đáp án B
Chất nào sau đây là chất điện li?
-
A.
C6H6.
-
B.
NaCl.
-
C.
C2H5OH.
-
D.
C6H12O6.
Đáp án : B
Dựa vào khái niệm chất điện li.
NaCl là chất điện li.
Đáp án B
Dung dịch chất nào sau đây có khả năng dẫn điện?
-
A.
C12H22O11.
-
B.
AlCl3
-
C.
C2H5OH.
-
D.
C6H12O6.
Đáp án : B
Các chất điện li có khả năng dẫn điện.
Dung dịch AlCl3 điện li thành các ion có khả năng dẫn điện.
Đáp án B
Chất nào sau đây là chất điện li mạnh?
-
A.
HCl.
-
B.
Fe(OH)2.
-
C.
H3PO4.
-
D.
H2S.
Đáp án : A
Dựa vào phân loại chất điện li.
HCl là acid mạnh: chất điện li mạnh
Đáp án A
Phân tử Nitrogen có cấu tạo
-
A.
N≡N.
-
B.
N=N.
-
C.
N-N.
-
D.
N→N.
Đáp án : A
Dựa vào cấu tạo của nitrogen.
Phân tử nitrogen có cấu tạo: N≡N.
Đáp án A
Trong hợp chất Nitrogen có các mức oxi hóa nào sau đây?
-
A.
-3, +3, +5.
-
B.
-3, 0, +3, +5.
-
C.
3, +1, +2, +3, +4, +5.
-
D.
-3, 0, +1, +2, +3, +4, +5.
Đáp án : C
Dựa vào tính chất hóa học của nitrogen.
Trong hợp chất nitrogen có các mức oxi hóa: -3, +1, +2, +3, +4, +5.
Đáp án C
Trong phân tử Nitrogen các nguyên tử liên kết với nhau bằng
-
A.
liên kết cộng hoá trị phân cực.
-
B.
liên kết ba kém bền vững.
-
C.
liên kết cho- nhận.
-
D.
liên kết cộng hoá trị không phân cực.
Đáp án : D
Dựa vào liên kết của phân tử nitrogen.
Trong phân tử nitrogen các nguyên tử liên kết với nhau bằng liên kết cộng hóa trị không phân cực.
Đáp án D
Tính base của NH3 do
-
A.
trên N còn cặp e tự do.
-
B.
phân tử có 3 liên kết cộng hóa trị phân cực.
-
C.
NH3 tan được nhiều trong nước.
-
D.
NH3 tác dụng với nước tạo NH4OH.
Đáp án : A
Dựa vào cấu tạo của phân tử NH3.
Tính base của NH3 do trên N còn cặp e tự do.
Đáp án A
Muối có trong bột khai sử dụng làm bánh là
-
A.
NH4HCO3.
-
B.
Na2CO3.
-
C.
NH4HSO3.
-
D.
NH4Cl.
Đáp án : A
Dựa vào ứng dụng của muối ammonium.
NH4HCO3 được sử dụng làm bột nở khi làm bánh.
Đáp án A
H2SO4 loãng tác dụng chất nào sau đây thuộc phản ứng oxi hóa khử:
-
A.
Fe.
-
B.
BaCl2
-
C.
Fe2O3
-
D.
Fe3O4
Đáp án : A
Dựa vào tính chất hóa học của H2SO4.
H2SO4 loãng thể hiện tính oxi hóa khi tác dụng với Fe vì Fe có tính khử.
Đáp án A
Trong các oxide của nitrogen thì oxide được điều chế trực tiếp từ phản ứng của nitrogen với oxygen là:
-
A.
NO2
-
B.
NO
-
C.
N2O
-
D.
N2O5
Đáp án : B
Dựa vào tính chất hóa học của nitrogen.
NO được điều chế trực tiếp từ phản ứng của nitrogen với oxygen.
Đáp án B
N2 phản ứng với O2 tạo thành NO ở điều kiện nào dưới đây?
-
A.
Điều kiện thường
-
B.
Nhiệt độ cao khoảng 1000oC
-
C.
Nhiệt độ cao khoảng 10000oC
-
D.
Nhiệt độ khoảng 3000oC
Đáp án : D
Dựa vào tính chất hóa học của nitrogen.
N2 phản ứng với O2 tạo thành NO ở điều kiện nhiệt độ khoảng 3000oC.
Đáp án D
Nước cường toan là hỗn hợp của dung dịch HNO3 đậm đặc với :
-
A.
Dung dịch HCl đậm đặc.
-
B.
Sulfuric acid đặc.
-
C.
Xút đậm đặc.
-
D.
Hỗn hợp HCl và H2SO4.
Đáp án : A
Dựa vào tính chất hóa học của HNO3.
Nước cường toan là hỗn hợp của dung dịch HNO3 đậm đặc với dung dịch HCl đậm đặc.
Đáp án A
Nguyên tố sulfur có số hiệu nguyên tử là 16, trong bảng tuần hoàn, sulfur thuộc nhóm nào?
-
A.
nhóm IIA.
-
B.
nhóm IVA.
-
C.
nhóm VIA.
-
D.
nhóm VIIA.
Đáp án : C
Dựa vào số hiệu nguyên tử của sulfur.
Cấu hình electron của S là: 1s22s22p63s23p4
Sulfur thuộc nhóm VIA
Đáp án C
Sulfur là chất rắn có màu
-
A.
đỏ.
-
B.
vàng.
-
C.
không màu.
-
D.
xanh.
Đáp án : B
Dựa vào trạng thái tự nhiên của sulfur.
Sulfur là chất rắn có màu vàng.
Đáp án B
Trong phản ứng: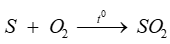 . Sulfur đóng vai trò là
. Sulfur đóng vai trò là
-
A.
chất khử.
-
B.
chất oxi hóa.
-
C.
chất bị khử.
-
D.
kim loại.
Đáp án : A
Dựa vào tính chất hóa học của sulfur.
Sulfur đóng vai trò là chất khử.
Đáp án A
Chọn nhận định về muối ammonium ?
Muối ammonium bền với nhiệt.
Các muối ammonium đều là chất điện li mạnh.
Tất cả các muối ammonium đều tan trong nước.
Các muối ammonium đều không bị thủy phân trong nước.
Muối ammonium bền với nhiệt.
Các muối ammonium đều là chất điện li mạnh.
Tất cả các muối ammonium đều tan trong nước.
Các muối ammonium đều không bị thủy phân trong nước.
Dựa vào tính chất của ammonium.
a. Sai, các muối ammonium không bền với nhiệt.
b. Đúng
c. Đúng
d. Sai, một số muối ammonium bị thủy phân trong nước
Trong những hiện tượng sau: Những hiện tượng sinh ra sulfur dioxide vào môi trường
Hiện tượng cháy rừng.
Nhà máy điện sử dụng nguồn năng lượng hóa thạch.
Các phương tiện giao thông vận tải.
Quá trình quang hợp của cây xanh.
Hiện tượng cháy rừng.
Nhà máy điện sử dụng nguồn năng lượng hóa thạch.
Các phương tiện giao thông vận tải.
Quá trình quang hợp của cây xanh.
Dựa vào tính chất của sulfur dioxide.
a. Sai, hiện tượng cháy rừng không sinh ra SO2.
b. Đúng
c. Đúng
d. Sai, quá trình quang hợp tạo khí O2.
Chọn nhận định trong các phát biểu sau:
Sulfur dioxide là chất oxi hoá khi tác dụng với halogen, potassium permanganate…
Sulfur dioxide là chất oxi hóa khi tác dụng với H2S, Mg…
Sulfur dioxide có thể đóng vai trò là chất oxi hóa hoặc chất khử.
Sulfur dioxide là chất khí sinh ra từ quá trình quang hợp của cây xanh.
Sulfur dioxide là chất oxi hoá khi tác dụng với halogen, potassium permanganate…
Sulfur dioxide là chất oxi hóa khi tác dụng với H2S, Mg…
Sulfur dioxide có thể đóng vai trò là chất oxi hóa hoặc chất khử.
Sulfur dioxide là chất khí sinh ra từ quá trình quang hợp của cây xanh.
Dựa vào tính chất của sulfur dioxide.
a. Sai, sulfur dioxide là chất khử khi tác dụng với halogen, potassium permanganate,…
b. đúng
c. đúng
d. sai, quá trình quang hợp tạo khí O2.
Học sinh A tiến hành thí nghiệm đốt cháy sulfur với bột sắt như sau:
Bước 1: lấy thìa nhỏ bột sắt và thìa nhỏ bột sulfur, trộn đều và cho vào ống nghiệm. Nút ống nghiệm bằng bông.
Bước 2: Đun nóng ống nghiệm có chứa hỗn hợp trên ngọn lửa đèn cồn đến khi có đốm sáng xuất hiện trong ống nghiệm thì ngừng đun, tắt đèn cồn.
Sau bước 1, phản ứng đã xảy ra nhưng chậm.
Sau bước 2, thấy hỗn hợp cháy sáng, kết thúc phản ứng hỗn hợp chuyển thành chất bột màu đen.
Sản phẩm tạo thành sau bước 2 là muối iron (III) sulfide.
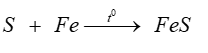
Phương trình phản ứng xảy ra ở bước 2 là:

Sau bước 1, phản ứng đã xảy ra nhưng chậm.
Sau bước 2, thấy hỗn hợp cháy sáng, kết thúc phản ứng hỗn hợp chuyển thành chất bột màu đen.
Sản phẩm tạo thành sau bước 2 là muối iron (III) sulfide.
Phương trình phản ứng xảy ra ở bước 2 là:

Dựa vào tính chất hóa học của sulfur.
a. Sai, ở bước 1 chưa xảy ra phản ứng.
b. Đúng
c. Sai, sản phẩm tạo thành từ bước 2 là FeS.
d. Đúng
Dựa vào các biện pháp bảo vệ môi trường.
(1), (3), (4) là fcác biện pháp làm giảm lượng khí thải SO2.
Đáp án 3
Dựa vào tính chất hóa học của lưu huỳnh.
nMg = 0,4 mol; nS = 0,3 mol
Mg + S \( \to \) MgS.
0,4 0,3
0,3 \( \leftarrow \)0,3 \( \to \) 0,3 mol
\( \to \)Rắn X ( 0,3 mol MgS và 0,1 mol Mg) + HCl \( \to \) 0,3 mol H2O và 0,1 mol H2.
\( \to \)V = 0,4.24,79 = 9,916 lít.
Dựa vào tính chất hóa học của sulfur.
Sulfur là chất oxi hóa khi tác dụng với: hydrogen, potassium chlorate, iron, mecury.
Đáp án 4
Dựa vào tính chất hóa học của nitric acid.
MX = 1,3125.32 = 42
n X = 9,916 : 24,79 = 0,4 mol
Gọi số mol NO2 và NO lần lượt là a và b mol
Ta có: \(\left\{ \begin{array}{l}a + b = 0,4\\46{\rm{a}} + 30b = 42.0,4\end{array} \right. \to \left\{ \begin{array}{l}a = 0,3\\b = 0,1\end{array} \right.\)
Bảo toàn electron ta có:
Fe0 \( \to \)Fe+3 + 3e N+5 +1e\( \to \)N+4
N+5 + 3e\( \to \)N+2
Áp dụng ĐLBTe \( \to \) nFe.3 = 1.nNO2 + 3.nNO \( \to \) nFe = 0,2 mol \( \to \) mFe = 11,2 gam.
Khí NH3 không thể hiện tính khử trong phản ứng nào sau đây?
Phản ứng nào sau đây viết sai
I. Phần trắc nghiệm
I. Phần trắc nghiệm
I. Trắc nghiệm
Câu 1: Điều nào sau đây là đúng khi nói về nồng độ của các sản phẩm, đối với một phản ứng hóa học đã ở trạng thái cân bằng, giả sử không có sự phá vỡ trạng thái cân bằng?
Trong quá trình tổng hợp ammonia, ở trạng thái cân bằng [N2] = 0,45 (M); [H2] = 0,14 (M);
Một phản ứng thuận nghịch đạt đến trạng thái cân bằng khi A. tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch. B. nồng độ của các chất tham gia phản ứng bằng nồng độ của các chất sản phẩm. C. phản ứng thuận đã kết thúc. D. phản ứng nghịch đã kết thúc.
Aspirin là một loại thuốc có thành phần chính là acetylsalicylic acid. Nếu hào tan thuốc này vào nước, người ta xác định được PH của dung dịch tạo thành 2,8. Nồng độ OH- của dung dịch tạo thành là:
Yếu tố nào sau đây luôn không thay đổi sự cân bằng hóa học ? A. Nhiệt độ B. Áp suất C. Xúc tác D. Nồng độ
Thao tác nào sau đây không làm chuyển dịch cân bằng ? A. Tăng nồng độ I2 B. Giảm nồng độ HI C. Giảm thấp nhiệt độ của hệ D. Thay đổi áp suất của hệ
Phát biểu nào sau đây đúng ? A. Nếu tăng áp suất của hệ thì cân bằng dịch chuyển theo chiều nghịch B. Nếu tăng nhiệt độ của hệ thì cân bằng dịch chuyển theo chiều thuận C. Nếu tăng lượng xúc tác V2O5 thì cân bằng dịch chuyển theo chiều thuận D. Nếu giảm nồng độ của SO3 thì cân bằng dịch chuyển theo chiều thuận


















Danh sách bình luận