Lý thuyết ancol
1. Định nghĩa , phân loại, đồng phân, danh pháp.
I. ĐỊNH NGHĨA, PHÂN LOẠI
- Ancol là những hợp chất hữu cơ mà phân tử có nhóm hiđroxyl (-OH) liên kết trực tiếp với nguyên tử cacbon no, công thức R(OH)n
- Phân loại :
+ Theo gốc hiđrocacbon: có ancol no, ancol không no, ancol thơm.
+ Theo số lượng nhóm hiđroxyl: ancol đơn chức, ancol đa chức.
+ Bậc của ancol = bậc của nguyên tử C liên kết với nhóm -OH.
II. ĐỒNG PHÂN, DANH PHÁP
1. Đồng phân
- Mạch cacbon khác nhau.
- Vị trí của các nhóm –OH khác nhau.
- Ngoài ra ancol đơn chức có đồng phân là ete: R-O-R’.
Ví dụ: Viết đồng phân của C3H8O.
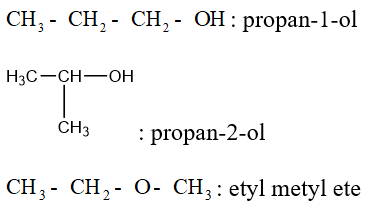
2. Danh pháp
-Tên gốc chức: Ancol + Tên gốc hidrocacbon + ic
Ví dụ:
CH3-CH2-OH: ancol etylic.
CH3-OH: ancol metylic.
+ Tên thay thế: số chỉ vị trí nhánh - tên nhánh - tên mạch chính - số chỉ vị trí nhóm - OH + ol
Lưu ý: Mạch chính là mạch cacbon dài nhất có chứa nhóm -OH
Đánh số thứ tự nguyên tử C mạch chính bắt đầu từ phía gần nhóm -OH hơn
Ví dụ:

II. TÍNH CHẤT VẬT LÍ
- Các ancol từ C1 đến khoảng C12 ở điều kiện thường là chất lỏng, từ C1 đến C3 tan vô hạn trong nước.
- Nhiệt độ nóng chảy, nhiệt độ sôi, độ tan trong nước của ancol đều cao hơn so với các hiđrocacbon có khối lượng mol phân tử tương đương, do tạo được liên kết hiđro giữa các phân tử ancol với nhau và giữa các phân tử ancol với nước.
III. TÍNH CHẤT HÓA HỌC
1. Phản ứng thế nguyên tử H trong nhóm OH
- Ancol tác dụng với kim loại kiềm M tạo ra muối ancolat. Phản ứng này chứng tỏ phân tử ancol có nguyên tử hiđro linh động.
2ROH + 2Na → 2RONa + H2↑
- Phản ứng riêng của glixerol: tác dụng với Cu(OH)2 tạo phức chất tan có màu xanh lam rất đặc trưng.
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
(ĐK: muốn tác dụng với Cu(OH)2 phải có 2 nhóm -OH trở lên liền kề nhau)
→ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có 2 nhóm OH cạnh nhau trong phân tử.
2. Phản ứng thế nhóm OH
- Phản ứng với axit vô cơ mạnh như HX, HNO3, H2SO4…
R-OH + HA → R-A + H2O ( A là: Hal, ONO2…)
- Phản ứng với ancol tạo ete:
R- OH + HO- R’ \(\xrightarrow{{{H_2}S{O_4}đặc,{t^o}}}\) R- O- R’ + H2O
3. Phản ứng tách nước tạo anken
Ancol khi tác dụng với H2SO4 đặc, đun nóng ở nhiệt độ 1700C cho phản ứng tách nước tương tự như phản ứng tách HX từ dẫn xuất halogen.
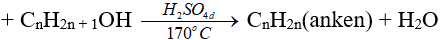
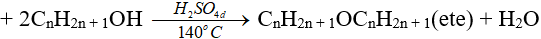
4. Phản ứng oxi hóa
a) Oxi hóa không hoàn toàn:
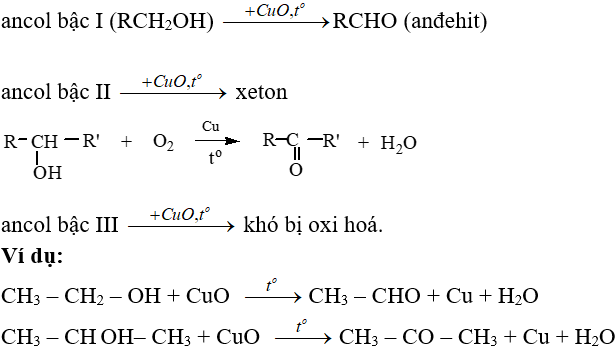
b) Oxi hóa hoàn toàn:
Ancol cháy tạo ra khí cacbonic, hơi nước và tỏa nhiều nhiệt
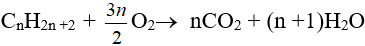
IV. ĐIỀU CHẾ
- Phương pháp tổng hợp: Tổng hợp etanol từ etilen có sẵn sau quá trình lọc dầu
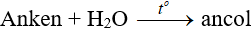
- Phương pháp sinh hóa: Từ các nguồn nguyên liệu chứa nhiều tinh bột trong tự nhiên ( gạo, lúa mì,...) sau quá trình lên men thu được etanol
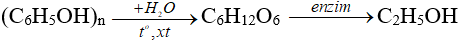
V. ỨNG DỤNG
Ancol ứng dựng nhiều trong công nghiệp thực phẩm, y tế, động cơ,....
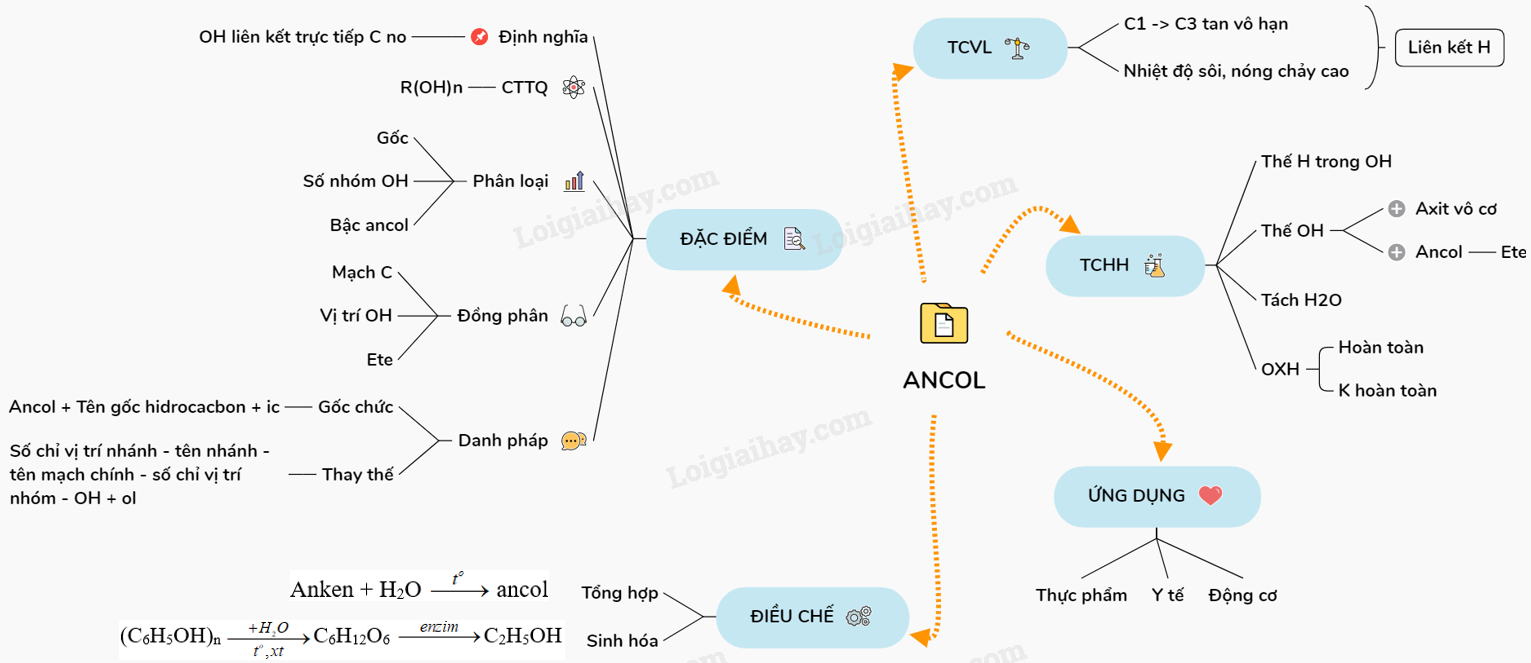
Sơ đồ tư duy: Ancol
Loigiaihay.com
Các bài khác cùng chuyên mục













Danh sách bình luận