40 bài tập lý thuyết về sự điện li của nước - pH có lời giải (phần 1)
Làm đề thiCâu hỏi 1 :
Phát biều không đúng là
- A Môi trường kiềm có pH < 7.
- B Môi trường kiềm có pH > 7.
- C Môi trường trung tính có pH = 7.
- D Môi trường axit có pH < 7.
Đáp án: A
Lời giải chi tiết:
Đáp án: A
Câu hỏi 2 :
Muối trung hoà là :
- A Muối mà dung dịch có pH = 7.
- B Muối không còn hiđro trong phân tử.
- C Muối có khả năng phản ứng với axit và bazơ.
- D Muối không còn hiđro có khả năng bị thay thế bởi kim loại.
Đáp án: D
Lời giải chi tiết:
Đáp án D
Muối trung hòa là muối không còn hiđro có khả năng bị thay thế bởi kim loại.
Câu hỏi 3 :
Chọn phát biểu đúng trong số các phát biểu sau đây ?
- A Giá trị pH tăng thì độ axit giảm.
- B Giá trị pH tăng thì độ axit tăng.
- C Dung dịch có pH < 7 làm quỳ tím hoá xanh.
- D Dung dịch có pH >7 làm quỳ tím hoá đỏ.
Đáp án: A
Lời giải chi tiết:
Đáp án: A
B. SAI
C. PH < 7 là môi trường axit => quỳ hóa đỏ
D. PH>7 là môi trường bazơ => quỳ hóa xanh
Câu hỏi 4 :
Dung dịch của một axit ở 250C có
- A [H+] = 1,0.10-7M.
- B [H+] > 1,0.10-7M.
- C [H+] < 1,0.10-7M.
- D [H+].[OH-] > 1,0.10-14.
Đáp án: B
Lời giải chi tiết:
Đáp án: B
Môi trường trung tính: [H+].[OH-] = 1,0.10-14
Môi trường axit [H+] > [OH-] => chọn B
Câu hỏi 5 :
Câu nào sai khi nói về pH và pOH của dung dịch ?
- A pH = -lg[H+].
- B [H+] = 10a thì pH = a.
- C pOH = -lg[OH-].
- D pH + pOH = 14.
Đáp án: B
Lời giải chi tiết:
Đáp án: B
B. SỬA [H+] = 10a thì pH = -a.
Câu hỏi 6 :
Chât có môi trường trung tính là:
- A HCl
- B CaCl2
- C NaOH
- D HNO3
Đáp án: B
Lời giải chi tiết:
A,D môi trường axit. C môi trường bazơ
Đáp án B
Câu hỏi 7 :
Phát biểu không đúng là
- A Môi trường kiềm có pH<7.
- B Môi trường kiềm có pH>7.
- C Môi trường trung tính có pH=7.
- D Môi trường axit có pH<7.
Đáp án: A
Lời giải chi tiết:
- MT kiềm pH>7
- MT trung tính pH=7
- MT axit pH<7
Đáp án A
Câu hỏi 8 :
Chất nào dưới đây có pH < 7 ?
- A KNO3.
- B NH4Cl.
- C KCl.
- D K2CO3.
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 9 :
Dung dịch nào sau đây có pH > 7 ?
- A HNO3
- B KOH
- C CH3OH
- D KCl
Đáp án: B
Lời giải chi tiết:
Dung dịch nào sau đây có pH > 7 nên có môi trường bazo
Đáp án B
Câu hỏi 10 :
Dung dịch có giá trị pH = 7 sẽ làm quỳ tím
- A chuyển sang màu đỏ.
- B chuyển sang màu xanh.
- C quỳ không đổi màu.
- D không xác định được.
Đáp án: C
Phương pháp giải:
MT trung tính không làm đổi màu quỳ tím.
MT kiềm làm quỳ tím chuyển xanh.
MT axit làm quỳ tím chuyển đỏ.
Lời giải chi tiết:
Dung dịch pH = 7 là MT trung tính, không làm đổi màu quỳ tím.
Đáp án C
Câu hỏi 11 :
Dung dịch của một axit ở 25oC có
- A [H+] = 1,0.10-7M.
- B [H+] > 1,0.10-7M.
- C [H+] < 1,0.10-7M.
- D [H+].[OH-] > 1,0.10-14.
Đáp án: B
Phương pháp giải:
Dung dịch axit có pH < 7. Dựa vào công thức tính pH = -log[H+] để suy ra nồng độ của H+ trong một dung dịch axit.
Lời giải chi tiết:
Ta có: [H+] = 10-pH
Dung dịch axit có pH < 7 => [H+] > 1,0.10-7M
Đáp án B
Câu hỏi 12 :
Chất nào dưới đây không phân li ra ion khi hòa tan trong nước ?
- A MgCl2.
- B HClO3.
- C Ba(OH)2.
- D C6H12O6 (glucozơ).
Đáp án: D
Lời giải chi tiết:
Đáp án D
Câu hỏi 13 :
Dung dịch nào sau đây có pH > 7?
- A NaCl.
- B NaOH.
- C HNO3.
- D H2SO4.
Đáp án: B
Lời giải chi tiết:
Đáp án B
Câu hỏi 14 :
Dung dịch chất nào sau trong H2O có pH <7 ?
- A Isoamyl axetat.
- B Toluen.
- C Cumen.
- D Ancol etylic
Đáp án: A
Lời giải chi tiết:
pH < 7 => môi trường có tính axit
Đáp án A
Câu hỏi 15 :
Cho các dung dịch sau: NaHCO3, Na2CO3, NaCl, CH3COONa, C6H5OH, NH3, CH3COOH, lysin, valin. Số dung dịch có pH>7 là:
- A 5
- B 4
- C 6
- D 8
Đáp án: A
Lời giải chi tiết:
Có 5 dung dịch pH>7 là: NaHCO3, Na2CO3, CH3COONa, NH3, lysin.
Đáp án A
Câu hỏi 16 :
Dung dịch nào sau đây có pH < 7?
- A NaOH.
- B HCl.
- C Na2CO3.
- D Na2SO4.
Đáp án: B
Phương pháp giải:
Dung dịch có pH < 7 là dung dịch có môi trường axit.
Lời giải chi tiết:
HCl là dung dịch có MT axit nên có pH < 7.
Đáp án B
Câu hỏi 17 :
Dung dịch nào sau đây có pH = 7?
- A NaOH.
- B H2SO4.
- C NaCl.
- D HCl.
Đáp án: C
Phương pháp giải:
- MT axit có pH < 7
- MT trung tính có pH = 7
- MT kiềm có pH > 7
Lời giải chi tiết:
NaOH có MT kiềm => pH > 7
H2SO4 và HCl có MT axit => pH < 7
NaCl có MT trung tính => pH = 7
Đáp án C
Câu hỏi 18 :
Điều khẳng định đúng là:
- A dung dịch có môi trường bazo thì pH>7.
- B dung dịch có môi trường trung tính thì pH<7.
- C dung dịch có môi trường axit thì pH=7.
- D dung dịch có môi trường trung tính thì pH>7.
Đáp án: A
Phương pháp giải:
+ Môi trường axit: pH < 7
+ Môi trường trung tính: pH = 7
+ Môi trường bazo: pH > 7
Lời giải chi tiết:
Khẳng định đúng là “Dung dịch có môi trường bazo thì pH>7”
Đáp án A
Câu hỏi 19 :
Có 4 dung dịch có nồng độ bằng nhau : HCl ( pH = a) ; H2SO4 (pH = b) ; NH4Cl (pH = c); NaOH ( pH = d). Kết quả nào sau đây đúng :
- A d < c < a < b
- B a < b < c < d
- C c < a < d < b
- D b < a < c < d
Đáp án: D
Lời giải chi tiết:
Cùng nồng độ mol => H2SO4 sinh ra nhiều H+ nhất => có pH thấp nhất
Đáp án D
Câu hỏi 20 :
Các dung dịch sau có cùng nồng độ: HNO3 (1), KOH (2), NaCl (3). Giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là:
- A (1), (2), (3).
- B (1), (3), (2).
- C (3), (2), (1).
- D (2), (1), (3).
Đáp án: B
Lời giải chi tiết:
Ta có: pHHNO3 < 7; pHNaCl = 7; pHKOH > 7
Vậy nên pH được sắp xếp theo chiều tăng từ trái sang phải là: (1), (3), (2).
Đáp án B
Câu hỏi 21 :
Đối với dung dịch axit yếu HNO2 0,1M, nếu bỏ qua sự điện li của nước thì đánh giá nào sau đây là đúng?
- A [H+] > 0,1M.
- B [H+] = 0,1M.
- C [H+] < 0,1M.
- D [H+] < [NO2-].
Đáp án: C
Lời giải chi tiết:
HNO2 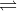 H+ + NO2-
H+ + NO2-
Vì HNO2 là axit yếu nên điện li không hoàn toàn => [H+] < 0,1M
Đáp án C
Câu hỏi 22 :
Phát biểu đúng là
- A Nồng độ H+ trong dịch HCl 0,01M và dung dịch HCOOH 0,01M là như nhau.
- B Nồng độ H+ trong dung dịch CH3COOH 0,01M lớn gấp 10 lần dung dịch CH3COOH 0,001M.
- C Dung dịch CH3COOH 0,01M có pH lớn hơn dung dịch HNO3 0,01M.
- D NaCl khan là chất dẫn điện tốt.
Đáp án: C
Lời giải chi tiết:
A sai do HCOOH là axit yếu phân li không hoàn toàn, HCl là axit mạnh phân li hoàn toàn nên nồng độ ion H+ trong HCOOH ít hơn so với HCl có cùng nồng độ ban đầu.
B sai do nồng độ khác nhau nên độ điện li khác nhau.
C đúng
Do CH3COOH là axit yếu phân li không hoàn toàn nên tạo [H+] ít hơn so với HNO3 cùng nồng độ
=> pHCH3COOH > pHHNO3 (cùng nồng độ).
D sai do NaCl rắn khan không dẫn được điện.
Đáp án C
Câu hỏi 23 :
Trong các dung dịch: K2CO3, KCl, NH4Cl, CH3COONa, Na2S, NaHSO4 có bao nhiêu dung dịch có môi trường axit (pH<7)?
- A 3
- B 1
- C 2
- D 4
Đáp án: C
Phương pháp giải:
- Cách xác định MT của một dung dịch muối:
+ Muối tạo bởi axit mạnh và bazo yếu => MT axit (pH < 7)
+ Muối tạo bởi axit yếu và bazo manh => MT kiềm (pH > 7)
+ Muối tạo bởi axit mạnh và bazo manh => MT trung tính (pH = 7)
Lời giải chi tiết:
K2CO3 tạo bởi bazo mạnh KOH, axit yếu H2CO3 => MT bazo
KCl tạo bởi bazo mạnh KOH, axit mạnh HCl => MT trung tính
NH4Cl tạo bởi bazo yếu NH3, axit mạnh HCl => MT axit
CH3COONa tạo bởi bazo mạnh NaOH, axit yếu CH3COOH => MT bazo
Na2S tạo bởi bazo mạnh NaOH, axit yếu H2S => MT bazo
NaHSO4 là muối axit => MT axit
Vậy có 2 dung dịch có tính axit (pH<7) là: NH4Cl, NaHSO4
Đáp án C
Câu hỏi 24 :
Dãy sắp xếp các dung dịch loãng có nồng độ mol/l như nhau theo thứ tự pH tăng dần là
- A KHSO4, HF, H2SO4, Na2CO3.
- B HF, H2SO4, Na2CO3, KHSO4
- C H2SO4, KHSO4, HF, Na2CO3.
- D HF, KHSO4, H2SO4, Na2CO3.
Đáp án: C
Lời giải chi tiết:
Đáp án: C
PH tăng dần tức tính axit giảm dần=> chọn C
Câu hỏi 25 :
Một dung dịch có $\left[ {{\rm{O}}{{\rm{H}}^ - }} \right] = 2,{5.10^{ - 10}}{\rm{M}}$ . Môi trường của dung dịch là:
- A Kiềm
- B Trung tính
- C Axit
- D Không xác định được
Đáp án: C
Lời giải chi tiết:
Đáp án: C
$\left[ {{\rm{O}}{{\rm{H}}^ - }} \right] = 2,{5.10^{ - 10}}{\rm{M = > pH = 14 - log[}}O{H^ - }{\rm{]) = 14 - 9,6 = 4,4}}$
pH = 4,4 < 7. Vậy dung dịch có môi trường axit
Câu hỏi 26 :
Dung dịch CH3COOH 0,1M có pH = a và dung dịch HCl 0,1M có pH = b. Phát biểu đúng là
- A a < b =1.
- B a > b = 1.
- C a = b = 1.
- D a = b > 1.
Đáp án: B
Lời giải chi tiết:
Đáp án: B
Dễ thấy HCl là axit mạnh nên phân li hoàn toàn => $${{\rm{[}}{{\rm{H}}^ + }{\rm{]}}_{HCl}} = 0,1 = > b = - \log ({\rm{[}}{{\rm{H}}^ + }{\rm{]) = 1}}$$
CH3COOH là ax yếu nên phân li 1 phần => $${{\rm{[}}{{\rm{H}}^ + }{\rm{]}}_{C{H_3}COOH}}{\rm{ < }}0,1 = > b = - \log {\rm{ }}({\rm{[}}{{\rm{H}}^ + }{\rm{]) < 1}}$$
Câu hỏi 27 :
Dung dịch muối nào sau đây có pH > 7 ?
- A NaCl.
- B Na2CO3.
- C Ba(NO3)2.
- D NH4Cl.
Đáp án: B
Phương pháp giải:
Cách xác định môi trường của một muối:
+ Muối được tạo bởi axit mạnh và bazo yếu thì có môi trường axit, pH < 7
+ Muối được tạo bởi axit yếu và bazo mạnh thì có môi trường bazo, pH > 7
+ Muối được tạo bởi axit mạnh và bazo mạnh thì có môi trường trung tính, pH = 7
Lời giải chi tiết:
NaCl tạo bởi bazo mạnh (NaOH) và axit mạnh (HCl) => MT trung tính (pH=7)
Na2CO3 tạo bởi bazo mạnh (NaOH) và axit yếu (H2CO3) => MT kiềm (pH>7)
Ba(NO3)2 tạo bởi bazo mạnh (Ba(OH)2) và axit mạnh (HNO3) => MT trung tính (pH=7)
NH4Cl tạo bởi bazo yếu (NH4OH) và axit mạnh (HCl) => MT axit (pH<7)
Đáp án B
Câu hỏi 28 :
Câu nào sai khi nói về pH và pOH của dung dịch?
- A pH = -lg[H+].
- B [H+] = 10a thì pH = a.
- C pOH = -lg[OH-].
- D pH + pOH = 14.
Đáp án: B
Phương pháp giải:
Lý thuyết về pH của dung dịch.
Lời giải chi tiết:
B sai, sửa lại thành [H+] = 10-a => pH = a
A, C, D đúng
Đáp án B
Câu hỏi 29 :
Cho các dung dịch có cùng nồng độ: Na2CO3 (1), H2SO4 (2), HCl (3), KNO3 (4).
Giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là
- A (2), (1), (3), (4).
- B (3), (2), (4), (1).
- C (2), (3), (4), (1).
- D (4), (1), (2), (3).
Đáp án: C
Lời giải chi tiết:
pH = - log[H+]
Nồng độ H+ càng cao thì pH càng nhỏ => pH (H2SO4) < pH (HCl)
Na2CO3 là muối của bazo mạnh và axit yếu => môi trường bazo
KNO3 là muối của kiềm mạnh và axit mạnh => môi trường trung tính
Đáp án C
Câu hỏi 30 :
Muối nào sau đây khi thuỷ phân tạo dung dịch có pH<7 ?
- A CaCl2.
- B CH3COONa.
- C NaCl.
- D NH4Cl.
Đáp án: D
Phương pháp giải:
- Dung dịch có MT kiềm có pH > 7.
- Cách xác định MT của một dung dịch muối:
+ Muối tạo bởi axit mạnh và bazo yếu => MT axit (pH < 7)
+ Muối tạo bởi axit yếu và bazo manh => MT kiềm (pH > 7)
+ Muối tạo bởi axit mạnh và bazo manh => MT trung tính (pH = 7)
Lời giải chi tiết:
NH4Cl là muối tạo bởi bazo yếu (NH3) và axit mạnh (HCl)
=> Thủy phân trong nước tạo môi trường axit (pH<7)
Đáp án D
Câu hỏi 31 :
Cho các dung dịch: NH3, NaOH, Ba(OH)2 có cùng nồng độ mol/l và có các giá trị pH là pH1, pH2 và pH3. Sự sắp xếp nào đúng?
- A pH1 < pH2< pH3
- B pH3 < pH2< pH1
- C pH3 < pH1< pH2
- D pH1 < pH3< pH2
Đáp án: A
Lời giải chi tiết:
Môi trường bazo có PH > 7 : bazo càng mạnh thì PH càng lớn
NH3 có tính bazo yếu hơn NaOH
Ba(OH)2 cùng số mol với NaOH nhưng cho số mol của OH- gấp đôi nên PH sẽ lớn nhất
Đáp án A
Câu hỏi 32 :
Trong số các dung dịch: Na2CO3, KCl, CH3COONa, NH4Cl, NaHSO4, C6H5ONa, những dung dịch có pH>7 là
- A Na2CO3, NH4Cl, KCl.
- B Na2CO3, C6H5ONa, CH3COONa.
- C NH4Cl, CH3COONa, NaHSO4.
- D KCl, C6H5ONa, CH3COONa.
Đáp án: B
Lời giải chi tiết:
- Nếu muối tạo ra từ bazo mạnh và axit yếu => pH > 7
- Nếu muối tạo ra từ bazo mạnh và axit mạnh => pH = 7
- Nếu muối tạo ra từ bazo yếu và axit mạnh => pH < 7
A, D. Loại vì có KCl pH = 7
C. Loại vì có NaHSO4 pH < 7
Đáp án B
Câu hỏi 33 :
Cho các muối sau đây: NaNO3 ; K2CO3 ; CuSO4 ; FeCl3 ; AlCl3 ; KCl. Các dung dịch có pH = 7 là:
- A NaNO3 ; KCl.
- B K2CO3 ; CuSO4 ; KCl.
- C CuSO4 ; FeCl3 ; AlCl3.
- D NaNO3 ; K2CO3 ; CuSO4.
Đáp án: A
Lời giải chi tiết:
Đáp án A
Câu hỏi 34 :
Dung dịch nào sau đây có nồng độ H+ lớn nhất?
- A Dung dịch HNO3 0,01M
- B Dung dịch H2SO4 0,01M
- C Dung dich HCl 0,015M
- D Dung dịch H2SO4 0,005M
Đáp án: B
Lời giải chi tiết:
A. HNO3 → H+ + NO3-
0,01 → 0,01
B. H2SO4 → 2H+ + SO42-
0,01 → 0,02
C. HCl → H+ + Cl-
0,015 → 0,015
D. H2SO4 → 2H+ + SO42-
0,005 → 0,01
Đáp án B
Câu hỏi 35 :
Dãy dung dịch đều có pH < 7 là
- A FeCl3, NaCl, HCl, NaOH.
- B CuSO4, FeCl2, AlCl3, NaHCO3.
- C Al2(SO4)3, CuCl2, HCl, NH4Cl.
- D NH4Cl, Na2CO3, NaHSO4, FeCl3.
Đáp án: C
Phương pháp giải:
Xác định pH của dung dịch axit, bazo, muối:
- Dung dịch axit có MT axit (pH < 7)
- Dung dịch bazo có MT kiềm (pH > 7)
- Dung dịch muối:
+ Muối tạo bởi bazo mạnh và axit mạnh => MT trung tính (pH = 7)
+ Muối tạo bởi bazo mạnh và axit yếu => MT kiềm (pH > 7)
+ Muối tạo bởi bazo yếu và axit mạnh => MT axit (pH < 7)
Lời giải chi tiết:
A. Loại NaOH (pH > 7)
B. Loại NaHCO3 (pH > 7)
C. Đúng
D. Loại Na2CO3 (pH > 7)
Đáp án C
Câu hỏi 36 :
Cho các dung dịch có cùng nồng độ: Na2CO3 (1), H2SO4 (2), HCl (3), KNO3 (4), CH3COOH (5). Giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái qua phải là:
- A (1), (4), (5), (3), (2)
- B (1), (4), (3), (2), (5)
- C (2), (3), (5), (4), (1)
- D (3), (2), (5), (4), (1)
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 37 :
Ba dung dịch axit sau có cùng nồng độ mol: HCl, H2SO4, CH3COOH.
Giá trị pH của chúng tăng theo thứ tự là:
- A HCl, H2SO4, CH3COOH.
- B CH3COOH, HCl, H2SO4.
- C H2SO4, HCl, CH3COOH.
- D HCl, CH3COOH, H2SO4.
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 38 :
Chọn câu đúng nhất trong số các câu sau đây:
- A Những dd có pH < 7 thì làm quỳ tím hóa đỏ.
- B giá trị pH tăng thì độ axit của dung dịch tăng.
- C Giá trị pH tăng thì độ axit của dung dịch giảm.
- D Những dd có pH > 7 thì làm quỳ tím hóa xanh.
Đáp án: C
Lời giải chi tiết:
A. sai
B. Sai pH tăng thì độ axit của dd giảm
C. đúng
D. Sai ví dụ như anilin ( C6H5NH2 có pH = 9,42) nhưng không làm quỳ tím chuyển sang màu xanh
Đáp án C
Câu hỏi 39 :
Chất nào sau đây khi cho vào nước không làm thay đổi độ pH của dung dịch?
- A Na2CO3.
- B Na2SO4.
- C HCl.
- D NH4Cl.
Đáp án: B
Phương pháp giải:
Chất trung tính khi cho vào nước không làm thay đổi pH của dung dịch.
Lời giải chi tiết:
A. Na2CO3 được tạo bởi bazo mạnh NaOH và axit yếu H2CO3 => môi trường bazo => làm pH tăng
B. Na2SO4 được tạo bởi bazo mạnh NaOH và axit mạnh H2SO4 => môi trường trung tính => không làm thay đổi pH
C. HCl có môi trường axit => làm pH giảm
D. NH4Cl được tạo bởi bazo yếu NH3 và axit mạnh HCl => môi trường axit => làm pH giảm
Đáp án B
Câu hỏi 40 :
Cẩm tú cầu là loài hoa được trồng nhiều nhất tại Sa Pa hay Đà Lạt. Màu của loại hoa này có thể thay đổi tùy thuộc vào pH của thổ nhưỡng nên có thể điều chỉnh màu hoa thông qua việc điều chỉnh độ pH của đất trồng
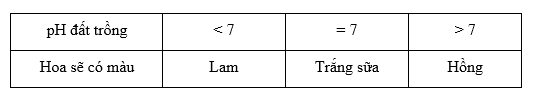
Khi trồng loài hoa trên, nếu ta bón thêm 1 ít vôi sống (CaO) trên môi trường đất trung tính và chỉ tưới nước thì khi thu hoạch hoa sẽ
- A Có màu lam.
- B Có màu hồng.
- C Có đủ cả 3 màu lam, trắng , hồng.
- D Có màu trắng sữa.
Đáp án: B
Phương pháp giải:
CaO tan trong nước tạo ra dd Ca(OH)2. Xác định được độ pH của dd Ca(OH)2 từ đó suy ra được màu sắc của hoa.
Lời giải chi tiết:
CaO tan trong nước tạo ra Ca(OH)2 có môi trường kiềm tức pH >7 => hoa cẩm tú cầu sẽ có màu hồng
Đáp án B
10 bài tập vận dụng cao về tính pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
20 bài tập vận dụng về tính pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
20 bài tập vận dụng về tính pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 30 bài tập vận dụng về cracking ankan có lời giải
- 30 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải
- 20 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải (phần 2)
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 bài tập vận dụng về cracking ankan có lời giải
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 1)
- 10 bài tập vận dụng cao về công thức phân tử hợp chất hữu cơ có lời giải









