20 bài tập vận dụng về tính pH có lời giải (phần 1)
Làm đề thiCâu hỏi 1 :
Trộn 50ml dung dịch NaOH 0,1M với 50ml dung dịch HCl 0,1M. pH của dung dịch thu được sau phản ứng là:
- A 0.
- B 1.
- C 7.
- D 13.
Đáp án: C
Phương pháp giải:
So sánh số mol NaOH và HCl từ đó xác định pH của dung dịch thu được sau phản ứng.
Lời giải chi tiết:
Ta thấy: nNaOH = nHCl = 0,005 mol
=> NaOH phản ứng vừa đủ với HCl
=> Sau phản ứng thì dung dịch chỉ có NaCl => pH = 7
Đáp án C
Câu hỏi 2 :
Trộn 100ml dung dịch HCl 0,1M với V ml dung dịch Ba(OH)2 0,1M, sau phản ứng thu được dung dịch có pH = 12,7. Giá trị của V là:
- A 50 ml.
- B 100 ml.
- C 150 ml.
- D 200 ml.
Đáp án: B
Phương pháp giải:
pHsau = 12,7 > 7 => OH- dư
Tính toán theo phương trình ion: H+ + OH- → H2O
Lời giải chi tiết:
nH+ = nHCl = 0,01 mol; nOH- = 2nBa(OH)2 = 0,2V mol
pHsau = 12,7 > 7 => OH- dư => pOH = 14 - 12,7 = 1,3 => [OH-] = 10-1,3
H+ + OH- → H2O
Bđ: 0,01 0,2V
Pư: 0,01 → 0,01
Sau: 0 0,2V - 0,01
\(\left[ {O{H^ - }} \right] = \frac{{{n_{O{H^ - }}}}}{V} \to {10^{ - 1,3}} = \frac{{0,2V - 0,01}}{{0,1 + V}}\) => V = 0,1 lít
Đáp án B
Câu hỏi 3 :
Cho dung dịch A chứa H2SO4 0,1M; HNO3 0,2M và HCl 0,3M. Trộn 300 ml dung dịch A với V lít dung dịch B gồm NaOH 0,2M và KOH 0,29M thu được dung dịch C có pH = 2. Giá trị của V là
- A 0,134.
- B 0,424.
- C 0,441.
- D 0,414.
Đáp án: D
Lời giải chi tiết:
Trong A : nH+ = 2nH2SO4 + nHNO3 + nHCl = 2.0,1.0,3 + 0,2.0,3 + 0,3.0,3 = 0,21 mol
Trong B : nOH- = nNaOH + nKOH = 0,2V + 0,29V = 0,49V mol
Dung dịch sau khi trộn có pH = 2 => MT axit => H+ dư, OH- hết
H+ + OH- → H2O
Bđ: 0,21 0,49V
Pư: 0,49V ← 0,49V
Sau: 0,21 - 0,49V 0
pH = 2 => [H+] = 10-2 => \(\frac{{0,21 - 0,49V}}{{0,3 + V}} = {10^{ - 2}}\) => V = 0,414 lít = 414 ml
Đáp án D
Câu hỏi 4 :
Hòa tan m gam Na vào nước được 100 ml dung dịch có pH = 13. Giá trị của m bằng
- A 0,23 gam
- B 2,3 gam
- C 3,45 gam
- D 0,46 gam
Đáp án: A
Lời giải chi tiết:
pH = 13 => pOH = 1 => [OH-] = 0,1 M => nNaOH = 0,01 mol = nNa ( BT nguyên tố )
=> m = 0,23g
Đáp án A
Câu hỏi 5 :
Dung dịch X chứa hỗn hợp NaOH 0,25M và Ba(OH)2 0,15M dung dịch Y chứa hỗn hợp H2SO4 0,5M và HNO3 0,2M.Trộn V lít dung dịch X với V’ lit dung dịch Y thu được dung dịch Z có pH =3. Tỉ lệ V/V’ là
- A 2,17
- B 1,25
- C 0,46
- D 0,08
Đáp án: A
Lời giải chi tiết:
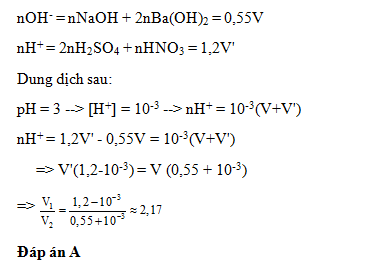
Câu hỏi 6 :
Cho m gam hỗn hợp Mg, Al vào 250 ml dung dịch X chứa hỗn hợp axit HCl 1 M và axit H2SO4 0,5 M thu được 5,32 lít H2 (ở đktc) và dung dịch Y (coi thể tích dung dịch không đổi). Dung dịch Y có pH là:
- A 1
- B 2
- C 6
- D 7
Đáp án: A
Lời giải chi tiết:
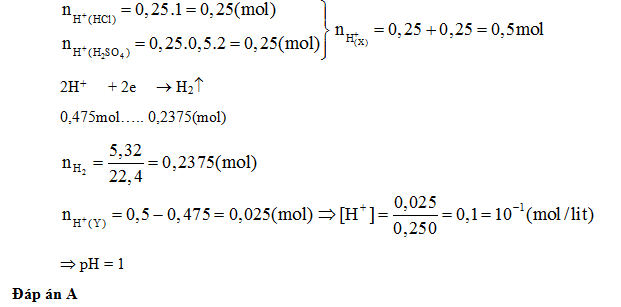
Câu hỏi 7 :
Trộn 100ml dung dịch (gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch (gồm H2SO4 0,0375 M và HCl 0,0125 M) thu được dung dịch X, giá trị pH của dung dịch X là:
- A 1
- B 2
- C 6
- D 7
Đáp án: B
Lời giải chi tiết:
\(\begin{gathered}
\left. \begin{gathered}
{n_{Ba{{(OH)}_2}}} = 0,01mol \hfill \\
{n_{NaOH}}\,\,\,\,\,\,\, = 0,01mol \hfill \\
\end{gathered} \right\}\,\, \Rightarrow \,{n_{O{H^ - }}} = 2.{n_{Ba{{(OH)}_2}}} + {n_{NaOH}} = 0,03(mol) \hfill \\
\left. \begin{gathered}
{n_{HCl}}\,\,\,\,\,\, = 0,005mol \hfill \\
{n_{{H_2}S{O_4}}} = 0,015mol \hfill \\
\end{gathered} \right\}\,\, \Rightarrow \,{n_{{H^ + }}} = {n_{HCl}} + 2.{n_{{H_2}S{O_4}}} = 0,035(mol) \hfill \\
\end{gathered} \)
Khi trộn xảy ra phản ứng trung hoà dạng ion là:
H+ + OH-à H2O
0,035 0,03
nH+ (dư) = 0,035 - 0,03 = 0,005 (mol) => [H+] = 0,005/(0,1+0,4) = 0,01
[H+] = 0,01 = 10-2 (mol/lít) Þ pH = 2
Đáp án B
Câu hỏi 8 :
Trộn 200 ml dd hỗn hợp gồm HNO3 0,3M và HClO4 0,5M với 200 ml dd Ba(OH)2 a mol/lit thu được dd có pH = 3. Vậy a có giá trị là:
- A 0,39
- B 0,798
- C 0,399
- D 0,398
Đáp án: C
Lời giải chi tiết:
Ta có: ∑nH+ = 0,2(0,3+ 0,5) = 0,16 mol; nOH- = 0,4.a
Sau khi phản ứng xảy ra dung dịch thu được có pH= 3 chứng tỏ axit dư.
[H+] sau phản ứng = (0,16-0,4a)/ 0,4 = 10-3
Vậy a = 0,399
Đáp án C
Câu hỏi 9 :
Thể tích của nước cần thêm vào 15 ml dung dịch axit HCl có pH=1 để được dung dịch axit có pH=3 là:
- A 1,68 lít
- B 2,24 lít
- C 1,12 lít
- D 1,485 lít
Đáp án: D
Lời giải chi tiết:
Gọi thể tích nước cần thêm là Vml. Số mol H+ không đổi trước và sau pha loãng nên:
15.10-1 = (15+ V).10-3
V= 1485ml = 1,485 lít
Đáp án D
Câu hỏi 10 :
Thêm 90 ml nước vào 10 ml dung dịch NaOH có pH=12 thì thu được dung dịch có pH là:
- A 3
- B 1
- C 11
- D 13
Đáp án: C
Lời giải chi tiết:
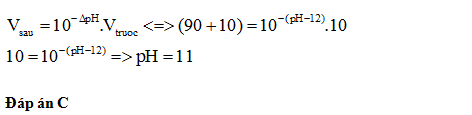
Câu hỏi 11 :
Tính pH của dung dịch dd HCl 2.10-7M
- A pH = 6,700
- B pH = 6,617
- C pH = 2
- D pH = 11
Đáp án: B
Lời giải chi tiết:
Ta thấy: Ca = 2.10-7 ≈ \(\sqrt {{K_{{H_2}O}}} = {10^{ - 7}}\)nên không thể bỏ qua sự phân li của H2O.
HCl → H+ + Cl-
2.10-7→ 2.10-7
H2O \(\underset{{}}{\overset{{}}{\longleftrightarrow}}\) H+ + OH- KH2O = 10-14
Bđ: 2.10-7
Pli: x x x
Sau: x + 2.10-7 x
=> KH2O = [H+][OH-] = (x + 2.10-7).x = 10-14
=> x = 4,142.10-8
=> [H+] = x + 2.10-7 = 4,142.10-8 + 2.10-7 = 2,4142.10-7
=> pH = -log[H+] = 6,617
Đáp án B
Câu hỏi 12 :
Tính pH của dung dịch HNO2 0,2M biết Ka = 4.10--4
- A 2
- B 1
- C 0,6
- D 2,05
Đáp án: D
Phương pháp giải:
Các quá trình điện li của
HNO2 \(\overset {} \leftrightarrows \) H+ + NO2- Ka = 4.10-4
H2O\(\overset {} \leftrightarrows \) H+ + OH- Kw = 10-14
Để tính pH của dung dịch thì ta phải đi tìm nồng độ H+ có trong dung dịch. Mà nồng độ H+ này có thể do HNO2 và H2O phân li ra.
Để xét xem có bỏ qua sự điện li của H2O tạo ra H+ hay không ta so sánh tích số
Ka.Ca với Kw
Nếu Ka. Ca >> Kw thì bỏ qua sư điện li của H2O
Nếu Ka. Ca ≈ Kw thì tính đến sự điện li của H2O
Lời giải chi tiết:
Các quá trình điện li:
HNO2 \(\overset {} \leftrightarrows \) H+ + NO2- Ka = 4.10-4
H2O \(\overset {} \leftrightarrows \) H+ + OH- Kw = 10-14
Ta thấy: Ka.Ca = 0,2.4.10-4 = 8.10-5 > > Kw = 10-14. Do vậy sự phân li của H2O tạo ra H+ là không đáng kể. Vì vậy bỏ qua sự điện li của H2O. Dung dịch chỉ có sự điện li của HNO2
HNO2 \(\overset {} \leftrightarrows \) H+ + NO2- Ka = 4.10-4
ban đầu: 0,2
phân li: x x x
cân bằng: (0,2 - x) x x
Ta có:\(Ka = {{{\rm{[}}{H^ + }{\rm{]}}.{\rm{[}}N{O_2}^ - {\rm{]}}} \over {{\rm{[}}HN{O_2}]}} = {{{x^2}} \over {0,2 - x}} = {4.10^{ - 4}}(*)\)
Cách 1: Giải phương trình bậc 2
→ x2 + 4.10-4x - 0,2.4.10-4 = 0
→ x = 8,7465.10-3 (M)
→ [H+] = x = 8,7465.10-3 (M)
→ pH = -lg[H+] = -lg(8,7465.10-3) = 2,058
Cách 2: Ta thấy \({{Ca} \over {Ka}} = {{0,2} \over {{{4.10}^{ - 4}}}} = 500\) (Chỉ cần Ca lớn gấp 100 lần Ka là coi như x rất nhỏ)
→ x << 0,2
→ coi 0,2 - x ≈ 0,2
Từ phương trình (*) →\({{{x^2}} \over {0,2}} = {4.10^{ - 4}} \Rightarrow x = \sqrt {0,{{2.4.10}^{ - 4}}} = 8,{944.10^{ - 3}}(M)\)
→ [H+] = x = 8,944.10-3 (M)
→ pH = -lg[H+] = -lg(8,944.10-3) = 2,048 ≈ 2,05
Đáp án D
Câu hỏi 13 :
Tính pH của 400 ml dung dịch (gồm H2SO4 0,025 M và HCl 0,05 M) ?
- A 1
- B 2
- C 6
- D 7
Đáp án: A
Lời giải chi tiết:
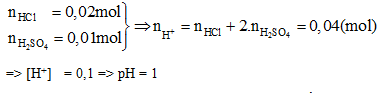
Câu hỏi 14 :
Tính pH của dung dịch CH3COOH 0,1M biết Ka = 1,8.10-5 ?
- A 1,00
- B 2,87
- C 6,05
- D 6,04
Đáp án: B
Lời giải chi tiết:
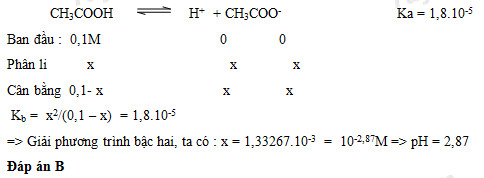
Câu hỏi 15 :
Trộn V1 lít dung dịch HCl (pH = 5) với V2 lít dung dịch NaOH (pH = 9)thu được dung dịch có pH = 8. Tỉ lệ V1/ V2 là:
- A 1/3
- B 3/1
- C 9/11
- D 11/9
Đáp án: C
Lời giải chi tiết:
pH của HCl = 5 => [HCl]= 10-5 => nHCl = CM. V1 = 10-5V1
pH của NaOH = 9 => pOH = 14 – 9 = 5 => [NaOH]= 10-5 => nNaOH = CM.V2= 10-5.V2
Vì dd sau phản ứng thu được có pH = 8 > 7 => môi trường bazo => dư OH-
=> pOH = 14 – 8 = 6
=> [NaOH] dư = 10-6
H+ + OH- → H2O
Ban đầu(mol) 10-5V1 10-5.V2
Phản ứng (mol) 10-5V1 10-5V1
Sau pư (mol) 0 10-6(V1+ V2)
Ta có: nOH- ban đầu = nOH- pư + nOH- dư
=> 10-5.V2 = 10-5V1 + 10-6(V1+ V2)
=> 10-5.V2 – 10-6V2 = 10-5V1 + 10-6V1
=> 9.10-6V2 = 1,1.10-5V1
\( = > \frac{{{V_1}}}{{{V_2}}} = \frac{{{{9.10}^{ - 6}}}}{{1,{{1.10}^{ - 5}}}} = \frac{9}{{11}}\)
Đáp án C
Câu hỏi 16 :
Trộn lẫn 50 ml dung dịch HCl 0,12M với 50 ml dung dịch NaOH 0,1M. Vậy pH của dung dịch thu được bằng bao nhiêu?
- A 2
- B 4
- C 3
- D 1
Đáp án: A
Lời giải chi tiết:
nH+ = 6.10-3 mol ; nOH- = 5.10-3 mol
H+ + OH- → H2O
Bđ: 6.10-3 5.10-3 (mol)
Pư: 5.10-3 ← 5.10-3 (mol)
Sau: 10-3 0 (mol)
Mà V dd sau pư = 50 + 50 = 100 ml = 0,1 lít
=> [H+] = 10-3 : 0,1 = 10-2M
=> pH = 2
Đáp án A
Câu hỏi 17 :
Cho 40 ml dung dịch HCl 0,75M vào 160 ml dung dịch chứa đồng thời Ba(OH)2 0,08M và KOH 0,04M. pH của dung dịch thu được:
- A 10
- B 12
- C 11
- D 13
Đáp án: B
Lời giải chi tiết:
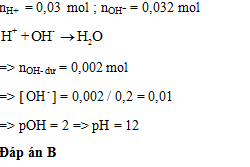
Câu hỏi 18 :
Dung dịch axit fomic HCOOH 0,007 M có độ điện li = 0,1. Tính pH của dung dịch HCOOH:
- A 3,15
- B 3,44
- C 3,55
- D 3,89
Đáp án: A
Lời giải chi tiết:

Câu hỏi 19 :
Dung dịch NaOH 0,001M có giá trị pH là:
- A 3.
- B 2.
- C 11.
- D 12.
Đáp án: C
Phương pháp giải:
Tính pOH = -log[OH-] => pH = 14 - pOH
Lời giải chi tiết:
NaOH là chất điện li mạnh => [OH-] = CM NaOH = 0,001M
=> pOH = -log[OH-] = -log(0,001) = 3
=> pH = 14 - pOH = 14 - 3 = 11
Đáp án C
Câu hỏi 20 :
Cho 100 ml dung dịch X chứa: 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. 100 ml dung dịch Y có chứa y mol H+, Cl-, NO3- và 0,01 mol Na+ (tổng số mol Cl- và NO3- là 0,042). Trộn 100 ml dung dịch X với 100 ml dung dịch Y thu được dung dịch Z. Dung dịch Z có pH là
- A 13
- B 2
- C 12
- D 1
Đáp án: B
Phương pháp giải:
Bảo toàn điện tích.
Lời giải chi tiết:
- Bảo toàn điện tích cho dung dịch X:
nOH- = nNa+ - 2nSO42- = 0,07 - 2.0,02 = 0,03 mol
- Bảo toàn điện tích cho dung dịch Y:
nH+ = (nCl- + nNO3-) - nNa+ = 0,042 - 0,01 = 0,032 mol
Khi trộn 100 ml X với 100 ml Y có phản ứng: H+ + OH- → H2O
=> nH+ dư = nH+ - nOH- = 0,032 - 0,03 = 0,002 mol
=> [H+] = \(\frac{{{n_{{H^ + }}}}}{{{V_{{\rm{dd}}\,sau\,pu}}}}\) = \(\frac{{0,002}}{{0,1 + 0,1}}\) = 0,01M
=> pH = -log[H+] = 2
Đáp án B
20 bài tập vận dụng về tính pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
10 bài tập vận dụng cao về tính pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
40 bài tập lý thuyết về sự điện li của nước - pH có đáp án và lời giải chi tiết từ cơ bản tới nâng cao, từ bài dễ tới bài khó đầy đủ các dạng đầy đủ từ trắc nghiệm tới tự luận.
Các bài khác cùng chuyên mục
- 30 bài tập vận dụng về cracking ankan có lời giải
- 30 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải
- 20 câu hỏi lý thuyết về mở đầu hợp chất hữu cơ có lời giải (phần 2)
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 bài tập vận dụng về cracking ankan có lời giải
- 15 câu hỏi lý thuyết về phản ứng hữu cơ có lời giải
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 2)
- 30 câu hỏi ôn tập về công thức phân tử hợp chất hữu cơ có lời giải (phần 1)
- 10 bài tập vận dụng cao về công thức phân tử hợp chất hữu cơ có lời giải

















