 Giải khoa học tự nhiên 8, soạn sgk khtn lớp 8 chân trời sáng tạo
Giải khoa học tự nhiên 8, soạn sgk khtn lớp 8 chân trời sáng tạo
 Chủ đề 2. Một số hợp chất vô cơ. Thang pH - KHTN 8 Chân..
Chủ đề 2. Một số hợp chất vô cơ. Thang pH - KHTN 8 Chân.. Bài 13. Muối trang 62, 63, 64 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
Thạch nhũ trong các hang động có thành phần chính là muối của calcium, nước biển chứa muối ăn và nhiều muối khác. Trong tự nhiên, các kim loại thường tồn tại ở dạng muối. Muối là gì? Muối có thành phần tính chất và mối quan hệ với acid, base, oxide như thế nào?
Tổng hợp đề thi học kì 2 lớp 8 tất cả các môn - Chân trời sáng tạo
Toán - Văn - Anh - Khoa học tự nhiên
Câu hỏi tr 62 CHMĐ
Trả lời câu hỏi mở đầu trang 62 SGK KHTN 8 Chân trời sáng tạo
Thạch nhũ trong các hang động có thành phần chính là muối của calcium, nước biển chứa muối ăn và nhiều muối khác. Trong tự nhiên, các kim loại thường tồn tại ở dạng muối. Muối là gì? Muối có thành phần tính chất và mối quan hệ với acid, base, oxide như thế nào?
Phương pháp giải:
Dựa vào khái niệm muối.
Lời giải chi tiết:
Muối là hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium (NH4+)
Muối được tạo ra từ phản ứng giữa acid, base, oxide.
Câu hỏi tr 62 CH 1
Trả lời câu hỏi 1 trang 62 SGK KHTN 8 Chân trời sáng tạo
Khi thay ion hydrogen trong phân tử sulfuric acid bởi mỗi ion Al3+, Cu2+ và NH4+ thì ta được hợp chất gì? Viết công thức hóa học của chúng.
Phương pháp giải:
Dựa vào khái niệm muối.
Lời giải chi tiết:
Khi thay ion hydrogen trong phân tử sulfuric acid bởi mỗi ion Al3+, Cu2+ và NH4+ thì ta được hợp chất muối.
Công thức hóa học của chúng là: Al2(SO4)3; CuSO4; (NH4)2SO4.
Câu hỏi tr 62 CH 2
Trả lời câu hỏi 2 trang 62 SGK KHTN 8 Chân trời sáng tạo
Sản phẩm thay thế ion hydrogen trong hydrochloric acid bởi ion magnesium sẽ được hợp chất gì? Viết phương trình hóa học ra hợp chất trên từ acid và base tương ứng.
Phương pháp giải:
Dựa vào khái niệm muối.
Lời giải chi tiết:
Sản phẩm thay thế ion hydrogen trong hydrochloric acid bởi ion magnesium sẽ được hợp chất muối.
PTHH: Mg(OH)2 + 2HCl \( \to \)MgCl2 + H2O
Câu hỏi tr 63 VD
Trả lời câu hỏi vận dụng trang 63 SGK KHTN 8 Chân trời sáng tạo
(X) là muối nitrate của kim loại M. Ở điều kiện thường, (X) là chất rắn, màu trắng (hình bên) và có nhiều ứng dụng trong đời sống; biết khối lượng phân tử của (X) bằng 101 amu.
a) Hãy cho biết công thức hoá học và tên gọi của muối (X).
b) Tìm hiểu qua internet, sách, báo, hãy nêu một số ứng dụng của muối (X).
Phương pháp giải:
Dựa vào kiến thức của muối.
Lời giải chi tiết:
a) Đặt công thức tổng quát của muối (X) là: M(NO3)n.
Theo bài ra: M + 62 × n = 80.
Biện luận thấy n = 1; M = 39 (thoả mãn).
Vậy công thức hoá học của muối (X) là: KNO3.
Tên muối: Potassium nitrate.
b) Một số ứng dụng của muối KNO3: chế tạo thuốc nổ đen; làm phân bón, cung cấp nguyên tố nitrogen và potassium cho cây trồng; bảo quản thực phẩm trong công nghiệp …
Câu hỏi tr 63 LT
Trả lời câu hỏi luyện tập trang 63 SGK KHTN 8 Chân trời sáng tạo
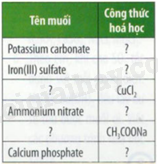
Dựa vào tên một số gốc acid ở Bảng 9.1, hoàn thành bảng theo mẫu sau:
Phương pháp giải:
Dựa vào tên gọi của muối.
Lời giải chi tiết:
|
Tên muối |
Công thức hóa học |
|
Potassium carbonate |
K2CO3 |
|
Iron(III) sulfate |
Fe2(SO4)3 |
|
Copper(II) chloride |
CuCl2 |
|
Ammonium nitrate |
NH4NO3 |
|
Sodium acetate |
CH3COONa |
|
Calcium phosphate |
Ca3(PO4)2 |
Câu hỏi tr 63 CH 1
Trả lời câu hỏi 1 trang 63 SGK KHTN 8 Chân trời sáng tạo
Dựa vào thông tin và Bảng tính tan ở Phụ lục, hãy chọn hai kim loại thay thế hydrogen ion trong hydrochloride acid và sulfuric acid để được biến muối đều tan trong nước. Viết công thức hóa học của các muối tan trên.
Phương pháp giải:
Dựa vào Bảng tính tan.
Lời giải chi tiết:
Công thức hóa học của các muối tan là: NaCl; Na2SO4; KCl; K2SO4.
Câu hỏi tr 63 CH 2
Trả lời câu hỏi 2 trang 63 SGK KHTN 8 Chân trời sáng tạo
Có hai muối MSO4 và MCO3 đều không tan trong nước, dựa vào bảng tính tan (Phụ lục) hãy cho biết tên của kim loại M.
Phương pháp giải:
Dựa vào bảng tính tan.
Lời giải chi tiết:
Kim loại M là Ba.
Câu hỏi tr 64 LT
Trả lời câu hỏi luyện tập trang 64 SGK KHTN 8 Chân trời sáng tạo
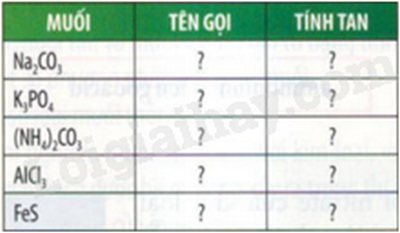
Dựa vào bảng tính tan ở Phụ lục 1, hãy hoàn thành bảng theo mẫu sau:
Phương pháp giải:
Dựa vào bảng tính tan ở Phụ lục 1
Lời giải chi tiết:
|
Muối |
Tên gọi |
Tính tan |
|
Na2CO3 |
Sodium carbonate |
T |
|
K3PO4 |
Potassium phosphate |
T |
|
(NH4)2CO3 |
Ammonium carbonate |
T |
|
AlCl3 |
Aluminium chloride |
T |
|
FeS |
Iron(II) sulfide |
K |
Câu hỏi tr 64 VD
Trả lời câu hỏi vận dụng trang 64 SGK KHTN 8 Chân trời sáng tạo
(X) là muối carbonate của kim loại R hóa trị II. (X) có khối lượng phân tử bằng 197 amu.
a) Xác định công thức hóa học và tên gọi của muối (X). Dựa vào bảng tính tan, hãy cho biết muối này có tan được trong nước không.
b) Tìm hiểu qua sách, báo, internet,…hãy nêu một số ứng dụng của muối (X).
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
a) Công thức tổng quát của X là: RCO3
M RCO3 = MR + M CO3 = 197
\( \to \)MR = 137 (Ba)
Công thức muối là: BaCO3 không tan trong nước
b) Ứng dụng để sản xuất barium.
Câu hỏi tr 65 CH 1
Trả lời câu hỏi 1 trang 65 SGK KHTN 8 Chân trời sáng tạo
Tương tự các ví dụ 2, 3, 4, 5 hãy viết phương trình hóa học tạo ra các muối sua: K2SO3, CaSO4, NaCl, MgCl2.
Phương pháp giải:
Dựa vào các Phương pháp điều chế muối.
Lời giải chi tiết:
CO2 + 2KOH \( \to \)K2CO3 + H2O
2HCl + Na2O \( \to \)2NaCl + H2O
Mg + 2HCl \( \to \)MgCl2 + H2
Câu hỏi tr 65 CH 2
Trả lời câu hỏi 2 trang 65 SGK KHTN 8 Chân trời sáng tạo
Theo em, khi cho SO2 tác dụng với mỗi dung dịch: NaOH, Ba(OH)2 đều lấy dư sẽ thu được muối gì. Viết các phương trình hóa học xảy ra.
Phương pháp giải:
Dựa vào phương pháp điều chế muối.
Lời giải chi tiết:
SO2 + 2NaOH \( \to \)Na2SO3 + H2O
SO2 + Ba(OH)2 \( \to \)BaSO3 + H2O
Câu hỏi tr 65 CH 3
Trả lời câu hỏi 3 trang 65 SGK KHTN 8 Chân trời sáng tạo
Từ các phương pháp điều chế muối, hãy viết 3 phương trình hóa học tạo ra iron(II) chloride.
Phương pháp giải:
Dựa vào phương pháp điều chế muối.
Lời giải chi tiết:
Fe + 2HCl \( \to \)FeCl2 + H2
FeO + 2HCl \( \to \)FeCl2 + H2O
Fe(OH)2 + 2HCl \( \to \)FeCl2 + 2H2O
Câu hỏi tr 65 LT
Trả lời câu hỏi luyện tập trang 65 SGK KHTN 8 Chân trời sáng tạo
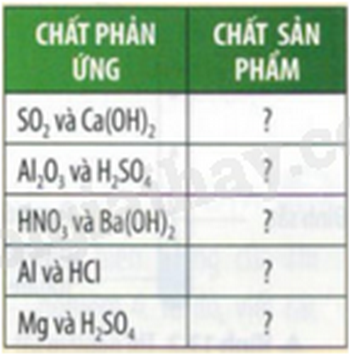
Hoàn thành bảng theo mẫu sau:
Phương pháp giải:
Dựa vào phương pháp điều chế muối.
Lời giải chi tiết:
|
Chất phản ứng |
Chất sản phẩm |
|
SO2 và Ca(OH)2 |
CaSO3 hoặc Ca(HSO3)2 |
|
Al2O3 và H2SO4 |
Al2(SO4)3 |
|
HNO3 và Ba(OH)2 |
BaNO3 |
|
Al và HCl |
AlCl3 |
|
Mg và H2SO4 |
MgSO4 |
Câu hỏi tr 65 VD
Trả lời câu hỏi vận dụng trang 65 SGK KHTN 8 Chân trời sáng tạo
Sodium sulfate ở điều kiện thường là chất rắn, màu trắng, được sử dụng nhiều trong các ngành công nghiệp.
a) Tìm hiểu qua internet, sách, báo,…hãy cho biết một số ứng dụng của sodium sulfate.
b) Hãy viết 3 phương trình hóa học tạo sodium sulfate.
Phương pháp giải:
Dựa vào ứng dụng của các loại muối.
Lời giải chi tiết:
a) Một số ứng dụng của sodium sulfate: sản xuất thuốc nhuộm, bột giấy …
b) 3 phương trình hoá học tạo sodium sulfate:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Na2O + H2SO4 → Na2SO4 + H2O
Na2CO3 + H2SO4 → Na2SO4 + CO2 + H2O.
Câu hỏi tr 66 CH 1
Trả lời câu hỏi 1 trang 66 SGK KHTN 8 Chân trời sáng tạo
Hãy nêu hiện tượng và viết phương trình hóa học của phản ứng ở Thí nghiệm 1.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
Hiện tượng: Đinh sắt tan dần, có kim loại bám trên đinh sắt, màu xanh của dung dịch nhạt dần rồi mất màu.
PTHH: Fe + CuSO4 \( \to \)FeSO4 + Cu.
Câu hỏi tr 66 LT
Trả lời câu hỏi luyện tập trang 66 SGK KHTN 8 Chân trời sáng tạo
Viết phương trình hóa học của phản ứng xảy ra trong các trường hợp sau:
a) Cho copper vào dung dịch silver nitrate.
b) Cho zinc vào dung dịch iron(II) sulfate.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
a) Cu + 2AgNO3 \( \to \)Cu(NO3)2 + 2Ag
b) Zn + FeSO4 \( \to \)ZnSO4 + Fe
Câu hỏi tr 66 CH 2
Trả lời câu hỏi 2 trang 66 SGK KHTN 8 Chân trời sáng tạo
Hãy nêu hiện tượng của Thí nghiệm 2 và đề xuất 3 phương trình hóa học khác tạo ra copper(II) hydroxide.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
Hiện tượng: Có kết tủa xanh xuất hiện.
PTHH: CuCl2 + 2NaOH \( \to \)Cu(OH)2 + 2NaCl
Cu(NO3)2 + 2KOH \( \to \)Cu(OH)2 + 2KNO3
CuSO4 + Ba(OH)2 \( \to \)Cu(OH)2 + BaSO4.
Câu hỏi tr 67 LT 1
Trả lời câu hỏi luyện tập 1 trang 67 SGK KHTN 8 Chân trời sáng tạo
Cho các dung dịch sau phản ứng với nhau, hoàn thành các phương trình hóa học:
a) Na2SO3 + Ba(OH)2
b) K2CO3 + Ba(OH)2
c) MgSO4 + Ba(OH)2
Nhận xét về sản phẩm của các phản ứng trên.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
a) Na2SO3 + Ba(OH)2 \( \to \)BaCO3 + 2NaOH
b) K2CO3 + Ba(OH)2 \( \to \)2KOH + BaCO3
c) MgSO4 + Ba(OH)2 \( \to \)BaSO4 + Mg(OH)2
Các phản ứng trên đều sinh ra muối kết tủa.
Câu hỏi tr 67 CH 1
Trả lời câu hỏi 1 trang 67 SGK KHTN 8 Chân trời sáng tạo
Hãy nêu hiện tượng của Thí nghiệm 3 và giải thích.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
Hiện tượng: có bọt khí thoát ra.
Giải thích: Na2CO3 tác dụng với HCl tạo ra khí CO2.
PTHH: Na2CO3 + 2HCl \( \to \)2NaCl + CO2 + H2O
Câu hỏi tr 67 LT 2
Trả lời câu hỏi luyện tập 2 trang 67 SGK KHTN 8 Chân trời sáng tạo
Hãy tìm 2 muối phản ứng được với dung dịch HCl và dung dịch H2SO4. Viết các phương trình hóa học của phản ứng đã xảy ra.
Phương pháp giải:
Dựa vào phản ứng muối và dung dịch acid.
Lời giải chi tiết:
K2CO3 + 2HCl \( \to \)2KCl + CO2 + H2O
Ba(NO3)2 + H2SO4 \( \to \)BaSO4 + 2HNO3
Câu hỏi tr 67 CH 2
Trả lời câu hỏi 2 trang 67 SGK KHTN 8 Chân trời sáng tạo
Nêu hiện tượng của Thí nghiệm 4. Từ đó, viết các phương trình hóa học sau:
a) Dung dịch potassium carbonate tác dụng với dung dịch calcium chloride.
b) Dung dịch sodium sufite tác dụng với dung dịch barium nitrate.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
Hiện tượng: có kết tủa trắng xuất hiện.
a) K2CO3 + CaCl2 \( \to \)2KCl + CaCO3
b) Na2S + Ba(NO3)2 \( \to \)BaS + 2NaNO3
Câu hỏi tr 67 LT 3
Trả lời câu hỏi luyện tập 3 trang 67 SGK KHTN 8 Chân trời sáng tạo
Hãy tìm 3 dung dịch muối có thể phản ứng được với dung dịch Na2CO3. Viết các phương trình hóa học của phản ứng đã xảy ra.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
CaCl2 + Na2CO3 \( \to \)2NaCl + CaCO3
Mg(NO3)2 + Na2CO3 \( \to \)MgCO3 + 2NaNO3
Ba(NO3)2 + Na2CO3 \( \to \)BaCO3 + 2NaNO3
Câu hỏi tr 68 VD
Trả lời câu hỏi vận dụng trang 68 SGK KHTN 8 Chân trời sáng tạo
Để làm sạch lớp cặn (thường là CaCO3) trong các dụng cụ đun nước, người ta dùng giấm ăn hoặc nước ép từ quả chanh. Giải thích.
Phương pháp giải:
Dựa vào tính chất hóa học của muối.
Lời giải chi tiết:
Vì trong nước ép quả chanh hoặc giấm ăn có chứa acetic acid (CH3COOH) có thể hòa tan được lớp cặn (thường là CaCO3).
PTHH: CaCO3 + 2CH3COOH \( \to \)(CH3COO)2Ca + CO2 + H2O
Câu hỏi tr 68 CH
Trả lời câu hỏi trang 68 SGK KHTN 8 Chân trời sáng tạo
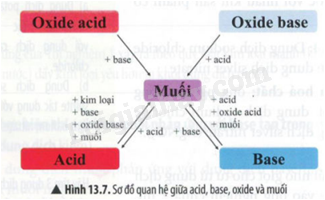
Hãy chọn chất thích hợp và viết các phương trình hóa học theo sơ đồ ở Hình 13.7
Phương pháp giải:
Dựa vào mối quan hệ giữa acid, base, oxide và muối.
Lời giải chi tiết:
PTHH: SO3 + 2NaOH \( \to \)Na2SO4 + H2O
Na2O + H2SO4 \( \to \)Na2SO4 + H2O
Na + H2SO4 \( \to \)Na2SO4 + H2
2NaOH + H2SO4 \( \to \)Na2SO4 + 2H2O
Na2CO3 + H2SO4 \( \to \)Na2SO4 + CO2 + H2O
Câu hỏi tr 68 LT
Trả lời câu hỏi luyện tập trang 68 SGK KHTN 8 Chân trời sáng tạo
Hãy viết phương trình hóa học của các phản ứng xảy ra theo sơ đồ sau:
a) CuO \( \to \)CuCl2 \( \to \)Cu(OH)2
b) CO2 \( \to \)Na2CO3 \( \to \)CaCO3 \( \to \)CO2
Phương pháp giải:
Dựa vào mối quan hệ giữa acid, base, oxide và muối.
Lời giải chi tiết:
a) CuO + 2HCl \( \to \)CuCl2 + H2O
CuCl2 + 2NaOH \( \to \)Cu(OH)2 + 2NaCl
b) CO2 + 2NaOH \( \to \)Na2CO3 + H2O
Na2CO3 + Ca(OH)2 \( \to \)2NaOH + CaCO3
- Bài 14. Phân bón hóa học trang 69, 70, 71 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Ôn tập chủ đề 2 trang 74, 75, 76 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 12. Oxide trang 56, 57, 58 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 11. Thang pH trang 53, 54, 55 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 10. Base trang 50, 51, 52 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
>> Xem thêm
Các bài khác cùng chuyên mục
- Ôn tập chủ đề 5 trang 133 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 28. Sự nở vì nhiệt trang 128, 129, 130 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 27. Sự truyền nhiệt trang 123, 124, 125 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Bài 26. Năng lượng nhiệt và nội năng trang 120, 121, 122 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo
- Ôn tập chủ đề 4 trang 119 SGK Khoa học tự nhiên 8 - Chân trời sáng tạo






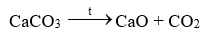








Danh sách bình luận