Bài 4 trang 108 SGK Hóa học 10
Có những sơ đồ phản ứng hóa học sau:
Đề bài
Có những sơ đồ phản ứng hóa học sau:
a) Cl2 + H2O → HCl + HClO
b) CaOCl2 + HCl → CaCl2 + Cl2 + H2O
c) Cl2 + KOH \(\xrightarrow{{{t^0}}}\) KCl + KClO3 + H2O
d) HCl + KClO3 → KCl + Cl2 + H2O
e) NaClO + CO2 + H2O → NaHCO3 + HClO
g) CaOCl2 → CaCl2 + O2
Cho biết những phản ứng nào là phản ứng oxi hóa khử và vai trò của các chất tham gia phản ứng oxi hóa khử. Hoàn thành phương trình hóa học.
Video hướng dẫn giải
Phương pháp giải - Xem chi tiết
Bước 1: Xác định số oxi hóa của các nguyên tố trước và sau phản ứng để xác định được chất khử và chất oxi hóa
- Bước 2: viết các quá trình nhường e, nhận e
- Bước 3: tìm hệ số thích hợp cho chất khử và chất oxi hóa
- Bước 4: đặt các hệ số chất khử và chất oxi hóa vào sơ đồ phản ứng. hoàn thành phương trình hóa học.
Ghi nhớ:
- chất khử là chất nhường electron, số oxi hóa tăng sau phản ứng
- Chất oxi hóa là chất nhận electron, số oxi hóa giảm sau phản ứng
Lời giải chi tiết
Những phản ứng sau là phản ứng oxi hóa khử:
a) \(\overset{0}{Cl_{2}}\) + H2O →\(\overset{+1}{HCl}\) + \(\overset{-1}{HClO}\)
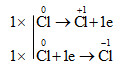
Cl2 vừa là chất khử vừa là chất oxi hóa.
b)
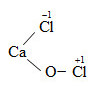 + 2HCl → CaCl2 + Cl2 + H2O
+ 2HCl → CaCl2 + Cl2 + H2O
CaOCl2 : phân tử tự oxi hóa khử, HCl đóng vai trò môi trường
c) 3 \(\overset{0}{Cl_{2}}\) + 6KOH → 5\(\overset{-1}{KCl}\) + \(\overset{+5}{KClO_{3}}\) + 3 H2O
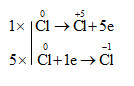
Cl2 vừa là chất oxi hóa, vừa là chất khử.
d) 6\(\overset{-1}{HCl}\) + \(\overset{+5}{KClO_{3}}\) → \(\overset{-1}{KCl}\) + 3\(\overset{0}{Cl_{2}}\) +3H2O
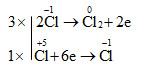
HCl là chất khử, KClO3 là chất oxi hóa
e) Không có sự thay đổi số oxi hóa
g) 2CaOCl2 → 2\(\overset{-1}{CaCl_{2}}\) + \(\overset{0}{O_{2}}\)
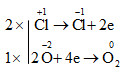
CaOCl2: phân tử tự oxi hóa
Loigiaihay.com
Các bài khác cùng chuyên mục













Danh sách bình luận