Lý thuyết liên kết ion - tinh thể ion
Khái niệm về liên kết hóa học
I. KHÁI NIỆM VỀ LIÊN KẾT HÓA HỌC
1. Khái niệm về liên kết
Trừ trường hợp các khí hiếm, ở điều kiện bình thường các nguyên tử của các nguyên tố không tồn tại ở trạng thái tự do, riêng rẽ mà liên kết với các nguyên tử khác nhau tạo thành phân tử hay tinh thể.
=> Liên kết hóa học là sự kết hợp giữa các nguyên tử để tạo thành phân tử hay tinh thể bền vững hơn.
2. Quy tắc bát tử (8 electron)
Theo quy tắc bát tử thì các nguyên tử của các nguyên tố có khuynh hướng liên kết với các nguyên tử khác để đạt cấu hình vững bền của các khí hiếm với 8 electron (hoặc 2 electron với heli) ở lớp ngoài cùng.
II. SỰ TẠO THÀNH LIÊN KẾT ION, ANION, CATION
1. Sự tạo thành ion.
- Trong phản ứng hóa học, khi nguyên tử, phân tử thêm hoặc mất bớt electron nó sẽ tạo thành các phần tử mang điện được gọi là ion. Các ion trái dấu hút nhau bằng lực hút tĩnh điện tạo thành hợp chất chứa liên kết ion.
- Điều kiện hình thành liên kết ion:
+ Liên kết được hình thành giữa các nguyên tố có tính chất khác hẳn nhau (kim loại điển hình và phi kim điển hình).
+ Quy ước hiệu độ âm điện giữa hai nguyên tử liên kết ≥ 1,7 là liên kết ion (trừ một số trường hợp).
- Dấu hiệu cho thấy phân tử có liên kết ion:
+ Phân tử hợp chất được hình thành từ kim loại điển hình (kim loại nhóm IA, IIA) và phi kim điển hình (phi kim nhóm VIIA và Oxi).
Ví dụ: Các phân tử NaCl, MgCl2, BaF2,…đều chứa liên kết ion, là liên kết được hình thành giữa các cation kim loại và anion phi kim.
+ Phân tử hợp chất muối chứa cation hoặc anion đa nguyên tử.
Ví dụ: Các phân tử NH4Cl, MgSO4, AgNO3,… đều chứa liên kết ion, là liên kết được hình thành giữa cation kim loại hoặc amoni và anion gốc axit.
- Đặc điểm của hợp chất ion: Các hợp chấy ion có nhiệt độ nóng chảy và nhiệt độ sôi cao, dẫn điện khi tan tròn nước hoặc nóng chảy.
- Ion được chia thành cation và anion:
Cation : Ion dương
Anion : Ion âm
2. Sự tạo thành cation
- Ion mang điện tích dương gọi là ion dương hay cation.
- Nếu các nguyên tử nhường bớt electron khi tham gia phản ứng hóa học nó sẽ trở thành các phần tử mang điện tích dương hay còn gọi là cation.
Ví dụ: Sự hình thành Cation của nguyên tử Li(Z=3)
Cấu hình e: 1s22s1
1s22s1 → 1s2 + 1e
(Li) (Li+)
Hay: Li → Li+ + 1e
Li+ gọi là cation liti
3. Sự tạo thành anion
- Ion mang điện tích âm gọi là ion âm hay anion.
- Nếu các nguyên tử nhận thêm electron khi tham gia phản ứng hóa học nó sẽ trở thành các phần tử mang điện tích âm hay còn gọi là anion.
Ví dụ: Sự hình thành anion của nguyên tử F(Z=9)
Cấu hình e: 1s22s22p5
1s22s22p5 + 1e → 1s22s22p6
(F) (F-)
Hay: F + 1e → F-
F-gọi là anion florua
4. Ion đơn nguyên tử và ion âm đa nguyên tử
- Ion đơn nguyên tử là ion tạo nên từ 1 nguyên tử .
Thí dụ: cation Li+, Na+, Mg2+và anion F-, Cl-…….
- Ion đa nguyên tử là những nhóm nguyên tử mang điện tích dương hay âm .
Thí dụ: cation amoni NH4+, anion hidroxit OH-, anion sunfat SO42-, …….
III. Sự tạo thành liên kết ion
- Liên kết ion là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Ví dụ: Na+ + Cl- → NaCl
=> Liên kết giữa cation Na+ và anion Cl- là liên kết ion.
Video mô phỏng - Liên kết ion
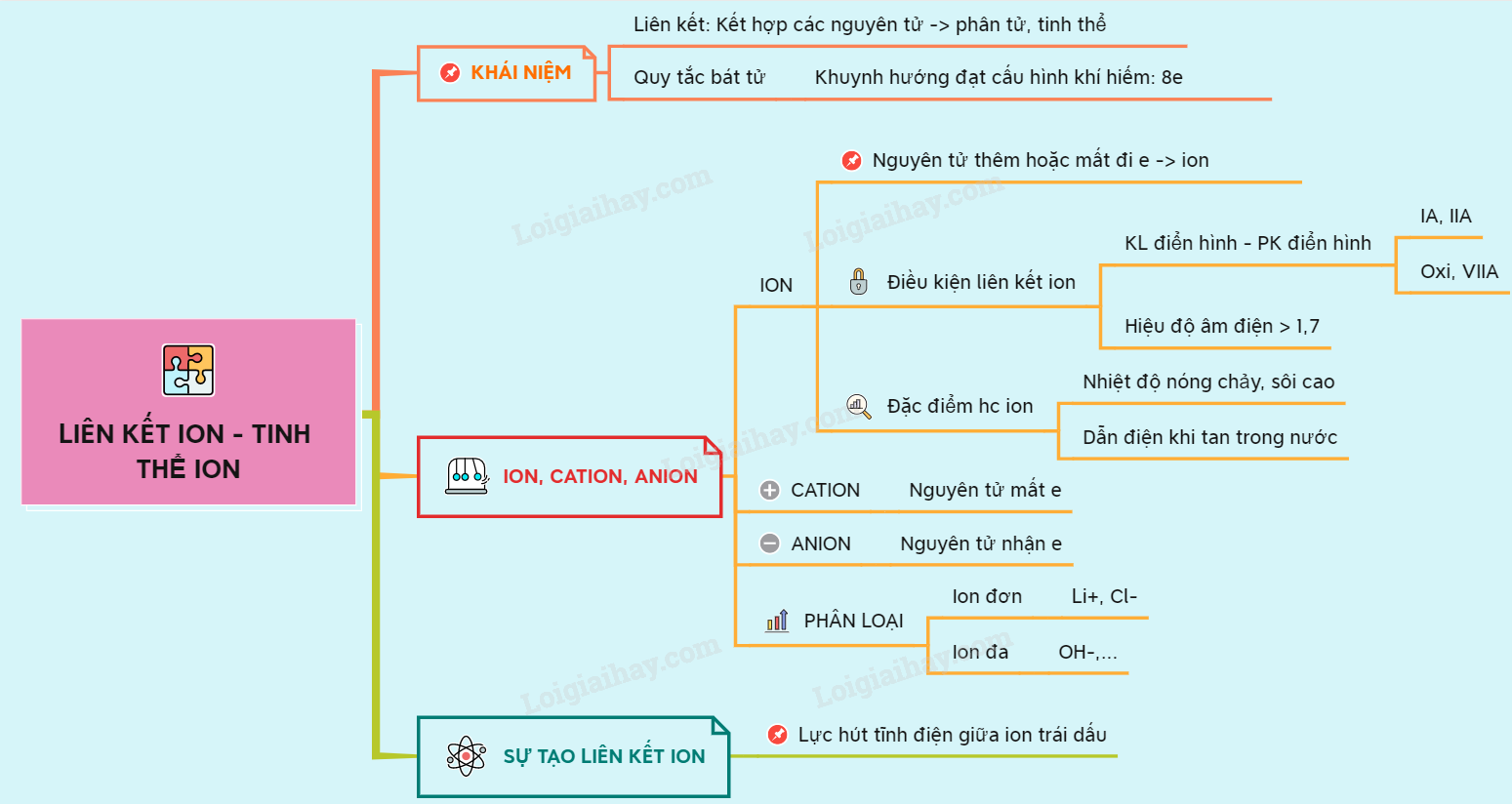
Sơ đồ tư duy: Liên kết ion - tinh thể ion
Loigiaihay.com
Các bài khác cùng chuyên mục













Danh sách bình luận