Đề thi thử THPT QG môn Hóa trường THPT Chuyên Hoàng Văn Thụ
Đề bài
Một mẫu nước cứng chứa các ion : Mg2+ , Ca2+ , Cl- , SO42-. Chất được dùng để làm mềm mẫu nước cứng trên là
-
A.
Na3PO4
-
B.
Ca(OH)2
-
C.
BaCl2
-
D.
NaHCO3
Cho các chất : C2H5OH, CH3COOH, C2H2 , C2H4. Có bao nhiêu chất sinh ra từ CH3CHO bằng một phản ứng
-
A.
3
-
B.
5
-
C.
4
-
D.
2
Chất nào sau đây là amin bậc hai
-
A.
(CH3)2NC2H5
-
B.
CH3NHC2H5
-
C.
(CH3)2CHNH2
-
D.
CH3NH2
Hợp chất nào sau đây dùng để bó bột, đúc tượng
-
A.
CaSO4
-
B.
CaSO4.H2O
-
C.
CaSO4.2H2O
-
D.
CaSO4.3H2O
Muối nào sau đây không bị nhiệt phân
-
A.
NaHCO3
-
B.
MgCO3
-
C.
Ca(HCO3)2
-
D.
Na2CO3
Chất nào sau đây không làm mất màu dung dịch nước brom ở điều kiện thường ?
-
A.
C2H5OH
-
B.
CH3CHO
-
C.
C2H4
-
D.
HCOOH
Tripeptit tham gia phản ứng màu biure tạo thành sản phẩm có màu
-
A.
tím
-
B.
đỏ
-
C.
vàng
-
D.
trắng
Dung dịch HCl có thể phản ứng với tất cả ion hay các chất rắn nào dưới đây
-
A.
Cu(OH)2, Fe(OH)2, FeO, CuO, Ag
-
B.
OH- , CO32-, Na+, K+
-
C.
HSO3- , HCO3-, S2- , AlO2-
-
D.
CaCO3, NaCl, Ba(HCO3)2
Khi thủy phân hợp chất hữu cơ X (không có phản ứng tráng bạc ) trong môi trường axit rồi trung hòa axit thì dung dịch thu được có phản ứng tráng bạc. X là
-
A.
Anđehit axetic
-
B.
Glixerol
-
C.
Saccarozo
-
D.
Mantozo
Chất nào sau đây tác dụng với lượng dư dung dịch Ba(OH)2 tạo thành kết tủa sau phản ứng ?
-
A.
ZnCl2
-
B.
NaHSO4
-
C.
NH4Cl
-
D.
Al(NO3)3
Kim loại nào sau đây có khả năng tác dụng mạnh với nước ở điều kiện thường
-
A.
Fe
-
B.
Al
-
C.
Ba
-
D.
Mg
Este nào sau đây thủy phân trong môi trường axit cho phenol
-
A.
Metyl benzoate
-
B.
Metyl axetat
-
C.
Phenyl axetat
-
D.
Etyl fomat
Khi làm bay hơi 8,14 gam một este đơn chức X thu được một thể tích đúng bằng 3,52 gam O2 đo ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của X là
-
A.
C3H4O2
-
B.
C3H6O2
-
C.
C4H8O2
-
D.
C4H6O2
Cho 0,1 mol FeCl3 phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
-
A.
38,7
-
B.
40,8
-
C.
43,05
-
D.
47,9
Cho m gam Na và Al vào nước thu được 4,48 lít khí H2 đktc. Mặt khác cho m gam hỗn hợp trên vào dung dịch NaOH dư thu được 11,2 lít H2 đktc.Giá trị của m là
-
A.
10,0
-
B.
10,4
-
C.
8,85
-
D.
12,0
Lên men hoàn toàn a gam glucozo, thu được C2H5OH và CO2 . Hấp thụ hết CO2 sinh ra vào dung dịch nước vôi trong dư thu được 15 gam kết tủa.Giá trị của a là
-
A.
30,6
-
B.
27,0
-
C.
13,5
-
D.
15,3
Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ chất rắn X như sau
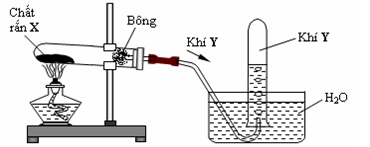
Hình vẽ trên minh họa cho phản ứng nào sau đây ?
-
A.
CaC2 + 2H2O → Ca(OH)2 + C2H2
-
B.
2KMnO4 $\xrightarrow{{{t^o}}}$ K2MnO4 + MnO2 + O2
-
C.
NH4Cl \(\xrightarrow{{{t^o}}}\) NH3 + HCl
-
D.
BaSO3 \(\xrightarrow{{{t^o}}}\) BaO + SO2
Quặng manhetit được dùng để điều chế kim loại nào
-
A.
Chì
-
B.
sắt
-
C.
nhôm
-
D.
đồng
Chất nào sau đây tác dụng với H2 (Ni, to) dư thu được ancol đơn chức
-
A.
HOC – CHO
-
B.
CH2=CH-CHO
-
C.
CH2=CHCOOH
-
D.
C2H4
Dung dịch nào sau đây có pH < 7
-
A.
HCl
-
B.
NaNO3
-
C.
NaCl
-
D.
NaOH
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác, khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư nung nóng, thu được dung dịch chứa a gam muối. Giá trị của a là
-
A.
8,34
-
B.
7,63
-
C.
4,87
-
D.
9,74
Cho các thí nghiệm sau
(a) Cho Ba vào dung dịch chứa phèn chua
(b) Cho FeCl2 vào dung dịch AgNO3
(c) Cho Ca(OH)2 vào Mg(HCO3)2
(d) Sục khí NH3 vào dung dịch hỗn hợp CuCl2 và AlCl3
(e) Cho một miếng nhôm vào dung dịch NaOH dư rồi sục khí CO2 vào
Tổng số thí nghiệm có khả năng tạo kết tủa là :
-
A.
2
-
B.
5
-
C.
3
-
D.
4
Cho hỗn hợp Na2CO3 và KHCO3 (tỉ lệ mol 2:1) vào bình chứa dung dịch Ba(HCO3)2thu được m gam kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 1M vào bình đến khi không còn khí thoát ra thì hết 320 ml. Biết toàn bộ Y phản ứng vừa đủ với 160 ml dung dịch NaOH 1M. Giá trị của m là
-
A.
11,82 gam
-
B.
9,456 gam
-
C.
15,76 gam
-
D.
7,88 gam
Tiến hành các thí nghiệm sau
(a) Ngâm lá đồng trong dung dịch AgNO3
(b) Ngâm lá kẽm trong dung dịch HCl loãng
(c) Ngâm lá nhôm trong dung dịch NaOH
(d) Ngâm lá sắt được cuốn dây đồng trong dung dịch NaOH
(e) Để một vật bằng gang ngoài không khí ẩm
(f) Ngâm một miếng đồng vào dung dịch Fe2(SO4)3
Số thí nghiệm xảy ra ăn mòn điện hóa là
-
A.
2
-
B.
1
-
C.
4
-
D.
3
Chất rắn màu lục, tan trong dung dịch HCl được dung dịch A. Cho A tác dụng với NaOH và Br2 được dung dịch màu vàng, cho dung dịch H2SO4 vào lại thành màu da cam. Chất rắn đó là
-
A.
Cr
-
B.
Cr2O3
-
C.
Cr2O
-
D.
CrO
Tiến hành các thí nghiệm sau :
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí H2S vào dung dịch FeCl3
(c) Cho FeS tác dụng với dung dịch HCl
(d) Cho dung dịch AgNO3 vào dung dịch HCl
(e) Cho tinh thể NaNO2 vào dung dịch NH4Cl bão hòa rồi đun nóng
Số thí nghiệm không sinh ra đơn chất là
-
A.
3
-
B.
4
-
C.
5
-
D.
2
Cho dãy các chất sau : propin, but – 2- in, axit fomic, axit axetic, anđehit axetic, anđehit acrylic, etyl fomat, metyl axetat. Số chất tác dụng với dung dịch AgNO3/NH3 tạo kết tủa là
-
A.
3
-
B.
6
-
C.
5
-
D.
4
Khi xà phòng hóa trieste X bằng dung dịch NaOH dư đun nóng, thu được sản phầm gồm glixerol, natri fomat, natri axetat và natri acrylat. Số đồng phân cấu tạo thỏa mãn tính chất trên của X là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Hợp chất X có công thức phân tử là C6H8O6. X phản ứng với NaOH theo tỉ lệ mol 1 : 3 và phản ứng với AgNO3/NH3 theo tỉ lệ mol 1: 6. X không phản ứng với NaHCO3. Có các kết luận sau :
(1) X có khả năng tham gia phản ứng thủy phân
(2) X có chứa nhóm chức axit cacboxylic
(3) X có chứa nhóm chức este
(4) X có phản ứng với Na
(5) X là hợp chất đa chức
(6) X có chứa liên kết ba đầu mạch
Số kết luận đúng về X là
-
A.
3
-
B.
5
-
C.
4
-
D.
2
Đốt cháy hoàn toàn m gam hidrocacbon ở thể khí, nhẹ hơn không khí, mạch hở thu được 7,04 gam CO2. Sục m gam hidrocacbon này vào nước brom dư đến phản ứng hoàn toàn, thấy có 25,6 gam brom phản ứng. Giá trị của m là
-
A.
3,02
-
B.
2,08
-
C.
3,06
-
D.
2,04
Cho các phát biểu sau :
(a) Đun nóng dung dịch saccarozo trong môi trường axit chỉ thu được glucozo
(b) Nhỏ dung dịch brom vào dung dịch phenol lấy dư thấy xuất hiện kết tủa trắng
(c) Để làm sạch lọ đựng dung dịch anilin thì rửa bằng dung dịch HCl sau đó rửa lại bằng nước
(d) Có thể sử dụng Cu(OH)2 để phân biệt hai dung dịch chứa gly – gly và gly – ala – ala
(e) Có 2 chất trong các chất sau : phenol, etyl axetat, ancol etylic, axit axetic. Số chất tác dụng được với dung dịch NaOH
(f) Dầu thực vật và dầu bôi trơn máy đều có thành phần chính là chất béo
Số phát biểu đúng là
-
A.
4
-
B.
3
-
C.
5
-
D.
2
X, Y, Z là ba axit cacboxylic đơn chức cùng dãy đồng đẳng ( MX < MY < MZ ), T là este tạo bởi X, Y, Z với một ancol no ba chức mạch hở E. Đốt cháy hoàn toàn 26,6 gam hỗn hợp M gồm X, Y, Z, T (trong đó Y, Z có cùng số mol) bằng một lượng khí vừa đủ O2, thu được 22,4 lít CO2 đktc và 16,2 gam H2O. Mặt khác đun nóng 26,6 gam M với lượng dư dung dịch AgNO3/NH3. Sau phản ứng xảy ra hoàn toàn thu được 21,6 gam Ag. Mặt khác cho 13,3 gam M phản ứng hết với 400 ml dung dịch NaOH 1M và đun nóng, thu được dung dịch N. Cô cạn dung dịch N thu được m gam chất rắn khan. Giá trị của m gần nhất với
-
A.
38,04
-
B.
16,74
-
C.
25,10
-
D.
24,74
Cho 0,05 mol hỗn hợp hai este đơn chức X và Y tác dụng vừa đủ với dung dịch NaOH thu được hỗn hợp các chất hữu cơ Z. Đốt cháy hoàn toàn Z thu được 0,12 mol CO2 và 0,03 mol Na2CO3. Làm bay hơi hỗn hợp Z thu được m gam chất rắn. Giá trị của m là
-
A.
3,48
-
B.
4,56
-
C.
5,64
-
D.
2,34
Cho m gam Zn vào 200 ml dung dịch CuSO4 1M và Fe2(SO4)3 0,5M sau phản ứng xảy ra hoàn toàn thu được dung dịch X có khối lượng tăng lên 6,62 gam. Giá trị của m là
-
A.
13,00
-
B.
16,25
-
C.
14,30
-
D.
11,70
Sục CO2 vào 200 gam dung dịch Ca(OH)2, kết quả thí nghiệm được biểu diễn bằng đồ thị sau :
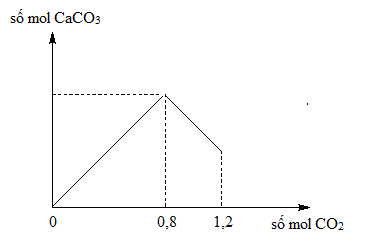
Nồng độ % chất tan trong dung dịch sau phản ứng là
-
A.
30,45%
-
B.
35,40%
-
C.
34,05%
-
D.
45,03%
Hỗn hợp X gồm chất Y ( C2H8O4N2) và chất Z ( C4H8N2O3); trong đó Y là muối của axit đa chức, Z là đipeptit mạch hở. Cho 25,6 gam X tác dụng với dung dịch NaOH dư, đun nóng, thu được 0,2 mol khí. Mặt khác 25,6 gam X tác dụng với dung dịch HCl dư thu được m gam chất hữu cơ. Giá trị của m là
-
A.
23,80
-
B.
31,30
-
C.
16,95
-
D.
20,15
Cho 46,6 gam hỗn hợp X gồm Na, K, Ba và Al2O3 ( trong đó oxi chiếm 30,9% về khối lượng) hòa tan hết trong nước thu được dung dịch Y và 8,96 lít H2 ( đktc). Cho 3,1 lít dung dịch HCl 0,5M vào dung dịch Y thu được m gam kết tủa. Giá trị của m là
-
A.
7,8
-
B.
15,6
-
C.
27,3
-
D.
35,1
Hòa tan hết 14,8 gam hỗn hợp Fe và Cu vào 126 gam dung dịch HNO3 48% thu được dung dịch X (không chứa muối amoni ). Cho X phản ứng với 400 ml dung dịch NaOH 1M và KOH 0,5M thu được kết tủa Y và dung dịch Z. Nung Y trong không khí đến khối lượng không đổi thu được 20 gam CuO và Fe2O3. Cô cạn dung dịch Z, thu được chất rắn khan T. Nung T trong không khí đến khối lượng không đổi thu được 42,86 gam hỗn hợp chất rắn. Nồng độ phần trăm của Fe(NO3)3 trong X có giá trị gần nhất với giá trị nào sau đây ?
-
A.
8,2
-
B.
7,9
-
C.
7,6
-
D.
6,9
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
-
A.
Khối lượng axit picric hình thành bằng 6,87 gam
-
B.
Axit sunfuric đặc đóng vai trò xúc tác cho phản ứng nitro hóa phenol
-
C.
Lượng HNO3 đã tham gia phản ứng là 0,03 mol
-
D.
Sản phẩm thu được có tên gọi là 2,4,6 - trinitrophenol
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là
-
A.
0,4
-
B.
0,6
-
C.
0,5
-
D.
0,3
Lời giải và đáp án
Một mẫu nước cứng chứa các ion : Mg2+ , Ca2+ , Cl- , SO42-. Chất được dùng để làm mềm mẫu nước cứng trên là
-
A.
Na3PO4
-
B.
Ca(OH)2
-
C.
BaCl2
-
D.
NaHCO3
Đáp án : A
Để làm mềm nước cứng thì cần kết tủa hết 2 ion Mg2+ , Ca2+
Chất được dùng để làm mềm mẫu nước cứng trên là Na3PO4 :
Mg2+ + PO43- → Mg3(PO4)2↓
Ca2+ + PO43- → Ca3(PO4)2↓
Cho các chất : C2H5OH, CH3COOH, C2H2 , C2H4. Có bao nhiêu chất sinh ra từ CH3CHO bằng một phản ứng
-
A.
3
-
B.
5
-
C.
4
-
D.
2
Đáp án : D
Xem lại tính chất hóa học của CH3CHO trong sgk hóa 11 – trang 200
Chất sinh ra từ CH3CHO bằng một phản ứng là C2H5OH, CH3COOH
2CH3CHO + O2 \(\xrightarrow{{lenmen}}\) 2CH3COOH
CH3CHO + H2 \(\xrightarrow{{{t^o}}}\) C2H5OH
Chất nào sau đây là amin bậc hai
-
A.
(CH3)2NC2H5
-
B.
CH3NHC2H5
-
C.
(CH3)2CHNH2
-
D.
CH3NH2
Đáp án : B
Bậc của amin bằng số nguyên tử H trong NH3 bị thay thế bằng các gốc R
A là amin bậc 3
B là amin bậc 2
C và D là amin bậc 1
Hợp chất nào sau đây dùng để bó bột, đúc tượng
-
A.
CaSO4
-
B.
CaSO4.H2O
-
C.
CaSO4.2H2O
-
D.
CaSO4.3H2O
Đáp án : B
Xem lại ứng dụng các hợp chất của canxi SGK hóa học lớp 12 trang 115
Hợp chất dùng để bó bột, đúc tượng CaSO4.H2O
Muối nào sau đây không bị nhiệt phân
-
A.
NaHCO3
-
B.
MgCO3
-
C.
Ca(HCO3)2
-
D.
Na2CO3
Đáp án : D
Tất cả muối hidrocacbonat đều bị nhiệt phân
Những muối cacbonat không tan mới bị nhiệt phân
2NaHCO3 \(\xrightarrow{{{t^o}}}\) Na2CO3 + H2O + CO2
MgCO3 \(\xrightarrow{{{t^o}}}\) MgO + CO2
Ca(HCO3)2 \(\xrightarrow{{{t^o}}}\) CaCO3 + H2O + CO2
Na2CO3 không bị nhiệt phân
Chất nào sau đây không làm mất màu dung dịch nước brom ở điều kiện thường ?
-
A.
C2H5OH
-
B.
CH3CHO
-
C.
C2H4
-
D.
HCOOH
Đáp án : A
Những chất có liên kết bội hoặc có nhóm chức như andehit thì tác dụng với dung dịch nước brom ở điều kiện thường
CH3CHO + Br2 + H2O → CH3COOH + 2HBr
C2H4 + Br2 → C2H4Br2
HCOOH + Br2 → CO2 + 2HBr
Tripeptit tham gia phản ứng màu biure tạo thành sản phẩm có màu
-
A.
tím
-
B.
đỏ
-
C.
vàng
-
D.
trắng
Đáp án : A
Tripeptit tham gia phản ứng màu biure tạo thành sản phẩm có màu tím
Dung dịch HCl có thể phản ứng với tất cả ion hay các chất rắn nào dưới đây
-
A.
Cu(OH)2, Fe(OH)2, FeO, CuO, Ag
-
B.
OH- , CO32-, Na+, K+
-
C.
HSO3- , HCO3-, S2- , AlO2-
-
D.
CaCO3, NaCl, Ba(HCO3)2
Đáp án : C
Ghi nhớ lại TCHH của HCl
+ làm quỳ tím đổi sang màu đỏ
+ tác dụng với oxit bazo, bazo
+ Tác dụng với kim loại (đứng trước H)
+ Tác dụng với muối
A có Ag không phản ứng với HCl
B có Na+, K+ không tác dụng với HCl
C phản ứng hết với HCl
D có NaCl không phản ứng
Khi thủy phân hợp chất hữu cơ X (không có phản ứng tráng bạc ) trong môi trường axit rồi trung hòa axit thì dung dịch thu được có phản ứng tráng bạc. X là
-
A.
Anđehit axetic
-
B.
Glixerol
-
C.
Saccarozo
-
D.
Mantozo
Đáp án : C
Xem lại TCHH của andehit, ancol, saccarozo và mantozo
X không có phản ứng tráng bạc nên X không thể là andehit axetic và mantozo
Khi thủy phân X trong môi trường axit thu được sản phẩm có khả năng tráng bạc nên X là saccazoro vì C12H22O11 thủy phân tạo C6H12O6 có khả năng tráng bạc
Chất nào sau đây tác dụng với lượng dư dung dịch Ba(OH)2 tạo thành kết tủa sau phản ứng ?
-
A.
ZnCl2
-
B.
NaHSO4
-
C.
NH4Cl
-
D.
Al(NO3)3
Đáp án : B
Xem lại TCHH của Ba(OH)2
Ba(OH)2 + NaHSO4 → BaSO4 + NaOH + H2O
Kim loại nào sau đây có khả năng tác dụng mạnh với nước ở điều kiện thường
-
A.
Fe
-
B.
Al
-
C.
Ba
-
D.
Mg
Đáp án : C
Những kim loại tác dụng với nước là kim loại kiềm và kiềm thổ (trừ Be, Mg)
Ba + 2H2O → Ba(OH)2 + H2↑
Este nào sau đây thủy phân trong môi trường axit cho phenol
-
A.
Metyl benzoate
-
B.
Metyl axetat
-
C.
Phenyl axetat
-
D.
Etyl fomat
Đáp án : C
Xem lại TCHH của este
Este thủy phân trong môi trường axit cho phenol là phenyl axetat
CH3COOC6H5 + H2O \(\xrightarrow{{{H^ + }}}\) CH3COOH + C6H5OH
Khi làm bay hơi 8,14 gam một este đơn chức X thu được một thể tích đúng bằng 3,52 gam O2 đo ở cùng điều kiện nhiệt độ và áp suất. Công thức phân tử của X là
-
A.
C3H4O2
-
B.
C3H6O2
-
C.
C4H8O2
-
D.
C4H6O2
Đáp án : B
nX = nO2 = 0,11 mol → MX = 8,14 : 0,11 = 74
→ Este đơn chức X có công thức dạng CxHyO2 → 12x + y + 32 =74
=> biện luận giá trị x, y thỏa mãn
nX = nO2 = 0,11 mol → MX = 8,14 : 0,11 = 74 (g/mol)
→ Este đơn chức X có công thức dạng CxHyO2 → 12x + y + 32 =74
→ 12x + y = 42
→ thỏa mãn x = 3 và y = 6 → X là C3H6O2
Cho 0,1 mol FeCl3 phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
-
A.
38,7
-
B.
40,8
-
C.
43,05
-
D.
47,9
Đáp án : C
Tính theo PTHH: FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl↓
FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl↓
0,1 → 0,3 mol
→ m ↓ = mAgCl = 0,3 . 143,5 = 43,05
Cho m gam Na và Al vào nước thu được 4,48 lít khí H2 đktc. Mặt khác cho m gam hỗn hợp trên vào dung dịch NaOH dư thu được 11,2 lít H2 đktc.Giá trị của m là
-
A.
10,0
-
B.
10,4
-
C.
8,85
-
D.
12,0
Đáp án : B
2Na + 2H2O → 2NaOH + H2↑
2NaOH + 2Al + 2H2O → 2NaAlO2 + 3H2↑
nH2(TH1) = 0,2 mol và nH2(TH2) = 0,5 mol
Vì nH2(TH1) < nH2(TH2) nên trường hợp 1 cho hỗn hợp vào nước thì Al chưa phản ứng hết
2Na + 2H2O → 2NaOH + H2
2NaOH + 2Al + 2H2O → 2NaAlO2 + 3H2
Đặt nNa = x và nAl = y
nH2(TH1) = 0,2 mol và nH2(TH2) = 0,5 mol
Vì nH2(TH1) < nH2(TH2) nên trường hợp 1 cho hỗn hợp vào nước thì Al chưa phản ứng hết
→ nH2(TH1) = \(\dfrac{x}{2} + \dfrac{{3x}}{2} = 2x = 0,2\) → x = 0,1 mol
Khi cho hỗn hợp vào dung dịch NaOH dư nên \({n_{{H_2}}} = \dfrac{x}{2} + \dfrac{{3y}}{2} = 0,5 \to y = 0,3\) mol
→ m = 23x + 27y = 23.0,1 + 27.0,3 = 10,4 g
Lên men hoàn toàn a gam glucozo, thu được C2H5OH và CO2 . Hấp thụ hết CO2 sinh ra vào dung dịch nước vôi trong dư thu được 15 gam kết tủa.Giá trị của a là
-
A.
30,6
-
B.
27,0
-
C.
13,5
-
D.
15,3
Đáp án : C
Glucozo → 2C2H5OH + 2CO2↑
CO2 + Ca(OH)2 → CaCO3↓ + H2O
BTNT “C”: nGlu = 1/2 nCO2 = 1/2 nCaCO3 =?
C6H12O6 → 2C2H5OH + 2CO2↑
CO2 + Ca(OH)2 → CaCO3↓ + H2O
nCaCO3 = 0,15 mol nên nCO2 = 0,15 mol
→ nglucozo = 0,075 mol → a = 0,075.180 = 13,5 g
Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ chất rắn X như sau

Hình vẽ trên minh họa cho phản ứng nào sau đây ?
-
A.
CaC2 + 2H2O → Ca(OH)2 + C2H2
-
B.
2KMnO4 $\xrightarrow{{{t^o}}}$ K2MnO4 + MnO2 + O2
-
C.
NH4Cl \(\xrightarrow{{{t^o}}}\) NH3 + HCl
-
D.
BaSO3 \(\xrightarrow{{{t^o}}}\) BaO + SO2
Đáp án : B
Thu được khí Y bằng phương pháp đẩy nước => Y không tan hoặc rất ít tan trong nước
=> chọn rắn X khi nhiệt phân tạo khí Y không tan hoặc rất ít tan trong nước
Đun nóng rắn X thu được khí Y không bị hòa tan trong nước nên đáp án B vì khí tạo ra là O2 vì O2 không bị hòa tan trong nước còn NH3 và SO2 tan nhiều trong nước
Quặng manhetit được dùng để điều chế kim loại nào
-
A.
Chì
-
B.
sắt
-
C.
nhôm
-
D.
đồng
Đáp án : B
Ghi nhớ tên gọi và các công thức hóa học phổ biến của sắt sgk hóa 12 – trang 140
Quặng manhetit là quặng Fe3O4
Quặng manhetit là Fe3O4→ được dùng để điều chế sắt
Chất nào sau đây tác dụng với H2 (Ni, to) dư thu được ancol đơn chức
-
A.
HOC – CHO
-
B.
CH2=CH-CHO
-
C.
CH2=CHCOOH
-
D.
C2H4
Đáp án : B
Ancol đơn chức được tạo ra từ phản ứng của andehit đơn chức hoặc xeton đơn chức tác dụng với H2 ( Ni, to )
Chất tác dụng với H2 tạo ancol đơn chức là CH2=CH-CHO
CH2=CH-CHO + H2 \(\xrightarrow{{Ni,{t^o}}}\) CH3-CH2-CH2OH
Dung dịch nào sau đây có pH < 7
-
A.
HCl
-
B.
NaNO3
-
C.
NaCl
-
D.
NaOH
Đáp án : A
Dung dịch axit có pH < 7. Dung dịch có tính bazo có pH > 7 và dung dịch trung tính có pH = 7
Dung dịch nào sau đây có pH < 7 là dung dịch axit HCl
Đốt cháy hoàn toàn 4,03 gam triglixerit X bằng một lượng oxi vừa đủ, cho toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng nước vôi trong dư thu được 25,5 gam kết tủa và khối lượng dung dịch thu được giảm 9,87 gam so với khối lượng nước vôi trong ban đầu. Mặt khác, khi thủy phân hoàn toàn 8,06 gam X trong dung dịch NaOH dư nung nóng, thu được dung dịch chứa a gam muối. Giá trị của a là
-
A.
8,34
-
B.
7,63
-
C.
4,87
-
D.
9,74
Đáp án : A
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3
mdd giảm = mkết tủa - mH2O – mCO2 → nH2O
→ X có nC = nCO2 và nH = 2nH2O → CTPT của X
Bảo toàn khối lượng tìm mmuối
4,03 gam X + O2 → CO2 + H2O
Đưa sản phẩm qua bình đựng nước vôi trong nCO2 = nCaCO3 = 0,255 mol
mdd giảm = mkết tủa - mH2O – mCO2 → 25,5 - mH2O - 0,255.44 = 9,87 → nH2O = 0,245 mol
→ X có nC = nCO2 =0,255 mol và nH = 2nH2O = 2.0,245 =0,49 mol
→ nO = \(\dfrac{{4,03 - 0,255.12 - 0,49.1}}{{16}} = 0,03\) mol
Vì X là triglixerit nên X có 6 O trong CTPT → \({n_X} = \dfrac{{{n_O}}}{6} = 0,005 \Rightarrow \left\{ \begin{gathered}C = \frac{{0,255}}{{0,005}} = 51 \hfill \\H = \dfrac{{0,49}}{{0,005}} = 98 \hfill \\\end{gathered} \right.\)
→ X : C51H98O6
Xét 8,06 g X + NaOH → muối + glixerol thì
nX = \(\dfrac{{8,06}}{{12.51 + 98.1 + 16.6}} = 0,01\) →nNaOH = 3nX =0,03 mol và nglixerol = nX = 0,01 mol
Bảo toàn khối lượng có mmuối = mX + mNaOH – mglixerol = 8,06 + 0,03.40 – 0,01 .92 =8,34 g
Cho các thí nghiệm sau
(a) Cho Ba vào dung dịch chứa phèn chua
(b) Cho FeCl2 vào dung dịch AgNO3
(c) Cho Ca(OH)2 vào Mg(HCO3)2
(d) Sục khí NH3 vào dung dịch hỗn hợp CuCl2 và AlCl3
(e) Cho một miếng nhôm vào dung dịch NaOH dư rồi sục khí CO2 vào
Tổng số thí nghiệm có khả năng tạo kết tủa là :
-
A.
2
-
B.
5
-
C.
3
-
D.
4
Đáp án : B
Viết PTHH xảy ra, từ đó xác định được các thí nghiệm có kết tủa.
(a) tạo kết tủa BaSO4 có thể có thêm Al(OH)3
Ba + 2H2O → Ba(OH)2 + H2↑
Ba2+ + SO42- → BaSO4↓ + H2O
Al3+ + 3OH- → Al(OH)3↓
(b) tạo kết tủa AgCl và Ag
FeCl2 + 2AgNO3 → 2AgCl↓ + Fe(NO3)2
Fe(NO3)2 + AgNO3 → Ag↓ + Fe(NO3)3
(c) tạo kết tủa CaCO3 và MgCO3
Ca(OH)2 + Mg(HCO3)2 → CaCO3↓ + MgCO3↓ + 2H2O
(d) tạo Al(OH)3 có thể có Cu(OH)2
NH3 + H2O + AlCl3 → Al(OH)3↓ + NH4Cl
NH3 + H2O + CuCl2 → Cu(OH)2↓ + NH4Cl
4NH3 + Cu(OH)2 → Cu(NH3)4(OH)2 phức tan
(e) tạo kết tủa Al(OH)3 không tan trong CO2
Al + NaOH + H2O → NaAlO2 + 3/2H2↑
Cho hỗn hợp Na2CO3 và KHCO3 (tỉ lệ mol 2:1) vào bình chứa dung dịch Ba(HCO3)2thu được m gam kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 1M vào bình đến khi không còn khí thoát ra thì hết 320 ml. Biết toàn bộ Y phản ứng vừa đủ với 160 ml dung dịch NaOH 1M. Giá trị của m là
-
A.
11,82 gam
-
B.
9,456 gam
-
C.
15,76 gam
-
D.
7,88 gam
Đáp án : A
Xét dung dịch Y :
Y tác dụng được với 0,16 mol NaOH nên Y có HCO3- : HCO3- + OH- → CO32- + H2O
→ nHCO3
Y + HCl : 0,32 mol thì H+ + HCO3- → H2O + CO2
BaCO3 +2H+ → Ba2+ +H2O + CO2
Có thế có : CO32- + 2H+ → H2O + CO2
→ nCO3 + nBaCO3
Bảo toàn C → nNa2CO3
Xét dung dịch Y :
Y tác dụng được với 0,16 mol NaOH nên Y có HCO3- : HCO3- + OH- → CO32- + H2O
→ nHCO3 = 0,16 mol
Y + HCl : 0,32 mol thì H+ + HCO3- → H2O + CO2
BaCO3 +2H+ → Ba2+ +H2O + CO2
Có thế có : CO32- + 2H+ → H2O + CO2
→ nCO3 + nBaCO3 = ( 0,32 – 0,16 ) : 2 = 0,08 mol
Xét phản ứng Na2CO3 và KHCO3 + Ba(HCO3)2
CO32- + Ba2+ → BaCO3
Bảo toàn C có nNa2CO3 = nCO3(Y) + nBaCO3 = 0,08 → nKHCO3 = 0,04
Sau pư có nHCO3 = 0,04 + 2nBa(HCO3)2 = 0,16
→ nBa(HCO3)2 = 0,06 → pư trên có CO32- dư nên nBaCO3 = 0,06
→ mBaCO3 = 11,82 g
Tiến hành các thí nghiệm sau
(a) Ngâm lá đồng trong dung dịch AgNO3
(b) Ngâm lá kẽm trong dung dịch HCl loãng
(c) Ngâm lá nhôm trong dung dịch NaOH
(d) Ngâm lá sắt được cuốn dây đồng trong dung dịch NaOH
(e) Để một vật bằng gang ngoài không khí ẩm
(f) Ngâm một miếng đồng vào dung dịch Fe2(SO4)3
Số thí nghiệm xảy ra ăn mòn điện hóa là
-
A.
2
-
B.
1
-
C.
4
-
D.
3
Đáp án : D
Điều kiện để xảy ra ăn mòn điện hóa học là
+ Xuất hiện ít nhất 2 điện cực khác nhau về bản chất như: KL –KL; KL – PK; KL- Hợp chất
+ các chất tham gia phản ứng tiếp xúc trực tiếp hoặc gián tiếp với nhau
+ Cùng nhúng trong 1 dung dịch chất điện li
(a) tạo ra 2 kim loại là Cu và Ag nên là ăn mòn điện hóa
(b) là ăn mòn hóa học
(c) là ăn mòn hóa học
(d) là ăn mòn điện hóa
(e) là ăn mòn điện hóa
(f) là ăn mòn hóa học
Chất rắn màu lục, tan trong dung dịch HCl được dung dịch A. Cho A tác dụng với NaOH và Br2 được dung dịch màu vàng, cho dung dịch H2SO4 vào lại thành màu da cam. Chất rắn đó là
-
A.
Cr
-
B.
Cr2O3
-
C.
Cr2O
-
D.
CrO
Đáp án : B
xem lại TCHH của các hợp chất của crom sgk hóa 12 – trang 152
A là chất rắn màu xanh lục nên A là Cr2O3
Cr2O3 + 6HCl → 2CrCl3 + 3H2O
CrCl3 + NaOH + Br2 →Na2CrO4 + NaBr
(màu vàng)
2Na2CrO4 + 2H+ → Na2Cr2O7 + 2Na+ + H2O
Tiến hành các thí nghiệm sau :
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí H2S vào dung dịch FeCl3
(c) Cho FeS tác dụng với dung dịch HCl
(d) Cho dung dịch AgNO3 vào dung dịch HCl
(e) Cho tinh thể NaNO2 vào dung dịch NH4Cl bão hòa rồi đun nóng
Số thí nghiệm không sinh ra đơn chất là
-
A.
3
-
B.
4
-
C.
5
-
D.
2
Đáp án : D
Viết PTHH
(a) Mg + Fe2(SO4)3 → MgSO4 + FeSO4
(b) H2S + FeCl3 → FeCl2 +HCl + S↓
(c) FeS + 2HCl → FeCl2 + H2S
(d) AgNO3 + HCl → AgCl↓ + HNO3
(e) NaNO2 + NH4Cl → NaCl + N2↑ + 2H2O
Số thí nghiệm không sinh đơn chất là 2
Cho dãy các chất sau : propin, but – 2- in, axit fomic, axit axetic, anđehit axetic, anđehit acrylic, etyl fomat, metyl axetat. Số chất tác dụng với dung dịch AgNO3/NH3 tạo kết tủa là
-
A.
3
-
B.
6
-
C.
5
-
D.
4
Đáp án : C
Chất tạo kết tủa với dung dịch AgNO3/NH3 là những chất có nối ba đầu mạch, andehit hoặc các chất có dạng nhóm andehit như este hay muối của axit fomic
Số chất tác dụng với dung dịch AgNO3/NH3 tạo kết tủa là propin, axit fomic, anđehit axetic, anđehit acrylic, etyl fomat
Khi xà phòng hóa trieste X bằng dung dịch NaOH dư đun nóng, thu được sản phầm gồm glixerol, natri fomat, natri axetat và natri acrylat. Số đồng phân cấu tạo thỏa mãn tính chất trên của X là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : C
Viết đồng phân trieste tạo bởi ancol glixerol và 3 axit khác nhau
X là Trieste của glixerol và 3 axit hữu cơ khác nhau là axit acrylic, axit fomic và axit axetic
→ X có số đồng phân là 3
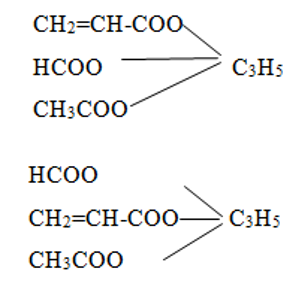
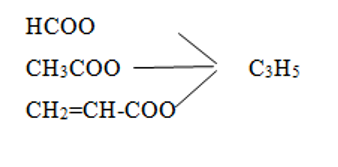
Hợp chất X có công thức phân tử là C6H8O6. X phản ứng với NaOH theo tỉ lệ mol 1 : 3 và phản ứng với AgNO3/NH3 theo tỉ lệ mol 1: 6. X không phản ứng với NaHCO3. Có các kết luận sau :
(1) X có khả năng tham gia phản ứng thủy phân
(2) X có chứa nhóm chức axit cacboxylic
(3) X có chứa nhóm chức este
(4) X có phản ứng với Na
(5) X là hợp chất đa chức
(6) X có chứa liên kết ba đầu mạch
Số kết luận đúng về X là
-
A.
3
-
B.
5
-
C.
4
-
D.
2
Đáp án : A
X có số liên kết pi + vòng = \(\dfrac{{2.6 - 8 + 2}}{2} = 3\)
X phản ứng với NaOH theo tỉ lệ 1 : 3 và phản ứng với AgNO3/NH3 theo tỉ lệ mol 1: 6 nên X là Trieste của HCOOH
X có số liên kết pi + vòng = \(\dfrac{{2.6 - 8 + 2}}{2} = 3\)
X phản ứng với NaOH theo tỉ lệ 1 : 3 và phản ứng với AgNO3/NH3 theo tỉ lệ mol 1: 6 nên X là Trieste của HCOOH
X là (HCOO)3C3H5
1. Đúng, X tham gia phản ứng thủy phân cả môi trường axit và bazo
2. Sai. X chứa nhóm coboxyl COO-
3. Đúng
4. Sai
5. Đúng
6. Sai
=> có 3 kết luận đúng
Đốt cháy hoàn toàn m gam hidrocacbon ở thể khí, nhẹ hơn không khí, mạch hở thu được 7,04 gam CO2. Sục m gam hidrocacbon này vào nước brom dư đến phản ứng hoàn toàn, thấy có 25,6 gam brom phản ứng. Giá trị của m là
-
A.
3,02
-
B.
2,08
-
C.
3,06
-
D.
2,04
Đáp án : B
Đặt CTPT : CnH2n+2-2k ( k là số liên kết pi)
CnH2n+2-2k + k Br2 → CnH2n+2-2k Br2k
Bảo toàn C có nhc = \(\frac{{{n_{C{O_2}}}}}{n} = \frac{{0,16}}{n}\) mol → nBr2 = \(\frac{{0,16}}{n}.k\) = 0,16 → k = n → biện luận với n ≤ 4
Đặt CTPT : CnH2n+2-2k ( k là số liên kết pi)
CnH2n+2-2k + k Br2 → CnH2n+2-2k Br2k
Bảo toàn C có nhc = \(\dfrac{{{n_{C{O_2}}}}}{n} = \dfrac{{0,16}}{n}\) mol → nBr2 = \(\dfrac{{0,16}}{n}.k\) = 0,16 → k = n → Hidrocacbon là CnH2
Với k = n = 1 thì HC là : CH2 loại
Với k = n = 2 thì HC là C2H2 → m = 0,08 . 26 =2,08 g
Với k = n = 3 thì HC là C3H2 ( không có CTHH thỏa mãn )
Với k = n =4 thì HC là C4H2 → m = 0,04.50 = 2 g
Cho các phát biểu sau :
(a) Đun nóng dung dịch saccarozo trong môi trường axit chỉ thu được glucozo
(b) Nhỏ dung dịch brom vào dung dịch phenol lấy dư thấy xuất hiện kết tủa trắng
(c) Để làm sạch lọ đựng dung dịch anilin thì rửa bằng dung dịch HCl sau đó rửa lại bằng nước
(d) Có thể sử dụng Cu(OH)2 để phân biệt hai dung dịch chứa gly – gly và gly – ala – ala
(e) Có 2 chất trong các chất sau : phenol, etyl axetat, ancol etylic, axit axetic. Số chất tác dụng được với dung dịch NaOH
(f) Dầu thực vật và dầu bôi trơn máy đều có thành phần chính là chất béo
Số phát biểu đúng là
-
A.
4
-
B.
3
-
C.
5
-
D.
2
Đáp án : B
Xem lại lý thuyết về cacbohidrat, phenol, amin, peptit, lipit
(a) Sai vì đun nóng dung dịch saccarozo trong môi trường axit thu được cả glucozo và fructozo
(b) Đúng
(c) Đúng vì tạo muối C6H5NH3Cl dễ tan
(d) Đúng vì gly – gly không có phản ứng biure nhưng gly – ala – ala thì có
(e) Sai vì có 3 chất tác dụng được với dung dịch NaOH : phenol, etyl axetat, axit axetic
(f) Sai vì dầu bôi trơn máy có thành phần chính là hidrocacbon
=> có 3 phát biểu đúng
X, Y, Z là ba axit cacboxylic đơn chức cùng dãy đồng đẳng ( MX < MY < MZ ), T là este tạo bởi X, Y, Z với một ancol no ba chức mạch hở E. Đốt cháy hoàn toàn 26,6 gam hỗn hợp M gồm X, Y, Z, T (trong đó Y, Z có cùng số mol) bằng một lượng khí vừa đủ O2, thu được 22,4 lít CO2 đktc và 16,2 gam H2O. Mặt khác đun nóng 26,6 gam M với lượng dư dung dịch AgNO3/NH3. Sau phản ứng xảy ra hoàn toàn thu được 21,6 gam Ag. Mặt khác cho 13,3 gam M phản ứng hết với 400 ml dung dịch NaOH 1M và đun nóng, thu được dung dịch N. Cô cạn dung dịch N thu được m gam chất rắn khan. Giá trị của m gần nhất với
-
A.
38,04
-
B.
16,74
-
C.
25,10
-
D.
24,74
Đáp án : D
M có phản ứng tráng bạc nên M có chứa HCOOH (X). Đặt Y là R1COOH; (Z) là R2COOH và (E): R'(OH)3
(T) : (HCOO)(R1COO)(R2COO)R’
Gọi x, y, z lần lượt là số mol X, Y, T → nZ = y mol. Vì Y và Z là 2 axit thuộc cùng dãy đồng đẳng của HCOOH nên khi đốt cháy thì thu được nCO2 = nH2O .
T là este no, mạch hở, ba chức nên khi đốt T thì thu được:
\(z = \dfrac{1}{2}({n_{C{O_2}(T)}} - {n_{{H_2}O(T)}}) = \dfrac{1}{2}({n_{C{O_2}(M)}} - {n_{{H_2}O(M)}})\)
Theo định luật bảo toàn khối lượng:
mM + mO2= mCO2 +mH2O→ mO2 → nO2
Theo bảo toàn nguyên tố O:x + 2y = ?
M + AgNO3/NH3:
→ nAg → x → y
→ mM theo R1, R2 và R’ → biện luận tìm ra R1, R2 và R’
M có phản ứng tráng bạc nên M có chứa HCOOH (X). Đặt Y là R1COOH; (Z) là R2COOH và (E): R'(OH)3
(T) : (HCOO)(R1COO)(R2COO)R’
nCO2 = 1 mol; nH2O =0,9 mol
Gọi x, y, z lần lượt là số mol X, Y, T → nZ = y mol. Vì Y và Z là 2 axit thuộc cùng dãy đồng đẳng của HCOOH nên khi đốt cháy thì thu được nCO2 = nH2O .
T là este no, mạch hở, ba chức nên khi đốt T thì thu được:
\(z = \dfrac{1}{2}({n_{C{O_2}(T)}} - {n_{{H_2}O(T)}}) = \dfrac{1}{2}({n_{C{O_2}(M)}} - {n_{{H_2}O(M)}}) = \dfrac{{1 - 0,9}}{2} = 0,05\)
Theo định luật bảo toàn khối lượng:
mM + mO2= mCO2 +mH2O → mO2 = 44 + 16,2 – 26,6 = 33,6 gam → nO2 =1,05 mol
Theo bảo toàn nguyên tố O:
2(x + 2y) + 6.0,05 + 2.1,05 = 2 + 0,9 → x + 2y = 0,25 (*)
M + AgNO3/NH3:
HCOOH \(\xrightarrow{{ + AgN{O_3}/N{H_3}}}2Ag\)
x 2x
(HCOO)(R1COO)(R2COO)R’\(\xrightarrow{{ + AgN{O_3}/N{H_3}}}2Ag\)
z 2z
→ nAg = 2x + 0,1 = 21,6: 108 = 0,2 → x = 0,05 mol thế vào (8) → y = 0,1 mol
→ mM = 46.0,05 + 0,1(R1+ 45) + 0,1(R2+ 45) + 0,05(133 + R1+ R2+ R') = 26,6
→ 0,15R1+ 0,15R2 + 0,05R' = 8,65
→ 3R1+ 3R2 + R' = 173
Do R1 ≥ 15; R2 ≥ 29; R' ≥ 41 → 3R1 + 3R2 + R' ≥ 173
Thỏa mãn là R1= 15 (CH3-); R2= 29 (C2H5-) và R' = 41 (C3H5)
→ Y là CH3COOH, Z là C2H5COOH và T là (HCOO)(CH3COO)(C2H5COO)C3H5
→ 13,3 gam M + 0,4 mol NaOH :
HCOOH + NaOH → HCOONa + H2O
0,025 0,025
CH3COOH + NaOH → CH3COONa + H2O
0,05 0,05
C2H5COOH + NaOH → C2H5COONa + H2O
0,05 0,05
(HCOO)(CH3COO)(C2H5COO)C3H5 + 3NaOH → HCOONa + CH3COONa + C2H5COONa + C3H5(OH)3
→ mchất rắn = 13,3 + 40.0,4 – 18.0,125 – 92.0,025 = 24,75 gam gần nhất với 24,74
Cho 0,05 mol hỗn hợp hai este đơn chức X và Y tác dụng vừa đủ với dung dịch NaOH thu được hỗn hợp các chất hữu cơ Z. Đốt cháy hoàn toàn Z thu được 0,12 mol CO2 và 0,03 mol Na2CO3. Làm bay hơi hỗn hợp Z thu được m gam chất rắn. Giá trị của m là
-
A.
3,48
-
B.
4,56
-
C.
5,64
-
D.
2,34
Đáp án : B
Bảo toàn Na có 2nNa2CO3 = nNaOH = 0,06 mol
→ vì 0,05 mol X và Y tác dụng với 0,06 mol NaOH nên 1 trong 2 chất là este của phenol
→ giả sử X là este của phenol : x mol và Y : y mol nên x + y =0,05 và 2x + y =0,06
→ x và y
Gọi số C của X là a, số C của Y là b thì 0,01a + 0,04 b = 0,12 + 0,03 = 0,15
→a và b → X và Y
Bảo toàn Na có 2nNa2CO3 = nNaOH = 0,06 mol
→ vì 0,05 mol X và Y tác dụng với 0,06 mol NaOH nên 1 trong 2 chất là este của phenol
→ giả sử X là este của phenol : x mol và Y : y mol nên x + y =0,05 và 2x + y =0,06
Nên x = 0,01 mol và y = 0,04 mol
Gọi số C của X là a, số C của Y là b thì 0,01a + 0,04 b = 0,12 + 0,03 = 0,15
Vì X là este của phenol nên a ≥ 7 → thỏa mãn a = 7 và b = 2
→ X là HCOOC6H5 và Y là HCOOCH3
→ Z gồm HCOONa : 0,05 mol; C6H5ONa : 0,01 ; CH3OH : 0,04
→ m = 4,56 (g)
Cho m gam Zn vào 200 ml dung dịch CuSO4 1M và Fe2(SO4)3 0,5M sau phản ứng xảy ra hoàn toàn thu được dung dịch X có khối lượng tăng lên 6,62 gam. Giá trị của m là
-
A.
13,00
-
B.
16,25
-
C.
14,30
-
D.
11,70
Đáp án : C
Zn tác dụng với dd chứa CuSO4 : 0,2 mol và Fe2(SO4)3 : 0,1 mol
Zn + 2Fe3+ → 2Fe2+ + Zn2+
0,1 ← 0,2 0,2
mtăng = 0,1.65 =6,5 gam nên tiếp tục có phản ứng
Zn + Cu2+ → Zn2+ + Cu
Xét mtăng khi Cu2+ phản ứng hết → nếu nhỏ hơn thì tiếp tục có phản ứng đẩy Fe2+
Nếu lớn hơn thì phản ứng trên dư Cu2+
Zn tác dụng với dd chứa CuSO4 : 0,2 mol và Fe2(SO4)3 : 0,1 mol
Zn + 2Fe3+ → 2Fe2+ + Zn2+
0,1 ← 0,2 0,2
mtăng = 0,1.65 =6,5 gam nên tiếp tục có phản ứng
Zn + Cu2+ → Zn2+ + Cu
0,2 0,2 0,2
→ mtăng = 6,5 + 0,2(65 – 64 ) =6,7 nên phản ứng trên Cu2+ dư
Đặt nCu(2+) pư = x thì mtăng = 6,5 + (65 – 64 ).x= 6,62 → x = 0,12 mol
→ mZn = (0,12 + 0,1) . 65 =14,3
Sục CO2 vào 200 gam dung dịch Ca(OH)2, kết quả thí nghiệm được biểu diễn bằng đồ thị sau :

Nồng độ % chất tan trong dung dịch sau phản ứng là
-
A.
30,45%
-
B.
35,40%
-
C.
34,05%
-
D.
45,03%
Đáp án : A
Tại thời điểm kết tủa lớn nhất Ca(OH)2 + CO2 → CaCO3 + H2O
→ nCa(OH)2 = nCO2 = 0,8 mol
Tại thời điểm CO2 : 1,2 mol thì sinh ra thêm phản ứng sau
CaCO3 + CO2 + H2O → Ca(HCO3)2
Tại thời điểm kết tủa lớn nhất Ca(OH)2 + CO2 → CaCO3 + H2O
→ nCa(OH)2 = nCO2 = 0,8 mol
Tại thời điểm CO2 : 1,2 mol thì CaCO3 + CO2 + H2O → Ca(HCO3)2
Ban đầu : 0,8 mol 0,4
Sau Pư 0,4 0 0,4
Bảo toàn khối lượng mdd sau pư = 1,2.44 + 200 – 0,4 .100 =212,8 gam
\( \to \% Ca{(HC{O_3})_2} = \dfrac{{0,4.162}}{{212,8}}.100\% = 30,45\% \)
Hỗn hợp X gồm chất Y ( C2H8O4N2) và chất Z ( C4H8N2O3); trong đó Y là muối của axit đa chức, Z là đipeptit mạch hở. Cho 25,6 gam X tác dụng với dung dịch NaOH dư, đun nóng, thu được 0,2 mol khí. Mặt khác 25,6 gam X tác dụng với dung dịch HCl dư thu được m gam chất hữu cơ. Giá trị của m là
-
A.
23,80
-
B.
31,30
-
C.
16,95
-
D.
20,15
Đáp án : B
Y là NH4 – OOC – COO – NH4
Z là H2N – CH2 – CO – NH – CH2 – COOH
Tính theo PTHH
Y là NH4 – OOC – COO – NH4 : a mol
Z là H2N – CH2 – CO – NH – CH2 – COOH : b mol
X + NaOH : nkhí = nNH3 = 2a = 0,2 mol
mX = 124a + 132b = 25,6 nên a = 0,1 và b = 0,1 mol
X + HCl thì → 0,1 mol (COOH)2 và 0,2 mol H3NCl – CH2 – COOH → m = 31,30 (g)
Cho 46,6 gam hỗn hợp X gồm Na, K, Ba và Al2O3 ( trong đó oxi chiếm 30,9% về khối lượng) hòa tan hết trong nước thu được dung dịch Y và 8,96 lít H2 ( đktc). Cho 3,1 lít dung dịch HCl 0,5M vào dung dịch Y thu được m gam kết tủa. Giá trị của m là
-
A.
7,8
-
B.
15,6
-
C.
27,3
-
D.
35,1
Đáp án : C
mO(X) = 46,6 . 0,309 = 14,4 gam nên nO = ?
→ \({n_{A{l_2}{O_3}}} = ?\) mol
X có nNa = x; nK = y; nBa = z mol
X + H2O có : Na → Na+ +1e K → K+ +1e
Ba → Ba2+ + 2e 2H+1 +2e → H2
Bảo toàn e có → x + y + 2z → nOH-
2OH- + Al2O3 → 2AlO2- + H2O
→ Sau phản ứng có X có : OH- : ? mol và AlO2- : ? mol, Ba2+, Na+, K+
mO(X) = 46,6 . 0,309 = 14,4 gam nên nO = 0,9 mol
Lại có \({n_{O(X)}} = 3{n_{A{l_2}{O_3}}} \Rightarrow {n_{A{l_2}{O_3}}} = 0,3\) mol
X có nNa = x; nK = y; nBa = z mol thì mX = 23x + 39y + 137z + 102.0,3 =46,6
X + H2O có : Na → Na+ +1e K → K+ +1e
Ba → Ba2+ + 2e 2H+1 +2e → H2
Bảo toàn e có x + y + 2z = 0,4.2 =0,8 mol → nOH- = x + y + 2z = 0,8 mol
2OH- + Al2O3 → 2AlO2- + H2O
→ Sau phản ứng có X có : OH- : 0,2 mol và AlO2- : 0,6 mol, Ba2+, Na+, K+
X + 1,55 mol HCl có
H+ + OH- → H2O
H+ + AlO2- + H2O → Al(OH)3
→ H+ dư : 1,55 – 0,8 = 0,75 mol
Al(OH)3 + 3H+ → Al3+ + 3H2O
0,25 ← 0,75
→ Al(OH)3 : 0,35 mol → mkết tủa = 0,35.78 = 27,3 (g)
Hòa tan hết 14,8 gam hỗn hợp Fe và Cu vào 126 gam dung dịch HNO3 48% thu được dung dịch X (không chứa muối amoni ). Cho X phản ứng với 400 ml dung dịch NaOH 1M và KOH 0,5M thu được kết tủa Y và dung dịch Z. Nung Y trong không khí đến khối lượng không đổi thu được 20 gam CuO và Fe2O3. Cô cạn dung dịch Z, thu được chất rắn khan T. Nung T trong không khí đến khối lượng không đổi thu được 42,86 gam hỗn hợp chất rắn. Nồng độ phần trăm của Fe(NO3)3 trong X có giá trị gần nhất với giá trị nào sau đây ?
-
A.
8,2
-
B.
7,9
-
C.
7,6
-
D.
6,9
Đáp án : B
Từ m hỗn hợp KL và m hỗn hợp CuO và Fe2O3 → số mol Cu và Fe
Xét dd Z : Z chỉ chứa 2 muối NaNO3 và KNO3 thì khi đun nóng thu được KNO2 và NaNO2
Bảo toàn nguyên tố có nNaNO2 = nNaOH và nKOH = nKNO2
→ mrắn > 42,86 nên Z còn chứa cả NaOH và KOH
Z chứa : Na+ : 0,4 mol; K+ : 0,2 mol; OH- : a mol và NO3- : b mol
→ bảo toàn điện tích và lập phương trình tính mrắn =42,86 → a và b
→ dd X chứa Fe2+ : c mol; Fe3+ : d mol và Cu2+ : ? mol; NO3- : ? mol
Bảo toàn điện tích và bảo toàn nguyên tố Fe → c và d
Quy đổi sản phẩm khử thành O và N
Bảo toàn khối lượng tính mdd X
nHNO3 = 0,96 mol và nNaOH = 0,4 mol, nKOH = 0,2
đặt nFe = x mol và nCu = y mol
Bảo toàn nguyên tố có nFe2O3 = ½ . nFe = ½ .x
nCuO = nCu = y
Ta có hệ phương trình sau 56x + 64 y = 14,8 gam và 80x + 80y = 20
→ x = 0,15 mol và y = 0,1 mol
Nếu dung dịch Z chỉ chứa 2 muối NaNO3 và KNO3 thì khi đun nóng thu được KNO2 và NaNO2
Bảo toàn nguyên tố có nNaNO2 = nNaOH = 0,4 và nKOH = 0,2 = nKNO2
→ mrắn = 0,4.69 +0,2. 85 = 44,6 gam > 42,86 nên Z còn chứa cả NaOH và KOH
Z chứa : Na+ : 0,4 mol; K+ : 0,2 mol; OH- : a mol và NO3- : b mol
Bảo toàn điện tích có 0,4 + 0,2 = a + b (*)
Đun nóng Z có 0,4 mol Na ; K+ : 0,2 mol; OH- : a mol và NO2- : b mol
→ 17a + 46b + 0,2.39 + 0,4.23 = 42,86 (**)
Từ (*) và (**) → a = 0,06 và b = 0,54
→ dd X chứa Fe2+ : c mol; Fe3+ : d mol và Cu2+ : 0,1 mol; NO3- : 0,54 mol (cùng bằng lượng NO3- trong Z )
Bảo toàn điện tích có 2c + 3d + 0,1.2 = 0,54 (***)
Bảo toàn Fe có c + d =0,15 (****)
Từ (***) và (****) → c = 0,11 và d =0,04 mol
Bảo toàn nguyên tố có nN (sp khử) = nHNO3 – nNO3(Y) = 0,96 – 0,54 =0,42 mol
Quy đổi khí sản phẩm khử là N : 0,42 mol và O : e mol
Bảo toàn e có 2nFe(2+) + 3nFe(3+) + 2nCu(2+) -2nO = 5nN
→ 5.0,42 = 2.0,11 +3.0,04 + 0,1.2 +2e
→ e =0,78 mol
Bảo toàn khối lượng mdd X =mKL +mHNO3 – mN – mO
= 14,8 + 126 – 0,42.14 – 0,78.16 =122,44 g
Nồng độ % của Fe(NO3)3 là : \(\dfrac{{0,04.242}}{{122,44}}.100\% = 7,9\% \)
Cho 0,01 mol phenol tác dụng hoàn toàn với lượng dư dung dịch hỗn hợp HNO3 đặc và H2SO4 đặc. Phát biểu nào sau đây không đúng
-
A.
Khối lượng axit picric hình thành bằng 6,87 gam
-
B.
Axit sunfuric đặc đóng vai trò xúc tác cho phản ứng nitro hóa phenol
-
C.
Lượng HNO3 đã tham gia phản ứng là 0,03 mol
-
D.
Sản phẩm thu được có tên gọi là 2,4,6 - trinitrophenol
Đáp án : A
Tính theo PTHH
C6H5OH + 3HNO3 → C6H2(O2N)3OH + 3H2O
0,01 → 0,03 → 0,01
→ maxit picric = 2,29 gam → A sai
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 với điện cực trơ, sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng thanh sắt giảm 1,8 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là
-
A.
0,4
-
B.
0,6
-
C.
0,5
-
D.
0,3
Đáp án : C
Vì dung dịch thu được có phản ứng với Fe rạo khí NO nên dung dịch có H+ và NO3-
Tại A có 2Cl- → Cl2 + 2e 2H2O → 4H+ + O2 + 4e
Tại K có Cu2+ + 2e → Cu
Bảo toàn e
Khối lượng của dung dịch giảm là mdd giảm = ? → nCu = ?
Dung dịch thu được sau phản ứng có : Cu2+ ; H+ ; NO3- , Na+
3Fe + 8H+ + 2NO3- → 3Fe2+ + 4H2O + 2NO
Cu2+ + Fe → Fe2+ + Cu
Vì dung dịch thu được có phản ứng với Fe rạo khí NO nên dung dịch có H+ và NO3-
Tại A có 2Cl- → Cl2 + 2e 2H2O → 4H+ + O2 + 4e
0,2 mol → 0,2 mol e y mol
Tại K có Cu2+ + 2e → Cu
Bảo toàn e có nCu = ( 0,2 + 4y) : 2
→ khối lượng của dung dịch giảm là mdd giảm = ( 0,2 + 4y) : 2 .64 + 0,1.71 + y.32 = 21,5
→ y = 0,05 mol → nCu = 0,2 mol
Dung dịch thu được sau phản ứng có : Cu2+ (x – 0,2) mol ; H+ : 0,2 mol; NO3- : 2x, Na+ : 0,1 mol
3Fe + 8H+ + 2NO3- → 3Fe2+ + 4H2O + 2NO
Cu2+ + Fe → Fe2+ + Cu
→mthanh giảm = 64.(x-0,2) – 56 .(x – 0.2 + \(\frac{3}{8}\) .0,2) = -1,8 → x = 0,5
















