Đề thi thử THPT QG môn Hóa trường THPT chuyên Đại học Vinh lần 3
Đề bài
Từ thời thượng cổ con người đã biết sơ chế các hợp chất hữu cơ. Cách làm nào sau đây là phương pháp kết tinh?
-
A.
Làm đường cát, đường phèn từ mía.
-
B.
Giã cây chàm, cho vào nước, lọc lấy dung dịch màu để nhuộm sợi, vải.Nấu rượu để uống.
-
C.
Nấu rượu để uống.
-
D.
Ngâm rượu thuốc.
Chất nào sau đây khi cho tác dụng với H2SO4 đặc, nóng không có khí thoát ra?
-
A.
FeO.
-
B.
Fe(OH)2.
-
C.
Fe2O3.
-
D.
Fe3O4.
Cho 16 gam Fe2O3 phản ứng vừa đủ với V ml dung dịch HCl 1M. Giá trị của V là
-
A.
400
-
B.
300
-
C.
200
-
D.
600
Chất nào sau đây làm đổi màu quỳ tím?
-
A.
Lysin.
-
B.
Glyxin.
-
C.
Alanin.
-
D.
Valin.
Trong máu người luôn có nồng độ gluxit X không đổi là 0,1%. Nếu lượng X trong máu giảm đi thì người đó mắc bệnh suy nhược.Ngược lại nếu lượng X trong máu tăng lên thì đó là người mắc bệnh tiểu đường hay đường huyết. Chất X là
-
A.
Glucozơ.
-
B.
Mantozơ.
-
C.
Saccarozơ.
-
D.
Fructozơ.
Môi trường không khí, đất, nước xung quanh các nhà máy hóa chất thường bị ô nhiễm nặng bởi khí độc, ion kim loại nặng và các hóa chất. Biện pháp nào sau đây không thể chống ô nhiễm môi trường?
-
A.
Sử dụng công nghệ sản xuất hiện đai, nhiên liệu sạch.
-
B.
Xả chất thải trực tiếp ra môi trường.
-
C.
Thực hiện chu trình khép kín để tận dụng chất thải một cách hiệu quả.
-
D.
Có hệ thống xử lí chất thải hợp lí trước khi xả thải ra môi trường.
Trong các kim loại sau, kim loại nào không phải là kim loại kiềm thổ?
-
A.
Ca.
-
B.
Be.
-
C.
Mg.
-
D.
Na.
Cho các chất sau: Fe(NO3)3, FeCl2, NaHCO3, Al(OH)3. Có bao nhiêu chất tác dụng với dung dịch HCl?
-
A.
1
-
B.
4
-
C.
3
-
D.
2
Polime nào sau đây có cấu trúc mạch phân nhánh?
-
A.
Xenlulozơ.
-
B.
Polietilen.
-
C.
Amilopectin.
-
D.
Amilozơ.
Khi cho chất X vào dung dịch kiềm, lúc đầu thu được kết tủa màu trắng hơi xanh, sau đó chuyển dần sang nâu đỏ khi đưa ra ngoài không khí. Chất X là
-
A.
FeSO4.
-
B.
AlCl3.
-
C.
MgSO4.
-
D.
CuSO4.
Kali nitrat được dùng làm phân bón và chế tạo thuốc nổ. Công thức của kali nitrat là?
-
A.
KHCO3.
-
B.
KNO2.
-
C.
K3PO4.
-
D.
KNO3.
Trong công nghiệp kim loại Cr được điều chế bằng phương pháp nào sau đây?
-
A.
Điện phân nóng chảy.
-
B.
Nhiệt nhôm.
-
C.
Điện phân dung dịch.
-
D.
Thủy luyện.
Benzyl axetat có mùi thơm của hoa nhài. Công thức phân tử của benzyl axetat là
-
A.
C9H8O2.
-
B.
C9H10O2.
-
C.
C8H10O2.
-
D.
C9H10O4.
Chất có khả năng tham gia phản ứng cộng với H2 (xúc tác Ni, đun nóng) là
-
A.
C2H5OH.
-
B.
CH3NH2.
-
C.
CH3COOC2H3.
-
D.
CH3COOH.
Xà phòng hóa este X hai chức có công thức phân tử C5H8O4 thu được sản phẩm có khả năng hòa tan Cu(OH)2 tạo dung dịch xanh lam. Số công thức cấu tạo phù hợp của X là
-
A.
4
-
B.
3
-
C.
1
-
D.
2
Nhóm các vật liệu được chế tạo từ polime trùng ngưng là
-
A.
Cao su, tơ tằm, tơ lapsan.
-
B.
Thủy tinh plexiglas, nilon-6,6, tơ nitron.
-
C.
Nilon-6,6, nilon-6, tơ lapsan.
-
D.
Tơ visco, nilon-6, nilon-6,6.
Đốt cháy hoàn toàn một amino axit X (phân tử có 1 nhóm NH2) thu được 8,8 gam CO2 và 1,12 lít N2. Công thức phân tử của X là
-
A.
C3H7NO2.
-
B.
C4H9NO2.
-
C.
C2H7NO2.
-
D.
C2H5NO2.
Cho m gam hỗn hợp gồm axit axetic, axit oxalic, axit glutamic tác dụng vừa đủ với V ml dung dịch NaOH 1M thu được dung dịch chứa (m + 8,8) gam muối. Giá trị của V là
-
A.
200
-
B.
400
-
C.
250
-
D.
300
Xenlulozơ trinitrat được điều chế từ xenlulozơ và axit nitric đặc có xúc tác là axit sunfuric đặc, đun nóng. Để có 59,4 kg xenlulozơ trinitrat cần dung dịch chứa m kg axit nitric (hiệu suất 90%). Giá trị của m là
-
A.
42,0.
-
B.
30,0.
-
C.
14,0.
-
D.
37,8.
Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch chứa chất X
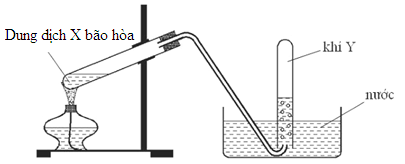
Cặp chất X, Y phù hợp là
-
A.
Cu(NO3)2 và NO2.
-
B.
NH4NO2 và N2.
-
C.
CH3COONa và CH4
-
D.
KClO3 và Cl2.
m gam chất rắn. Giá trị của m là Cho 12 gam Fe vào 100 ml dung dịch chứa CuSO4 1M và Fe2(SO4)3 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được
-
A.
12,8.
-
B.
9,2.
-
C.
7,2.
-
D.
6,4.
Nhận xét nào sau đây là sai?
-
A.
Để gang hoặc thép trong không khí ẩm sẽ xảy ra hiện tượng ăn mòn điện hóa học.
-
B.
Trong ăn mòn hóa học, electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
-
C.
Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài của vỏ tàu (phần chìm dưới nước) những lá Zn - đây là cách chống ăn mòn kim loại bằng phương pháp bảo vệ bề mặt.
-
D.
Trong tự nhiên, sự ăn mòn kim loại xảy ra phức tạp, có thể xảy ra đồng thời quá trình ăn mòn điện hóa học và ăn mòn hóa học.
Đốt cháy hoàn toàn este X thu được CO2 và H2O có số mol bằng nhau, X có thể là este
-
A.
No, mạch hở, đơn chức.
-
B.
No, ba chức.
-
C.
No, mạch hở, hai chức.
-
D.
Không no, mạch hở, đơn chức.
Phản ứng nào sau đây không phải là phản ứng trao đổi?
-
A.
FeCO3 + 2HCl → FeCl2 + CO2 + H2O.
-
B.
NH4Cl + NaOH → NaCl + NH3 + H2O.
-
C.
Na2SO4 + BaCl2 → BaSO4 + 2NaCl.
-
D.
2FeCO3 + 4H2SO4 → Fe2(SO4)3 + SO2 + 2CO2+ 4H2O.
Cho 200 ml dung dịch NaOH 3M vào 100 ml dung dịch AlCl3 1M thu được dung dịch X. Nhỏ từ từ đến hết V ml dung dịch HCl 1M vào dung dịch X thu được 5,85 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị lớn nhất của V là
-
A.
425
-
B.
275.
-
C.
175
-
D.
375
Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước dư thu được dung dịch X. Điện phân dung dịch X với điện cực trơ đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối hơi so với H2 bằng 30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử hiệu suất của quá trình điện phân là 100%, khí sinh ra không tan trong dung dịch. Giá trị của m là
-
A.
48,25
-
B.
64,25
-
C.
62,25
-
D.
56,25
Cho các thí nghiệm sau:
(1) Cho hỗn hợp gồm x mol Cu và x mol Fe3O4 vào dung dịch chứa 4x mol H2SO4 loãng.
(2) Cho hỗn hợp NaHSO4 và KHCO3 (tỉ lệ mol 1:1) vào nước dư.
(3) Cho x mol Fe vào dung dịch chứa 2,5x mol AgNO3.
(4) Cho dung dịch chứa x mol Ba(OH)2 vào dung dịch chứa x mol NaHCO3.
(5) Cho Na2CO3 dư vào dung dịch chứa BaCl2.
(6) Cho x mol Fe3O4 vào dung dịch chứa 8x mol HCl.
Sau khi các phản ứng kết thúc mà sau thí nghiệm thu được dung dịch chứa 2 muối là
-
A.
4
-
B.
6
-
C.
5
-
D.
3
Hấp thụ hết 0,2 mol khí CO2 vào dung dịch chứa x mol NaOH và y mol Na2CO3 thu được 100 ml dung dịch X. Lấy 50 ml dung dịch X tác dụng với dung dịch Ca(OH)2 dư thu được 20 gam kết tủa. Mặt khác, khi lấy 50 ml dung dịch X cho từ từ vào 150 ml dung dịch HCl 1M thu được 0,12 mol khí CO2. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x và y lần lượt là
-
A.
0,1 và 0,45
-
B.
0,14 và 0,2.
-
C.
0,12 và 0,3
-
D.
0,1 và 0,2
Hỗn hợp X gồm các triglixerit trong phân tử đều chứa axit stearic, axit oleic, axit linoleic. Đốt cháy hoàn toàn m gam X cần a mol O2 thu được 0,285 mol CO2. Xà phòng hóa hoàn toàn m gam X bằng dung dịch NaOH vừa đủ được m1 gam muối. Giá trị a và m1 lần lượt là
-
A.
0,8 và 8,82.
-
B.
0,4 và 4,32.
-
C.
0,4 và 4,56.
-
D.
0,75 và 5,62.
Bảng dưới đây ghi lại hiện tượng phản ứng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z và T
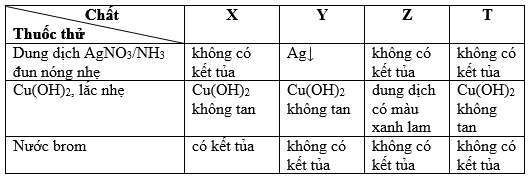
Các chất X, Y, Z, T lần lượt là
-
A.
phenol, anđehit fomic, glixerol, etanol.
-
B.
anilin, gilxerol, anđehit fomic, metyl fomat
-
C.
phenol, axetanđehit, etanol, anđehit fomic
-
D.
glixerol, etylen glicol, metanol, axetanđehit.
Cho từ từ dung dịch HCl loãng vào dung dịch chứa NaOH và NaAlO2 (hay Na[Al(OH)4]. Sự phụ thuộc của số mol kết tủa thu được vào số mol của HCl được biểu diễn theo đồ thị sau:
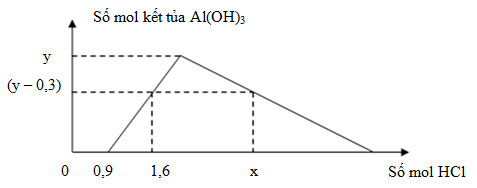
Tổng giá trị của (x + y) là
-
A.
3,5
-
B.
3,8
-
C.
3,1
-
D.
2,2
Cho 14,6 gam Gly-Ala tác dụng hết với dung dịch HCl dư được dung dịch X. Cô cạn dung dịch X được bao nhiêu gam muối khan?
-
A.
23,7 gam.
-
B.
28,6 gam.
-
C.
19,8 gam.
-
D.
21,9 gam.
Cho các phát biểu sau:
(1) Este có nhiệt độ sôi thấp hơn so với axit và ancol có cùng số nguyên tử cacbon.
(2) Dầu ăn và mỡ bôi trơn có cùng thành phần nguyên tố.
(3) Tên thay thế của amin có công thức (CH3)3N là trimetylamin
(4) Dung dịch 37 - 40% fomanđehit trong nước gọi là fomalin (còn gọi là fomon) được dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng.
(5) Các chất: cocain, amphetamin, heroin, moocphin là những chất gây nghiện, hết sức nguy hại cho sức khỏe con người.
Có bao nhiêu phát biểu sai?
-
A.
3
-
B.
1
-
C.
4
-
D.
2
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm metan, axetilen, buta-1,3-đien và vinyl axetilen thu được 24,2 gam CO2 và 7,2 gam nước. Biết a mol hỗn hợp X làm mất màu tối đa 112 gam Br2 trong dung dịch. Giá trị của a là
-
A.
0,2
-
B.
0,4
-
C.
0,1
-
D.
0,3
Chia hỗn hợp X gồm Fe, Fe3O4, Fe(OH)3 và FeCO3 thành hai phần bằng nhau. Hòa tan hết phần 1 trong dung dịch HCl dư, thu được 0,1 mol hỗn hợp 2 khí có tỉ khối so với He bằng 4,7 và dung dịch Y. Cho phần 2 tác dụng với lượng dư dung dịch H2SO4 đặc nóng, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Z và 0,2075 mol hỗn hợp khí T gồm CO2 và SO2 (sản phẩm khử duy nhất của S+6).
Khối lượng FeCl2 trong dung dịch Y là
-
A.
25,307 gam.
-
B.
27,305 gam.
-
C.
23,705 gam.
-
D.
25,075 gam.
Hòa tan hoàn toàn 2 chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch NH3 dư vào dung dịch Z thu được x1 mol kết tủa
Thí nghiệm 2: Cho dung dịch Na2CO3 dư vào dung dịch Z thu được x2 mol kết tủa
Thí nghiệm 3: Cho dung dịch Ba(OH)2 dư vào dung dịch Z thu được x3 mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và x1 < x2 < x3. Hai chất X, Y lần lượt là
-
A.
BaCl2 và FeCl2
-
B.
AlCl3 và FeCl3
-
C.
ZnSO4 và Al2(SO4)3
-
D.
FeSO4 và Fe2(SO4)3
Hỗn hợp E gồm axit no, đơn chức X, axit đa chức Y (phân tử có 3 liên kết π, mạch không phân nhánh) đều mạch hở và este Z (chỉ chứa nhóm chức este, không chứa nhóm chức khác) tạo bởi ancol đa chức T với X và Y. Đốt cháy hoàn toàn 14,93 gam E cần dùng 0,3825 mol O2. Mặt khác, 14,93 gam E phản ứng tối đa với 260 ml dung dịch NaOH 1M thu được m gam ancol T. Đốt cháy hoàn toàn m gam T thu được 1,98 gam CO2 và 1,08 gam H2O. Nhận xét nào sau đây sai
-
A.
Tổng số nguyên tử H trong phân tử Z là 10.
-
B.
Có thể dùng dung dịch Br2 để nhận biết X, Y, T.
-
C.
Y có đồng phân hình học cis – trans.
-
D.
Z có 2 công thức cấu tạo phù hợp.
Hỗn hợp M gồm 2 axit cacboxylic no, mạch hở (phân tử chỉ chứa nhóm chức –COOH) và một ancol no, mạch hở. Đốt cháy hoàn toàn m gam M thu được CO2 và 10,8 gam H2O. Nếu đun nóng m gam M trên (với xúc tác H2SO4 đặc) thấy các chất trong hỗn hợp phản ứng với nhau vừa đủ, chỉ thu được H2O và este X (phân tử chỉ chứa chức este, giả thiết phản ứng este hóa đạt hiệu suất 100%). Để đốt cháy hoàn toàn lượng X sinh ra thì cần dùng vừa đủ 0,5625 mol O2 thu được hỗn hợp CO2 và H2O thỏa mãn điều kiện 3nX phản ứng = nCO2 - nH2O. Công thức phân tử của X là
-
A.
C8H8O4.
-
B.
C7H8O6.
-
C.
C7H6O6.
-
D.
C8H10O6.
Hòa tan hoàn toàn 20,7 gam hỗn hợp X gồm Na, Ba, BaO và Na2O vào nước dư thu được 4 lít dung dịch Y có pH = 13 và 0,05 mol khí H2. Cho 4 lít dung dịch Y tác dụng với 100 ml dung dịch chứa H2SO4 0,3M và Al2(SO4)3 0,5M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m gần nhất với
-
A.
35
-
B.
30
-
C.
25
-
D.
42
Cho 0,2 mol hỗn hợp gồm X (C3H10O2N2) và Y (C4H12O4N2) tác dụng vừa đủ với 300 ml dung dịch NaOH 1M thu được amin Z có tỉ khối so với H2 bằng 15,5 và dung dịch T. Cô cạn dung dịch T thu được hỗn hợp G gồm 2 muối có số nguyên tử C bằng nhau. Phần trăm khối lượng của muối có phân tử khối lớn hơn trong G có giá trị gần nhất với giá trị nào sau đây?
-
A.
64
-
B.
42
-
C.
58
-
D.
35
Lời giải và đáp án
Từ thời thượng cổ con người đã biết sơ chế các hợp chất hữu cơ. Cách làm nào sau đây là phương pháp kết tinh?
-
A.
Làm đường cát, đường phèn từ mía.
-
B.
Giã cây chàm, cho vào nước, lọc lấy dung dịch màu để nhuộm sợi, vải.Nấu rượu để uống.
-
C.
Nấu rượu để uống.
-
D.
Ngâm rượu thuốc.
Đáp án : A
Phương pháp kết tinh dùng để tách hỗn hợp các chất rắn có độ tan khác nhau và sự thay đổi độ tan theo nhiệt độ của chúng để tách và tinh chế
a) phương pháp kết tinh
b) phương pháp chiết
c) phương pháp chưng cất
d) phương pháp chiết
Chất nào sau đây khi cho tác dụng với H2SO4 đặc, nóng không có khí thoát ra?
-
A.
FeO.
-
B.
Fe(OH)2.
-
C.
Fe2O3.
-
D.
Fe3O4.
Đáp án : C
Chất nào chỉ xảy ra phản ứng trao đổi sẽ không có khí thoát ra
Fe2O3 + H2SO4 đặc, nóng chỉ xảy ra phản ứng trao đổi nên không có khí thoát ra
Fe2O3 + 3H2SO4 đặc, nóng → Fe2(SO4)3 + 3H2O
Cho 16 gam Fe2O3 phản ứng vừa đủ với V ml dung dịch HCl 1M. Giá trị của V là
-
A.
400
-
B.
300
-
C.
200
-
D.
600
Đáp án : D
Tính mol HCl theo mol Fe2O3 dựa vào PTHH sau: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
nFe2O3 = 16 : 160 = 0,1 (mol)
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
0,1 → 0,6 (mol)
=> VHCl = nHCl : CM = 0,6 : 1 = 0,6 (lít) = 600 (ml)
Chất nào sau đây làm đổi màu quỳ tím?
-
A.
Lysin.
-
B.
Glyxin.
-
C.
Alanin.
-
D.
Valin.
Đáp án : A
amino axit có dạng: R(COOH)x(NH2)y
+ Nếu x = y thì không làm quỳ tím chuyển màu
+ Nếu x < y thì quỳ tím chuyển sang màu xanh
+ Nếu x > y thì quỳ tím chuyển sang màu đỏ
Lysin (H2N-[CH2]4-CH2(NH2)-COOH) phân tử có 2 nhóm NH2 và 1 nhóm -COOH nên có tính bazo do vậy làm quỳ tím chuyển sang màu xanh
Các chất còn lại: Glyxin, alanin, valin không làm quỳ tím chuyển màu vì có 1 nhóm NH2 và 1 nhóm -COOH
Trong máu người luôn có nồng độ gluxit X không đổi là 0,1%. Nếu lượng X trong máu giảm đi thì người đó mắc bệnh suy nhược.Ngược lại nếu lượng X trong máu tăng lên thì đó là người mắc bệnh tiểu đường hay đường huyết. Chất X là
-
A.
Glucozơ.
-
B.
Mantozơ.
-
C.
Saccarozơ.
-
D.
Fructozơ.
Đáp án : A
Dựa vào ứng dụng của các chất trong nhóm cacbohidart
Chất X là Glucozơ
Môi trường không khí, đất, nước xung quanh các nhà máy hóa chất thường bị ô nhiễm nặng bởi khí độc, ion kim loại nặng và các hóa chất. Biện pháp nào sau đây không thể chống ô nhiễm môi trường?
-
A.
Sử dụng công nghệ sản xuất hiện đai, nhiên liệu sạch.
-
B.
Xả chất thải trực tiếp ra môi trường.
-
C.
Thực hiện chu trình khép kín để tận dụng chất thải một cách hiệu quả.
-
D.
Có hệ thống xử lí chất thải hợp lí trước khi xả thải ra môi trường.
Đáp án : B
Dựa vào kiến thức hiểu biết thực tế
Xả chất thải trực tiếp ra môi trường không thể chống được ô nhiễm môi trường
Trong các kim loại sau, kim loại nào không phải là kim loại kiềm thổ?
-
A.
Ca.
-
B.
Be.
-
C.
Mg.
-
D.
Na.
Đáp án : D
Dựa vào kiến thức ghi nhớ các kim loại kiềm thổ là các kim loại thuộc nhóm IIA trong bảng hệ thống tuần hoàn.
Na là kim loại kiềm chứ không phải kim loại kiềm thổ
Cho các chất sau: Fe(NO3)3, FeCl2, NaHCO3, Al(OH)3. Có bao nhiêu chất tác dụng với dung dịch HCl?
-
A.
1
-
B.
4
-
C.
3
-
D.
2
Đáp án : D
Điều kiện để 1 chất có phản ứng với dd HCl là sinh ra chất kết tủa, bay hơi hoặc chất điện li yếu như H2O.
Các chất tác dụng được với dung dịch HCl là: NaHCO3, Al(OH)3.
NaHCO3 + HCl → NaCl + CO2↑ + H2O
Al(OH)3 + 3HCl → AlCl3 + 3H2O
→ có 2 chất
Polime nào sau đây có cấu trúc mạch phân nhánh?
-
A.
Xenlulozơ.
-
B.
Polietilen.
-
C.
Amilopectin.
-
D.
Amilozơ.
Đáp án : C
Amilopectin có cấu trúc mạch phân nhánh
Khi cho chất X vào dung dịch kiềm, lúc đầu thu được kết tủa màu trắng hơi xanh, sau đó chuyển dần sang nâu đỏ khi đưa ra ngoài không khí. Chất X là
-
A.
FeSO4.
-
B.
AlCl3.
-
C.
MgSO4.
-
D.
CuSO4.
Đáp án : A
Nhớ màu sắc kết tủa của các hidroxit: Fe(OH)2 màu trắng xanh; Fe(OH)3 màu nâu đỏ; Al(OH)3: trắng keo
Mg(OH)2: màu trắng; Cu(OH)2: màu xanh
Từ đó chọn được X phù hợp
Chất X là FeSO4; kết tủa trắng xanh là Fe(OH)2; kết tủa nâu đỏ là Fe(OH)3
Kali nitrat được dùng làm phân bón và chế tạo thuốc nổ. Công thức của kali nitrat là?
-
A.
KHCO3.
-
B.
KNO2.
-
C.
K3PO4.
-
D.
KNO3.
Đáp án : D
Công thức của kali nitrat là KNO3
Trong công nghiệp kim loại Cr được điều chế bằng phương pháp nào sau đây?
-
A.
Điện phân nóng chảy.
-
B.
Nhiệt nhôm.
-
C.
Điện phân dung dịch.
-
D.
Thủy luyện.
Đáp án : B
Dựa vào kiến thức điều chế crom trong sgk hóa 12
Trong công nghiệp, Cr được điều chế bằng phương pháp nhiệt nhôm
Cr2O3 + 2Al \(\xrightarrow{{{t^0}}}\) Cr + Al2O3
Phương pháp này điều chế được Cr có độ tinh khiết từ 97-99%
Benzyl axetat có mùi thơm của hoa nhài. Công thức phân tử của benzyl axetat là
-
A.
C9H8O2.
-
B.
C9H10O2.
-
C.
C8H10O2.
-
D.
C9H10O4.
Đáp án : B
Tên este: RCOOR' = tên gốc R' + gốc RCOO + at
Công thức của benzyl axetat là CH3COOCH2C6H5 → có CTPT là: C9H10O2
Chất có khả năng tham gia phản ứng cộng với H2 (xúc tác Ni, đun nóng) là
-
A.
C2H5OH.
-
B.
CH3NH2.
-
C.
CH3COOC2H3.
-
D.
CH3COOH.
Đáp án : C
Chất có liên kết bội (nối đôi, ba) trong phân tử sẽ có phản ứng với H2 (xúc tác Ni, đun nóng)
CH3COOCH=CH2 + H2 \(\xrightarrow{{Ni,{t^0}}}\) CH3COOCH2-CH3
Xà phòng hóa este X hai chức có công thức phân tử C5H8O4 thu được sản phẩm có khả năng hòa tan Cu(OH)2 tạo dung dịch xanh lam. Số công thức cấu tạo phù hợp của X là
-
A.
4
-
B.
3
-
C.
1
-
D.
2
Đáp án : D
→ X là este 2 chức tạo bởi axit đơn chức và ancol 2 chức có 2 nhóm -OH cạnh nhau
→ Viết các CTCT thỏa mãn
C5H8O4 có độ bất bão hòa k = (5.2+2-8)/2 = 2
X + NaOH → chất có khả năng hòa tan dd Cu(OH)2 taoh dd màu xanh lam
→ X là este 2 chức tạo bởi axit đơn chức và ancol 2 chức có 2 nhóm -OH cạnh nhau
→ Có 2 CTCT thỏa mãn
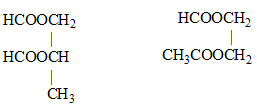
Nhóm các vật liệu được chế tạo từ polime trùng ngưng là
-
A.
Cao su, tơ tằm, tơ lapsan.
-
B.
Thủy tinh plexiglas, nilon-6,6, tơ nitron.
-
C.
Nilon-6,6, nilon-6, tơ lapsan.
-
D.
Tơ visco, nilon-6, nilon-6,6.
Đáp án : C
A. loại tơ tằm là polime thiên nhiên, cao su điều chế bằng pư trùng hợp
B. loại Thủy tinh plexiglas và tơ nitron điều chế bằng pư trùng hợp
C. thỏa mãn tất cả các polime điều chế bằng phản ứng trùng ngưng
D. loại tơ visco là tơ bán tổng hợp
Đốt cháy hoàn toàn một amino axit X (phân tử có 1 nhóm NH2) thu được 8,8 gam CO2 và 1,12 lít N2. Công thức phân tử của X là
-
A.
C3H7NO2.
-
B.
C4H9NO2.
-
C.
C2H7NO2.
-
D.
C2H5NO2.
Đáp án : D
BTNT nito → nX = 2nN2 =>
Số C trong X = nCO2: nX = ?
Từ đáp án chọn được công thức phù hợp
nCO2 = 8,8:44 = 0,2 (mol)
nN2(đktc) = 1,12 :22,4 = 0,05 (mol)
BTNT "N": nX = 2nN2 = 2.0,05 = 0,1 (mol)
Tất cả đáp án đều có 2 oxi nên đặt công thức aminoaxit có dạng: CxHyO2N: 0,1 (mol)
=> x = nCO2: nX = 0,2 : 0,1 = 2
=> y chỉ có thể bằng 5 thỏa mãn, y bằng 7 không thỏa mãn được
Vậy công thức của aminoaxit là C2H5NO2
Cho m gam hỗn hợp gồm axit axetic, axit oxalic, axit glutamic tác dụng vừa đủ với V ml dung dịch NaOH 1M thu được dung dịch chứa (m + 8,8) gam muối. Giá trị của V là
-
A.
200
-
B.
400
-
C.
250
-
D.
300
Đáp án : B
Sử dụng phương pháp tăng giảm khối lượng: nNaOH = 8,8/ (23-1) = ?
Đặt công thức chung của các axit là R(COOH)x
R(COOH)x + xNaOH → R(COONa)x + xH2O
Vì khối lượng tăng chính là khối lượng của Na thay thế H trong gốc -COOH của axit
Đặt số mol gốc -COOH = a(mol)
-COOH → -COONa
a → a (mol)=> Khối lượng tăng là 22a gam
Theo bài => 22a = 8,8
→ a= 0,4 (mol)
→ nNaOH = 0,4 (mol) → VNaOH = nNaOH: CM = 0,4 :1 = 0,4 (lít) = 400 (ml)
Xenlulozơ trinitrat được điều chế từ xenlulozơ và axit nitric đặc có xúc tác là axit sunfuric đặc, đun nóng. Để có 59,4 kg xenlulozơ trinitrat cần dung dịch chứa m kg axit nitric (hiệu suất 90%). Giá trị của m là
-
A.
42,0.
-
B.
30,0.
-
C.
14,0.
-
D.
37,8.
Đáp án : A
Tính theo PTHH: C6H7O2(OH)3 + 3HNO3 \(\xrightarrow{{{H_2}S{O_4}dac,{t^0}}}\) C6H7O2(ONO2)3 + 3H2O
\(\% H = \frac{{{m_{HN{O_3}}}{\,_{li\,thuyet}}}}{{{m_{HN{O_3}}}{\,_{thuc\,te}}}}.100\% \) với lượng HNO3 lí thuyết là tính theo PTHH
PTHH: C6H7O2(OH)3 + 3HNO3 \(\xrightarrow{{{H_2}S{O_4}dac,{t^0}}}\) C6H7O2(ONO2)3 + 3H2O
Theo PT: 186 → 297 (kg)
Theo ĐB: x =? ← 59,4 (kg)
→ mHNO3 lí thuyết =\(\dfrac{{59,4 \times 186}}{{297}} = 37,8(kg)\)
Vì %H= 90% nên → mHNO3 thực tế = \(\dfrac{{{m_{HN{O_{3\,}}}}li\,thuyet}}{{\% H}} \times 100\% = \dfrac{{37,8}}{{90\% }} \times 100\% = 42(kg)\)
Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch chứa chất X

Cặp chất X, Y phù hợp là
-
A.
Cu(NO3)2 và NO2.
-
B.
NH4NO2 và N2.
-
C.
CH3COONa và CH4
-
D.
KClO3 và Cl2.
Đáp án : B
Từ hình vẽ ta thấy khí Y thu bằng phương pháp đẩy nước → khí Y không tan hoặc tan rất ít trong nước
→ Chọn X,Y phù hợp
Từ hình vẽ ta thấy khí Y thu bằng phương pháp đẩy nước → khí Y không tan hoặc tan rất ít trong nước
Vậy cặp chất X, Y phù hợp là NH4NO2 và N2
\(N{H_4}N{O_2}\xrightarrow{{{t^0}}}{N_2} + 2{H_2}O\)
m gam chất rắn. Giá trị của m là Cho 12 gam Fe vào 100 ml dung dịch chứa CuSO4 1M và Fe2(SO4)3 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được
-
A.
12,8.
-
B.
9,2.
-
C.
7,2.
-
D.
6,4.
Đáp án : C
bảo toàn điện tích: nFe2+ = nSO42-
bảo toàn khối lượng kim loại ta có: mFe + mCu2+ + mFe3+ = mFe2+ + m
nFe = 12: 56 ≈ 0,21 (mol)
nCuSO4 = nFe2(SO4)3 = 0,1.1 = 0,1 (mol)
Khi cho Fe vào hh 2 muối xảy ra phản ứng theo thứ tự là:
Fe + Fe3+ → Fe2+
Fe + Cu2+ → Cu↓ + Fe2+
Dung dịch sau phản ứng chứa Fe2+ và SO42-
Mà ∑ nSO42- = 0,1 + 0,1.3 = 0,4 (mol) → nFe2+ = nSO42- = 0,4 (mol)
BTKL kim loại ta có: 12 + 0,1.64 + 0,1.2.56 = 0,4.56 + m
→ m = 7,2 (g)
Nhận xét nào sau đây là sai?
-
A.
Để gang hoặc thép trong không khí ẩm sẽ xảy ra hiện tượng ăn mòn điện hóa học.
-
B.
Trong ăn mòn hóa học, electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
-
C.
Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài của vỏ tàu (phần chìm dưới nước) những lá Zn - đây là cách chống ăn mòn kim loại bằng phương pháp bảo vệ bề mặt.
-
D.
Trong tự nhiên, sự ăn mòn kim loại xảy ra phức tạp, có thể xảy ra đồng thời quá trình ăn mòn điện hóa học và ăn mòn hóa học.
Đáp án : C
Dựa vào kiến thức về ăn mòn kim loại
A. Đúng vì xuất hiện cặp điện cực Fe-C ăn mòn điện hóa trong không khí ẩm
B. Đúng
C. Sai đây là cách chống ăn mòn bằng phương pháp điện hóa, dùng vật hi sinh là Zn thay thế cho Fe
D. Đúng
Đốt cháy hoàn toàn este X thu được CO2 và H2O có số mol bằng nhau, X có thể là este
-
A.
No, mạch hở, đơn chức.
-
B.
No, ba chức.
-
C.
No, mạch hở, hai chức.
-
D.
Không no, mạch hở, đơn chức.
Đáp án : A
Từ mối quan hệ CO2 = H2O suy ra este có độ bất bão hòa là 1, từ đó suy ra được nhận xét đúng
Đốt cháy este thu được nCO2 = nH2O → este no, mạch hở, đơn chức.
Phản ứng nào sau đây không phải là phản ứng trao đổi?
-
A.
FeCO3 + 2HCl → FeCl2 + CO2 + H2O.
-
B.
NH4Cl + NaOH → NaCl + NH3 + H2O.
-
C.
Na2SO4 + BaCl2 → BaSO4 + 2NaCl.
-
D.
2FeCO3 + 4H2SO4 → Fe2(SO4)3 + SO2 + 2CO2+ 4H2O.
Đáp án : D
Phản ứng trao đổi là phản ứng hóa học, trong đó các chất trao đổi cho nhau thành phần cấu tạo của nó mà không làm thay đổi số oxi hóa. Từ sự trao đổi này, tạo ra các sản phẩm mới.
Phản ứng: 2FeCO3 + 4H2SO4 → Fe2(SO4)3 + SO2 + 2CO2+ 4H2O là phản ứng oxi hóa khử, không phải pư trao đổi, vì số oxi hóa của các nguyên tố trước và sau phản ứng thay đổi
Cho 200 ml dung dịch NaOH 3M vào 100 ml dung dịch AlCl3 1M thu được dung dịch X. Nhỏ từ từ đến hết V ml dung dịch HCl 1M vào dung dịch X thu được 5,85 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị lớn nhất của V là
-
A.
425
-
B.
275.
-
C.
175
-
D.
375
Đáp án : D
Lập tỉ lệ nOH-/nAl3+ → xác định được phản ứng tạo ra muối AlO2‑, OH- còn dư sau phản ứng
Xác định thành phần các chất trong dd X gồm: AlO2-; OH‑ và Cl‑
Cho dd X + V ml HCl → tạo ra 5,85 gam kết tủa. V lớn nhất ứng với trường hợp tạo kết tủa Al(OH)3 sau đó kết tủa hòa tan 1 phần
CT nhanh: nH+ = nOH- + 4nAlO2- - 3nAl(OH)3 còn lại
nNaOH = 0,2.3 = 0,6 (mol)
nAlCl3 = 0,1.1 = 0,1 (mol)
Ta có: \(\dfrac{{{n_{O{H^ - }}}}}{{{n_{A{l^{3 + }}}}}} = \dfrac{{0,6}}{{0,1}} = 6 > 4\)→ phản ứng tạo ra muối AlO2-, kết tủa Al(OH)3 tan hoàn toàn, dd sau pư dư OH-
Al3+ + 4OH- → AlO2- + H2O
0,1 → 0,4 → 0,1 (mol)
Vậy dd X thu được sau pư chứa: \(\left\{ \begin{gathered}Al{O_2}^ - :0,1\,(mol) \hfill \\O{H^ - }:0,6 - 0,4 = 0,2\,(mol) \hfill \\C{l^ - }:0,3\,(mol) \hfill \\ \end{gathered} \right.\)
Cho dd X + V ml HCl → tạo ra 5,85 gam kết tủa. V lớn nhất ứng với trường hợp tạo kết tủa Al(OH)3 sau đó kết tủa hòa tan 1 phần
nAl(OH)3 = 5,85:78 = 0,075 (mol)
H+ + OH- → H2O
0,2 ← 0,2 (mol)
AlO2- + H+ + H2O → Al(OH)3↓
0,1 → 0,1 → 0,1 (mol)
Al(OH)3 + 3H+ → Al3+ + 3H2O
(0,1 - 0,075)→ 0,075 (mol)
→ ∑ nH+ = 0,2 + 0,1 + 0,075 = 0,375 (mol)
→ VHCl = nHCl : CM = 0,375 : 1 = 0,375 (lít) = 375 (ml)
Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước dư thu được dung dịch X. Điện phân dung dịch X với điện cực trơ đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối hơi so với H2 bằng 30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử hiệu suất của quá trình điện phân là 100%, khí sinh ra không tan trong dung dịch. Giá trị của m là
-
A.
48,25
-
B.
64,25
-
C.
62,25
-
D.
56,25
Đáp án : B
Hai khí thoát ra ở anot là Cl2 và O2:
Ta có hệ phương trình: \(\left\{ \begin{gathered}\sum {{n_{hh}} = {n_{C{l_2}}} + {n_{{O_2}}} = 0,2} \hfill \\\sum {{m_{hh}} = 71{n_{C{l_2}}} + 32{n_{{O_2}}} = 30,625.2.0,2} \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered}{n_{C{l_2}}} = ? \hfill \\{n_{{O_2}}} = ? \hfill \\ \end{gathered} \right.\)
Sau phản ứng thu được 2 muối có nồng độ bằng nhau → số mol 2 muối bằng nhau
→ Fe3+ điện phân hết, Cu2+ điện phân dư
BTNT "Cl" → nFeCl3 = 2/3nCl2 = ? (mol)
nCu2+ dư = nFe2+ = nFe3+ = ?
Viết các bán phản ứng xảy ra ở mỗi điện cực, dùng bảo toàn e sẽ tính được mol Cu2+ điện phân
BTNT "Cu": nCuSO4 = nCu2+ dư + nCu2+ điện phân
Hai khí thoát ra ở anot là Cl2 và O2:
Ta có hệ phương trình:
\(\left\{ \begin{gathered}
\sum {{n_{hh}} = {n_{C{l_2}}} + {n_{{O_2}}} = 0,2} \hfill \\
\sum {{m_{hh}} = 71{n_{C{l_2}}} + 32{n_{{O_2}}} = 30,625.2.0,2} \hfill \\
\end{gathered} \right. \Rightarrow \left\{ \begin{gathered}
{n_{C{l_2}}} = 0,15 \hfill \\
{n_{{O_2}}} = 0,05 \hfill \\
\end{gathered} \right.\)
Sau phản ứng thu được 2 muối có nồng độ bằng nhau → số mol 2 muối bằng nhau
→ Fe3+ điện phân hết, Cu2+ điện phân dư
BTNT "Cl": 3nFeCl3 = 2nCl2 → nFeCl3 = 2/3. 0,15 = 0,1 (mol)
→ nCu2+ dư = nFe2+ = nFe3+ = 0,1 (mol)
Đặt nCu2+ điện phân = a (mol)
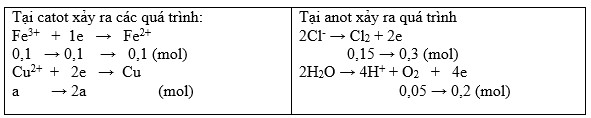
BT e ta có: 0,1 + 2a = 0,3 + 0,2 → a = 0,2 (mol)
BTNT "Cu": nCuSO4 = nCu2+ điện phân + nCu2+ dư = 0,2 + 0,1 = 0,3 (mol)
→ m = mCuSO4 + mFeCl3 = 0,3.160 + 0,1.162,5 = 64,25 (g)
Cho các thí nghiệm sau:
(1) Cho hỗn hợp gồm x mol Cu và x mol Fe3O4 vào dung dịch chứa 4x mol H2SO4 loãng.
(2) Cho hỗn hợp NaHSO4 và KHCO3 (tỉ lệ mol 1:1) vào nước dư.
(3) Cho x mol Fe vào dung dịch chứa 2,5x mol AgNO3.
(4) Cho dung dịch chứa x mol Ba(OH)2 vào dung dịch chứa x mol NaHCO3.
(5) Cho Na2CO3 dư vào dung dịch chứa BaCl2.
(6) Cho x mol Fe3O4 vào dung dịch chứa 8x mol HCl.
Sau khi các phản ứng kết thúc mà sau thí nghiệm thu được dung dịch chứa 2 muối là
-
A.
4
-
B.
6
-
C.
5
-
D.
3
Đáp án : C
Viết các PTHH xảy ra, chú ý đến giữ kiện đề bài cho tỉ lệ số mol để xác định được chất hết, chất dư, muối thu được.
(1) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
x → 4x → x (mol)
Cu + Fe2(SO4)3 → CuSO4 + FeSO4
x → x (mol)
→ sau pư thu được 2 muối CuSO4 + FeSO4
(2) 2NaHSO4 + 2KHCO3 → Na2SO4 + K2SO4 + 2CO2 + 2H2O → thu được 2 muối Na2SO4 + K2SO4
(3) Fe + 2AgNO3 → Fe(NO3)2 + Ag↓
x → 2x → x (mol)
AgNO3 còn dư 0,5x (mol) nên tiếp tục phản ứng với Fe(NO3)2
AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag↓
0,5x → 0,5x → 0,5x (mol)
Vậy sau phản ứng vẫn thu được 2 muối Fe(NO3)2: 0,5x (mol) và Fe(NO3)3:0,5x (mol)
(4) Ba(OH)2 + NaHCO3 → BaCO3↓ + NaOH + 2H2O
→ dd không thu được muối
(5) Na2CO3 + BaCl2 → BaCO3↓ + 2NaCl
→ thu được 2 muối là NaCl và Na2CO3 dư
(6) Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + H2O
x → 8x (mol)
→ Thu được 2 muối FeCl2 và FeCl3
Vậy có 5 thí nghiệm dung dịch thu được 2 muối là: (1), (2), (3), (5), (6)
Hấp thụ hết 0,2 mol khí CO2 vào dung dịch chứa x mol NaOH và y mol Na2CO3 thu được 100 ml dung dịch X. Lấy 50 ml dung dịch X tác dụng với dung dịch Ca(OH)2 dư thu được 20 gam kết tủa. Mặt khác, khi lấy 50 ml dung dịch X cho từ từ vào 150 ml dung dịch HCl 1M thu được 0,12 mol khí CO2. Biết các phản ứng xảy ra hoàn toàn. Giá trị của x và y lần lượt là
-
A.
0,1 và 0,45
-
B.
0,14 và 0,2.
-
C.
0,12 và 0,3
-
D.
0,1 và 0,2
Đáp án : D
Dung dịch X thu được chứa 2 muối CO32- và HCO3-
Phản ứng với Ca(OH)2 dư thì
Trong 50 ml X, đặt a,b là số mol CO32- và HCO3-
Với Ca(OH)2 dư → nCaCO3 = a + b = 0,2 (1)
Với HCl, đặt ka, kb là số mol của CO32- và HCO3- đã phản ứng.
→ nHCl = 2ka + kb = 0,15
nCO2 = ka + kb = 0,12
giải hệ trên được ka = ? và kb = ?
suy ra được tỉ lệ a và b (2)
Từ (1) và (2) giải ra được a và b
Quay lại xét trong 100 ml dd X, dùng BTĐT và BTNT"C" sẽ ra được số mol mỗi chất x, y
nHCl = 0,15 (mol) < 2nCO2 nên X chứa hai muối CO32- và HCO3-
Trong 50 ml X, đặt a,b là số mol CO32- và HCO3-
Với Ca(OH)2 dư → nCaCO3 = a + b = 0,2 (1)
Với HCl, đặt ka, kb là số mol của CO32- và HCO3- đã phản ứng.
→ nHCl = 2ka + kb = 0,15
nCO2 = ka + kb = 0,12
giải hệ trên được ka = 0,03 và kb = 0,09
→ 3a = b (2)
Từ (1) và (2) → a= 0,05 và b = 0,15
Trong 100 ml X chứa CO32-: 0,01 (mol) và HCO3-: 0,3 (mol)
Bảo toàn điện tích: x + 2y = 0,1.2 + 0,3
Bảo toàn C → 0,2 + y =0,1 + 0,3
→ x = 0,1 và y = 0,2
Hỗn hợp X gồm các triglixerit trong phân tử đều chứa axit stearic, axit oleic, axit linoleic. Đốt cháy hoàn toàn m gam X cần a mol O2 thu được 0,285 mol CO2. Xà phòng hóa hoàn toàn m gam X bằng dung dịch NaOH vừa đủ được m1 gam muối. Giá trị a và m1 lần lượt là
-
A.
0,8 và 8,82.
-
B.
0,4 và 4,32.
-
C.
0,4 và 4,56.
-
D.
0,75 và 5,62.
Đáp án : C
X có CTPT chung là C57H104O6
Tìm được → nX = nCO2/57 =?
Tìm được nH2O = = 104/2. nX =?
BTNT "O": 6nX + 2nO2 = 2nCO2 + nH2O → nO2 = ?
Muối thu được gồm: C17H35COONa; C17H33COONa ; C17H31COONa: số mol mỗi chất bằng mol X → m1 = ?
X là các đồng phân của (C17H35COO)(C17H33COO)(C17H31COO)C3H5 hay đều có công thức phân tử C57H104O6
→ nX = nCO2/57 = 0,285/57 = 0,005 (mol)
→ nH2O = 104/2. nX = 104/2. 0,005 = 0,26 (mol)
BTNT "O": 6nX + 2nO2 = 2nCO2 + nH2O
→ 6.0,005 + 2nO2 = 2.0,285 + 0,26
→ nO2 = a = 0,4 (mol)
Muối thu được gồm: C17H35COONa: 0,005 (mol); C17H33COONa: 0,005 (mol); C17H31COONa: 0,005 (mol)
→ m1 = 0,005. (306 + 304 + 302) = 4,56 (g)
Bảng dưới đây ghi lại hiện tượng phản ứng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z và T

Các chất X, Y, Z, T lần lượt là
-
A.
phenol, anđehit fomic, glixerol, etanol.
-
B.
anilin, gilxerol, anđehit fomic, metyl fomat
-
C.
phenol, axetanđehit, etanol, anđehit fomic
-
D.
glixerol, etylen glicol, metanol, axetanđehit.
Đáp án : A
Suy luận như sau:
X tạo kết tủa với dd Br2 → X có thể là phenol hoặc anilin
Y có kết tủa với dd AgNO3/NH3 → Y là anđehit
Z có tạo kết tủa màu xanh lam với dd Cu(OH)2 → trong phân tử Z phải chứa nhiều nhóm -OH kề nhau
Kết hợp đáp án đề cho suy ra X, Y, Z, T thỏa mãn
X tạo kết tủa với dd Br2 → X có thể là phenol hoặc anilin
Y có kết tủa với dd AgNO3/NH3 → Y là anđehit
Z có tạo kết tủa màu xanh lam với dd Cu(OH)2 → trong phân tử Z phải chứa nhiều nhóm -OH kề nhau
T không có hiện tượng gì với tất cả các thuốc thử → T là ancol etylic
Vậy dựa vào đáp án và suy luận trên thứ tự X,Y,Z,T phù hợp lần lượt là: phenol, anđehit fomic, glixerol, etanol.
Cho từ từ dung dịch HCl loãng vào dung dịch chứa NaOH và NaAlO2 (hay Na[Al(OH)4]. Sự phụ thuộc của số mol kết tủa thu được vào số mol của HCl được biểu diễn theo đồ thị sau:

Tổng giá trị của (x + y) là
-
A.
3,5
-
B.
3,8
-
C.
3,1
-
D.
2,2
Đáp án : B
Bài toán cho H+ vào hỗn hợp dung dịch OH- và AlO2-:
+ Khi kết tủa chưa bị hòa tan: nH+ = nOH- + nAl(OH)3
+ Khi kết tủa bị hòa tan một phần: nH+ = nOH- + 4nAlO2- - 3nAl(OH)3
(1) NaOH + HCl → NaCl + H2O
(2) NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
(3) Al(OH)3 + 3HCl → AlCl3 + 3H2O
+ Tại nHCl = 0,9 mol thì NaOH vừa bị trung hòa hết => nNaOH = nHCl = 0,9 mol
+ Tại nHCl = 1,6 mol thì tủa chưa đạt cực đại:
nHCl = nNaOH + nAl(OH)3 => 1,6 = 0,9 + (y - 0,3) => y = 1 mol
=> nNaAlO2 = 1 mol
+ Tại nHCl = x mol thì Al(OH)3 bị hòa tan một phần:
Áp dụng công thức giải nhanh: nHCl = nNaOH + 4nAlO2- - 3nAl(OH)3
=> x = 0,9 + 4.1 - 3(1 - 0,3) = 2,8
Vậy x + y = 2,8 + 1 = 3,8
Cho 14,6 gam Gly-Ala tác dụng hết với dung dịch HCl dư được dung dịch X. Cô cạn dung dịch X được bao nhiêu gam muối khan?
-
A.
23,7 gam.
-
B.
28,6 gam.
-
C.
19,8 gam.
-
D.
21,9 gam.
Đáp án : A
Tính số mol của Gly-Ala
Gly-Ala + H2O + 2HCl → Muối
BTKL: m muối = mGly-Ala + mH2O + mHCl
nGly-Ala = 14,6 : (75 + 89 - 18) = 0,1 mol
Gly-Ala + H2O + 2HCl → Muối
0,1 mol 0,1 mol 0,2 mol
BTKL: m muối = mGly-Ala + mH2O + mHCl = 14,6 + 0,1.18 + 0,2.36,5 = 23,7 gam
Cho các phát biểu sau:
(1) Este có nhiệt độ sôi thấp hơn so với axit và ancol có cùng số nguyên tử cacbon.
(2) Dầu ăn và mỡ bôi trơn có cùng thành phần nguyên tố.
(3) Tên thay thế của amin có công thức (CH3)3N là trimetylamin
(4) Dung dịch 37 - 40% fomanđehit trong nước gọi là fomalin (còn gọi là fomon) được dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng.
(5) Các chất: cocain, amphetamin, heroin, moocphin là những chất gây nghiện, hết sức nguy hại cho sức khỏe con người.
Có bao nhiêu phát biểu sai?
-
A.
3
-
B.
1
-
C.
4
-
D.
2
Đáp án : D
Xem lại lý thuyết phần este, lipit, amin, andehit
(1) đúng vì este không tạo được liên kết H như ancol và axit
(2) sai vì dầu ăn thành phần chính là chất béo còn dầu bôi trơn có thành phần chính là các hidrocacbon
(3) sai vì đó là tên gốc chức (không phải tên thay thế)
(4) đúng
(5) đúng
Vậy có 2 phát biểu sai
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm metan, axetilen, buta-1,3-đien và vinyl axetilen thu được 24,2 gam CO2 và 7,2 gam nước. Biết a mol hỗn hợp X làm mất màu tối đa 112 gam Br2 trong dung dịch. Giá trị của a là
-
A.
0,2
-
B.
0,4
-
C.
0,1
-
D.
0,3
Đáp án : B
- Đặt công thức chung của các chất là CnHm
Từ số mol CO2 và H2O suy ra giá trị của n và m
- Tính giá trị độ bất bão hòa dựa theo công thức: Độ bất bão hòa: k = (2C + 2 - H)/2
X + k Br2 → ...
Từ số mol Br2 phản ứng suy ra số mol của X.
nCO2 = 0,55 mol; nH2O = 0,4 mol
Đặt công thức chung của các chất là CnHm
CnHm → nCO2 + 0,5mH2O
0,2 → 0,2n → 0,1m
+ nCO2 = 0,2n = 0,55 => n = 2,75
+ nH2O = 0,1m = 0,4 => m = 4
Vậy công thức trung bình của hỗn hợp X là C2,75H4
Độ bất bão hòa: k = (2C + 2 - H)/2 = (2.2,75 + 2 - 4)/2 = 1,75
Khi cho a mol X tác dụng với Br2: nBr2 = 112 : 160 = 0,7 mol
C2,75H4+ 1,75Br2 → ...
0,4 ← 0,7
Vậy a = 0,4
Chia hỗn hợp X gồm Fe, Fe3O4, Fe(OH)3 và FeCO3 thành hai phần bằng nhau. Hòa tan hết phần 1 trong dung dịch HCl dư, thu được 0,1 mol hỗn hợp 2 khí có tỉ khối so với He bằng 4,7 và dung dịch Y. Cho phần 2 tác dụng với lượng dư dung dịch H2SO4 đặc nóng, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Z và 0,2075 mol hỗn hợp khí T gồm CO2 và SO2 (sản phẩm khử duy nhất của S+6).
Khối lượng FeCl2 trong dung dịch Y là
-
A.
25,307 gam.
-
B.
27,305 gam.
-
C.
23,705 gam.
-
D.
25,075 gam.
Đáp án : B
*Phần 1: Hòa tan 1 phần hỗn hợp vào HCl dư
Tính được số mol H2 và CO2 từ đó suy ra số mol của Fe và FeCO3.
*Phần 2: Hòa tan 1 phần vào dung dịch H2SO4 đặc dư
nSO2 = n khí - nCO2 = ?
Quá trình cho và nhận e:
Fe0 → Fe+3 + 3e S+6 + 2e → S+4
3Fe+8/3 → 3Fe+3 + 1e
Fe+2 → Fe+3 + 1e
Áp dụng định luật bảo toàn electron:
3nFe + nFe3O4 + nFeCO3 = 2nSO2 => nFe3O4
Như vậy, dựa theo các PTHH ở phần 1 ta có:
nFeCl2 = nFe + nFe3O4 + nFeCO3 = ?
*Phần 1: Hòa tan 1 phần hỗn hợp vào HCl dư
Đặt nH2 = a và nCO2 = b (mol)
+ n khí = a + b = 0,1 (1)
+ m khí = n khí.M khí => 2a + 44b = 0,1.4,7.4 (2)
Giải hệ thu được a = 0,06 và b = 0,04
Fe + 2HCl → FeCl2 + H2
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
FeCO3 + 2HCl → FeCl2 + CO2 + H2O
=> nFe = nH2 = 0,06 mol; nFeCO3 = nCO2 = 0,04 mol
*Phần 2: Hòa tan 1 phần vào dung dịch H2SO4 đặc dư
nSO2 = n khí - nCO2 = 0,2075 - 0,04 = 0,1675 mol
Quá trình cho và nhận e:
Fe0 → Fe+3 + 3e S+6 + 2e → S+4
3Fe+8/3 → 3Fe+3 + 1e
Fe+2 → Fe+3 + 1e
Áp dụng định luật bảo toàn electron:
3nFe + nFe3O4 + nFeCO3 = 2nSO2 => 3.0,06 + nFe3O4 + 0,04 = 2.0,1675
=> nFe3O4 = 0,115 mol
Như vậy, dựa theo các PTHH ở phần 1 ta có:
nFeCl2 = nFe + nFe3O4 + nFeCO3 = 0,06 + 0,115 + 0,04 = 0,215 mol
=> mFeCl2 = 0,215.127 = 27,305 gam
Hòa tan hoàn toàn 2 chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch NH3 dư vào dung dịch Z thu được x1 mol kết tủa
Thí nghiệm 2: Cho dung dịch Na2CO3 dư vào dung dịch Z thu được x2 mol kết tủa
Thí nghiệm 3: Cho dung dịch Ba(OH)2 dư vào dung dịch Z thu được x3 mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và x1 < x2 < x3. Hai chất X, Y lần lượt là
-
A.
BaCl2 và FeCl2
-
B.
AlCl3 và FeCl3
-
C.
ZnSO4 và Al2(SO4)3
-
D.
FeSO4 và Fe2(SO4)3
Đáp án : C
Giả sử số mol mỗi chất X, Y là 1 mol.
- Phương án A:
TN1: Kết tủa gồm Fe(OH)2 (1 mol) => x1 = 1
TN2: Kết tủa gồm BaCO3 (1 mol) và FeCO3 (1 mol) => x2 = 2
TN3: Kết tủa gồm Fe(OH)2 (1 mol) => x3 = 1
=> Không thỏa mãn x1 < x2 < x3
- Phương án B:
TN1: Kết tủa gồm 1 mol Al(OH)3 và 1 mol Fe(OH)3 => x1 = 2
TN2: Kết tủa gồm 1 mol Al(OH)3 (do Al2(CO3)3 phân hủy thành) và 1 mol Fe(OH)3 (do Fe2(CO3)3 phân hủy thành) => x2 = 2
TN3: Kết tủa gồm 1 mol Fe(OH)3 => x3 = 1
=> Không thỏa mãn x1 < x2 < x3
- Phương án C:
TN1: Kết tủa gồm 2 mol Al(OH)3 (chú ý Zn(OH)2 tạo phức với NH3 nên bị tan) => x1 = 2
TN2: Kết tủa gồm 1 mol ZnCO3 (1 mol) và 2 mol Al(OH)3 (do Al2(CO3)3 phân hủy thành) => x2 = 3
TN3: Kết tủa gồm 4 mol BaSO4 => x3 = 4
=> Thỏa mãn x1 < x2 < x3
- Phương án D:
TN1: Kết tủa gồm 1 mol Fe(OH)2 và 2 mol Fe(OH)3 => x1 = 3
TN2: Kết tủa gồm 1 mol FeCO3 và 2 mol Fe(OH)3 (do Fe2(CO3)3 phân hủy thành) => x2 = 3
TN3: Kết tủa gồm 1 mol Fe(OH)2; 2 mol Fe(OH)3 và 4 mol BaSO4 => x3 = 7 mol
=> Không thỏa mãn x1 < x2 < x3
Hỗn hợp E gồm axit no, đơn chức X, axit đa chức Y (phân tử có 3 liên kết π, mạch không phân nhánh) đều mạch hở và este Z (chỉ chứa nhóm chức este, không chứa nhóm chức khác) tạo bởi ancol đa chức T với X và Y. Đốt cháy hoàn toàn 14,93 gam E cần dùng 0,3825 mol O2. Mặt khác, 14,93 gam E phản ứng tối đa với 260 ml dung dịch NaOH 1M thu được m gam ancol T. Đốt cháy hoàn toàn m gam T thu được 1,98 gam CO2 và 1,08 gam H2O. Nhận xét nào sau đây sai
-
A.
Tổng số nguyên tử H trong phân tử Z là 10.
-
B.
Có thể dùng dung dịch Br2 để nhận biết X, Y, T.
-
C.
Y có đồng phân hình học cis – trans.
-
D.
Z có 2 công thức cấu tạo phù hợp.
Đáp án : A
Bảo toàn khối lượng, bảo toàn electron, quy đổi, biện luận.
nNaOH = 0,26 mol; nCO2 = 0,045 mol; nH2O = 0,06 mol
Do axit Y đa chức, không phân nhánh nên Y là axit hai chức
Este Z được tạo bởi ancol T và X, Y => Ancol T là ancol ba chức.
*Xét phản ứng đốt cháy ancol T: nCO2 = 0,045 mol; nH2O = 0,06 mol
nCO2 < nH2O => T là ancol no, mạch hở
n ancol = nH2O - nCO2 = 0,06 - 0,045 = 0,015 mol
=> Số C = nCO2 : nT = 0,045 : 0,015 = 3
Vậy T là C3H5(OH)3
*E phản ứng với NaOH: nCOO = nNaOH = 0,26 mol => nO(E) = 2nCOO = 0,52 mol
*Xét phản ứng đốt cháy hỗn hợp E:
+ BTKL: mCO2 + mH2O = mE + mO2 => 44nCO2 + 18nH2O = 14,93 + 32.0,3825
+ BTNT "O": 2nCO2 + nH2O = nO(E) + 2nO2 => nCO2 + nH2O = 0,52 + 2.0,3825
Giải hệ được nCO2 = 0,505 và nH2O = 0,275
*Quy đổi hỗn hợp E thành:
CnH2nO2: x
CmH2m-4O4: y
C3H8O3: 0,015
H2O: -0,045
Ta có hệ phương trình:
\(\left\{ \matrix{
{n_{NaOH}} = x + 2y = 0,026 \hfill \cr
{n_{C{O_2}}} = nx + my + 0,015.3 = 0,505 \hfill \cr
{n_{{H_2}O}} = nx + (m - 2)y + 4.0,015 - 0,045 = 0,275 \hfill \cr} \right. \to \left\{ \matrix{
x = 0,06 \hfill \cr
y = 0,1 \hfill \cr
3n + 5m = 23 \hfill \cr} \right.\)
Chỉ có cặp n = 1; m = 4 thỏa mãn
Vậy X là HCOOH và Y là HOOC-CH=CH-COOH
=> Z có thể là
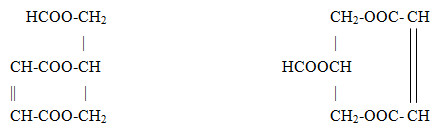
- Phương án A sai vì tổng số nguyên tử H trong Z là 8
- Phương án B đúng
+ X làm mất màu dung dịch Br2 khi đun nóng
+ Y làm mất màu dung dịch Br2 ở nhiệt độ thường
+ T không làm mất màu dung dịch Br2
- Phương án C đúng
- Phương án D đúng.
Hỗn hợp M gồm 2 axit cacboxylic no, mạch hở (phân tử chỉ chứa nhóm chức –COOH) và một ancol no, mạch hở. Đốt cháy hoàn toàn m gam M thu được CO2 và 10,8 gam H2O. Nếu đun nóng m gam M trên (với xúc tác H2SO4 đặc) thấy các chất trong hỗn hợp phản ứng với nhau vừa đủ, chỉ thu được H2O và este X (phân tử chỉ chứa chức este, giả thiết phản ứng este hóa đạt hiệu suất 100%). Để đốt cháy hoàn toàn lượng X sinh ra thì cần dùng vừa đủ 0,5625 mol O2 thu được hỗn hợp CO2 và H2O thỏa mãn điều kiện 3nX phản ứng = nCO2 - nH2O. Công thức phân tử của X là
-
A.
C8H8O4.
-
B.
C7H8O6.
-
C.
C7H6O6.
-
D.
C8H10O6.
Đáp án : D
Quy đổi, bảo toàn khối lượng, bảo toàn nguyên tố.
Các axit và ancol đều no nên X là este no.
3nX phản ứng = nCO2 - nH2O => X có k = 4 (dựa vào công thức: nX = (nCO2-nH2O)/(k-1))
X tạo bởi 2 axit và 1 ancol nên X có 3 nhóm COO và 1 vòng
Giả sử X có công thức: B(COO)2(ACOO)R (a mol)
=> M gồm ACOOH (a mol); B(COOH)2 (a mol), R(OH)3 (a mol)
Quy đổi hỗn hợp M thành HCOOH (a); (COOH)2 (a); C3H5(OH)3 (a) và CH2 (b)
+ nH2O = a + a + 4a + b = 0,6
Lượng O2 dùng để đốt X cũng như đốt M nên:
+ nO2 = 0,5a + 0,5a + 3,5a + 1,5b = 0,5625
Giải hệ trên thu được a = 0,075 và b = 0,15
Do b = 2a nên X là HCOO(COO)2C3H5.2CH2
=> X là C8H10O6
Hòa tan hoàn toàn 20,7 gam hỗn hợp X gồm Na, Ba, BaO và Na2O vào nước dư thu được 4 lít dung dịch Y có pH = 13 và 0,05 mol khí H2. Cho 4 lít dung dịch Y tác dụng với 100 ml dung dịch chứa H2SO4 0,3M và Al2(SO4)3 0,5M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m gần nhất với
-
A.
35
-
B.
30
-
C.
25
-
D.
42
Đáp án : B
*Quy đổi hỗn hợp thành: Na (x mol); Ba (y mol) và O (z mol)
+ mX => (1)
+ Dung dịch thu được gồm: Na+ (x mol); Ba2+ (y mol) và OH-
BTĐT => nOH- = nNa+ + 2nBa2+ => (2)
+ BTe: nNa + 2nBa = 2nO + 2nH2 => (3)
Giải hệ thu được x, y, z.
Sau đó tính toán theo PTHH để xác định được khối lượng kết tủa thu được sau khi cho dung dịch Y phản ứng với hỗn hợp H2SO4 và Al2(SO4)3
*Quy đổi hỗn hợp thành: Na (x mol); Ba (y mol) và O (z mol)
+ mX = 23x + 137y + 16z = 20,7 (1)
+ Dung dịch thu được gồm: Na+ (x mol); Ba2+ (y mol) và OH-
pH = 13 => pOH = 14 - 13 = 1 => [OH-] = 10-1 = 0,1M => nOH- = 0,1.4 = 0,4 mol
BTĐT => nOH- = nNa+ + 2nBa2+ => x + 2y = 0,4 (mol) (2)
+ BTe: nNa + 2nBa = 2nO + 2nH2 => x + 2y = 2z + 2.0,05 (3)
Giải hệ (1) (2) (3) thu được x = 0,2; y = 0,1; z = 0,15
*Cho Y {Na+ (0,2); Ba2+ (0,1); OH- (0,4)} tác dụng với hỗn hợp H2SO4 (0,03 mol) và Al2(SO4)3 (0,05 mol):
nH+ = 2nH2SO4 = 0,06 mol;
nAl3+ = 2nAl2(SO4)3 = 0,1 mol;
nSO42- = nH2SO4 + 3nAl2(SO4)3 = 0,18 mol
PTHH:
H+ + OH- → H2O
0,06 → 0,06 dư 0,34
Al3+ + 3OH- → Al(OH)3
0,1 → 0,3 dư 0,04 → 0,1
Al(OH)3 + OH- → AlO2- + 2H2O
0,04 còn 0,06 ← 0,04
Ba2+ + SO42- → BaSO4
0,1 → 0,1 → 0,1
Vậy kết tủa gồm Al(OH)3 (0,06 mol) và BaSO4 (0,1 mol)
=> m kết tủa = 0,06.78 + 0,1.233 = 27,98 gam gần nhất với 30 gam
Cho 0,2 mol hỗn hợp gồm X (C3H10O2N2) và Y (C4H12O4N2) tác dụng vừa đủ với 300 ml dung dịch NaOH 1M thu được amin Z có tỉ khối so với H2 bằng 15,5 và dung dịch T. Cô cạn dung dịch T thu được hỗn hợp G gồm 2 muối có số nguyên tử C bằng nhau. Phần trăm khối lượng của muối có phân tử khối lớn hơn trong G có giá trị gần nhất với giá trị nào sau đây?
-
A.
64
-
B.
42
-
C.
58
-
D.
35
Đáp án : C
Từ MZ => Z là CH3NH2
=> X là H2N-CH2-COONH3CH3 => Muối có chứa 2 nguyên tử C
=> Y là CH3NH3OOC-COONH3CH3
MZ = 15,5.2 = 31 => Z là CH3NH2
=> X là H2N-CH2-COONH3CH3 => Muối có chứa 2 nguyên tử C
=> Y là CH3NH3OOC-COONH3CH3
Giả sử số mol của X, Y lần lượt là x và y (mol)
Giải hệ: n hh = x + y = 0,2 và nNaOH = x + 2y = 0,3 được x = y = 0,1 mol
Muối gồm: H2N-CH2-COONa (0,1 mol) và (COONa)2 (0,1 mol)
=> %m(COONa)2 = 0,1.134/(0,1.97 + 0,1.134) = 0,58 = 58%
















