Đề khảo sát chất lượng đầu năm Hóa 12 - Đề số 5
Đề bài
Chất nào sau đây là chất điện li mạnh?
-
A.
HF
-
B.
NaCl
-
C.
H2O
-
D.
CH3COOH
Oxit kim loại bị khử bởi khí CO ở nhiệt độ cao là
-
A.
K2O
-
B.
Al2O3
-
C.
MgO
-
D.
CuO
Ancol nào sau đây có số nguyên tử cacbon bằng số nhóm -OH?
-
A.
Glixerol
-
B.
Etilenglicol
-
C.
Ancol benzylic
-
D.
Propan-1,2-diol
Dung dịch 37-40% fomandehit trong nước gọi là fomon được dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng… Công thức hóa học của fomandehit là
-
A.
HCHO
-
B.
CH3CHO
-
C.
OHC-CHO
-
D.
CH2=CHCHO
Thành phần chính của phân ure là
-
A.
(NH4)2HPO4
-
B.
NH4H2PO4
-
C.
(NH4)2CO3
-
D.
(NH2)2CO
Cho phản ứng: Cu + HNO3 → Cu(NO3)2 + NO + H2O. Khi hệ số cân bằng phản ứng là nguyên và tối giản thì số phân tử HNO3 bị khử là
-
A.
6
-
B.
2
-
C.
8
-
D.
4
Một hidrocacbon X cộng hợp với axit HCl theo tỉ lệ mol 1:1 tạo sản phẩm có thành phần khối lượng clo là 45,223%. Công thức phân tử của X là
-
A.
C3H4
-
B.
C2H4
-
C.
C3H6
-
D.
C4H8
Đốt cháy hoàn toàn m gam hỗn hợp 3 ancol đơn chức, thuộc cùng dãy đồng đẳng, thu được 3,808 lít khí CO2 (đktc) và 5,4 gam H2O. Giá trị của m là
-
A.
5,42
-
B.
7.42
-
C.
5.72
-
D.
4,72
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
-
A.
3,5 gam
-
B.
7,0 gam
-
C.
5,6 gam
-
D.
2,8 gam
Hòa tan hoàn toàn 1,02 gam Al2O3 trong dung dịch H2SO4 loãng dư, thu được khối lượng muối là
-
A.
5,13 gam
-
B.
5,81 gam
-
C.
3,42 gam
-
D.
6,84 gam
Cho hỗn hợp A gồm 0,01 mol HCHO và 0,02 mol CH3CHO và dung dịch AgNO3 trong NH3 dư đun nóng. Sau khi phản ứng hoàn toàn khối lượng Ag thu được là
-
A.
8,64 gam
-
B.
6,48 gam
-
C.
12,96 gam
-
D.
4,32 gam
Số ancol đồng phân cấu tạo của nhau có công thức phân tử C5H12O, tác dụng với CuO đun nóng sinh ra xeton là
-
A.
4
-
B.
3
-
C.
2
-
D.
5
Đốt cháy hoàn toàn hidrocacbon X bằng lượng oxi vừa đủ, thu được CO2 và H2O có tổng số mol bằng tổng số mol của X và O2 tham gia phản ứng. Số nguyên tử hidro (H) có trong X là
-
A.
8
-
B.
6
-
C.
4
-
D.
2
Hỗn hợp X gồm Al2O3 (0,12 mol), Mg (0,2 mol), Zn (0,1 mol). Cho X tác dụng hết với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 23,54g. Số mol HNO3 phản ứng là
-
A.
0,96 mol
-
B.
1,47 mol
-
C.
1,11 mol
-
D.
0,75 mol
Nhận định nào sau đây sai?
-
A.
Dung dịch HF hòa tan được SiO2
-
B.
Trong các hợp chất, ngoài mức oxi hóa là -1, flo và clo còn có số oxi hóa là +1, +3, +5, +7
-
C.
Muối AgF tan được trong nước
-
D.
Flo có tính oxi hóa mạnh hơn clo
Cho các chất: FeS, Cu2S, FeSO4, H2S, Ag, Fe, KMnO4, Na2SO3, Fe(OH)2. Số chất có thể phản ứng với H2SO4 đặc nóng tạo ra SO2 là
-
A.
7
-
B.
8
-
C.
6
-
D.
9
Cho các dung dịch NaOH, BaCl2, Na2CO3, NaHSO4 được dán nhãn X, Y, Z, T không theo thứ tự. Thực hiện các thí nghiệm đối với 4 dung dịch X, Y, Z, T và có kết quả như bảng sau
| Chất | X | Y | Z | T | ↑: khí thoát ra ↓: kết tủa (+): có phản ứng |
| X | (-) | ↓ | ↑ | (+) | |
| Y | ↓ | (-) | ↓ | (-) |
-
A.
Na2CO3, NaHSO4
-
B.
BaCl2, NaOH
-
C.
BaCl2, NaHSO4
-
D.
Na2CO3, NaOH
Tiến hành các thí nghiệm sau:
(1) O3 tác dụng với dung dịch KI
(2) Axit HF tác dụng với SiO2
(3) Cho khí Cl2 tác dụng với khí H2S
(4) Khí SO2 tác dụng với nước Cl2
(5) KClO3 tác dụng với dung dịch HCl đặc, đun nóng
(6) Cho H2O2 vào dung dịch KMnO4/H2SO4
(7) MnO2 tác dụng với dung dịch HCl đặc, đun nóng
Số thí nghiệm tạo ra đơn chất là
-
A.
4
-
B.
6
-
C.
5
-
D.
3
Hỗn hợp khí X gồm vinylaxetilen, axetilen và propan (x gam). Chia X làm 3 phần bằng nhau.
- Phần 1 tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 20,76 gam kết tủa
- Phần 2 phản ứng tối đa với 0,24 mol H2 (xúc tác Ni, to)
- Đốt cháy hoàn toàn phần 3 với lượng oxi vừa đủ, thu được CO2 và H2O có tỉ lệ mol 1:1
Giá trị của x là
-
A.
18,48 gam
-
B.
21,12 gam
-
C.
17,68 gam
-
D.
19,80 gam
Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối với H2 bằng 5. Tỉ lệ a:b bằng
-
A.
1 : 2
-
B.
2 : 1
-
C.
1 : 1
-
D.
2 : 3
Lời giải và đáp án
Chất nào sau đây là chất điện li mạnh?
-
A.
HF
-
B.
NaCl
-
C.
H2O
-
D.
CH3COOH
Đáp án : B
Chất điện li mạnh là chất khi tan trong nước, phân li hoàn toàn ra ion
NaCl khi tan trong nước phân li hoàn toàn ra ion Na+ và Cl-
Oxit kim loại bị khử bởi khí CO ở nhiệt độ cao là
-
A.
K2O
-
B.
Al2O3
-
C.
MgO
-
D.
CuO
Đáp án : D
Kim loại đứng sau Al trong dãy điện hóa sẽ bị CO khử ở nhiệt độ cao
CuO bị CO khử thành kim loại Cu
CuO + CO → Cu + CO2
Ancol nào sau đây có số nguyên tử cacbon bằng số nhóm -OH?
-
A.
Glixerol
-
B.
Etilenglicol
-
C.
Ancol benzylic
-
D.
Propan-1,2-diol
Đáp án : A
Xác định công thức cấu tạo của các chất
Glixerol: CH2(OH) – CH(OH) – CH2(OH) => Có 3 nhóm -OH, 3 C
Etilenclicol: CH2(OH) – CH2 – CH2(OH) => Có 2 nhóm -OH, 3 C
Ancol benzylic: C6H5CH2OH => Có 1 nhóm -OH, 7 C
Propan-1,2-diol: CH2(OH) – CH(OH) – CH3 => Có 2 nhóm -OH, 3 C
=> Glixerol có số cacbon bằng số nhóm -OH
Dung dịch 37-40% fomandehit trong nước gọi là fomon được dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng… Công thức hóa học của fomandehit là
-
A.
HCHO
-
B.
CH3CHO
-
C.
OHC-CHO
-
D.
CH2=CHCHO
Đáp án : A
Công thức hóa học của fomandehit là HCHO
Thành phần chính của phân ure là
-
A.
(NH4)2HPO4
-
B.
NH4H2PO4
-
C.
(NH4)2CO3
-
D.
(NH2)2CO
Đáp án : D
Thành phần chính của phân ure là (NH2)2CO
Cho phản ứng: Cu + HNO3 → Cu(NO3)2 + NO + H2O. Khi hệ số cân bằng phản ứng là nguyên và tối giản thì số phân tử HNO3 bị khử là
-
A.
6
-
B.
2
-
C.
8
-
D.
4
Đáp án : B
Sử dụng phương pháp thăng bằng electron
3x/ Cu → Cu2+ + 2e
2x/ N+5 + 3e → N+2
=> Có 2 phân tử HNO3 bị khử thành NO
Một hidrocacbon X cộng hợp với axit HCl theo tỉ lệ mol 1:1 tạo sản phẩm có thành phần khối lượng clo là 45,223%. Công thức phân tử của X là
-
A.
C3H4
-
B.
C2H4
-
C.
C3H6
-
D.
C4H8
Đáp án : C
X + HCl theo tỉ lệ 1:1 => Có 1 nối đôi
=> CnH2n + HCl → CnH2n+1Cl
X + HCl theo tỉ lệ 1:1 => Có 1 nối đôi
=> CnH2n + HCl → CnH2n+1Cl
- Thành phần khối lượng clo là 45,223%
=> 45,223% = 35,5/(14n + 36,5) x 100%
=> n = 3
Vậy công thức của X là C3H6
Đốt cháy hoàn toàn m gam hỗn hợp 3 ancol đơn chức, thuộc cùng dãy đồng đẳng, thu được 3,808 lít khí CO2 (đktc) và 5,4 gam H2O. Giá trị của m là
-
A.
5,42
-
B.
7.42
-
C.
5.72
-
D.
4,72
Đáp án : D
nCO2 = 3,808 : 22,4 = 0,17 (mol)
nH2O = 5,4 : 18 = 0,3 (mol)
=> no (trong ancol) = 0,3 – 0,17 = 0,13 (mol)
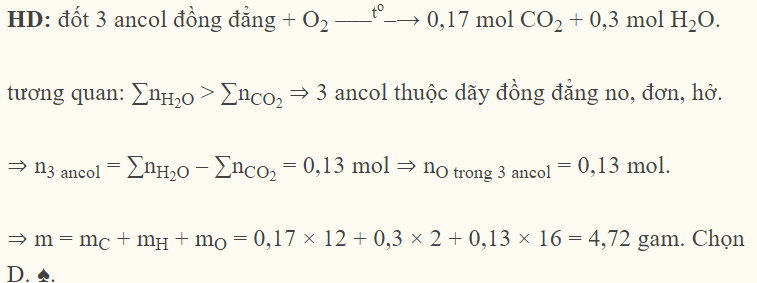
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
-
A.
3,5 gam
-
B.
7,0 gam
-
C.
5,6 gam
-
D.
2,8 gam
Đáp án : B
Áp dụng định luật tăng giảm khối lượng
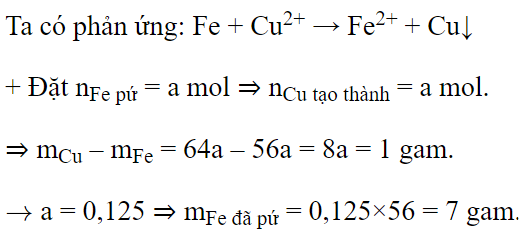
Hòa tan hoàn toàn 1,02 gam Al2O3 trong dung dịch H2SO4 loãng dư, thu được khối lượng muối là
-
A.
5,13 gam
-
B.
5,81 gam
-
C.
3,42 gam
-
D.
6,84 gam
Đáp án : C
nAl2O3 = 1,02 : 102 = 0,01 mol
Muối: Al2(SO4)3: 0,01 mol
nAl2O3 = 1,02 : 102 = 0,01 mol
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
nAl2O3 = nAl2(SO4)3
=> mmuối = 0,01.(27.2 + 96.3) = 3,42 gam
Cho hỗn hợp A gồm 0,01 mol HCHO và 0,02 mol CH3CHO và dung dịch AgNO3 trong NH3 dư đun nóng. Sau khi phản ứng hoàn toàn khối lượng Ag thu được là
-
A.
8,64 gam
-
B.
6,48 gam
-
C.
12,96 gam
-
D.
4,32 gam
Đáp án : A
1 HCHO tạo ra 4 Ag
1 CH3CHO tạo ra 2 Ag
1 HCHO tạo ra 4 Ag
=> 0,01 mol HCHO tạo ra 0,04 mol Ag
1 CH3CHO tạo ra 2 Ag
=> 0,02 mol CH3CHO tạo ra 0,04 mol Ag
=> Sau khi phản ứng hoàn toàn khối lượng Ag thu được = 108 .(0,04 + 0,04) = 8,64 gam
Số ancol đồng phân cấu tạo của nhau có công thức phân tử C5H12O, tác dụng với CuO đun nóng sinh ra xeton là
-
A.
4
-
B.
3
-
C.
2
-
D.
5
Đáp án : B
Ancol bậc 2 tác dụng với CuO tạo ra xeton
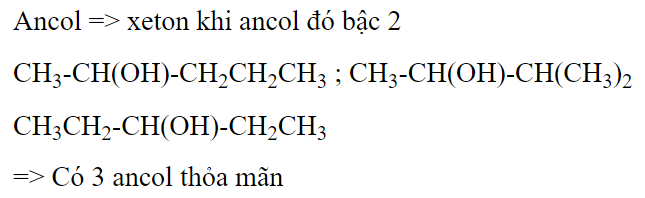
Đốt cháy hoàn toàn hidrocacbon X bằng lượng oxi vừa đủ, thu được CO2 và H2O có tổng số mol bằng tổng số mol của X và O2 tham gia phản ứng. Số nguyên tử hidro (H) có trong X là
-
A.
8
-
B.
6
-
C.
4
-
D.
2
Đáp án : C
CxH2y + (2x+y)/2O2 → xCO2 + yH2O
Giả sử mol CxHy là 1
=> 1 + (2x + y)/2 = x + y
CxH2y + (2x+y)/2 O2 → xCO2 + yH2O
Giả sử mol CxHy là 1 mol
=> 1 + (2x+y)/2 = x + y
=> 2 + 2x + y = 2x + 2y
=> y =2
Hỗn hợp X gồm Al2O3 (0,12 mol), Mg (0,2 mol), Zn (0,1 mol). Cho X tác dụng hết với dung dịch HNO3 loãng (dư), sau phản ứng khối lượng dung dịch tăng 23,54g. Số mol HNO3 phản ứng là
-
A.
0,96 mol
-
B.
1,47 mol
-
C.
1,11 mol
-
D.
0,75 mol
Đáp án : B
Nhận xét: mX = mtăng = 23,54 gam
=> Không có khí thoát ra
=> Sản phẩm khử là NH4NO3
Bảo toàn electron: 8nNH4NO3 = 2nMg + 2nZn
nHNO3 = 10nNH4NO3 + 2nO = 1,47
Ta thấy: mX = mtăng = 23,54 gam
=> Không có khí thoát ra
=> Sản phẩm khử là NH4NO3
- Bảo toàn electron: 8nNH4NO3 = 2nMg + 2nZn
=> nNH4NO3 = 0,075 mol
=> nHNO3 = 10nNH4NO3 + 2nO = 1,47 mol
Nhận định nào sau đây sai?
-
A.
Dung dịch HF hòa tan được SiO2
-
B.
Trong các hợp chất, ngoài mức oxi hóa là -1, flo và clo còn có số oxi hóa là +1, +3, +5, +7
-
C.
Muối AgF tan được trong nước
-
D.
Flo có tính oxi hóa mạnh hơn clo
Đáp án : B
Flo là nguyên tử có độ âm điện lớn nhất trong bảng tuần hoàn
Đáp án B sai vì Flo là nguyên tử có độ âm điện lớn nhất trong bảng tuần hoàn
=> Trong hợp chất chỉ có số oxi hóa là -1
Cho các chất: FeS, Cu2S, FeSO4, H2S, Ag, Fe, KMnO4, Na2SO3, Fe(OH)2. Số chất có thể phản ứng với H2SO4 đặc nóng tạo ra SO2 là
-
A.
7
-
B.
8
-
C.
6
-
D.
9
Đáp án : B
Dựa vào tính chất hóa học của H2SO4 đặc, nóng
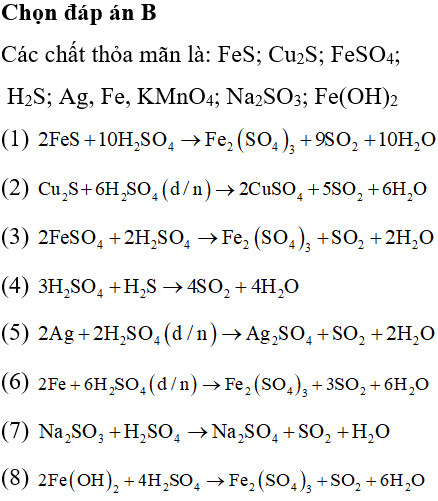
Cho các dung dịch NaOH, BaCl2, Na2CO3, NaHSO4 được dán nhãn X, Y, Z, T không theo thứ tự. Thực hiện các thí nghiệm đối với 4 dung dịch X, Y, Z, T và có kết quả như bảng sau
| Chất | X | Y | Z | T | ↑: khí thoát ra ↓: kết tủa (+): có phản ứng |
| X | (-) | ↓ | ↑ | (+) | |
| Y | ↓ | (-) | ↓ | (-) |
-
A.
Na2CO3, NaHSO4
-
B.
BaCl2, NaOH
-
C.
BaCl2, NaHSO4
-
D.
Na2CO3, NaOH
Đáp án : B
X + Y → kết tủa
X + Z → khí
Ta có:
BaCl2 + Na2CO3 → BaCO3↓ + 2NaCl
2NaHSO4 + Na2CO3 → 2Na2SO4 + CO2 + H2O
=> X là Na2CO3, Y là BaCl2, Z là NaHSO4
=> T là NaOH
Tiến hành các thí nghiệm sau:
(1) O3 tác dụng với dung dịch KI
(2) Axit HF tác dụng với SiO2
(3) Cho khí Cl2 tác dụng với khí H2S
(4) Khí SO2 tác dụng với nước Cl2
(5) KClO3 tác dụng với dung dịch HCl đặc, đun nóng
(6) Cho H2O2 vào dung dịch KMnO4/H2SO4
(7) MnO2 tác dụng với dung dịch HCl đặc, đun nóng
Số thí nghiệm tạo ra đơn chất là
-
A.
4
-
B.
6
-
C.
5
-
D.
3
Đáp án : C
Viết phương trình của từng phản ứng
(1) O3 + 2KI + H2O → 2KOH + O2 + I2
(2) 4HF + SiO2 → SiF4 + 2H2O
(3) Cl2 + H2S → 2HCl + S
(4) SO2 + Cl2 + H2O → H2SO4 + HCl
(5) KClO3 + HCl → KCl + Cl2 + H2O
(6) H2O2 + 2KMnO4 + 3H2SO4 → 2MnSO4 + O2 + K2SO4 + 4H2O
(7) MnO2 + HCl → MnCl2 + Cl2 + H2O
=> Có 5 thí nghiệm tạo ra đơn chất
Hỗn hợp khí X gồm vinylaxetilen, axetilen và propan (x gam). Chia X làm 3 phần bằng nhau.
- Phần 1 tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 20,76 gam kết tủa
- Phần 2 phản ứng tối đa với 0,24 mol H2 (xúc tác Ni, to)
- Đốt cháy hoàn toàn phần 3 với lượng oxi vừa đủ, thu được CO2 và H2O có tỉ lệ mol 1:1
Giá trị của x là
-
A.
18,48 gam
-
B.
21,12 gam
-
C.
17,68 gam
-
D.
19,80 gam
Đáp án : A
Gọi số mol của 3 chất lần lượt là a, b, c mol
- Phần 1: 159a + 240b = 20,76
- Phần 2: 3a + 2b = 0,24
- Phần 3: 4a + 2b + 3c = 2a + b + 4c

Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối với H2 bằng 5. Tỉ lệ a:b bằng
-
A.
1 : 2
-
B.
2 : 1
-
C.
1 : 1
-
D.
2 : 3
Đáp án : B
Bước 1: Y: FeS, Fe dư, S dư
Z: H2, H2S
Bước 2: Tính tỉ lệ mol của H2 và H2S
Bước 3: Giả sử số mol của 2 khí
Bước 4: Bảo toàn mol Fe để tính mol Fe ban đầu
Bước 5: Lập luận phản ứng tính theo nguyên tố S
Bước 5: Tính mol S ban đầu

















