Đề khảo sát chất lượng đầu năm Hóa 12 - Đề số 3
Đề bài
Hợp chất thơm X có CTPT C7H8O. X có thể tác dụng với Na và NaOH. Số đồng phân X thỏa mãn là:
-
A.
3
-
B.
1
-
C.
2
-
D.
4
Cho sơ đồ sau: X + Y → CaCO3 + BaCO3 + H2O
X,Y có thể là
-
A.
Ba(AlO2)2 và Ca(OH)2
-
B.
Ba(OH)2 và Ca(HCO3)2
-
C.
Ba(OH)2 và CO2
-
D.
BaCl2 và Ca(HCO3)2
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
-
A.
HCOOH
-
B.
HCHO.
-
C.
CH3OH.
-
D.
C2H5OH.
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
-
A.
có kết tủa xanh.
-
B.
có kết tủa nâu đen.
-
C.
có kết tủa trắng.
-
D.
có kết tủa vàng.
Cho etin phản ứng với dung dịch brom dư thu được sản phẩm là
-
A.
CH2Br – CH2Br.
-
B.
CHBr2 – CHBr2.
-
C.
CHBr = CHBr.
-
D.
CH2Br – CHBr2.
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là
-
A.
O2 < F2 < N2.
-
B.
O2 < N2 < F2.
-
C.
N2 < O2 < F2.
-
D.
N2 < F2 < O2.
Chất nào trong các chất sau đây không phải là chất lưỡng tính
-
A.
NaHCO3
-
B.
Al(OH)3
-
C.
ZnO
-
D.
Al
Cho N (Z = 7). Cấu hình electron của Nitơ là?
-
A.
1s22s22p4.
-
B.
1s22s22p6.
-
C.
1s22s22p3 .
-
D.
1s22s22p5.
Cho 20 gam Fe tác dụng với HNO3 loãng thu được sản phẩm khử duy nhất NO. Sau khi phản ứng xảy ra hoàn toàn còn dư 3,2 gam Fe. Thể tích NO thu được ở đktc là :
-
A.
2,24 lít.
-
B.
11,2 lít.
-
C.
4,48 lít.
-
D.
6,72 lít.
Tính pH của 300ml dung dịch (gồm 100 ml Ba(OH)2 0,1M và 200 ml NaOH 0,05M)
-
A.
12
-
B.
13
-
C.
10
-
D.
11
Thể tích (ml) của dung dịch NaOH 0,3M cần để trung hòa 3 lít dung dịch HCl 0,01M là
-
A.
0,1
-
B.
1
-
C.
10
-
D.
100
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
-
A.
anken.
-
B.
ankan.
-
C.
ankan và xicloankan.
-
D.
ankin.
Để nhận biết các mẫu chất rắn khan NH4NO3, Na3PO4, KCl người ta dùng dung dịch :
-
A.
NaOH
-
B.
Ba(OH)2
-
C.
KOH
-
D.
Na2CO3
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
-
A.
các chất phản ứng phải là chất điện li mạnh.
-
B.
một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
-
C.
các chất phản ứng phải là những chất dễ tan.
-
D.
phản ứng phải là thuận nghịch.
Cách nào sau đây dùng để điều chế etyl axetat ?
-
A.
Đun hồi lưu hỗn hợp etanol, giấm và axit sunfuric đặc.
-
B.
Đun hồi lưu hỗn hợp axit axetic, rượu trắng và axit sunfuric.
-
C.
Đun hỗn hợp etanol, axit axetic và axit sunfuric đặc trong cốc thuỷ tinh chịu nhiệt.
-
D.
Đun hồi lưu hỗn hợp etanol, axit axetic và axit sunfuric đặc.
Ancol no, mạch hở, đơn chức có công thức tổng quát là
-
A.
CnH2n+2-2π-2vO (n ≥ 1)
-
B.
CnH2n+2On (n ≥ 1)
-
C.
CnH2n+2O (n ≥ 1)
-
D.
CnH2nO (n ≥ 2)
Theo A-rê-ni-ut, chất nào sau đây là axit ?
-
A.
NH4+
-
B.
HCl
-
C.
H3O+
-
D.
NaOH
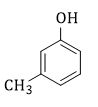
Chất X có CTCT như hình bên. X có tên gọi
-
A.
4 – metylphenol.
-
B.
2 – metylphenol.
-
C.
5 – metylphenol.
-
D.
3 – metylphenol.
Đánh giá độ dinh dưỡng của phân lân bằng hàm lượng %
-
A.
P2O5.
-
B.
H3PO4.
-
C.
P.
-
D.
PO43-.
Đime hóa axetilen trong điều kiện thích hợp thu được chất nào sau đây ?
-
A.
buta-1,3-đien.
-
B.
đivinyl.
-
C.
vinylaxetilen.
-
D.
but-1-in.
HNO3 chỉ thể hiện tính oxi hóa khi tác dụng với các chất thuộc dãy nào dưới đây?
-
A.
Mg, H2S, C, Fe3O4, Fe(OH)2.
-
B.
Na2SO3, P, CuO, CaCO3, Ag.
-
C.
Al, FeCO3, HI, CaO, FeO.
-
D.
Cu, C, Fe2O3, Fe(OH)2, SO2.
Khi tách nước từ một chất X có công thức phân tử C4H10O tạo thành 3 anken là đồng phân của nhau (tính cả đồng phân hình học). Công thức cấu tạo thu gọn của X là :
-
A.
CH3CH(OH)CH2CH3
-
B.
(CH3)3COH
-
C.
CH3OCH2CH2CH3
-
D.
CH3CH(CH3)CH2OH
Có bao nhiêu đồng phân C4H10O khi tác dụng với CuO nung nóng sinh ra anđehit?
-
A.
3
-
B.
4
-
C.
2
-
D.
1
Cho Cu và dung dịch H2SO4 loãng tác dụng với chất X (một loại phân bón hóa học), thấy thoát ra khí không màu, hóa nâu trong không khí. Mặt khác, khi X tác dụng với dung dịch NaOH thì có mùi khai thoát ra. Chất X là
-
A.
amophot.
-
B.
ure.
-
C.
natri nitrat.
-
D.
amoni nitrat.
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
-
A.
1 lít.
-
B.
1,5 lít.
-
C.
0,8 lít.
-
D.
2 lít.
Thành phần chính của khí than ướt là
-
A.
\(CO,C{O_2},{H_2},{N_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{H_2},N{O_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Axit panmitic là axit nào sau đây ?
-
A.
C15H31COOH.
-
B.
C17H33COOH.
-
C.
C17H35COOH.
-
D.
C17H31COOH.
Đốt cháy hoàn toàn một lượng ancol A thu được số mol nước gấp đôi số mol CO2. Tên gọi của A là
-
A.
ancol etylic
-
B.
ancol metylic
-
C.
ancol benzylic
-
D.
propenol
pH của dung dịch H2SO4 0,0005 M và pH của dung dịch CH3COOH 0,1 M (α = 4,25%) lần lượt là
-
A.
3; 2,37
-
B.
3; 3,90
-
C.
5; 3,37
-
D.
4; 3,38
Một dung dịch chứa 0,01 mol Mg2+, 0,03 mol Na+, x mol Cl- và y mol PO43−. Tổng khối lượng các muối tan có trong dung dịch là 2,59 gam. Giá trị của x và y lần lượt là:
-
A.
0,01 và 0,03.
-
B.
0,01 và 0,01.
-
C.
0,03 và 0,02.
-
D.
0,02 và 0,01.
Dung dịch Y chứa 0,02 mol Mg2+; 0,03 mol Na+; 0,03 mol Cl- và y mol SO42-. Giá trị của y là
-
A.
0,01.
-
B.
0,02.
-
C.
0,015.
-
D.
0,025.
Cho 0,001 mol NH4Cl vào 100 ml dung dịch NaOH có pH = 12 và đun sôi, sau đó làm nguội, thêm vào một ít phenolphtalein, dung dịch thu được có màu
-
A.
xanh
-
B.
hồng
-
C.
trắng
-
D.
không màu
Khối lượng NaNO2 cần dùng trong phòng thí nghiệm để thu được 6,72 lít N2 (đktc) là
-
A.
19,2 gam
-
B.
20,1 gam
-
C.
27,0 gam
-
D.
20,7 gam
Phân bón nào dưới đây có hàm lượng N cao nhất?
-
A.
NH4Cl
-
B.
NH4NO3
-
C.
Ca(NO3)2
-
D.
(NH2)2CO
Khi sục từ từ đến dư khí CO2 vào dung dịch hỗn hợp chứa a mol Ca(OH)2 và b mol NaOH. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
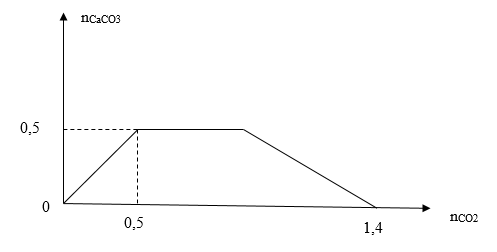
Tỉ lệ a: b là
-
A.
5: 4.
-
B.
2:3.
-
C.
4:3.
-
D.
4:5
Đun nóng hỗn hợp khí gồm 0,06 mol C2H2 và 0,04 mol H2 với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư) thì còn lại 0,448 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với O2 là 0,5. Khối lượng bình dung dịch brom tăng là
-
A.
1,20 gam.
-
B.
1,04 gam.
-
C.
1,64 gam.
-
D.
1,32 gam.
Đề hiđro hoá etylbenzen ta được stiren; trùng hợp stiren ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là:
-
A.
13,52 tấn.
-
B.
10,60 tấn.
-
C.
13,25 tấn.
-
D.
8,48 tấn.
Chất hữu cơ A trong phân tử chứa 1 nguyên tử Oxi, có M = 46. Đốt cháy A chỉ thu được CO2 và H2O. Có bao nhiêu CTCT phù hợp với A
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Gọi m là số nhóm chức của ancol A. Cho 1 mol ancol A tác dụng với Na dư thì thể tích khí H2 sinh ra (ở đktc) là
-
A.
11,2m lít.
-
B.
22,4m lít.
-
C.
$\frac{m}{{11,2}}$ lít.
-
D.
$\frac{m}{{22,4}}$ lít.
Oxi hoá 0,1 mol ancol etylic thu được m gam hỗn hợp Y gồm axetanđehit, nước và ancol etylic dư. Cho Na dư vào m gam hỗn hợp Y sinh ra V lít hiđro (đktc). Phát biểu đúng là
-
A.
V = 2,24 lít
-
B.
V = 1,12 lít
-
C.
Hiệu suất phản ứng oxi hoá ancol là 100%
-
D.
Số mol Na phản ứng là 0,2 mol
Cho 15,8 gam hỗn hợp gồm CH3OH, C6H5OH tác dụng với dung dịch brom dư, thì làm mất màu vừa hết 48 gam Br2. Nếu đốt cháy hoàn toàn hỗn hợp trên thì thể tích CO2 thu được ở điều kiện tiêu chuẩn là
-
A.
16,80 lít.
-
B.
44,80 lít.
-
C.
22,40 lít.
-
D.
17,92 lít.
Fomalin hay fomon (dùng để bảo quản xác động vật chống thối rữa) là
-
A.
dung dịch HCHO 37% - 40% về khối lượng trong nước.
-
B.
rượu etylic 46o.
-
C.
dung dịch HCHO 25% - 30% về thể tích trong nước.
-
D.
dung dịch CH3CHO 40% về thể tích trong nước.
Cho 0,2 mol một anđehit đơn chức, mạch hở X phản ứng vừa đủ với 300 ml dung dịch chứa AgNO3 2M trong NH3. Sau khi phản ứng xảy ra hoàn toàn thu được 87,2 gam kết tủa. Công thức phân tử của anđehit là:
-
A.
C3H3CHO
-
B.
C4H5CHO
-
C.
C3H5CHO.
-
D.
C4H3CHO
Cho 0,04 mol một hỗn hợp X gồm CH2=CH-COOH, CH3COOH và CH2=CH-CHO phản ứng vừa đủ với dung dịch chứa 6,4 gam brom. Mặt khác, để trung hoà 0,04 mol X cần dùng vừa đủ 40 ml dung dịch NaOH 0,75 M. Khối lượng của CH2=CH-COOH trong X là
-
A.
0,56 gam.
-
B.
1,44 gam.
-
C.
0,72 gam.
-
D.
2,88 gam.
Trong phân tử axit cacboxylic X có số nguyên tử cacbon bằng số nhóm chức. Đốt cháy hoàn toàn một lượng X thu được số mol CO2 bằng số mol H2O. Tên gọi của X là
-
A.
axit axetic.
-
B.
axit malonic.
-
C.
axit oxalic.
-
D.
axit fomic.
Đốt cháy hết a mol axit X được 2a mol CO2. Để trung hoà vừa hết a mol X cần 2a mol NaOH. Tìm X
-
A.
C2H4(COOH)2
-
B.
CH2(COOH)2
-
C.
CH3COOH
-
D.
(COOH)2
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2, thu được 25 gam kết tủa và dung dịch X. Thêm tối thiểu 200 ml dung dịch NaOH 1M vào X, thì được lượng kết tủa lớn nhất. Tính V
-
A.
10,08
-
B.
14,56
-
C.
7,84
-
D.
12,32
X là hỗn hợp gồm HOOC-COOH, OHC-COOH, OHC-C≡C-CHO, OHC-C≡C-COOH; Y là axit cacboxylic no, đơn chức, mạch hở. Đun nóng m gam X với lượng dư dung dịch AgNO3 trong NH3, thu được 23,76 gam Ag. Nếu cho m gam X tác dụng với NaHCO3 dư thì thu được 0,07 mol CO2. Đốt cháy hoàn toàn hỗn hợp gồm m gam X và m gam Y cần 0,805 mol O2, thu được 0,785 mol CO2. Giá trị của m là
-
A.
8,8.
-
B.
4,6.
-
C.
6,0.
7,4.
-
D.
7,4.
Dung dịch HCl và CH3COOH có cùng nồng độ. pH của hai dung dịch này tương ứng là x và y. Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li. Quan hệ giữa x và y là:
-
A.
y = 100x
-
B.
y = 2x
-
C.
y = x – 2
-
D.
y = x + 2
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
-
A.
NaOH và Al(OH)3.
-
B.
NaOH, NaAlO2 và Al(OH)3.
-
C.
NaAlO2 và BaCO3.
-
D.
Ba(OH)2, NaOH và BaCO3.
Lời giải và đáp án
Hợp chất thơm X có CTPT C7H8O. X có thể tác dụng với Na và NaOH. Số đồng phân X thỏa mãn là:
-
A.
3
-
B.
1
-
C.
2
-
D.
4
Đáp án : A
X có thể tác dụng với Na và NaOH nên X là phenol.
Vậy X có 3 đồng phân là: 2-metylphenol; 3-metylphenol; 4-metylphenol
Cho sơ đồ sau: X + Y → CaCO3 + BaCO3 + H2O
X,Y có thể là
-
A.
Ba(AlO2)2 và Ca(OH)2
-
B.
Ba(OH)2 và Ca(HCO3)2
-
C.
Ba(OH)2 và CO2
-
D.
BaCl2 và Ca(HCO3)2
Đáp án : B
A. không có phản ứng
B. Ba(OH)2 + Ca(HCO3)2 → CaCO3 + BaCO3 +2 H2O
C. \(Ba{(OH)_2} + C{O_2} \to BaC{{\text{O}}_3} + {H_2}O\)
Hoặc \(Ba{(OH)_2} + C{O_2} \to Ba{(HC{O_3})_2}\)
D. không có phản ứng
Chất nào sau đây ở thể khí ở nhiệt độ thường ?
-
A.
HCOOH
-
B.
HCHO.
-
C.
CH3OH.
-
D.
C2H5OH.
Đáp án : B
- Ở điều kiện thường, các axit cacboxylic đều là những chất lỏng hoặc rắn.
- HCHO là những chất khí tan tốt trong nước
- CH3OH và C2H5HO là những chất lỏng
Khi cho axetilen vào dung dịch AgNO3 trong NH3 dư, hiện tượng quan sát được là
-
A.
có kết tủa xanh.
-
B.
có kết tủa nâu đen.
-
C.
có kết tủa trắng.
-
D.
có kết tủa vàng.
Đáp án : D
Cho axetilen vào dung dịch AgNO3 :
CH≡CH + 2AgNO3 + 2NH3 → CAg≡CAg ↓vàng nhạt + 2NH4NO3
=> phản ứng tạo kết tủa vàng nhạt
Cho etin phản ứng với dung dịch brom dư thu được sản phẩm là
-
A.
CH2Br – CH2Br.
-
B.
CHBr2 – CHBr2.
-
C.
CHBr = CHBr.
-
D.
CH2Br – CHBr2.
Đáp án : B
CH≡CH + 2Br2 → CHBr2 – CHBr2
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là
-
A.
O2 < F2 < N2.
-
B.
O2 < N2 < F2.
-
C.
N2 < O2 < F2.
-
D.
N2 < F2 < O2.
Đáp án : C
Thứ tự tăng dần tính oxi hóa của các đơn chất O2, F2, N2 là: N2 < O2 < F2.
Chất nào trong các chất sau đây không phải là chất lưỡng tính
-
A.
NaHCO3
-
B.
Al(OH)3
-
C.
ZnO
-
D.
Al
Đáp án : D
Chất không phải là chất có tính lưỡng tính là Al vì Al tác dụng với NaOH và HCl thay đổi số oxi hóa nên không coi là phản ứng axit – bazơ.
Cho N (Z = 7). Cấu hình electron của Nitơ là?
-
A.
1s22s22p4.
-
B.
1s22s22p6.
-
C.
1s22s22p3 .
-
D.
1s22s22p5.
Đáp án : C
Nito có cấu hình e là: 1s22s22p3
Cho 20 gam Fe tác dụng với HNO3 loãng thu được sản phẩm khử duy nhất NO. Sau khi phản ứng xảy ra hoàn toàn còn dư 3,2 gam Fe. Thể tích NO thu được ở đktc là :
-
A.
2,24 lít.
-
B.
11,2 lít.
-
C.
4,48 lít.
-
D.
6,72 lít.
Đáp án : C
Do Fe dư nên tạo thành muối Fe2+
Sử dụng định luật bảo toàn e: 2nFe = 3nNO => nNO = ?
Do Fe dư nên tạo thành muối Fe2+
nFe = (20 – 3,2)/56 = 0,3 mol
BTe ta có: 2nFe = 3nNO => nNO = 2.0,3/3 = 0,2 mol
=> V = 4,48 lít
Tính pH của 300ml dung dịch (gồm 100 ml Ba(OH)2 0,1M và 200 ml NaOH 0,05M)
-
A.
12
-
B.
13
-
C.
10
-
D.
11
Đáp án : B
Từ số mol của Ba(OH)2 và NaOH \( \to {n_{O{H^ - }}} = 2{n_{Ba{{(OH)}_2}}} + {n_{NaOH}}\)
\( \to {\text{[}}O{H^ - }{\text{] = }}\dfrac{{{n_{O{H^ - }}}}}{{0,3}}\)
Mà [OH-].[H+] = 10-14
\( \to [{H^ + }] \to pH\)
\({n_{Ba{{(OH)}_2}}} = 0,1.0,1 = 0,01\,\,mol;{n_{NaOH}} = 0,2.0,05 = 0,01\,\,mol\)
\( \to {n_{OH - }} = 2{n_{Ba{{(OH)}_2}}} + {n_{NaOH}} = 2.0,01 + 0,01 = 0,03\,\,mol\)
\( \to [O{H^ - }] = \dfrac{{0,03}}{{0,3}} = 0,1\,\,M\)
Mà [OH-].[H+] = 10-14
\( \to [{H^ + }] = \dfrac{{{{10}^{ - 14}}}}{{0,1}} = {10^{ - 13}}\)
\( \to pH = - \log {10^{ - 13}} = 13\)
Thể tích (ml) của dung dịch NaOH 0,3M cần để trung hòa 3 lít dung dịch HCl 0,01M là
-
A.
0,1
-
B.
1
-
C.
10
-
D.
100
Đáp án : D
Tính theo PTHH: NaOH + HCl → NaCl + H2O
nHCl = 3.0,01 = 0,03 mol
PTHH: NaOH + HCl → NaCl + H2O
nNaOH = nHCl = 0,03 mol
=> V dd NaOH = n : CM = 0,03 : 0,3 = 0,1 lít = 100 ml
Hợp chất hữu cơ X có công thức phân tử dạng CnH2n+2. X thuộc dãy đồng đẳng của
-
A.
anken.
-
B.
ankan.
-
C.
ankan và xicloankan.
-
D.
ankin.
Đáp án : B
X thuộc dãy đồng đẳng của ankan.
Để nhận biết các mẫu chất rắn khan NH4NO3, Na3PO4, KCl người ta dùng dung dịch :
-
A.
NaOH
-
B.
Ba(OH)2
-
C.
KOH
-
D.
Na2CO3
Đáp án : B
Xem lại lí thuyết phân bón hóa học
ta dùng dung dịch Ba(OH)2
|
|
NH4NO3 |
Na3PO4 |
KCl |
|
Dung dịch Ba(OH)2 |
Tan, tạo khí mùi khai |
Tan, có kết tủa trắng |
Tan, tạo dung dịch trong suốt |
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
-
A.
các chất phản ứng phải là chất điện li mạnh.
-
B.
một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
-
C.
các chất phản ứng phải là những chất dễ tan.
-
D.
phản ứng phải là thuận nghịch.
Đáp án : B
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng.
Cách nào sau đây dùng để điều chế etyl axetat ?
-
A.
Đun hồi lưu hỗn hợp etanol, giấm và axit sunfuric đặc.
-
B.
Đun hồi lưu hỗn hợp axit axetic, rượu trắng và axit sunfuric.
-
C.
Đun hỗn hợp etanol, axit axetic và axit sunfuric đặc trong cốc thuỷ tinh chịu nhiệt.
-
D.
Đun hồi lưu hỗn hợp etanol, axit axetic và axit sunfuric đặc.
Đáp án : D
Xem lại lí thuyết phản ứng este hóa
Cách dùng để điều chế etyl axetat là đun hồi lưu hỗn hợp etanol, axit axetic và axit sunfuric đặc. Không dùng giấm và rượu trắng vì độ tinh khiết không cao => hiệu suất thấp
Ancol no, mạch hở, đơn chức có công thức tổng quát là
-
A.
CnH2n+2-2π-2vO (n ≥ 1)
-
B.
CnH2n+2On (n ≥ 1)
-
C.
CnH2n+2O (n ≥ 1)
-
D.
CnH2nO (n ≥ 2)
Đáp án : C
Ancol no, mạch hở, đơn chức có công thức tổng quát là CnH2n+2O (n ≥ 1)
Theo A-rê-ni-ut, chất nào sau đây là axit ?
-
A.
NH4+
-
B.
HCl
-
C.
H3O+
-
D.
NaOH
Đáp án : B
Theo A-rê-ni-ut, axit là chất phân li ra H+ => HCl là axit
Chất X có CTCT như hình bên. X có tên gọi

-
A.
4 – metylphenol.
-
B.
2 – metylphenol.
-
C.
5 – metylphenol.
-
D.
3 – metylphenol.
Đáp án : D
Đánh số từ nhóm OH => tên gọi: 3-metylphenol
Đánh giá độ dinh dưỡng của phân lân bằng hàm lượng %
-
A.
P2O5.
-
B.
H3PO4.
-
C.
P.
-
D.
PO43-.
Đáp án : A
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của P2O5.
Ngoài ra, HS ghi nhớ thêm:
Độ dinh dưỡng của phân đạm được đánh giá bằng hàm lượng % của N.
Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng % của K2O.
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của P2O5.
Đime hóa axetilen trong điều kiện thích hợp thu được chất nào sau đây ?
-
A.
buta-1,3-đien.
-
B.
đivinyl.
-
C.
vinylaxetilen.
-
D.
but-1-in.
Đáp án : C
Phản ứng đime hóa: 2CH≡CH $\xrightarrow{xt,{{t}^{o}}}$ CH2=CH–C≡CH
=> thu được vinylaxetilen
HNO3 chỉ thể hiện tính oxi hóa khi tác dụng với các chất thuộc dãy nào dưới đây?
-
A.
Mg, H2S, C, Fe3O4, Fe(OH)2.
-
B.
Na2SO3, P, CuO, CaCO3, Ag.
-
C.
Al, FeCO3, HI, CaO, FeO.
-
D.
Cu, C, Fe2O3, Fe(OH)2, SO2.
Đáp án : A
HNO3 thể hiện tính oxi hóa khi phản ứng với các chất khử (chất có khả năng tăng số oxi hóa)
A đúng
B loại CuO, CaCO3
C loại CaO
D loại Fe2O3
Khi tách nước từ một chất X có công thức phân tử C4H10O tạo thành 3 anken là đồng phân của nhau (tính cả đồng phân hình học). Công thức cấu tạo thu gọn của X là :
-
A.
CH3CH(OH)CH2CH3
-
B.
(CH3)3COH
-
C.
CH3OCH2CH2CH3
-
D.
CH3CH(CH3)CH2OH
Đáp án : A
Loại dần đáp án không phù hợp; Loại B và C vì B, C không bị tách nước
Loại D do D chỉ có một hướng tách nên không thể tạo ra 3 anken
A đúng vì CH3CH(OH)CH2CH3 có 2 hướng tách và tạo đồng phân hình học
Có bao nhiêu đồng phân C4H10O khi tác dụng với CuO nung nóng sinh ra anđehit?
-
A.
3
-
B.
4
-
C.
2
-
D.
1
Đáp án : C
Xem lại lí thuyết phản ứng oxi hóa không hoàn toàn
Ancol bậc 1 tác dụng với CuO nung nóng sinh ra anđehit
CH3-CH2-CH2-CH2OH
CH3-CH(CH3)-CH2OH
Có 2 đồng phân
Cho Cu và dung dịch H2SO4 loãng tác dụng với chất X (một loại phân bón hóa học), thấy thoát ra khí không màu, hóa nâu trong không khí. Mặt khác, khi X tác dụng với dung dịch NaOH thì có mùi khai thoát ra. Chất X là
-
A.
amophot.
-
B.
ure.
-
C.
natri nitrat.
-
D.
amoni nitrat.
Đáp án : D
Khí X không màu là NO, khí mùi khai là NH3. Từ sản phẩm thu được suy ngược lại thành phần của X
Cu và H2SO4 tác dụng với chất X có khí không màu, hóa nâu trong không khí là NO => Trong X có nhóm NO3-
Khi X tác dụng với dd NaOH → khí mùi khai → khí đó là NH3
Vậy công thức của X là NH4NO3: amoni nitrat
PTHH: Cu + 4H2SO4 + 8NH4NO3 → 4(NH4)2SO4 + 3Cu(NO3)2 + 4H2O + 2NO↑
NaOH + NH4NO3 → NaNO3 + NH3↑(mùi khai) + H2O
Từ 1 lít hỗn hợp CO và CO2 có thể điều chế tối đa bao nhiêu lít CO2? (H = 100%)
-
A.
1 lít.
-
B.
1,5 lít.
-
C.
0,8 lít.
-
D.
2 lít.
Đáp án : A
Bảo toàn nguyên tố C.
Bảo toàn nguyên tố C ta có: nCO2 thu được = nCO + nCO2 bđ
Hay V CO2 thu được = VCO + VCO2 bđ = 1 lít
Thành phần chính của khí than ướt là
-
A.
\(CO,C{O_2},{H_2},{N_2}\)
-
B.
\(C{H_4},CO,C{O_2},{N_2}\)
-
C.
\(CO,C{O_2},{H_2},N{O_2}\)
-
D.
\(CO,C{O_2},N{H_3},{N_2}\)
Đáp án : A
Thành phần chính của khí than ướt là CO, CO2, H2, N2
Axit panmitic là axit nào sau đây ?
-
A.
C15H31COOH.
-
B.
C17H33COOH.
-
C.
C17H35COOH.
-
D.
C17H31COOH.
Đáp án : A
Axit panmitic có CTPT là C15H31COOH.
Đốt cháy hoàn toàn một lượng ancol A thu được số mol nước gấp đôi số mol CO2. Tên gọi của A là
-
A.
ancol etylic
-
B.
ancol metylic
-
C.
ancol benzylic
-
D.
propenol
Đáp án : B
Nếu đốt cháy ancol cho nH2O > 1,5.nCO2 thì ancol là CH3OH. Chỉ có CH4 và CH3OH có tính chất này (không kể amin)
nH2O > 1,5.nCO2 => ancol đốt cháy là CH3OH
pH của dung dịch H2SO4 0,0005 M và pH của dung dịch CH3COOH 0,1 M (α = 4,25%) lần lượt là
-
A.
3; 2,37
-
B.
3; 3,90
-
C.
5; 3,37
-
D.
4; 3,38
Đáp án : A
áp dụng công thức: pH = -log[H+] và độ điện li α = Cphân li / Cban đầu
${H_2}S{O_4}{\text{ }}\xrightarrow{{}}{\text{ }}2{H^ + }{\text{ }} + {\text{ }}S{O_4}^{2 - }$
$0,0005{\text{ }}M{\text{ }}\xrightarrow{{}}{\text{ 0,001 M = > pH = - log[ }}{{\text{H}}^ + }] = 3$
$C{H_3}COOH{\text{ }}\underset {} \leftrightarrows {\text{ }}C{H_3}CO{O^ - }{\text{ }} + {\text{ }}{H^ + }$
Ban đầu (CM) 0,1 0 0
Phân li (CM) x x x
$ = > {\text{ độ điện li }} = \dfrac{{{{[C{H_3}COOH]}_{P{\text{hân li}}}}}}{{[C{H_3}COOH]{\text{ban đầu}}}}.100\% = > \dfrac{x}{{0,1}}.100\% = 4,25\% $
$= > x = 4,{25.10^{ - 3}}M = [{H^ + }]$
$= > pH = - \log ([{H^ + }]) = 2,37$
Một dung dịch chứa 0,01 mol Mg2+, 0,03 mol Na+, x mol Cl- và y mol PO43−. Tổng khối lượng các muối tan có trong dung dịch là 2,59 gam. Giá trị của x và y lần lượt là:
-
A.
0,01 và 0,03.
-
B.
0,01 và 0,01.
-
C.
0,03 và 0,02.
-
D.
0,02 và 0,01.
Đáp án : D
+) Áp dụng định luật bảo toàn điện tích có PT(1)
+) Áp dụng định luật bảo toàn khối lượng ta có:
mmuối = ${\text{ }}\sum {{m_{ion}}} $ => PT (2)
Áp dụng định luật bảo toàn điện tích ta có:
0,01.2 + 0,03.1 = x.1 + y.3 (1)
Áp dụng định luật bảo toàn khối lượng ta có:
mmuối = ${\text{ }}\sum {{m_{ion}}} {\text{ = > 2,59 = 0,01}}{\text{.24 + 0,03}}{\text{.23 + x}}{\text{.35,5 + y}}{\text{.95 (2)}}$
- Giải hệ hai phương trình (1) và (2) ta được: x = 0,02; y = 0,01
Dung dịch Y chứa 0,02 mol Mg2+; 0,03 mol Na+; 0,03 mol Cl- và y mol SO42-. Giá trị của y là
-
A.
0,01.
-
B.
0,02.
-
C.
0,015.
-
D.
0,025.
Đáp án : B
Áp dụng định luật bảo toàn điện tích cho dung dịch Y.
Áp dụng định luật bảo toàn điện tích cho dung dịch Y ta có:
\(2{n_{M{g^{2 + }}}} + {n_{N{a^ + }}} = {n_{C{l^ - }}} + 2{n_{SO_4^{2 - }}}\) => 2.0,02 + 0,03 = 0,03 + 2.y
=> y = 0,02
Cho 0,001 mol NH4Cl vào 100 ml dung dịch NaOH có pH = 12 và đun sôi, sau đó làm nguội, thêm vào một ít phenolphtalein, dung dịch thu được có màu
-
A.
xanh
-
B.
hồng
-
C.
trắng
-
D.
không màu
Đáp án : D
Tính toán theo PTHH: NH4Cl + NaOH → NaCl + NH3 + H2O
+ Dung dịch sau phản ứng có môi trường kiềm thì phenolphtalein chuyển màu hồng
+ Dung dịch sau phản ứng có môi trường axit hoặc trung tính thì phenolphtalein không đổi màu
pOH = 14 – pH = 2 => CM NaOH = (OH-) = 0,01M
nNaOH = 0,1.0,01 = 0,001 mol
PTHH: NH4Cl + NaOH → NaCl + NH3 + H2O
Pư: 0,001 0,001
Do phản ứng vừa đủ nên sau khi đun sôi thì NH3 bay hơi hết, dung dịch thu được chỉ còn lại NaCl có môi trường trung tính nên không làm đổi màu dung dịch phenolphtalein
Khối lượng NaNO2 cần dùng trong phòng thí nghiệm để thu được 6,72 lít N2 (đktc) là
-
A.
19,2 gam
-
B.
20,1 gam
-
C.
27,0 gam
-
D.
20,7 gam
Đáp án : D
Trong phòng thí nghiệm người ta điều chế N2 bằng phản ứng:
NH4Cl + NaNO2 \(\xrightarrow{{{t}^{o}}}\) N2 + NaCl + 2H2O
- Tính toán theo PTHH.
NH4Cl + NaNO2 \(\xrightarrow{{{t}^{o}}}\) N2 + NaCl + 2H2O
Theo PTHH: nNaNO2 = nN2 = 6,72:22,4 = 0,3 mol
=> mNaNO2 = 0,3.69 = 20,7 gam
Phân bón nào dưới đây có hàm lượng N cao nhất?
-
A.
NH4Cl
-
B.
NH4NO3
-
C.
Ca(NO3)2
-
D.
(NH2)2CO
Đáp án : D
Ure (NH2)2CO là phân bón có thành phần N lớn nhất.
Khi sục từ từ đến dư khí CO2 vào dung dịch hỗn hợp chứa a mol Ca(OH)2 và b mol NaOH. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:

Tỉ lệ a: b là
-
A.
5: 4.
-
B.
2:3.
-
C.
4:3.
-
D.
4:5
Đáp án : A
Chia đồ thị ra làm 3 giai đoạn:
+ giai đoạn 1: đồ thị đi lên xảy ra phản ứng
CO2 + Ca(OH)2 → CaCO3↓ + H2O
+ giai đoạn 2: đồ thị đi ngang do xảy ra phản ứng
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + Na2CO3 + H2O → 2NaHCO3
+ giai đoạn 3: đồ thị đi xuống do xảy ra phản ứng
CO2 + CaCO3 + H2O → Ca(HCO3)2
+ Tại giai đoạn 1: đồ thị đi lên do xảy ra phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
→ nCaCO3 max = 0,5 (mol).
BTNT "Ca": nCa(OH)2 bđ = 0,5 (mol) = a
+ Tại giai đoạn 3: đồ thị đi xuống khi hòa tan hoàn toàn kết tủa
→ Muối thu được gồm: NaHCO3 và Ca(HCO3)2
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 = 0,5 (mol)
BTNT "C": nCO2 = nNaHCO3 + 2nCa(HCO3)2
→ 1,4 = b + 2.0,5 → b = 0,4 (mol)
Vậy a : b = 0,5 : 0,4 = 5 : 4
Đun nóng hỗn hợp khí gồm 0,06 mol C2H2 và 0,04 mol H2 với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn toàn bộ hỗn hợp Y lội từ từ qua bình đựng dung dịch brom (dư) thì còn lại 0,448 lít hỗn hợp khí Z (ở đktc) có tỉ khối so với O2 là 0,5. Khối lượng bình dung dịch brom tăng là
-
A.
1,20 gam.
-
B.
1,04 gam.
-
C.
1,64 gam.
-
D.
1,32 gam.
Đáp án : D
Bảo toàn khối lượng ta có: mC2H2 + mH2 = mY = mZ + m
Bảo toàn khối lượng ta có: mC2H2 + mH2 = mY = mZ + m
=> 0,06.26 + 0,04.2 = m + 0,02.0,5.32
=> m = 1,32 gam
Đề hiđro hoá etylbenzen ta được stiren; trùng hợp stiren ta được polistiren với hiệu suất chung 80%. Khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polisitren là:
-
A.
13,52 tấn.
-
B.
10,60 tấn.
-
C.
13,25 tấn.
-
D.
8,48 tấn.
Đáp án : C
$n{C_6}{H_5}C{H_2}C{H_3}\xrightarrow{{ - {H_2},{t^o},xt}}n{C_6}{H_5}CH = C{H_2}\;\xrightarrow{{{t^o},\,p,\,xt}}{\rlap{-} (CH({C_6}{H_5})-C{H_2}\rlap{-} )_n}$
gam: 106n → 104n
tấn: x.80% → 10,4
Sơ đồ phản ứng:
$n{C_6}{H_5}C{H_2}C{H_3}\xrightarrow{{-{H_2},\,{t^o},\,xt}}n{C_6}{H_5}CH = C{H_2}\;\xrightarrow{{{t^o},\,p,\,xt}}{\rlap{-} (\,CH({C_6}{H_5})-C{H_2}\rlap{-} )_n}$
gam: 106n → 104n
tấn: x.80% → 10,4
Vậy khối lượng etylbenzen cần dùng để sản xuất 10,4 tấn polistiren với hiệu suất 80% là :
x = $\frac{{10,4.106n}}{{104n.80\% }} = 13,25$ tấn
Chất hữu cơ A trong phân tử chứa 1 nguyên tử Oxi, có M = 46. Đốt cháy A chỉ thu được CO2 và H2O. Có bao nhiêu CTCT phù hợp với A
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đáp án : A
Đốt cháy A chỉ thu được CO2 và H2O => trong A chứa C, H và có thể có O
Gọi CTPT của A là CxHyOz => 12x + y + 16z = 46
Nếu z = 0 không có cặp x và y thỏa mãn
Nếu z = 1 => x = 2, y = 6 thoản mãn => CTPT: C2H6O
=> có 2 CTCT: CH3-CH2OH và CH3-O-CH3
Gọi m là số nhóm chức của ancol A. Cho 1 mol ancol A tác dụng với Na dư thì thể tích khí H2 sinh ra (ở đktc) là
-
A.
11,2m lít.
-
B.
22,4m lít.
-
C.
$\frac{m}{{11,2}}$ lít.
-
D.
$\frac{m}{{22,4}}$ lít.
Đáp án : A
Gọi ancol A có dạng R(OH)m
2R(OH)m + 2Na → 2R(ONa)m + mH2
Gọi ancol A có dạng R(OH)m
2R(OH)m + 2Na → 2R(ONa)m + mH2
1 mol → 0,5m mol
=> VH2 = 22,4.0,5m = 11,2m lít
Oxi hoá 0,1 mol ancol etylic thu được m gam hỗn hợp Y gồm axetanđehit, nước và ancol etylic dư. Cho Na dư vào m gam hỗn hợp Y sinh ra V lít hiđro (đktc). Phát biểu đúng là
-
A.
V = 2,24 lít
-
B.
V = 1,12 lít
-
C.
Hiệu suất phản ứng oxi hoá ancol là 100%
-
D.
Số mol Na phản ứng là 0,2 mol
Đáp án : B
+) nancol bđ = 2nH2
Ta có: nancol bđ = 2nH2=> nH= $\frac{{0,1}}{2}$ = 0,05 mol
Vậy V = 0,05. 22,4 = 1,12 lít
Cho 15,8 gam hỗn hợp gồm CH3OH, C6H5OH tác dụng với dung dịch brom dư, thì làm mất màu vừa hết 48 gam Br2. Nếu đốt cháy hoàn toàn hỗn hợp trên thì thể tích CO2 thu được ở điều kiện tiêu chuẩn là
-
A.
16,80 lít.
-
B.
44,80 lít.
-
C.
22,40 lít.
-
D.
17,92 lít.
Đáp án : D
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
Từ số mol Br2 tính số mol C6H5OH => số mol CH3OH
+) Bảo toàn nguyên tố C: ${n_{C{O_2}}} = {n_{C{H_3}OH}} + \,6.{n_{{C_6}{H_5}OH}}$
${n_{B{r_2}}} = \,\frac{{48}}{{160}}\, = 0,3\,mol$
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
0,1 mol ← 0,3 mol
→ ${m_{{C_6}{H_5}OH}} = \,0,1.94 = 9,4\,gam$→ ${m_{C{H_3}OH}} = \,15,8 - 9,4 = 6,4\,gam$ → ${n_{C{H_3}OH}} = \frac{{6,4}}{{32}} = 0,2\,mol$
Bảo toàn nguyên tố C:
→ ${n_{C{O_2}}} = {n_{C{H_3}OH}} + \,6.{n_{{C_6}{H_5}OH}} = 0,2 + 6.0,1 = 0,8\,mol$
→ ${V_{C{O_2}(\,ktc)}} = 0,8.22,4 = 17,92\,$ lít
Fomalin hay fomon (dùng để bảo quản xác động vật chống thối rữa) là
-
A.
dung dịch HCHO 37% - 40% về khối lượng trong nước.
-
B.
rượu etylic 46o.
-
C.
dung dịch HCHO 25% - 30% về thể tích trong nước.
-
D.
dung dịch CH3CHO 40% về thể tích trong nước.
Đáp án : A
Dung dịch nước của anđehit fomic được gọi là fomon. Dung dịch bão hòa của anđehit fomic (có nồng độ 37-40%) được gọi là fomlin.
Cho 0,2 mol một anđehit đơn chức, mạch hở X phản ứng vừa đủ với 300 ml dung dịch chứa AgNO3 2M trong NH3. Sau khi phản ứng xảy ra hoàn toàn thu được 87,2 gam kết tủa. Công thức phân tử của anđehit là:
-
A.
C3H3CHO
-
B.
C4H5CHO
-
C.
C3H5CHO.
-
D.
C4H3CHO
Đáp án : D
+) nAgNO3 = 3nX => X phải chứa liên kết ba C≡C– ở đầu mạch và có 1 nhóm CHO
Đặt CT của X là CH≡C–R–CHO
+) Lượng kết tủa bao gồm \(\left\{ \begin{array}{l}0,02{\rm{ }}mol{\rm{ }}AgC \equiv C-R-COON{H_4}\\0,04{\rm{ }}mol{\rm{ }}Ag\end{array} \right.\)
+) mkết tủa = 0,02.(194 + R) + 0,04.108
Có nAgNO3 = 0,6 mol = 3nX
Mà X đơn chức => X phải chứa liên kết ba C≡C– ở đầu mạch và có 1 nhóm CHO
Đặt CT của X là CH≡C–R–CHO
=> Lượng kết tủa bao gồm \(\left\{ \begin{array}{l}0,2{\rm{ }}mol{\rm{ }}AgC \equiv C-R-COON{H_4}\\0,4{\rm{ }}mol{\rm{ }}Ag\end{array} \right.\)
=> mkết tủa = 0,2.(194 + R) + 0,4.108 = 87,2 gam
=> R = 26 (C2H2)
=> X là C4H3CHO
Cho 0,04 mol một hỗn hợp X gồm CH2=CH-COOH, CH3COOH và CH2=CH-CHO phản ứng vừa đủ với dung dịch chứa 6,4 gam brom. Mặt khác, để trung hoà 0,04 mol X cần dùng vừa đủ 40 ml dung dịch NaOH 0,75 M. Khối lượng của CH2=CH-COOH trong X là
-
A.
0,56 gam.
-
B.
1,44 gam.
-
C.
0,72 gam.
-
D.
2,88 gam.
Đáp án : B
+) X phản ứng vừa đủ với 0,04 mol Br2 => nBr2 = nCH2=CH-COOH + 2.nCH2=CH-CHO
+) nNaOH = nCH2=CH-COOH + nCH3COOH
Gọi n CH2=CH-COOH = x mol; n CH3COOH = y mol và n CH2=CH-CHO = z mol
=> x + y + z = 0,04 (1)
X phản ứng vừa đủ với 0,04 mol Br2 => nBr2 = nCH2=CH-COOH + 2.nCH2=CH-CHO => x + 2z = 0,04 (2)
nNaOH = nCH2=CH-COOH + nCH3COOH => x + y = 0,03 mol (3)
Từ (1), (2) và (3) => x = 0,02; y = 0,01; z = 0,01
=> m CH2=CH-COOH = 0,02.72 = 1,44 gam
Trong phân tử axit cacboxylic X có số nguyên tử cacbon bằng số nhóm chức. Đốt cháy hoàn toàn một lượng X thu được số mol CO2 bằng số mol H2O. Tên gọi của X là
-
A.
axit axetic.
-
B.
axit malonic.
-
C.
axit oxalic.
-
D.
axit fomic.
Đáp án : D
+) nCO2 = nH2O => X có dạng CnH2nOz
Số nguyên tử C = số nhóm chức => số O trong X gấp đôi số C => X có dạng: CnH2nO2n
Vì đốt cháy X thu được nCO2 = nH2O => X có dạng CnH2nOz
Số nguyên tử C = số nhóm chức => số O trong X gấp đôi số C
=> X có dạng: CnH2nO2n
Với n = 1 => X là CH2O2 > X là axit fomic: HCOOH
Với n =2 => X là C2H4O4 (không thỏa mãn)
Đốt cháy hết a mol axit X được 2a mol CO2. Để trung hoà vừa hết a mol X cần 2a mol NaOH. Tìm X
-
A.
C2H4(COOH)2
-
B.
CH2(COOH)2
-
C.
CH3COOH
-
D.
(COOH)2
Đáp án : D
+) nCO2 / nX = 2
X tác dụng với NaOH theo tỉ lệ 1 : 2 => X chứa 2 nhóm –COOH
nCO2 / nX = 2 => X chứa 2 C
X tác dụng với NaOH theo tỉ lệ 1 : 2 => X chứa 2 nhóm –COOH
=> X là HOOC-COOH
Hấp thụ hoàn toàn V lít CO2 vào dung dịch Ca(OH)2, thu được 25 gam kết tủa và dung dịch X. Thêm tối thiểu 200 ml dung dịch NaOH 1M vào X, thì được lượng kết tủa lớn nhất. Tính V
-
A.
10,08
-
B.
14,56
-
C.
7,84
-
D.
12,32
Đáp án : B
+) Chú ý lượng NaOH tối thiểu => sinh ra muối NaHCO3, nếu lượng NaOH tối đa sinh ra muối Na2CO3
+) Bảo toàn C => nCO2 = 2nCa(HCO3)2 + nCaCO3
Chú ý lượng NaOH tối thiểu => sinh ra muối NaHCO3, nếu lượng NaOH tối đa sinh ra muối Na2CO3
Ca(HCO3)2 + NaOH → CaCO3↓ + NaHCO3 + H2O
0,2 ← 0,2
nCaCO3 = 0,25mol
Bảo toàn C => nCO2 = 2nCa(HCO3)2 + nCaCO3 = 0,2 . 2 + 0,25 = 0,65mol
=> V = 14,56 lít
X là hỗn hợp gồm HOOC-COOH, OHC-COOH, OHC-C≡C-CHO, OHC-C≡C-COOH; Y là axit cacboxylic no, đơn chức, mạch hở. Đun nóng m gam X với lượng dư dung dịch AgNO3 trong NH3, thu được 23,76 gam Ag. Nếu cho m gam X tác dụng với NaHCO3 dư thì thu được 0,07 mol CO2. Đốt cháy hoàn toàn hỗn hợp gồm m gam X và m gam Y cần 0,805 mol O2, thu được 0,785 mol CO2. Giá trị của m là
-
A.
8,8.
-
B.
4,6.
-
C.
6,0.
7,4.
-
D.
7,4.
Đáp án : A
+) Gọi số mol 4 chất trong X lần lượt là : a, b, c, d
+) nCHO = 0,22 = 2b + 4c + 2d => b + 2c + d = 0,11
+) nCO2 = nCOOH = 2a + b + d = 0,07
+) a + b + c + d = 0,09 mol = nX = 2nH
Khi đốt cháy do Y no đơn hở => nCO2 = nH2O = y mol
Bảo toàn khối lượng cho phản ứng cháy : 2.(12x + 0,18 + 0,25.16) + 0,805.32 = 0,785.44 + 18.(0,09 + y)
Gọi số mol C trong X là x và số mol C trong Y là y
Ta có : nCO2 = x + y = 0,785 mol
Gọi số mol 4 chất trong X lần lượt là : a, b, c, d
nAg = 0,22 mol => nCHO = 0,22. = 2b + 4c + 2d => b + 2c + d = 0,11
Lại có : nCO2 = nCOOH = 2a + b + d = 0,07
=> a + b + c + d = 0,09 mol = nX = 2nH
=> Trong X có : x mol C ; 0,18 mol H ; 0,25 mol O
Khi đốt cháy do Y no đơn hở => nCO2 = nH2O = y mol
Bảo toàn khối lượng cho phản ứng cháy :
2.(12x + 0,18 + 0,25.16) + 0,805.32 = 0,785.44 + 18.( 0,09 + y)
=> 24x – 18y = 2,04g
=> x = 0,385 mol ; y = 0,4 mol
=> m = 8,8 gam
Dung dịch HCl và CH3COOH có cùng nồng độ. pH của hai dung dịch này tương ứng là x và y. Cứ 100 phân tử CH3COOH thì có 1 phân tử phân li. Quan hệ giữa x và y là:
-
A.
y = 100x
-
B.
y = 2x
-
C.
y = x – 2
-
D.
y = x + 2
Đáp án : D
+) Với HCl điện li hoàn toàn => [H+] = a
+) Với CH3COOH điện li yếu => [H+] = 0,01a
+) Sử dụng công thức: pH = -log[H+]
Đặt a là nồng độ mol/l của 2 axit
Với HCl điện li hoàn toàn => [H+] = a
=> pH = x = -log[H+] = -log(a)
Với CH3COOH điện li yếu, 100 phân tử CH3COOH mới có 1 phân tử phân li => [H+] = 0,01a
=> pH = y = -log[H+] = -log(0,01a) = 2 – log(a) = 2 + x
Vậy y = x + 2
Nhiệt phân hoàn toàn hỗn hợp BaCO3, MgCO3, Al2O3 được rắn X và khí Y. Hoà tan rắn X vào nước thu được kết tủa E và dung dịch Z. Sục khí Y dư vào dung dịch Z thấy xuất hiện kết tủa F, hoà tan E vào dung dịch NaOH dư thấy tan một phần được dung dịch G. Các chất trong dung dịch G và kết tủa F là
-
A.
NaOH và Al(OH)3.
-
B.
NaOH, NaAlO2 và Al(OH)3.
-
C.
NaAlO2 và BaCO3.
-
D.
Ba(OH)2, NaOH và BaCO3.
Đáp án : B
Dựa vào các phản ứng hóa học => xác định sản phẩm sau phản ứng
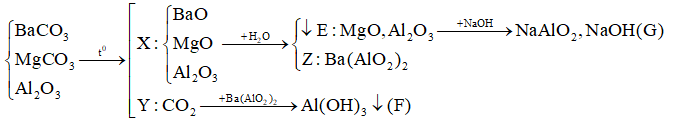
(Vì E tan 1 phần trong kiềm => trong E chứa Al2O3 còn dư => dung dịch Z không còn Ba(OH)2
















