40 bài tập lý thuyết về Hạt nhân nguyên tử, nguyên tố hóa học, đồng vị có lời giải (phần 1)
Làm đề thiCâu hỏi 1 :
Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là:
- A electron và proton.
- B notron và electron.
- C notron và proton.
- D electron, proton và notron.
Đáp án: C
Lời giải chi tiết:
Hầu hết các nguyên tử được cấu tạo từ các hạt: electron, proton và notron.
Đáp án C
Câu hỏi 2 :
Nguyên tố hoá học là những nguyên tử có cùng:
- A số khối.
- B số notron.
- C số proton.
- D số notron và số proton.
Đáp án: C
Lời giải chi tiết:
Nguyên tố hóa học là tập hợp những nguyên tử có cùng số proton.
Đáp án C
Câu hỏi 3 :
Đồng vị là hiện tượng các nguyên tố:
- A Có cùng số proton và khác số notron.
- B Có cùng số notron và khác số proton.
- C Có cùng số proton và cùng số notron.
- D Khác số protron và khác số notron.
Đáp án: A
Lời giải chi tiết:
Đồng vị là tập hợp những nguyên tử có cùng số proton nhưng khác nhau về số notron.
Đáp án A
Câu hỏi 4 :
Nguyên tố Na được kí hiệu: \({}_{11}^{23}Na\). Số p, n, e trong nguyên tử Na lần lượt là:
- A 11, 23, 11.
- B 11, 12, 11.
- C 12, 11, 12.
- D 12, 23, 12.
Đáp án: B
Lời giải chi tiết:
p = e = 11
n = A - p = 12
Đáp án B
Câu hỏi 5 :
Nhận định nào sau đây là đúng khi nói về 3 nguyên tử 2613X, 5526Y, 2612Z:
- A X và Z có cùng số khối.
- B X và Z là hai đồng vị của cùng một nguyên tố hoá học.
- C X và Y thuộc cùng một nguyên tố hoá học.
- D X và Y có cùng số notron.
Đáp án: A
Lời giải chi tiết:
B Sai vì đồng vị phải cùng số proton.
C Sai vì cùng 1 nguyên tố hóa học thì số proton phải bằng nhau.
D Sai vì nX = 13 còn nY = 29.
=>A
Câu hỏi 6 :
Cacbon có 2 đồng vị 12C và 13C. Oxi có 3 đồng vị 16O ; 17O ; 18O. Số loại phân tử CO2 có tạo thành là
- A 12
- B 10
- C 8
- D 6
Đáp án: A
Phương pháp giải:
Ghép từng đồng vị để tạo thành phân tử CO2
Lời giải chi tiết:
Các loại phân tửa CO2 có thể tạo ra là:
12C 16O16O ; 12C 17O17O; 12C 8O18O; 12C 16O17O; 12C 16O18O; 12C 17O18O
13C 16O16O ; 13C 17O17O; 13C 18O18O; 13C 16O17O; 13C 16O18O; 13C 17O18O
Đáp án A
Câu hỏi 7 :
Cho ba nguyên tử có kí hiệu là 24Mg, 25Mg, 26Mg. Phát biểu nào sau đây là sai ?
- A Nguyên tố Mg có 3 đồng vị.
- B Số hạt electron của các nguyên tử lần lượt là: 12, 13, 14
- C Ba nguyên tử trên đều thuộc nguyên tố Mg.
- D Hạt nhân của mỗi nguyên tử đều có 12 proton.
Đáp án: B
Lời giải chi tiết:
Đáp án B
Số electron = số proton = 12
Câu hỏi 8 :
Điều khẳng định nào sau đây là sai ?
- A Hạt nhân nguyên tử được cấu tạo nên bởi các hạt proton, electron, nơtron.
- B Trong nguyên tử số hạt proton bằng số hạt electron.
- C Số khối A bằng tổng số proton (Z) và tổng số nơtron (N).
- D Nguyên tử được cấu tạo nên bởi các hạt proton, electron, nơtron.
Đáp án: A
Lời giải chi tiết:
Đáp án A
Hạt nhân nguyên tử chỉ được tạo thành từ proton và notron
Câu hỏi 9 :
Có các đồng vị sau 1H, 2H, 35Cl, 37Cl . Có thể tạo ra số phân tử hidroclorua HCl là:
- A 2
- B 5
- C 3
- D 4
Đáp án: D
Lời giải chi tiết:
Đáp án D
Có 2.2 = 4 cặp H-Cl
Câu hỏi 10 :
Số khối của nguyên tử bằng tổng:
- A số n và e
- B số p và e
- C tổng số n, e, p.
- D số p và n
Đáp án: D
Lời giải chi tiết:
Đáp án D
Câu hỏi 11 :
Oxi có 3 đồng vị 16O, 17O, 18O và Cacbon có 2 đồng vị 12C, 13C . Hãy viết công thức các loại phân tử cacbonđioxit (CO2)
Lời giải chi tiết:
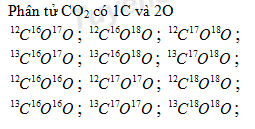
Câu hỏi 12 :
Nguyên tố cacbon và oxi có các đồng vị sau: 12C, 14C ; 16O; 17O; 18O. Số phân tử CO2 tối đa tạo từ các đồng vị trên là:
- A 9.
- B 8.
- C 18.
- D 12.
Đáp án: D
Lời giải chi tiết:
Đáp án D
O = C = O
=> Có 2 cách chọn C và 6 cách chọn O2
=> Số cách chọn CO2 = 2.6 = 12
Câu hỏi 13 :
Cho các nguyên tử có kí hiệu sau: 1326X ; 2655Y ; 1226T. Nhận định nào sau đây đúng khi nói về 3 nguyên tử trên:
- A X, Y thuộc cùng một nguyên tố hoá học
- B X, T là 2 đồng vị của cùng một nguyên tố hoá học
- C X và T có cùng số khối
- D X và Y có cùng số nơtron
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 14 :
Hạt mạng điện trong hạt nhân nguyên tử là:
- A electron
- B proton
- C nơtron
- D nơtron và electron
Đáp án: B
Lời giải chi tiết:
Hạt mạng điện trong hạt nhân nguyên tử là: proton
Electron cũng mang điện nhưng không ở hạt nhân
Đáp án B
Câu hỏi 15 :
Một nguyên tố X có 11electron và 12 nơtron. Nguyên tố X có kí hiệu nguyên tử là:
- A
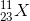
- B
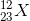
- C
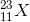
- D
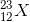
Đáp án: C
Lời giải chi tiết:
X có số khối là 12 + 11 =23 (đvC)
Vậy X có kí hiệu là 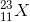
Đáp án C
Câu hỏi 16 :
Hiđro có 3 đồng vị là \({}_1^1H,\,{}_1^2H,\,{}_1^3H\); Oxi có 3 đồng vị là \({}_8^{16}O,{}_8^{17}O,{}_8^{18}O\). Trong tự nhiên, loại phân tử nước có phân tử khối nhỏ nhất là:
- A 18 u
- B 19u
- C 17u
- D 20u
Đáp án: A
Lời giải chi tiết:
Nước có ptk nhỏ nhất tạo bởi 2 và 1 có ptk là 18u
Đáp án A
Câu hỏi 17 :
Một nguyên tố X có 12 electron và 12 nơtron. Nguyên tố X có kí hiệu nguyên tử là:
- A
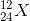
- B
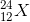
- C
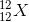
- D
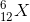
Đáp án: B
Lời giải chi tiết:
Nguyên tố X có kí hiệu nguyên tử là 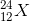
Đáp án B
Câu hỏi 18 :
Hạt không mạng điện trong nhân nguyên tử là:
- A electron
- B proton
- C nơtron
- D nơtron và electron
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 19 :
Cấu hình e của nguyên tố X: 1s22s22p3 số hiệu nguyên tử của X là
- A 2
- B 4
- C 7
- D 9
Đáp án: C
Lời giải chi tiết:
X có 7 e nên X có số hiệu nguyên tử là 7
Đáp án C
Câu hỏi 20 :
Một nguyên tố X có 13 electron và 14 nơtron. Nguyên tố X có kí hiệu nguyên tử là:
- A
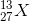
- B
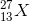
- C
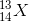
- D
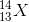
Đáp án: B
Lời giải chi tiết:
Nguyên tố X có kí hiệu nguyên tử 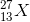
Đáp án B
Câu hỏi 21 :
Số hiệu nguyên tử (Z) của nguyên tố trong bảng hệ thống tuần hoàn bằng:
- A số proton
- B số nơtron
- C số khối
- D tổng số proton và electron
Đáp án: A
Lời giải chi tiết:
đáp án A
Câu hỏi 22 :
Cấu hình e của nguyên tố X: 1s22s22p4 số hiệu nguyên tử của X là:
- A 4
- B 8
- C 7
- D 9
Đáp án: B
Lời giải chi tiết:
X có 8 e nên X có 8 proton nên số hiệu nguyên tử của X là 8
Đáp án B
Câu hỏi 23 :
Hạt nhân của hầu hết các nguyên tử do các loại hạt sau cấu tạo nên
- A electron, proton và nơ tron
- B electron và nơtron
- C proton và nơtron
- D electron và proton
Đáp án: C
Lời giải chi tiết:
Đáp án C
Câu hỏi 24 :
Một nguyên tố X có 11 electron và 12 nơtron. Nguyên tố X có kí hiệu nguyên tử là:
- A 23X11
- B 11X23
- C 11X12
- D 12X11
Đáp án: B
Lời giải chi tiết:
Đáp án B
ZXA : Z = số E và A = số P + số N = Số E + số N = 11 + 12 = 23
=> 23X11
Câu hỏi 25 :
Nguyên tử 13Al27 có:
- A 13p, 13e, 14n
- B 13p, 14e, 14n
- C 13p, 13e, 13n
- D 14p, 14e, 13n
Đáp án: A
Lời giải chi tiết:
Đáp án A
ZXA : Z = số E và A = số P + số N = Số E + số N
=> Số e = 13 = số p : A = 27 = Số E + số N
=> Số n = 27 – 13 = 14
Câu hỏi 26 :
Nguyên tử canxi có kí hiệu là \({}_{20}^{40}Ca\). Phát biểu nào sau đây sai?
- A Nguyên tử Ca có 2 electron lớp ngoài cùng.
- B Số hiệu nguyên tử của Ca là 20.
- C Nguyên tử Ca có số p = số e = 20.
- D Nguyên tử Ca trung hòa về điện vì có số n = số p = 20.
Đáp án: D
Lời giải chi tiết:
Nguyên tử trung hòa về điện vì có số hạt mang điện âm (số e) bằng số hạt mang điện dương (số p).
Đáp án D
Câu hỏi 27 :
Chọn câu phát biểu không đúng
- A Số khối bằng tổng số hạt p và n.
- B Tổng số p và e được gọi là số khối.
- C Trong 1 nguyên tử, số p = số e = điện tích hạt nhân.
- D Số p bằng số e.
Đáp án: B
Lời giải chi tiết:
Sai vì : Số khối bằng tổng số hạt p và n
Đáp án B
Câu hỏi 28 :
Cacbon có 2 đồng vị, chúng khác nhau về:
- A Cấu hình electron
- B Số khối
- C Số hiệu nguyên tử
- D Số proton
Đáp án: B
Lời giải chi tiết:
Đáp án B
Các đồng vị của cùng một nguyên tố là những nguyên tử có cùng số proton nhưng khác nhau về số notron, do đó có số khối A khác nhau.
Câu hỏi 29 :
Kí hiệu hóa học biểu thị đầy đủ đặc trưng cho nguyên tử của nguyên tố hóa học vì nó cho biết:
- A số A và số hiệu nguyên tử Z
- B số electron và số p
- C nguyên tử khối của nguyên tử
- D Số hiệu nguyên tử
Đáp án: A
Lời giải chi tiết:
Đáp án A.
Câu hỏi 30 :
Cho 3 nguyên tử \({}_{12}^{24}Mg\); \({}_{12}^{25}Mg\); \({}_{12}^{26}Mg\). Phát biểu nào sau đây sai?
- A Đây là 3 đồng vị
- B Ba nguyên tử trên thuộc nguyên tố Mg
- C Số proton mỗi nguyên tử đều là 12
- D Số electron của các nguyên tử lần lượt là 12,13,14
Đáp án: D
Lời giải chi tiết:
Đáp án D
Sai là do: Số n của các nguyên tử lần lượt là 12,13,14 chứ không phải số e.
Câu hỏi 31 :
Trong nguyên tử \({}_{37}^{86}Rb\)có tổng số hạt là:
- A 49
- B 37
- C 123
- D 86
Đáp án: C
Lời giải chi tiết:
Đáp án C
Tổng số hạt = P + E + N = Z +A = 86 + 37 = 123
Câu hỏi 32 :
Nhận định nào sau đây không đúng?
- A Các đồng vị có cùng điện tích hạt nhân.
- B Các đồng vị có số electron khác nhau.
- C Các đồng vị có số khối khác nhau.
- D Các đồng vị có số nơtron khác nhau.
Đáp án: B
Phương pháp giải:
Dựa vào khái niệm về đồng vị: Đồng vị là các nguyên tử có cùng số p nhưng khác nhau về số n.
Lời giải chi tiết:
Đồng vị là các nguyên tử có cùng số p nhưng khác nhau về số n.
A. Đ vì có cùng số p
B. S vì có cùng số e
C. Đ vì số n khác nhau, số p giống nhau => A khác nhau
D. Đ
Đáp án B
Câu hỏi 33 :
Nguyên tử Na, Mg, F lần lượt có số hiệu nguyên tử là 11, 12, 9. Các ion Na+, Mg2+, F- khác nhau về
- A số electron lớp ngoài cùng.
- B số electron.
- C số lớp electron.
- D số proton.
Đáp án: D
Lời giải chi tiết:
Những ion thuộc những nguyên tố khác nhau thì có số p khác nhau
Đáp án D
Câu hỏi 34 :
Số electron và số nơtron của nguyên tử \({}_{15}^{31}P\) lần lượt là
- A 15 và 31
- B 15 và 15
- C 16 và 15
- D 15 và 16
Đáp án: D
Lời giải chi tiết:
Z = p = e = 15
A = p + n = 31 => n = 31 – 15 = 16
Đáp án D
Câu hỏi 35 :
Nguyên tử nào sau đây là đồng vị của \({}_{17}^{35}X\)
- A \({}_{17}^{37}Y\)
- B \({}_{16}^{32}Z\)
- C \({}_{14}^{28}T\)
- D \({}_{15}^{31}M\)
Đáp án: A
Phương pháp giải:
Dựa vào khái niệm đồng vị:
Đồng vị là những nguyên tử có cùng số proton nhưng khác nhau về số notron (tức là chúng có cùng Z và khác A).
Lời giải chi tiết:
Đồng vị của \({}_{17}^{35}X\) là \({}_{17}^{37}Y\)
Đáp án A
Câu hỏi 36 :
Cacbon có 2 đồng vị: 12C và 13C. Oxi có 3 đồng vị: 16O, 17O, 18O. Số phân tử CO khác nhau được tạo nên từ các đồng vị trên là
- A 4
- B 6
- C 10
- D 12
Đáp án: B
Lời giải chi tiết:
Các phân tử CO khác nhau được tạo nên từ các đồng vị trên là:
12C16O 12C16O
12C17O 12C17O
12C18O 12C18O
Đáp án B
Câu hỏi 37 :
Phát biểu nào sau đây là không đúng?
- A Đồng vị là những nguyên tố có cùng số proton nhưng khác số notron.
- B Những electron ở lớp K có mức năng lượng thấp nhất.
- C Đặc trưng cơ bản của nguyên tử là số đơn vị điện tích hạt nhân và số khối.
- D Các electron trên cùng một phân lớp có mức năng lượng bằng nhau.
Đáp án: A
Lời giải chi tiết:
A sai vì đồng vị là những nguyên tử có cùng số proton nhưng khác số notron.
Đáp án A
Câu hỏi 38 :
Số nơtron, electron trong ion \({}_{48}^{112}C{d^{2 + }}\) lần lượt là
- A 64, 48
- B 64, 46
- C 64, 50
- D 46, 48
Đáp án: B
Phương pháp giải:
Nguyên tử trung hòa X được kí hiệu: \({}_Z^AX\)
Số p = số e = Z
Số n = A – Z
Lời giải chi tiết:
\({}_{48}^{112}C{d^{2 + }}\)
Z = 48
A = 112
Số n: N = A – Z = 112 – 48 = 64
Vì Cd nhường 2e để thành Cd2+ nên số e là 48 – 2 = 46
Đáp án B
Câu hỏi 39 :
Nguyên tử kali có 19 proton, 19 electron và 20 nơtron. Số khối của nguyên tử kali là
- A 20
- B 39
- C 38
- D 19
Đáp án: B
Phương pháp giải:
Số khối A = Z + N (với Z là số p hay e; N là số n)
Lời giải chi tiết:
Số khối A = Z + N = 19 + 20 = 39
Đáp án B
Câu hỏi 40 :
Sắp xếp các nguyên tử sau theo thứ tự tăng dần số nơtron: \({}_{11}^{23}Na\)(1); \({}_6^{13}C\) (2); \({}_9^{19}F\)(3); \({}_{17}^{38}Cl\)(4)
- A 1,2,3,4
- B 3,2,1,4
- C 2,3,1,4
- D 4,3,2,1
Đáp án: C
Lời giải chi tiết:
Đáp án C
A = Z + N
=> N C = 13 – 6 = 7
=> N F = 19 – 9 = 10
=> N Na = 23 – 11 = 12
=> N Cl = 38 – 17 = 21
Các bài khác cùng chuyên mục
- 20 câu hỏi cân bằng phản ứng OXH - Khử mức độ vận dụng, vận dụng cao có lời giải
- 50 câu hỏi ôn tập về bảng tuần hoàn các nguyên tố và định luật tuần hoàn có lời giải
- 40 câu hỏi lý thuyết về axit sunfuric - muối sunfat có lời giải (phần 1)
- 30 bài tập thông hiểu về cấu hình electron có lời giải (phần 1)
- 20 bài tập vận dụng về cấu hình electron có lời giải
- 20 câu hỏi cân bằng phản ứng OXH - Khử mức độ vận dụng, vận dụng cao có lời giải
- 50 câu hỏi ôn tập về bảng tuần hoàn các nguyên tố và định luật tuần hoàn có lời giải
- 40 câu hỏi lý thuyết về axit sunfuric - muối sunfat có lời giải (phần 1)
- 30 bài tập thông hiểu về cấu hình electron có lời giải (phần 1)
- 20 bài tập vận dụng về cấu hình electron có lời giải

















