Đề thi giữa kì 2 Hóa 12 - Đề số 3
Đề bài
Cấu hình electron của Ni (Z = 28) là
-
A.
[Ar]3d84s2
-
B.
[Ar]3d74s8.
-
C.
[Ar]3d54s5
-
D.
[Ar]3d94s1
Đốt cháy hoàn toàn bột crom trong oxi (dư) thu được 4,56 gam một oxit (duy nhất). Khối lượng crom bị đốt cháy là
-
A.
0,78 gam
-
B.
3,12 gam
-
C.
1,74 gam
-
D.
1,19 gam
Điện phân một dung dịch gồm a mol CuSO4 và b mol NaCl. Nếu b > 2a mà ở catot chưa có khí thoát ra thì dung dịch sau điện phân chứa
-
A.
Na+, SO42-, Cl-.
-
B.
Na+, SO42-, Cu2+.
-
C.
Na+, Cl-.
-
D.
Na+, SO42-, Cu2+, Cl-.
Các kim loại nào sau đây luôn được bảo vệ trong môi trường không khí, nước nhờ lớp màng oxit?
-
A.
Al và Ca.
-
B.
Fe và Cr.
-
C.
Cr và Al
-
D.
Fe và Mg.
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
-
A.
2,58 gam
-
B.
2,22 gam
-
C.
2,31 gam
-
D.
2,44 gam
So với nguyên tử canxi, nguyên tử kali có
-
A.
bán kính lớn hơn và độ âm điện lớn hơn
-
B.
bán kính lớn hơn và độ âm điện nhỏ hơn
-
C.
bán kính nhỏ hơn và độ âm điện nhỏ hơn
-
D.
bán kính nhỏ hơn và độ âm điện lớn hơn
Dùng m gam Al để khử hết 1,6 gam Fe2O3 đến khi phản ứng hoàn toàn, sản phẩm sau phản ứng tác dụng với lượng dư dung dịch NaOH tạo 0,672 lít khí (đktc). Tính m?
-
A.
1,080 gam
-
B.
0,810 gam
-
C.
0,540 gam
-
D.
1,755 gam
Hoà tan hoàn toàn 3 kim loại Zn, Fe, Cu bằng dung dịch HNO3 loãng. Sau khi phản ứng xảy ra hoàn toàn, thu được chất rắn không tan là Cu. Các chất tan có trong dung dịch sau phản ứng là
-
A.
Zn(NO3)2; Fe(NO3)3.
-
B.
Zn(NO3)2; Fe(NO3)2.
-
C.
Zn(NO3)2; Fe(NO3)3; Cu(NO3)2.
-
D.
Zn(NO3)2; Fe(NO3)2; Cu(NO3)2.
Để hoàn tan hoàn toàn 9,6 gam Cu cần dùng 500 ml dung dịch HNO3 (lấy dư 25% so với lượng cần thiết), thu được khí NO duy nhất. Nồng độ mol của dung dịch HNO3 đã dùng là
-
A.
3,0M.
-
B.
2,0M.
-
C.
1,0M.
-
D.
2,5M.
Hỗn hợp X chứa một oxit sắt; 0,02 mol Cr2O3 và 0,04 mol Al. Thực hiện phản ứng nhiệt nhôm hỗn hợp X sau một thời gian thu được hỗn hợp chất rắn Y. Chia Y thành 2 phần bằng nhau. Phần 1 tác dụng với H2SO4 đặc, nóng dư thu được 0,896 lít SO2 (đktc, sản phẩm khử duy nhất). Phần 2 tác dụng vừa đủ với 250 ml dung dịch HCl 1M thu được dung dịch Z và 0,336 lít khí H2 (đktc). Dung dịch Z tác dụng tối đa với z mol NaOH thu được 6,6 gam hỗn hợp kết tủa. Biết các phản ứng xảy ra trong môi trường không có oxi. Giá trị của z gần nhất với
-
A.
0,25
-
B.
0,32
-
C.
0,23
-
D.
0,27
Khi điện phân điện cực trơ có màng ngăn dung dịch hỗn hợp gồm NaCl và CuSO4 đến khi NaCl và CuSO4 đều hết nếu dung dịch sau điện phân hoà tan được Fe và sinh khí thì dung dịch sau điện phân chắc chắn chứa
-
A.
CuCl2
-
B.
CuSO4
-
C.
HCl, CuSO4
-
D.
H2SO4
Cho Al đến dư vào dung dịch gồm NO3-, Cu2+, Fe3+, Ag+. Số phản ứng xảy ra (không kể phản ứng của Al với H2O) là
-
A.
4
-
B.
2
-
C.
5
-
D.
3
Cho hỗn hợp bột gồm 0,56 gam Fe và 0,65 gam Zn vào V ml dung dịch AgNO3 0,1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được chất rắn có khối lượng tăng 2,31 gam so với ban đầu. Giá trị của V là
-
A.
0,25.
-
B.
250.
-
C.
300.
-
D.
200.
X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y lần lượt là (biết thứ tự trong dãy điện hoá : Fe3+/Fe2+ đứng trước Ag+/Ag)
-
A.
Ag, Mg.
-
B.
Cu, Fe.
-
C.
Fe, Cu.
-
D.
Mg, Ag.
lon Mg2+ bị khử trong trường hợp
-
A.
Điện phân dung dịch MgCl2.
-
B.
Điện phân MgCl2 nóng chảy.
-
C.
Thả Na vào dung dịch MgCl2.
-
D.
Cho dd MgCl2 tác dụng dd Na2CO3.
Chọn X, Y, Z, T, E theo đúng trật tự tương ứng sơ đồ sau : X → Y → Z → T → E
-
A.
AlCl3; Al(OH)3; NaAlO2; Al2O3; Al2(SO4)3
-
B.
AlCl3; NaAlO2; Al2O3; Al(OH)3; Al2(SO4)3
-
C.
Al(OH)3; AlCl3; Al2O3; NaAlO2; Al2(SO4)3
-
D.
AlCl3; NaAlO2; Al(OH)3; Al2O3; Al2(SO4)3
Chọn phát biểu sai:
-
A.
Cr2O3 là chất rắn màu lục thẫm.
-
B.
Cr(OH)3 là chất rắn màu lục xám.
-
C.
CrO3 là chất rắn màu đỏ thẫm.
-
D.
Cr(OH)2 là chất rắn màu trắng xanh.
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X có tỉ khối so với khí hiđro bằng 18,8. Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
-
A.
9,40 gam.
-
B.
11,28 gam.
-
C.
8,60 gam.
-
D.
47,00 gam.
Từ hai muối X và Y thực hiện các phản ứng sau:
X → X1 + CO2
X1 + H2O → X2
X2 + Y → X + Y1 + H 2O
X2 + 2Y → X + Y2 + H2O
Hai muối X, Y tương ứng là
-
A.
CaCO3, NaHSO4.
-
B.
BaCO3, Na2CO3.
-
C.
CaCO3, NaHCO3.
-
D.
MgCO3, NaHCO3.
Hòa tan 5,9 gam hỗn hợp X gồm K và Ca vào nước dư, sau phản ứng thu được 2,24 lít khí H2. Khối lượng Ca có trong hỗn hợp X là
-
A.
3,9 gam.
-
B.
2 gam.
-
C.
4,8 gam.
-
D.
4 gam.
Kim loại nào sau đây bị thụ động hóa với dung dịch axit sunfuric đặc nguội?
-
A.
Ag
-
B.
Cu
-
C.
Zn
-
D.
Fe
Cho m gam K tan hết vào 100 ml dung dịch gồm (H2SO4 1M và HCl 2M) thu được 5,6 lít khí H2 (ở đktc). Cô cạn dung dịch sau phản ứng khối lượng chất rắn thu được là
-
A.
32,3
-
B.
37,9 gam.
-
C.
24,95 gam.
-
D.
30,1gam.
Ion kim loại nào sau đây không bị Zn khử thành kim loại ?
-
A.
Cu2+
-
B.
Ag+
-
C.
Sn2+.
-
D.
Al3+.
Hỗn hợp bột X gồm BaCO3, Fe(OH)2, Al(OH)3, Fe2O3 . Nung X trong không khí đến khối lượng không đối được hỗn hợp rắn A. Cho A vào nước dư khuấy đều được dung dịch B chứa 2 chất tan và phần không tan C. Cho khí CO dư qua bình chứa C nung nóng được hỗn hợp rắn E (Cho các phản ứng xảy ra hoàn toàn). E có thể chứa tối đa sản phẩm là
-
A.
Fe, Al2O3
-
B.
Fe2O3, Al2O3
-
C.
Fe
-
D.
BaO, Fe, Al2O3
Cho lá Mg vào dung dịch HCl, có khí thoát ra. Thêm vài giọt X vào thì tốc độ thoát khí lớn hơn. X là?
-
A.
NaOH
-
B.
FeCl2
-
C.
BaCl2
-
D.
H2O
Khi cho mẫu Zn vào bình đựng dung dịch X, thì thấy khối lượng thanh Zn trong giảm đi (giả thiết kim loại sinh ra bám hết trên thanh Zn). Dung dịch X là:
-
A.
Cu(NO3)2.
-
B.
AgNO3.
-
C.
Ba(NO3)2.
-
D.
NaNO3.
Cho 12,04 gam hỗn hợp rắn X gồm Fe, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,42 mol HCl và 0,04 mol HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y (không chứa NH4+) và 0,045 mol hỗn hợp khí Z gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Y, sau phản ứng thấy thoát ra 0,0075 mol NO (sản phẩm khử duy nhất của N+5), đồng thời thu được 70,8 gam kết tủa. Phần trăm khối lượng Fe trong hỗn hợp X có giá trị gần nhấtvới giá trị nào sau đây?
-
A.
46,51%.
-
B.
37,8%.
-
C.
35,8%.
-
D.
49,6%.
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol Fe2(SO4)3 và z mol H2SO4, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
-
A.
x = y + z.
-
B.
2x = y + z.
-
C.
x = y – 2z.
-
D.
y = 2x.
Phản ứng của Fe với O2 như hình vẽ
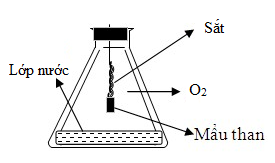
Cho các phát biểu sau đây:
(a) Vai trò của mẩu than để làm mồi cung cấp nhiệt cho phản ứng.
(b) Phản ứng tỏa nhiều nhiệt làm đầu dây sắt nóng chảy có thể thành cục tròn.
(c) Vai trò của lớp nước ở đáy bình là để tránh vỡ bình.
(d) Phản ứng cháy sáng, có các tia lửa bắn ra từ dây sắt.
Số phát biểu sai là
-
A.
2.
-
B.
0.
-
C.
1.
-
D.
3.
Hòa tan hết a mol FeCO3 vào dung dịch HCl (lấy dư 10% so với lượng cần dùng) thu được dung dịch X. Cho dung dịch AgNO3 dư vào dung dịch X thu được b gam kết tủa. Biết sản phẩm khử của N+5
là khí NO duy nhất, các phản ứng đều xảy ra hoàn toàn. Biểu thức về mối quan hệ giữa a và b là
-
A.
b = 315,7a
-
B.
b = 407,5a
-
C.
b = 287a
-
D.
b = 423,7b
Ở trạng thái cơ bản, nguyên tử Al (Z = 13) có số electron lớp ngoài cùng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Cho từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp x mol HNO3 và y mol Al(NO3)3, kết quả thí nghiệm được biểu diễn trên đồ thị sau
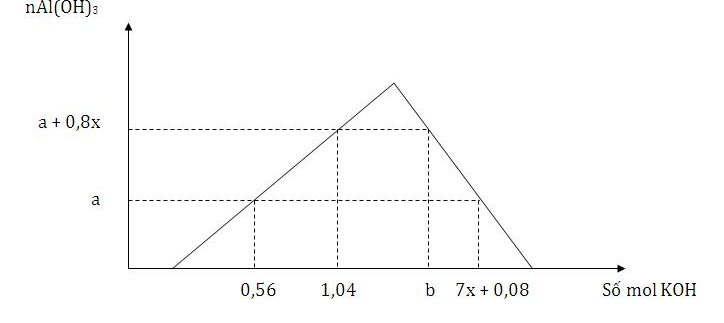
Tỉ lệ của b : a có giá trị là
-
A.
14
-
B.
13
-
C.
12
-
D.
11
Phương pháp thường được áp dụng để chống ăn mòn kim loại là
-
A.
Phương pháp bảo vệ bề mặt, phương pháp điện hóa.
-
B.
Phương pháp nhiệt luyện, thủy luyện.
-
C.
Phương pháp điện phân nóng chảy, điện phân dung dịch.
-
D.
Tất cả các phương pháp trên.
Đun 0,04 mol hỗn hợp gồm hơi nước và khí CO2 qua cacbon nung đỏ, thu được 0,07 mol hỗn hợp Y gồm CO, H2 và CO2. Cho Y đi qua ống đựng 20 gam hỗn hợp gồm Fe2O3 và CuO (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
-
A.
19,52.
-
B.
18,56.
-
C.
19,04.
-
D.
18,40.
Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước dư thu được dung dịch X. Điện phân dung dịch X với điện cực trơ đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối hơi so với H2 bằng 30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử hiệu suất của quá trình điện phân là 100%, khí sinh ra không tan trong dung dịch. Giá trị của m là
-
A.
48,25
-
B.
64,25
-
C.
62,25
-
D.
56,25
Khi nung hỗn hợp các chất Fe(NO3)2, Fe(OH)3 và FeCO3 trong không khí đến khối lượng không đổi, thu được một chất rắn là
-
A.
Fe3O4.
-
B.
FeO.
-
C.
Fe.
-
D.
Fe2O3.
Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 loãng ( dư),thu được dung dịch X. Trong các chất: NaOH, Cu, KNO3, KMnO4, BaCl2, Cl2, Al, NaCl, số chất có khả năng phản ứng được với dung dịch X là
-
A.
8
-
B.
6
-
C.
7
-
D.
5
Loại quặng sắt dùng để sản xuất gang thường chứa từ 30 - 95% oxit sắt và phải
-
A.
chứa nhiều photpho.
-
B.
chứa nhiều lưu huỳnh.
-
C.
chứa nhiều SiO2.
-
D.
chứa rất ít phot pho, lưu huỳnh.
Chất nào sau đây được dùng để làm mềm nước cứng vĩnh cửu?
-
A.
NaNO3.
-
B.
NaOH.
-
C.
H2SO4.
-
D.
Na2CO3.
Ở điều kiện thường, kim loại nào sau đây không tan được trong dung dịch NaOH?
-
A.
Na.
-
B.
K.
-
C.
Al.
-
D.
Fe.
Lời giải và đáp án
Cấu hình electron của Ni (Z = 28) là
-
A.
[Ar]3d84s2
-
B.
[Ar]3d74s8.
-
C.
[Ar]3d54s5
-
D.
[Ar]3d94s1
Đáp án : A
Xem lại lí thuyết một số kim loại khác
Cấu hình electron của Ni là [Ar]3d84s2
Đốt cháy hoàn toàn bột crom trong oxi (dư) thu được 4,56 gam một oxit (duy nhất). Khối lượng crom bị đốt cháy là
-
A.
0,78 gam
-
B.
3,12 gam
-
C.
1,74 gam
-
D.
1,19 gam
Đáp án : B
Cr tác dụng với O2 lên số oxi hóa +3
${n}_{C{{\text{r}}_{2}}{{\text{O}}_{3}}}=\frac{4,56}{152}=0,03(mol)$
4Cr + 3O2 → 2Cr2O3
0,06 0,03
=> mCr = 0,06.52 = 3,12 (g)
Điện phân một dung dịch gồm a mol CuSO4 và b mol NaCl. Nếu b > 2a mà ở catot chưa có khí thoát ra thì dung dịch sau điện phân chứa
-
A.
Na+, SO42-, Cl-.
-
B.
Na+, SO42-, Cu2+.
-
C.
Na+, Cl-.
-
D.
Na+, SO42-, Cu2+, Cl-.
Đáp án : D
xem lại lí thuyết điện phân hỗn hợp
Catot (-) Cu2+, Na+, H2O Anot (+) SO42- , Cl-, H2O
(1) Cu2+ + 2e → Cu (1) 2Cl- → Cl2 + 2e
a → 2a → a b → b/2 → b
Vì catot chưa có khí thoát ra và b>2a => Dung dịch sau điện phân chứa: Na+, SO42-, Cu2+, Cl-.
Các kim loại nào sau đây luôn được bảo vệ trong môi trường không khí, nước nhờ lớp màng oxit?
-
A.
Al và Ca.
-
B.
Fe và Cr.
-
C.
Cr và Al
-
D.
Fe và Mg.
Đáp án : C
Xem lại lí thuyết crom và hợp chất
Các kim loại luôn được bảo vệ trong môi trường không khí, nước nhờ lớp màng oxit là Al và Cr
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
-
A.
2,58 gam
-
B.
2,22 gam
-
C.
2,31 gam
-
D.
2,44 gam
Đáp án : C
+) nOH > 2nCO2=> OH‑ dư
=> nCO3 = nCO2 = 0,015 mol
Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -$2{n_{CO_3^{2 - }}}$
+) mrắn = mNa + mK + mCO3 + mOH dư
nCO2 = 0,015 mol; nOH = nNaOH + nKOH = 0,04 mol > 2nCO2
=> OH‑ dư
=> nCO3 = nCO2 = 0,015 mol
Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -$2{n_{CO_3^{2 - }}}$= 0,01 mol
=> mrắn = mNa + mK + mCO3 + mOH dư = 2,31 gam
So với nguyên tử canxi, nguyên tử kali có
-
A.
bán kính lớn hơn và độ âm điện lớn hơn
-
B.
bán kính lớn hơn và độ âm điện nhỏ hơn
-
C.
bán kính nhỏ hơn và độ âm điện nhỏ hơn
-
D.
bán kính nhỏ hơn và độ âm điện lớn hơn
Đáp án : B
Xem lại lí thuyết kim loại kiềm thổ
So với nguyên tử canxi, nguyên tử K có bán kính lớn hơn và độ âm điện nhỏ hơn
Dùng m gam Al để khử hết 1,6 gam Fe2O3 đến khi phản ứng hoàn toàn, sản phẩm sau phản ứng tác dụng với lượng dư dung dịch NaOH tạo 0,672 lít khí (đktc). Tính m?
-
A.
1,080 gam
-
B.
0,810 gam
-
C.
0,540 gam
-
D.
1,755 gam
Đáp án : A
${n_{Al}}$dư$ = \,\,\frac{2}{3}{n_{{H_2}}} = 0,02\,\,mol$
Fe2O3 + 2Al $\xrightarrow{{{t^o}}}$ 2Fe + Al2O3
0,01 → 0,02
→ mAl = m = (0,02 + 0,02).27 = 1,08 gam
${n_{F{e_2}{O_3}}} = 0,01\,\,mol;\,\,{n_{{H_2}}} = 0,03\,\,mol$
${n_{Al}}$dư$ = \,\,\frac{2}{3}{n_{{H_2}}} = 0,02\,\,mol$
Fe2O3 + 2Al $\xrightarrow{{{t^o}}}$ 2Fe + Al2O3
0,01 → 0,02
→ mAl = m = (0,02 + 0,02).27 = 1,08 gam
Hoà tan hoàn toàn 3 kim loại Zn, Fe, Cu bằng dung dịch HNO3 loãng. Sau khi phản ứng xảy ra hoàn toàn, thu được chất rắn không tan là Cu. Các chất tan có trong dung dịch sau phản ứng là
-
A.
Zn(NO3)2; Fe(NO3)3.
-
B.
Zn(NO3)2; Fe(NO3)2.
-
C.
Zn(NO3)2; Fe(NO3)3; Cu(NO3)2.
-
D.
Zn(NO3)2; Fe(NO3)2; Cu(NO3)2.
Đáp án : D
Sau phản ứng thu được chất rắn không tan là Cu → trong dung dịch không còn muối Fe(NO3)3
Để hoàn tan hoàn toàn 9,6 gam Cu cần dùng 500 ml dung dịch HNO3 (lấy dư 25% so với lượng cần thiết), thu được khí NO duy nhất. Nồng độ mol của dung dịch HNO3 đã dùng là
-
A.
3,0M.
-
B.
2,0M.
-
C.
1,0M.
-
D.
2,5M.
Đáp án : C
Bảo toàn e: 2nCu = 3nNO
+) nHNO3 phản ứng = 4nNO
+) HNO3 lấy dư 25% => nHNO3 ban đầu = 0,4.1,25
nCu = 0,15 mol
Bảo toàn e: 2nCu = 3nNO => nNO = 0,1 mol
=> nHNO3 phản ứng = 4nNO = 4.0,1 = 0,4 mol
HNO3 lấy dư 25% => nHNO3 ban đầu = 0,4.1,25 = 0,5 mol
=> CM HNO3 = 0,5 / 0,5 = 1M
Hỗn hợp X chứa một oxit sắt; 0,02 mol Cr2O3 và 0,04 mol Al. Thực hiện phản ứng nhiệt nhôm hỗn hợp X sau một thời gian thu được hỗn hợp chất rắn Y. Chia Y thành 2 phần bằng nhau. Phần 1 tác dụng với H2SO4 đặc, nóng dư thu được 0,896 lít SO2 (đktc, sản phẩm khử duy nhất). Phần 2 tác dụng vừa đủ với 250 ml dung dịch HCl 1M thu được dung dịch Z và 0,336 lít khí H2 (đktc). Dung dịch Z tác dụng tối đa với z mol NaOH thu được 6,6 gam hỗn hợp kết tủa. Biết các phản ứng xảy ra trong môi trường không có oxi. Giá trị của z gần nhất với
-
A.
0,25
-
B.
0,32
-
C.
0,23
-
D.
0,27
Đáp án : D
Phần 1 : H2SO4 nhận e, Al và FexOy cho e
Bảo toàn e : 2.nSO2 = 3nAl + ne cho oxit sắt => ne cho oxit sắt = 2.0,04 – 0,02.3 = 0,02
Ta thấy : nếu oxit sắt là FeO thì nFeO = ne cho oxit sắt
Nếu oxit sắt là Fe2O3 thì không cho e
Nếu oxit sắt là Fe3O4 thì nFe3O4 = ne cho oxit sắt => nFexOy = 0,02 mol
Phần 2 :
Bảo toàn nguyên tố H : ${{n}_{HCl}}=2{{n}_{{{H}_{2}}}}+2{{n}_{{{H}_{2}}O}}\to \,\,{{n}_{{{H}_{2}}O}}=\frac{0,25-2.0,015}{2}=0,11\,\,mol$
Bảo toàn nguyên tố O : nO trong oxit sắt + $3{{n}_{C{{\text{r}}_{2}}{{O}_{3}}}}={{n}_{{{H}_{2}}O}}$=> nO trong oxit sắt = 0,11 – 3.0,01 = 0,08 mol
=> y = $\frac{{{n}_{O\,\,trong\,\text{ox}it}}}{{{n}_{F{{e}_{x}}{{O}_{y}}}}}=\frac{0,08}{0,02}=4$ → oxit sắt là Fe3O4
Vì dung dịch Z phản ứng tối đa với NaOH nên kết tủa Al(OH)3 và Cr(OH)3 đều tan hết
→ dung dịch tạo thành chứa :
$N{{a}^{+}}\,\,(z\text{ }mol);\text{ }C{{l}^{-}}\,\,(0,25\,\,mol);\text{ }AlO_{2}^{-}\text{ (0,02}\,\,\text{mol); }CrO_{2}^{-}\text{ (a}\,\,\text{mol)}$
Bảo toàn điện tích : z = 0,25 + 0,02 + a (1)
Bảo toàn Cr : $2{{n}_{C{{\text{r}}_{2}}{{O}_{3}}}}={{n}_{C\text{r}O_{2}^{-}}}+{{n}_{\text{Cr}{{(OH)}_{2}}}}\to {{n}_{C\text{r}{{(OH)}_{2}}}}=2.0,01-a=0,02-a$
Bảo toàn Fe : nFe trong kết tủa = 3.nFe3O4 = 0,06
=> mkết tủa = mCr + mFe + mOH → mOH = 6,6 – 52.(0,02 – a) – 0,06.56 = 2,2 +52a
$=>\,\,{{n}_{OH}}=\frac{2,2+52a}{17}\,\,mol$
=> nNaOH = nOH trong kết tủa + 4.nAl(OH)3 + 4.nCr(OH)3 => z $=\frac{2,2+52a}{17}\,+\text{ }4.0,02\text{ }+\text{ }4a\text{ }\left( 2 \right)$
Giải hệ (1), (2) → z = 0,28; a = 0,01
Khi điện phân điện cực trơ có màng ngăn dung dịch hỗn hợp gồm NaCl và CuSO4 đến khi NaCl và CuSO4 đều hết nếu dung dịch sau điện phân hoà tan được Fe và sinh khí thì dung dịch sau điện phân chắc chắn chứa
-
A.
CuCl2
-
B.
CuSO4
-
C.
HCl, CuSO4
-
D.
H2SO4
Đáp án : D
Ta thấy khi điện phân hết NaCl và CuSO4 thì chỉ có Cu2+ và Cl- bị điện phân hết tạo Cu và Cl2 .Mà dung dịch sau điện phân hòa tan được Fe và sinh khí => dung dịch sau điện phân chứa axit
=> dung dịch chắc chắn chứa H2SO4 (vì SO42- không bị điện phân)
Cho Al đến dư vào dung dịch gồm NO3-, Cu2+, Fe3+, Ag+. Số phản ứng xảy ra (không kể phản ứng của Al với H2O) là
-
A.
4
-
B.
2
-
C.
5
-
D.
3
Đáp án : A
xem lại lí thuyết nhôm
Al + 3Ag+ → Al3+ + Ag
Al + 3Fe3+ → Al3+ + 3Fe2+
2Al + 3Cu2+ → 2Al3+ + 3Cu
2Al + 3Fe2+ → 2Al3+ + 3Fe
Cho hỗn hợp bột gồm 0,56 gam Fe và 0,65 gam Zn vào V ml dung dịch AgNO3 0,1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được chất rắn có khối lượng tăng 2,31 gam so với ban đầu. Giá trị của V là
-
A.
0,25.
-
B.
250.
-
C.
300.
-
D.
200.
Đáp án : C
+) Giả sử Ag+ phản ứng hết với Zn2+ và Fe2+
=> ne cho tối đa = 0,01.2 + 0,01.2 = 0,04 mol
=> nAg+ = 0,04mol => m tăng = 3,11g > 2,31g
=> Ag+ hết, kim loại dư
+) Giả sử Ag+ phản ứng hết với Zn2+
Zn + 2Ag+ → 2Ag + Zn2+
=> m tăng = 1,51g < 2,31
=> Vẫn còn phản ứng
Fe + 2Ag+ → Fe2+ + 2Ag
x 2x 2x => m tăng = 2,31 – 1,51 = >x
=> nAg+
=> V
nFe = 0,01mol; nZn = 0,01mol
=> n e cho tối đa = 0,01.2 + 0,01.2 = 0,04 mol
=> nAg+ = 0,04mol
=> m tăng = 0,04 . 108 – (0,56 + 0,65) = 3,11g > 2,31g
=> Ag+ hết, kim loại dư
Zn + 2Ag+ → 2Ag + Zn2+
0,01 0,02 0,02 => m tăng = 0,02 . 108 – 0,01 . 65 = 1,51g < 2,31
=> còn phản ứng
Fe + 2Ag+ → Fe2+ + 2Ag
x 2x 2x => m tăng = 2,31 – 1,51 = 108 . 2x – 56x => x = 0,005
=> nAg+ = 0,03mol => V = 0,3lít = 300 ml
X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y lần lượt là (biết thứ tự trong dãy điện hoá : Fe3+/Fe2+ đứng trước Ag+/Ag)
-
A.
Ag, Mg.
-
B.
Cu, Fe.
-
C.
Fe, Cu.
-
D.
Mg, Ag.
Đáp án : C
Sử dụng dãy điện hóa
X là kim loại phản ứng được với dung dịch H2SO4 → X có tính khử mạnh hơn H+ trong dãy điện hóa
→ loại đáp án A và B
Y là kim loại tác dụng được với dung dịch Fe(NO3)3 → Y có tính khử mạnh hơn Fe3+ trong dãy điện hóa
→ loại đáp án D
Phương trình phản ứng :
Fe + H2SO4 → FeSO4 + H2
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
lon Mg2+ bị khử trong trường hợp
-
A.
Điện phân dung dịch MgCl2.
-
B.
Điện phân MgCl2 nóng chảy.
-
C.
Thả Na vào dung dịch MgCl2.
-
D.
Cho dd MgCl2 tác dụng dd Na2CO3.
Đáp án : B
lon Mg2+ bị khử trong trường hợp : Điện phân MgCl2 nóng chảy.
Chọn X, Y, Z, T, E theo đúng trật tự tương ứng sơ đồ sau : X → Y → Z → T → E
-
A.
AlCl3; Al(OH)3; NaAlO2; Al2O3; Al2(SO4)3
-
B.
AlCl3; NaAlO2; Al2O3; Al(OH)3; Al2(SO4)3
-
C.
Al(OH)3; AlCl3; Al2O3; NaAlO2; Al2(SO4)3
-
D.
AlCl3; NaAlO2; Al(OH)3; Al2O3; Al2(SO4)3
Đáp án : D
xem lại lí thuyết hợp chất nhôm
Trật tự đúng là: AlCl3 →NaAlO2 →Al(OH)3 →Al2O3→Al2(SO4)3.
A, B sai vì từ NaAlO2 không tạo trực tiếp được Al2O3
C sai vì từ AlCl3 không điều chế trực tiếp được ra Al2O3
Chọn phát biểu sai:
-
A.
Cr2O3 là chất rắn màu lục thẫm.
-
B.
Cr(OH)3 là chất rắn màu lục xám.
-
C.
CrO3 là chất rắn màu đỏ thẫm.
-
D.
Cr(OH)2 là chất rắn màu trắng xanh.
Đáp án : D
Xem lại lí thuyết crom và hợp chất
Phát biểu sai là: Cr(OH)2 là chất rắn màu trắng xanh
Vì Cr(OH)2 là chất rắn màu vàng
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X có tỉ khối so với khí hiđro bằng 18,8. Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
-
A.
9,40 gam.
-
B.
11,28 gam.
-
C.
8,60 gam.
-
D.
47,00 gam.
Đáp án : A
$\left\{\begin{gathered}101{\text{x}}+188y=34,65 \hfill \\\frac{{(0,5{\text{x}} + 0,5y).32 + 2y.46}}{{0,5{\text{x}} + 0,5y + 2y}} = 18,8.2 \hfill \\ \end{gathered} \right.$
2KNO3 → 2KNO2 + O2
x → 0,5x
2Cu(NO3)2 → 2CuO + 4NO2 + O2
y → 2y → 0,5y
Ta có hệ phương trình: $\left\{ \begin{gathered} 101{\text{x}} + 188y = 34,65 \hfill \\ \frac{{(0,5{\text{x}} + 0,5y).32 + 2y.46}}{{0,5{\text{x}} + 0,5y + 2y}} = 18,8.2 \hfill \\ \end{gathered} \right. = > \left\{ \begin{gathered} x = 0,25 \hfill \\ y = 0,05 \hfill \\ \end{gathered} \right.$
=> mCu(NO3)2 = 0,05.188 = 9,4 gam
lấy nhầm số mol KNO3 => chọn nhầm D
Từ hai muối X và Y thực hiện các phản ứng sau:
X → X1 + CO2
X1 + H2O → X2
X2 + Y → X + Y1 + H 2O
X2 + 2Y → X + Y2 + H2O
Hai muối X, Y tương ứng là
-
A.
CaCO3, NaHSO4.
-
B.
BaCO3, Na2CO3.
-
C.
CaCO3, NaHCO3.
-
D.
MgCO3, NaHCO3.
Đáp án : C
X là CaCO3, Y là NaHCO3.
CaCO3 $\xrightarrow{{{t^ \circ }}}$ CaO + CO2↑
X X1
CaO + H2O $\xrightarrow{{}}$ Ca(OH)2
X2
Ca(OH)2 + NaHCO3 $\xrightarrow{{}}$ CaCO3 + NaOH + H2O
Y Y1
Ca(OH)2 + 2NaHCO3 $\xrightarrow{{}}$ CaCO3 + Na2CO3 + 2H2O
Y Y2
Hòa tan 5,9 gam hỗn hợp X gồm K và Ca vào nước dư, sau phản ứng thu được 2,24 lít khí H2. Khối lượng Ca có trong hỗn hợp X là
-
A.
3,9 gam.
-
B.
2 gam.
-
C.
4,8 gam.
-
D.
4 gam.
Đáp án : B
Bảo toàn electron: nK + 2nCa = 2nH2
Gọi nK = x mol; nCa = y mol => mhỗn hợp = 39x + 40y = 5,9 (1)
Bảo toàn electron: nK + 2nCa = 2nH2 => x + 2y = 0,1.2 (2)
Từ (1), (2) => x = 0,1; y = 0,05
=> mca = 2 gam
Kim loại nào sau đây bị thụ động hóa với dung dịch axit sunfuric đặc nguội?
-
A.
Ag
-
B.
Cu
-
C.
Zn
-
D.
Fe
Đáp án : D
Al, Fe, Cr không tác dụng với H2SO4 đặc nguội và HNO3 đặc nguội (xem lại lí thuyết chung về kim loại)
Cho m gam K tan hết vào 100 ml dung dịch gồm (H2SO4 1M và HCl 2M) thu được 5,6 lít khí H2 (ở đktc). Cô cạn dung dịch sau phản ứng khối lượng chất rắn thu được là
-
A.
32,3
-
B.
37,9 gam.
-
C.
24,95 gam.
-
D.
30,1gam.
Đáp án : B
+) nH2 = 0,4 mol >\({1 \over 2}{n_{{H^ + }}}\)=> sau khi phản ứng với axit, K phản ứng với nước sinh ra H2
2K + 2H+ → 2K+ + H2
2K + H2O → 2KOH + H2
+) mcrắn khan = \({m_{{K^ + }}}\)trong muối +\({m_{C{l^ - }}} + {m_{SO_4^{2 - }}} + {m_{KOH}}\)
nH2SO4 = 0,1 mol; nHCl = 0,2 mol=> nH+ = 0,1.2 + 0,2 = 0,4
nH2 = 0,25 mol >\({1 \over 2}{n_{{H^ + }}}\)=>sau khi phản ứng với axit, K phản ứng với nước sinh ra H2
2K+ 2H+ → 2K+ + H2
0,4 ← 0,4 → 0,4 → 0,2
2K+ H2O → 2KOH + H2
0,1 ←0,1 ← 0,05
=> mcrắn khan = \({m_{{K^ + }}}\)trong muối +\({m_{C{l^ - }}} + {m_{SO_4^{2 - }}} + {m_{KOH}}\)= 0,4.39 + 0,1.96 + 0,2.35,5 + 0,1.56 = 37,9 gam
Ion kim loại nào sau đây không bị Zn khử thành kim loại ?
-
A.
Cu2+
-
B.
Ag+
-
C.
Sn2+.
-
D.
Al3+.
Đáp án : D
xem lại lí thuyết điều chế kim loại
Các ion kim loại nào sau đây không bị Zn khử là những kim loại đứng trước Zn: Al3+.
Hỗn hợp bột X gồm BaCO3, Fe(OH)2, Al(OH)3, Fe2O3 . Nung X trong không khí đến khối lượng không đối được hỗn hợp rắn A. Cho A vào nước dư khuấy đều được dung dịch B chứa 2 chất tan và phần không tan C. Cho khí CO dư qua bình chứa C nung nóng được hỗn hợp rắn E (Cho các phản ứng xảy ra hoàn toàn). E có thể chứa tối đa sản phẩm là
-
A.
Fe, Al2O3
-
B.
Fe2O3, Al2O3
-
C.
Fe
-
D.
BaO, Fe, Al2O3
Đáp án : C
xem lại lí thuyết điều chế kim loại
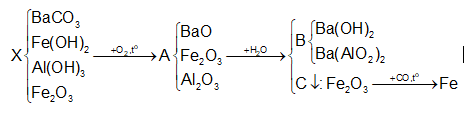
Cho lá Mg vào dung dịch HCl, có khí thoát ra. Thêm vài giọt X vào thì tốc độ thoát khí lớn hơn. X là?
-
A.
NaOH
-
B.
FeCl2
-
C.
BaCl2
-
D.
H2O
Đáp án : B
Khi thêm vài giọt FeCl2 vào dung dịch sẽ hình thành cặp pin điện hóa Mg-Fe làm cho khí thoát ra nhanh hơn
Khi cho mẫu Zn vào bình đựng dung dịch X, thì thấy khối lượng thanh Zn trong giảm đi (giả thiết kim loại sinh ra bám hết trên thanh Zn). Dung dịch X là:
-
A.
Cu(NO3)2.
-
B.
AgNO3.
-
C.
Ba(NO3)2.
-
D.
NaNO3.
Đáp án : A
tăng giảm khối lượng
Khối lượng thanh Zn giảm => khối lượng kim loại tạo ra nhỏ hơn Zn => loại B vì Mkim loại > MZn
Loại C, D vì Zn không đẩy được Ba2+ và Na+
Cho 12,04 gam hỗn hợp rắn X gồm Fe, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,42 mol HCl và 0,04 mol HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y (không chứa NH4+) và 0,045 mol hỗn hợp khí Z gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Y, sau phản ứng thấy thoát ra 0,0075 mol NO (sản phẩm khử duy nhất của N+5), đồng thời thu được 70,8 gam kết tủa. Phần trăm khối lượng Fe trong hỗn hợp X có giá trị gần nhấtvới giá trị nào sau đây?
-
A.
46,51%.
-
B.
37,8%.
-
C.
35,8%.
-
D.
49,6%.
Đáp án : A
Bảo toàn electron
Bảo toàn điện tích
Bảo toàn nguyên tố Fe, H, O
+) Phần kết tủa có AgCl => nAg
+) Bảo toàn electron: nFe2+ = nAg + 3 nNO
+) nH+ dư = 4.nNO
Đặt a, b, c là số mol Fe, Fe3O4, Fe(NO3)2 trong X
=> mX = PT (1)
Dung dịch Y còn H+ dư và Fe2+ nên NO3- đã hết.
+) Bảo toàn điện tích => nFe3+
+) Bảo toàn Fe => PT (2)
Bảo toàn H => nH2O
Bảo toàn O: 4. nFe3O4 + 6 nFe(NO3)2 + 3 nHNO3 = nZ + nH2O => PT (3)
Giải hệ (1),(2),(3) => a; b; c
Phần kết tủa có nAgCl = 0,42 => nAg = 0,0975
Bảo toàn electron: nFe2+ = nAg + 3 nNO = 0,12
nNO = 0,0075 => nH+ dư = 4.nNO = 0,03
Đặt a, b, c là số mol Fe, Fe3O4, Fe(NO3)2 trong X
=> mX = 56a + 232b + 180c = 12,04 (1)
Dung dịch Y còn H+ dư và Fe2+ nên NO3- đã hết.
Vậy Y chứa Fe2+ (0,12 mol), H+ (0,03 mol), Cl- (0,42 mol), Fe3+
Bảo toàn điện tích => nFe3+ = 0,05
Bảo toàn Fe => a + 3b + c = 0,05 + 0,12 (2)
Bảo toàn H => nH2O = 0,215
Bảo toàn O: 4. nFe3O4 + 6 nFe(NO3)2 + 3 nHNO3 = nZ + nH2O
=> 4b + 6c + 0,04.3 = 0,215 + 0,045 (3)
Giải hệ (1),(2),(3) => a = 0,1 mol; b = 0,02 mol; c = 0,01 mol
=> %mFe = 46,51%
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol Fe2(SO4)3 và z mol H2SO4, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
-
A.
x = y + z.
-
B.
2x = y + z.
-
C.
x = y – 2z.
-
D.
y = 2x.
Đáp án : A
Sử dụng phương pháp bảo toàn e
Dung dịch chỉ chứa một chất tan duy nhất là muối FeSO4
\(\eqalign{
& \mathop {Fe}\limits^0 \, - 2e \to \mathop {Fe}\limits^{ + 2} \cr
& \mathop {Fe}\limits^{ + 3} + 1e \to \mathop {Fe}\limits^{ + 2} \cr
& 2\mathop H\limits^ + + 2e \to {H_2} \cr} \)
Bảo toàn electron: 2x = 2y +2z
=> x = y + z
Phản ứng của Fe với O2 như hình vẽ

Cho các phát biểu sau đây:
(a) Vai trò của mẩu than để làm mồi cung cấp nhiệt cho phản ứng.
(b) Phản ứng tỏa nhiều nhiệt làm đầu dây sắt nóng chảy có thể thành cục tròn.
(c) Vai trò của lớp nước ở đáy bình là để tránh vỡ bình.
(d) Phản ứng cháy sáng, có các tia lửa bắn ra từ dây sắt.
Số phát biểu sai là
-
A.
2.
-
B.
0.
-
C.
1.
-
D.
3.
Đáp án : B
Dựa vào kiến thức phản ứng đốt cháy của Fe với O2
Tất cả các đáp án đều đúng → có 0 phát biểu sai
Hòa tan hết a mol FeCO3 vào dung dịch HCl (lấy dư 10% so với lượng cần dùng) thu được dung dịch X. Cho dung dịch AgNO3 dư vào dung dịch X thu được b gam kết tủa. Biết sản phẩm khử của N+5
là khí NO duy nhất, các phản ứng đều xảy ra hoàn toàn. Biểu thức về mối quan hệ giữa a và b là
-
A.
b = 315,7a
-
B.
b = 407,5a
-
C.
b = 287a
-
D.
b = 423,7b
Đáp án : B
FeCO3 + 2HCl → FeCl2 + H2O + CO2
3Fe+2 + NO3- + 4H+ → 3Fe+3 + 2H2O + NO
Fe+2 + Ag+ → Fe+3 + Ag
Ag+ + Cl- → AgCl
FeCO3 + 2HCl → FeCl2 + H2O + CO2
a 2a a
HCl lấy dư 10% nên X có nHCl dư = 0,2a mol → nCl- = 2a + 0,2a = 2,2a mol
nFe2+ = a mol; nH+ = 0,2 mol
X + AgNO3 thì 3Fe+2 + NO3- + 4H+ → 3Fe+3 + 2H2O + NO
0,15a 0,2a
Fe+2 + Ag+ → Fe+3 + Ag
0,85a 0,85a
Ag+ + Cl- → AgCl
2,2a 2,2a mol
→ mkết tủa = mAg + mAgCl = 0,85a. 108 + 2,2a.143,5 = 407,5a = b
Ở trạng thái cơ bản, nguyên tử Al (Z = 13) có số electron lớp ngoài cùng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : C
Viết cấu hình e của Al từ đó → tìm e lớp ngoài cùng
Al có cấu hình e là 1s22s22p63s23p1 nên lớp ngoài cùng có 3e
Cho từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp x mol HNO3 và y mol Al(NO3)3, kết quả thí nghiệm được biểu diễn trên đồ thị sau

Tỉ lệ của b : a có giá trị là
-
A.
14
-
B.
13
-
C.
12
-
D.
11
Đáp án : D
Thứ tự xảy ra phản ứng
KOH + HNO3 → KNO3 + H2O
3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3
KOH + Al(OH)3 → KAlO2 + 2H2O
Xét số mol KOH tại các thời điểm
KOH + HNO3 → KNO3 + H2O
3KOH + Al(NO3)3 → 3KNO3 + Al(OH)3
KOH + Al(OH)3 → KAlO2 + 2H2O
Xét tại các thời điểm
+) có 0,56 mol KOH thì chỉ xảy ra 2 phản ứng đầu
→ nKOH = nHNO3 + 3nAl(OH)3 = x + 3a = 0,56 mol
+) có 1,04 mol KOH thì chỉ có 2 phản ứng đầu xảy ra
→ nKOH = nHNO3 + 3nAl(OH)3 = x + 3(a + 0,8x ) =1,04
→ x = 0,2 mol và a = 0,12 mol
+) tại thời điểm b mol KOH thì xảy ra cả 3 phản ứng và thu được
nAl(OH)3 = a + 0,8x = 0,28 mol
→ nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan = x + 3y + (y – 0,28) =0,2 + 4y – 0,28 = 4y – 0,08 (mol) = b(1)
+) tại thời điểm (7x + 0,08) mol KOH hay 1,48 mol KOH thì nAl(OH)3 = 0,12 mol và cả 3 phản ứng xảy ra
→ nKOH = nHNO3 + 3nAl(NO3)3 + nAl(OH)3 bị hòa tan
= x + 3y + (y – 0,12) = 4y + 0,08 = 1,48 → y = 0,35 (2)
Từ (1) và (2) suy ra b = 1,32 mol
→ b : a = 1,32 : 0,12 = 11
Phương pháp thường được áp dụng để chống ăn mòn kim loại là
-
A.
Phương pháp bảo vệ bề mặt, phương pháp điện hóa.
-
B.
Phương pháp nhiệt luyện, thủy luyện.
-
C.
Phương pháp điện phân nóng chảy, điện phân dung dịch.
-
D.
Tất cả các phương pháp trên.
Đáp án : A
Các phương pháp bảo vệ kim loại không bị ăn mòn là:
+ Phương pháp bảo vệ bề mặt.
+ Phương pháp điện hóa.

Đun 0,04 mol hỗn hợp gồm hơi nước và khí CO2 qua cacbon nung đỏ, thu được 0,07 mol hỗn hợp Y gồm CO, H2 và CO2. Cho Y đi qua ống đựng 20 gam hỗn hợp gồm Fe2O3 và CuO (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
-
A.
19,52.
-
B.
18,56.
-
C.
19,04.
-
D.
18,40.
Đáp án : C
Sử dụng định luật bảo toàn khối lượng và bảo toàn nguyên tố để giải bài toán
\(0,04\left( {mol} \right)X\left\{ \begin{array}{l}{H_2}O\\C{O_2}\end{array} \right. + C \to 0,07\left( {mol} \right)\left\{ \begin{array}{l}CO\\{H_2}\\C{O_2}\end{array} \right. + 30\left( g \right)\left\{ \begin{array}{l}F{{\rm{e}}_2}{O_3}\\CuO\end{array} \right. \to {m_{chat\,ran}} = ?\)
Nhận thấy, C là nguyên nhân làm cho số mol hỗn hợp khí tăng lên => nC = 0,07 - 0,04 = 0,03 mol
Sau khi cho Y tác dụng với Fe2O3, CuO dư tạo thành H2O, CO2 nên ta có thể coi hỗn hợp Y gồm {H2O, CO2, C} như vậy ta thấy chỉ có C có phản ứng: C + 2O → CO2
=> nO(pư) = 2nC = 0,06 mol
=> m chất rắn = mFe2O3, CuO - mO(pư) = 20 - 0,06.16 = 19,04 gam
Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước dư thu được dung dịch X. Điện phân dung dịch X với điện cực trơ đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối hơi so với H2 bằng 30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử hiệu suất của quá trình điện phân là 100%, khí sinh ra không tan trong dung dịch. Giá trị của m là
-
A.
48,25
-
B.
64,25
-
C.
62,25
-
D.
56,25
Đáp án : B
- Tính lượng khí Cl2, O2 sinh ra sau quá trình điện phân
- Áp dụng định luật bảo toàn e, bảo toàn nguyên tố => nCuSO4 ban đầu => m
Khí tại anot gồm nCl2 = 0,15 mol; nO2 = 0,05 mol
=> Bảo toàn nguyên tố Cl => nFeCl3 = 0,1 mol
=> Dung dịch sau phản ứng có chứa Cu2+ và Fe2+
=> Tại catot chỉ có chứa kim loại Cu
=>Sau điện phân dung dịch gồm: nCuSO4 = nFeSO4 = 0,1 (mol) và H2SO4 = x (mol)
Bảo toàn nguyên tố S => nCuSO4 (ban đầu) = nS = 0,2 +x
=> nCu ở catot = 0,1 + x (mol)
Áp dụng định luật bảo toàn => nFe3+ + 2 * nCu (catot) = 2 nCl2 + 4nO2
=> 0,1 + 2 * (0,1 +x) = 0,5 => x = 0,1 (mol)
m = nCuSO4 (ban đầu) + nFeCl3 = 0,3 * 160 + 0,1 * 162,5 = 64,25 (gam)
Khi nung hỗn hợp các chất Fe(NO3)2, Fe(OH)3 và FeCO3 trong không khí đến khối lượng không đổi, thu được một chất rắn là
-
A.
Fe3O4.
-
B.
FeO.
-
C.
Fe.
-
D.
Fe2O3.
Đáp án : D
Dựa vào tính chất của các hợp chất của sắt, viết phương trình phản ứng và kết luận.
4Fe(NO3)2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 8NO2 + O2
2Fe(OH)3 \(\xrightarrow{{{t^o}}}\) Fe2O3 + 3H2O
4FeCO3 + O2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 4CO2
Vậy chất rắn thu được là Fe2O3.
Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 loãng ( dư),thu được dung dịch X. Trong các chất: NaOH, Cu, KNO3, KMnO4, BaCl2, Cl2, Al, NaCl, số chất có khả năng phản ứng được với dung dịch X là
-
A.
8
-
B.
6
-
C.
7
-
D.
5
Đáp án : C
NO3- trong môi trường H+ có tính oxi hóa giống hệt với HNO3
Fe3O4 + 3H2SO4 dư → FeSO4 + Fe2(SO4)3 + 3H2O
Vậy dd X thu được có: Fe2+, Fe3+ và H+ dư, SO42-
=> dd X tác dụng được với các chất: NaOH, Cu, KNO3, KMnO4, BaCl2, Cl2, Al => có 7 chất
Dưới đây là phương trình minh họa đại diện phản ứng xảy ra với từng chất ( các phương trình còn lại hs tự viết)
Fe2+ + OH- → Fe(OH)2↓
2Fe3+ + Cu → Cu2+ + 2Fe2+
3Fe2+ + NO3- + 4H+ → 3Fe3+ + NO + 2H2O
3Fe2+ + MnO4- + 4H+ → 3Fe+3 + MnO2↓ + 2H2O
SO42- + Ba2+ → BaSO4↓
Fe2+ + Cl2 → Fe3+ + 2Cl-
Fe2+ + Al → Al3+ + Fe↓
Loại quặng sắt dùng để sản xuất gang thường chứa từ 30 - 95% oxit sắt và phải
-
A.
chứa nhiều photpho.
-
B.
chứa nhiều lưu huỳnh.
-
C.
chứa nhiều SiO2.
-
D.
chứa rất ít phot pho, lưu huỳnh.
Đáp án : D
Dựa vào lý thuyết về quá trình sản xuất gang
Loại quặng sắt dùng để sản xuất gang thường chứa từ 30 – 95% oxit sắt và phải chứa rất ít photpho, lưu huỳnh
Chất nào sau đây được dùng để làm mềm nước cứng vĩnh cửu?
-
A.
NaNO3.
-
B.
NaOH.
-
C.
H2SO4.
-
D.
Na2CO3.
Đáp án : D
Để làm mềm nước cứng vĩnh cửu ta cần dùng chất có khả năng kết tủa hết Ca2+, Mg2+ ⟹ chất phù hợp
Để làm mềm nước cứng vĩnh cửu ta cần dùng chất có khả năng kết tủa hết Ca2+, Mg2+ ⟹ chọn Na2CO3
Ca2+ + CO32- → CaCO3 ↓
Mg2+ + CO32- → MgCO3 ↓
Ở điều kiện thường, kim loại nào sau đây không tan được trong dung dịch NaOH?
-
A.
Na.
-
B.
K.
-
C.
Al.
-
D.
Fe.
Đáp án : D
Dựa vào tính chất hóa học kim loại kiềm, Al và Fe được học trong sgk hóa 12
Na và K tan được trong nước có trong dd NaOH
PTHH: 2Na + 2H2O → 2NaOH + H2 ; K + H2O → 2KOH + H2
Al tan được trong dd NaOH: 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
Fe không tan được trong dd NaOH
>> 2K8 Chú ý! Lộ Trình Sun 2026 - 3IN1 - 1 lộ trình ôn 3 kì thi (Luyện thi 26+ TN THPT, 90+ ĐGNL HN, 900+ ĐGNL HCM, 70+ ĐGTD - Click xem ngay) tại Tuyensinh247.com.Đầy đủ theo 3 đầu sách, Thầy Cô giáo giỏi, luyện thi theo 3 giai đoạn: Nền tảng lớp 12, Luyện thi chuyên sâu, Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |










Danh sách bình luận