Đề thi giữa kì 2 Hóa 12 - Đề số 1
Đề bài
Điện phân dung dịch gồm a mol CuSO4 và 2a mol NaCl sau khi ở catot bắt đầu thoát khí thì dừng lại. Chất tan trong dung dịch thu được sau điện phân là
-
A.
CuSO4;Na2SO4.
-
B.
CuSO4; NaCl.
-
C.
Na2SO4.
-
D.
H2SO4; Na2SO4.
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
-
A.
a : b < 1 : 4
-
B.
a : b = 1 : 3
-
C.
a : b = 1 : 4
-
D.
a : b > 1 : 4
Dãy kim loại nào sau đây đều tan trong dung dịch H2SO4 loãng và đặc nguội ?
-
A.
K, Fe, Mg, Zn.
-
B.
Na, Cu, Al, Mg.
-
C.
Mg, Zn, K, Na.
-
D.
Fe, Al, Cu, K.
Hoà tan hoàn toàn 16 gam hỗn hợp Mg và Fe bằng dung dịch H2SO4 loãng vừa đủ. Sau phản ứng thấy khối lượng dung dịch tăng thêm 15,2 gam so với ban đầu. Khối lượng muối khan thu được khi cô cạn dung dịch sau phản ứng là
-
A.
53,6 gam.
-
B.
54,4 gam.
-
C.
92 gam.
-
D.
92,8 gam
Kim loại nào sau đây khử được ion Fe2+ trong dung dịch ?
-
A.
Ag
-
B.
Mg
-
C.
Cu
-
D.
Fe
Hòa tan m gam hỗn hợp X (gồm Al, Fe, Zn và Mg) bằng dung dịch HCl dư. Sau phản ứng, khối lượng dung dịch axit tăng thêm (m - 2) gam. Khối lượng (gam) của muối tạo thành trong dung dịch sau phản ứng là
-
A.
m + 34,5.
-
B.
m + 35,5.
-
C.
m + 69.
-
D.
m + 71.
Dựa vào nguyên tắc nào sau đây để làm mềm nước cứng ?
-
A.
Loại bỏ ion $HCO_3^ - $
-
B.
Giảm nồng độ ion Ca2+ và ion Mg2+
-
C.
Giảm nồng độ ion Cl-, SO42-
-
D.
Nguyên tắc khác
Cho 2,24 gam bột sắt vào 200 ml dung dịch CuSO4 0,05M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
-
A.
3,84.
-
B.
2,32.
-
C.
1,68.
-
D.
0,64.
Điện phân 500 ml dung dịch hỗn họp FeSO4 0,1M, Fe2(SO4)3 0,2M và CuSO4 0,1M với điện cực trơ. Điện phân cho đến khi khối lượng catot tăng 8,8 gam thì ngừng điện phân. Biết cường độ dòng điện đem điện phân là 10A. Thời gian điện phân là:
-
A.
4583,75 giây.
-
B.
3860 giây.
-
C.
4825 giây.
-
D.
2653,75 giây.
Điện phân dung dịch NaCl điện cực trơ, không có vách ngăn. Sản phấm thu được gồm
-
A.
H2, Cl2, NaOH
-
B.
H2, Cl2, NaOH, nước Giaven
-
C.
H2, Cl2, nước Giaven
-
D.
H2, nước Giaven
Hoà tan hoàn toàn 3 kim loại Zn, Fe, Cu bằng dung dịch HNO3 loãng. Sau khi phản ứng xảy ra hoàn toàn, thu được chất rắn không tan là Cu. Các chất tan có trong dung dịch sau phản ứng là
-
A.
Zn(NO3)2; Fe(NO3)3.
-
B.
Zn(NO3)2; Fe(NO3)2.
-
C.
Zn(NO3)2; Fe(NO3)3; Cu(NO3)2.
-
D.
Zn(NO3)2; Fe(NO3)2; Cu(NO3)2.
Chia 47,2 gam hỗn hợp gồm CuO, Fe2O3 và Fe3O4 thành 2 phần bằng nhau. Phần 1 khử hoàn toàn bằng CO dư ở nhiệt độ cao thu được 17,2 gam 2 kim loại. Phần 2 cho tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được m gam muối. Giá trị của m là
-
A.
124.
-
B.
49,2.
-
C.
55,6.
-
D.
197,2.
Hoà tan hoàn toàn 35 gam hỗn hợp gồm Na, K và Ba vào nước, thu được dung dịch X và 22,4 lít khí H2 (đktc). Dung dịch Y gồm HCl và H2SO4, tỉ lệ mol tương ứng là 3 : 1. Trung hoà dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
-
A.
73,4 gam
-
B.
77,6 gam
-
C.
116,0 gam
-
D.
75,5 gam
Cho m gam hỗn hợp X gồm Al và Cu vào dung dịch HCl dư sau khi phản ứng kết thúc thu được 3,36 lít khí H2 (đktc). Nếu cho m gam hỗn hợp X trên tác dụng với HNO3 đặc nguội dư, sau phản ứng thu được 6,72 lít khí NO2 (đktc). Giá trị của m là
-
A.
15,6.
-
B.
10,5.
-
C.
11,5.
-
D.
12,3.
Cho 1,44 gam Mg tác dụng với 500 ml dung dịch X chứa Zn(NO3)2 0,1M và Cu(NO3)2 0,02M. Sau khi phản ứng kết thúc thu được m gam chất rắn. Giá trị của m là :
-
A.
3,89.
-
B.
3,84.
-
C.
5,64
-
D.
5,68.
Cho khí CO qua hỗn hợp T gồm Fe và Fe2O3 nung nóng thu được hỗn hợp khí B và hỗn hợp chất rắn D. Cho B qua dung dịch Ca(OH)2 dư thu được 6 gam kết tủa. Mặt khác, hòa tan hỗn hợp D bằng dung dịch H2SO4 đặc, nóng, dư thu được 0,18 mol SO2 (sản phẩm khử duy nhất) và 24 gam muối. Phần trăm số mol của Fe trong hỗn hợp T là
-
A.
80%
-
B.
45%
-
C.
50%
-
D.
75%
Tiến hành phản ứng nhiệt nhôm hỗn hợp A gồm Al và FexOy (trong điều kiện không có không khí) được hỗn hợp B. Nghiền nhỏ, trộn đều hỗn hợp B rồi chia thành hai phần.
Phần 1 : có khối lượng 4,83 gam được hòa tan hết trong dung dịch HNO3 dư, đun nóng thu được dung dịch C và 1,232 lít NO (sản phẩm khử duy nhất).
Phần 2 : tác dụng với dung dịch NaOH dư đun nóng thu được 1,008 lít H2 và còn lại 7,56 gam chất rắn.
Biết các phản ứng xảy ra hoàn toàn, thể tích các khí đo ở đktc. Công thức FexOy là
-
A.
Fe3O4
-
B.
FeO
-
C.
Fe2O3
-
D.
FeO hoặc Fe3O4
Điện phân dung dịch chứa a mol CuSO4 và b mol NaCl với 2a < b (điện cực trơ). Cho vài giọt quì vào dung dịch, màu của dung dịch sẽ biến đổi thế nào trong quá trình điện phân:
-
A.
Tím sang đỏ
-
B.
Đỏ sang tím rồi xanh
-
C.
Tím sang xanh
-
D.
Không đổi màu
Cho m gam tinh thể CuSO4.5H2O vào dung dịch KCl thu được dung dịch X. Tiến hành điện phân dung dịch X với điện cực trơ, màng ngăn xốp và cường độ dòng điện không đổi, ở thời gian t giây thu được dung dịch Y đồng thời ở anot thu được 0,15 mol hỗn hợp khí. Nếu thời gian điện phân là 2t giây, tổng số mol khí thoát ra ở cả hai điện cực là 0,393 mol. Nhúng thanh Mg vào dung dịch Y, kết thúc phản ứng thấy khối lượng thanh không đổi so với trước phản ứng. Giá trị của m là
-
A.
70,5.
-
B.
71,0.
-
C.
73,0.
-
D.
73,5.
Chỉ dùng CO2 và nước có thể phân biệt được dãy các chất nào?
-
A.
Na, K, Ba
-
B.
Na, Ca, Al
-
C.
Ca, Fe; Cu
-
D.
K, Na, Ca
Cho dd Ba(OH)2 lần lượt tác dụng với các dd sau: CaCl2, Ca(NO3)2, Ba(HSO4)2 , NaHSO4, Ca(HCO3)2, H2SO4, HCl. Số phản ứng tạo ra kết tủa là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Nếu đun sôi nước cứng tạm thời sẽ thấy hiện tượng?
-
A.
Nước sôi.
-
B.
Chỉ thấy thoát khí CO2.
-
C.
Dung dịch chuyển màu xanh.
-
D.
Thấy thoát khí CO2 và đồng thời xuất hiện kết tủa trắng .
Sục từ từ V lít khí CO2 (đktc) từ từ vào 100 ml dung dịch hỗn hợp NaOH 2M; KOH 2M và Ba(OH)2 3 M. Kết thúc phản ứng thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
-
A.
8,96.
-
B.
4,48.
-
C.
17,92.
-
D.
13,44.
Cho Al đến dư vào dung dịch gồm NO3-, Cu2+, Fe3+, Ag+, sau phản ứng hoàn toàn thu được chất rắn X. Không kể phản ứng của Al với H2O trong X chứa
-
A.
Ag, Al
-
B.
Ag, Fe, Cu.
-
C.
Fe, Cu
-
D.
Ag, Fe, Cu, Al
Cho 8,6 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với lượng dư dung dịch HCl loãng, thu được 4,48 lít khí (đktc). Kim loại X, Y là
-
A.
Rb và Ba
-
B.
Liti và beri.
-
C.
Natri và Canxi.
-
D.
Ba và Cs.
Trong các ion kim loại sau, ion kim loại có tính oxi hóa lớn nhất là?
-
A.
Na+
-
B.
Cu2+
-
C.
Al3+
-
D.
Fe3+
Cho biết thế điện cực chuẩn của các cặp oxi hóa - khử Mg2+/Mg ; Zn2+/Zn ; Cu2+/Cu ; Ag+/Ag ; Hg2+/Hg lần lượt là –2,37 V; –0,76 V ; 0,34 V ; 0,8 V ; và 0,85 V. E0(pin) = 1,56 V là suất điện động chuẩn của pin nào trong số các pin sau ?
-
A.
Zn – Ag
-
B.
Mg – Zn
-
C.
Zn – Hg
-
D.
Mg – Hg
Để điều chế K người ta có thể dùng phương pháp nào
-
A.
Điện phân dung dịch KCl có vách ngăn xốp.
-
B.
Dùng CO để khử K ra khỏi K2O.
-
C.
Điện phân nóng chảy KOH.
-
D.
Dùng Li để khử K ra khỏi dd KCl.
Phát biểu nào sau đây là đúng?
-
A.
Ăn mòn kim loại là sự phá hủy kim loại do tác động cơ học.
-
B.
Ăn mòn kim loại là sự hình thành kim loại do môi trường xung quanh tác dụng vào dung dịch muối.
-
C.
Ăn mòn kim loại là sự phá hủy kim loại do kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện.
-
D.
Ăn mòn kim loại là sự phá hủy kim loại do tác dụng hoá học của môi trường xung quanh.
Al2O3 không tan được trong dung dịch chứa chất nào sau đây?
-
A.
HCl.
-
B.
NaCl.
-
C.
Ba(OH)2.
-
D.
HNO3
Hòa tan hoàn toàn hỗn hợp gồm 0,25 mol Al2O3 và 0,4 mol BaO vào nước dư thu được dung dịch E. Nhỏ từ từ dung dịch HCl k (M) vào E, số mol kết tủa (y mol) thu được phụ thuộc vào số mol HCl phản ứng (x mol) được biểu diễn theo sơ đồ sau:
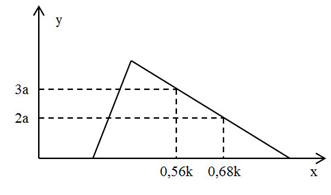
Giá trị của k là:
-
A.
2,0
-
B.
1,5
-
C.
2,5
-
D.
1,8
Hòa tan hoàn toàn a gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO (trong đó oxi chiếm 7,99% về khối lượng) vào nước dư. Sau phản ứng, thu được dung dịch Y gồm NaOH, KOH và Ba(OH)2 có tỉ lệ mol tương ứng là 3: 2: 7 và 0,784 lít khí H2(đktc). Cho Y tác dụng với dung dịch gồm 0,02 mol Al2(SO4)3, 0,01 mol H2SO4 và 0,04 mol KHSO4 thu được m gam kết tủa. Giá trị của m là:
-
A.
24,17
-
B.
17,87
-
C.
17,09
-
D.
18,65
Kim loại nào sau đây không phải kim loại kiềm
-
A.
Ca
-
B.
K
-
C.
Cs
-
D.
Li
Cho 1,82 g một kim loại kiềm tác dụng hết với 48,44 gam nước, sau phản ứng thu được 2,912 lít khí H2 (đktc) và dung dịch X. Kim loại kiềm và nồng độ phần trăm dung dịch X là
-
A.
Li; 44%.
-
B.
Na; 31,65 %.
-
C.
Li; 12,48 %.
-
D.
Na; 44%.
Kim loại nào sau đây là kim loại kiềm?
-
A.
Ba.
-
B.
Ca.
-
C.
Al.
-
D.
Cs.
Dựa vào khối lượng riêng của kim loại, hãy tính thể tích mol kim loại và ghi kết quả vào bảng sau:
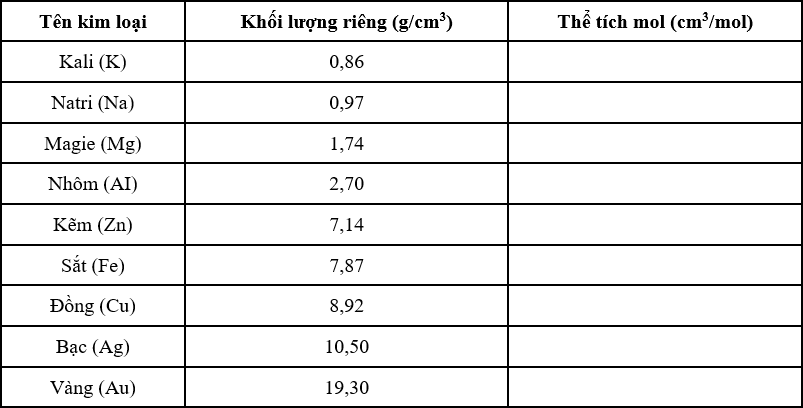
Chọn phát biểu không đúng trong các phát biểu sau:
-
A.
Thể tích mol của K là 45,46 cm3.
-
B.
Thể tích mol của Mg là 19,73 cm3.
-
C.
Thể tích mol của Al là 9,99 cm3.
-
D.
Thể tích mol của Au là 10,20 cm3.
Phát biểu nào sau đây là đúng khi nói về ăn mòn hoá học ?
-
A.
Ăn mòn hoá học làm phát sinh dòng điện một chiều.
-
B.
Kim loại tinh khiết sẽ không bị ăn mòn hoá học.
-
C.
Về bản chất, ăn mòn hóa học cũng là một dạng của ăn mòn điện hoá.
-
D.
Ăn mòn hoá học không làm phát sinh dòng điện.
Hỗn hợp X gồm Fe3O4 và Al có tỉ lệ mol tương ứng là 1 : 3 thực hiện phản ứng nhiệt nhôm X (không có không khí) đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm
-
A.
Al,Fe,Fe3O4 và Al2O3.
-
B.
Al2O3,Fe và Fe3O4.
-
C.
Al2O3và Fe.
-
D.
Al,Fe và Al2O3.
Cho ba kim loại là Al, Fe, Cu và bốn dung dịch muối riêng biệt là ZnSO4, AgNO3, CuCl2, MgSO4. Kim loại nào tác dụng được với cả bốn dung dịch muối đã cho ?
-
A.
Al.
-
B.
Fe.
-
C.
Cu.
-
D.
Không kim loại nào tác dụng được.
Hòa tan hoàn toàn m gam hỗn hợp X gồm Mg, Al, Zn trong 500 ml dung dịch HNO3 4M, sau phản ứng hoàn toàn thu được dung dịch Y và 4,48 lít (đktc) hỗn hợp gồm hai khí không màu có tỉ khối so với H2 là 18,5 trong đó có 1 khí hóa nâu ngoài không khí. Trung hòa dung dịch Y bằng lượng vừa đủ 100 ml dung dịch NaOH 1M, thu được dung dịch Z. Cô cạn Z, thu được 134,5 gam muối khan. Giá trị của m là
-
A.
30,0.
-
B.
29,4.
-
C.
30,6.
-
D.
29,0.
Lời giải và đáp án
Điện phân dung dịch gồm a mol CuSO4 và 2a mol NaCl sau khi ở catot bắt đầu thoát khí thì dừng lại. Chất tan trong dung dịch thu được sau điện phân là
-
A.
CuSO4;Na2SO4.
-
B.
CuSO4; NaCl.
-
C.
Na2SO4.
-
D.
H2SO4; Na2SO4.
Đáp án : C
(1) 2NaCl + CuSO4 → Cu +Cl2 + Na2SO4
Ở (1) NaCl phản ứng vừa đủ với CuSO4 => Dung dịch sau điện phân chỉ có Na2SO4
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
-
A.
a : b < 1 : 4
-
B.
a : b = 1 : 3
-
C.
a : b = 1 : 4
-
D.
a : b > 1 : 4
Đáp án : D
xem lại lí thuyết nhôm và hợp chất tác dụng với dung dịch kiềm
Nếu b ≥ 4a thì kết tủa bị hoà tan hoàn toàn => để thu được kết tủa thì b < 4a
Dãy kim loại nào sau đây đều tan trong dung dịch H2SO4 loãng và đặc nguội ?
-
A.
K, Fe, Mg, Zn.
-
B.
Na, Cu, Al, Mg.
-
C.
Mg, Zn, K, Na.
-
D.
Fe, Al, Cu, K.
Đáp án : C
Các kim loại đứng sau H trong dãy hoạt động hóa học thì không tác dụng với H2SO4 loãng => loại B và D vì có Cu
Al, Fe, Cr không tác dụng với H2SO4 đặc nguội => loại A
Hoà tan hoàn toàn 16 gam hỗn hợp Mg và Fe bằng dung dịch H2SO4 loãng vừa đủ. Sau phản ứng thấy khối lượng dung dịch tăng thêm 15,2 gam so với ban đầu. Khối lượng muối khan thu được khi cô cạn dung dịch sau phản ứng là
-
A.
53,6 gam.
-
B.
54,4 gam.
-
C.
92 gam.
-
D.
92,8 gam
Đáp án : B
+) mdung dịch tăng = mkim loại – mH2
+) nSO4 = nH2SO4 = nH2 = 0,4 mol
+) Bảo toàn khối lượng: mmuối = mkim loại + mH2
mdung dịch tăng = mkim loại – mH2 = 15,2
=> mH2 = mkim loại – 15,2 = 16 – 15,2 = 0,8 gam
=> nH2 = 0,4 mol => nSO4 = nH2SO4 = nH2 = 0,4 mol
Bảo toàn khối lượng: mmuối = mkim loại + mSO4 = 16 + 0,4.96 = 54,4 gam
Kim loại nào sau đây khử được ion Fe2+ trong dung dịch ?
-
A.
Ag
-
B.
Mg
-
C.
Cu
-
D.
Fe
Đáp án : B
Kim loại khử được ion Fe2+ trong dung dịch là kim loại đứng trước Fe trong dãy điện hóa
Hòa tan m gam hỗn hợp X (gồm Al, Fe, Zn và Mg) bằng dung dịch HCl dư. Sau phản ứng, khối lượng dung dịch axit tăng thêm (m - 2) gam. Khối lượng (gam) của muối tạo thành trong dung dịch sau phản ứng là
-
A.
m + 34,5.
-
B.
m + 35,5.
-
C.
m + 69.
-
D.
m + 71.
Đáp án : D
+) mdung dịch tăng = mkim loại – mH2
+) Bảo toàn nguyên tố: nCl = nHCl = 2nH2 = 2 mol
+) mmuối = mkim loại + mgốc Cl
mdung dịch tăng = mkim loại – mH2 = m – 2
→ mH2 = 2 gam → nH2 = 1 mol
Bảo toàn nguyên tố: nCl = nHCl = 2nH2 = 2 mol
=> khối lượng muối thu được là: mmuối = mkim loại + mgốc Cl = m + 2,35,5 = m + 71 gam
Dựa vào nguyên tắc nào sau đây để làm mềm nước cứng ?
-
A.
Loại bỏ ion $HCO_3^ - $
-
B.
Giảm nồng độ ion Ca2+ và ion Mg2+
-
C.
Giảm nồng độ ion Cl-, SO42-
-
D.
Nguyên tắc khác
Đáp án : B
Nguyên tắc làm mềm nước cứng: giảm nồng độ ion Ca2+ và ion Mg2+
Cho 2,24 gam bột sắt vào 200 ml dung dịch CuSO4 0,05M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
-
A.
3,84.
-
B.
2,32.
-
C.
1,68.
-
D.
0,64.
Đáp án : B
sử dụng tăng giảm khối lượng
Fe + CuSO4 → FeSO4 + Cu
0,01 ← 0,01 → 0,01
=> độ tăng khối lượng = mCu – mFe = 0,01.(64 – 56) = 0,08 gam
=> mchất rắn Y = 2,24 + mtăng = 2,24 + 0,08 = 2,32 gam
nFe = 0,04 mol; nCuSO4 = 0,01 mol
Fe + CuSO4 → FeSO4 + Cu
0,01 ← 0,01 → 0,01
=> độ tăng khối lượng = mCu – mFe = 0,01.(64 – 56) = 0,08 gam
=> mchất rắn Y = 2,24 + mtăng = 2,24 + 0,08 = 2,32 gam
Điện phân 500 ml dung dịch hỗn họp FeSO4 0,1M, Fe2(SO4)3 0,2M và CuSO4 0,1M với điện cực trơ. Điện phân cho đến khi khối lượng catot tăng 8,8 gam thì ngừng điện phân. Biết cường độ dòng điện đem điện phân là 10A. Thời gian điện phân là:
-
A.
4583,75 giây.
-
B.
3860 giây.
-
C.
4825 giây.
-
D.
2653,75 giây.
Đáp án : C
Từ mcatot tăng => Khối lượng kim loại bám vào
Xác định chất bị điện phân : gồm Cu2+, Fe3+ và Fe2+ bị điện phân 1 phần
Tính ${{n}_{{{e}_{td}}}}=\frac{It}{F}\Rightarrow t$
nFe3+ = 0,2 mol ; nCu2+ = 0,05mol ; nFe2+ =0,05mol
mtăng = mCu + mFe => mFe = 8,8 – 0,05.64 = 5,6g => nFe = 0,1mol
Các ion đã điện phân ở catot: Fe3+ , Cu2+, Fe2+ điện phân 1 phần
netđ = nFe3+ + 2nCu2+ + 2nFe2+ = 0,2 + 0,05.2 + 0,1.2 = 0,5 mol
=> $t=\frac{F.{{n}_{{{e}_{t\text{d}}}}}}{I} =\frac{96500.0,5}{10}=4825s$
Điện phân dung dịch NaCl điện cực trơ, không có vách ngăn. Sản phấm thu được gồm
-
A.
H2, Cl2, NaOH
-
B.
H2, Cl2, NaOH, nước Giaven
-
C.
H2, Cl2, nước Giaven
-
D.
H2, nước Giaven
Đáp án : D
Phương trình điện phân có màng ngăn: 2NaCl + 2H2O → 2NaOH + H2 + Cl2
Nếu không có màng ngăn thì: Cl2 + 2NaOH → NaCl + NaClO + H2O
=> phương trình điện phân: NaCl + H2O → NaClO + H2
Hoà tan hoàn toàn 3 kim loại Zn, Fe, Cu bằng dung dịch HNO3 loãng. Sau khi phản ứng xảy ra hoàn toàn, thu được chất rắn không tan là Cu. Các chất tan có trong dung dịch sau phản ứng là
-
A.
Zn(NO3)2; Fe(NO3)3.
-
B.
Zn(NO3)2; Fe(NO3)2.
-
C.
Zn(NO3)2; Fe(NO3)3; Cu(NO3)2.
-
D.
Zn(NO3)2; Fe(NO3)2; Cu(NO3)2.
Đáp án : D
Sau phản ứng thu được chất rắn không tan là Cu → trong dung dịch không còn muối Fe(NO3)3
Chia 47,2 gam hỗn hợp gồm CuO, Fe2O3 và Fe3O4 thành 2 phần bằng nhau. Phần 1 khử hoàn toàn bằng CO dư ở nhiệt độ cao thu được 17,2 gam 2 kim loại. Phần 2 cho tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được m gam muối. Giá trị của m là
-
A.
124.
-
B.
49,2.
-
C.
55,6.
-
D.
197,2.
Đáp án : C
+) mO (trong oxit) + mkim loại = moxit
1 mol O (trong oxit) đổi lấy 1 mol gốc SO4
0,4 mol O ----------------- 0,4 mol gốc SO4
+) mmuối = mkim loại + mgốc SO4
mO (trong oxit) + mkim loại = moxit => mO (trong oxit) = 47,2 / 2 – 17,2 = 6,4 gam
=> nO (trong oxit) = 0,4 mol
1 mol O (trong oxit) đổi lấy 1 mol gốc SO4
0,4 mol O ----------------- 0,4 mol gốc SO4
=> mmuối = mkim loại + mgốc SO4 = 17,2 + 0,4.96 = 55,6 gam
quên không chia 2 của mhỗn hợp oxit => chọn nhầm D
Hoà tan hoàn toàn 35 gam hỗn hợp gồm Na, K và Ba vào nước, thu được dung dịch X và 22,4 lít khí H2 (đktc). Dung dịch Y gồm HCl và H2SO4, tỉ lệ mol tương ứng là 3 : 1. Trung hoà dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
-
A.
73,4 gam
-
B.
77,6 gam
-
C.
116,0 gam
-
D.
75,5 gam
Đáp án : C
Gọi nHCl = 3a mol => nH2SO4 = a mol
+) nH+ = 3a + 2a = 2
+) mmuối = mKim loại + mCl + mSO4
nH2 = 1 mol => nH+ cần trung hòa = 2nH2 = 2 mol
Gọi nHCl = 3a mol => nH2SO4 = a mol
=> nH+ = 3a + 2a = 2 => a = 0,4
=> nCl = nHCl = 3.0,4 = 1,2 mol; nSO4 = nH2SO4 = 0,4 mol
Ta có mmuối = mKim loại + mCl + mSO4 = 35 + 1,2.35,5 + 0,4.96 = 116 gam
+ quên không tính khối lượng gốc Cl => Chọn nhầm A
+ quên không tính khối lượng gốc SO4 => chọn nhầm B
+ nhầm tỉ lệ nH+ cần trung hòa = nH2 => chọn nhầm D
Cho m gam hỗn hợp X gồm Al và Cu vào dung dịch HCl dư sau khi phản ứng kết thúc thu được 3,36 lít khí H2 (đktc). Nếu cho m gam hỗn hợp X trên tác dụng với HNO3 đặc nguội dư, sau phản ứng thu được 6,72 lít khí NO2 (đktc). Giá trị của m là
-
A.
15,6.
-
B.
10,5.
-
C.
11,5.
-
D.
12,3.
Đáp án : D
+) X + HCl => chỉ có Al phản ứng
Bảo toàn electron: 3nAl = 2nH2
+) X + HNO3 đặc nguội => chỉ có Cu phản ứng
Bảo toàn e: 2nCu = nNO2
X + HCl => chỉ có Al phản ứng
nH2 = 0,15 mol
Bảo toàn electron: 3nAl = 2nH2 => nAl = 2.0,15 / 3 = 0,1 mol
X + HNO3 đặc nguội => chỉ có Cu phản ứng
nNO2 = 0,3 mol
Bảo toàn e: 2nCu = nNO2 => nCu = 0,3 / 2 = 0,15 mol
=> m = mAl + mCu = 0,1.27 + 0,15.64 = 12,3 gam
Cho 1,44 gam Mg tác dụng với 500 ml dung dịch X chứa Zn(NO3)2 0,1M và Cu(NO3)2 0,02M. Sau khi phản ứng kết thúc thu được m gam chất rắn. Giá trị của m là :
-
A.
3,89.
-
B.
3,84.
-
C.
5,64
-
D.
5,68.
Đáp án : A
ne Mg cho tối đa = 0,06.2 = 0,12 mol
ne Cu2+ nhận = 0,01.2 = 0,02 mol; ne Zn2+ nhận = 0,1 mol => ne nhận tối đa = 0,02 + 0,1 = 0,12 mol
Ta thấy ne cho tối đa = ne nhận tối đa = 0,12 mol => Mg phản ứng vừa đủ với Cu2+ và Zn2+
nMg = 0,06 mol; nZn(NO3)2 = 0,05 mol; nCu(NO3)2 = 0,01
ne Mg cho tối đa = 0,06.2 = 0,12 mol
ne Cu2+ nhận = 0,01.2 = 0,02 mol; ne Zn2+ nhận = 0,1 mol => ne nhận tối đa = 0,02 + 0,1 = 0,12 mol
Ta thấy ne cho tối đa = ne nhận tối đa = 0,12 mol => Mg phản ứng vừa đủ với Cu2+ và Zn2+
=> chất rắn thu được gồm Cu (0,01 mol) và Zn (0,05 mol)
=> m = 3,89 gam
+ tính số mol Cu = số mol Mg = 0,06 => chọn nhầm B
Cho khí CO qua hỗn hợp T gồm Fe và Fe2O3 nung nóng thu được hỗn hợp khí B và hỗn hợp chất rắn D. Cho B qua dung dịch Ca(OH)2 dư thu được 6 gam kết tủa. Mặt khác, hòa tan hỗn hợp D bằng dung dịch H2SO4 đặc, nóng, dư thu được 0,18 mol SO2 (sản phẩm khử duy nhất) và 24 gam muối. Phần trăm số mol của Fe trong hỗn hợp T là
-
A.
80%
-
B.
45%
-
C.
50%
-
D.
75%
Đáp án : A
+) nCaCO3 = nCO phản ứng = nCO2
Gọi nFe = x mol; nFe2O3 = y mol
+) Xét toàn bộ quá trình có Fe và CO cho e; H2SO4 nhận e
+)Bảo toàn e: 3nFe + 2nCO = 2nSO2
nFe2(SO4)3 = 0,06 mol
+) Bảo toàn Fe: x + 2y = 0,06.2
nCaCO3 = 0,06 mol => nCO phản ứng = nCO2 = 0,06 mol
Gọi nFe = x mol; nFe2O3 = y mol
Xét toàn bộ quá trình có Fe và CO cho e; H2SO4 nhận e
Bảo toàn e: 3nFe + 2nCO = 2nSO2 => 3x + 2.0,06 = 2.0,18 => x = 0,08 mol
nFe2(SO4)3 = 0,06 mol
Bảo toàn Fe: x + 2y = 0,06.2 => y = 0,02 mol
$ = > \,\,\% {m_{Fe}} = \dfrac{{0,08}}{{0,08 + 0,02}}.100\% = 80\% $
Tiến hành phản ứng nhiệt nhôm hỗn hợp A gồm Al và FexOy (trong điều kiện không có không khí) được hỗn hợp B. Nghiền nhỏ, trộn đều hỗn hợp B rồi chia thành hai phần.
Phần 1 : có khối lượng 4,83 gam được hòa tan hết trong dung dịch HNO3 dư, đun nóng thu được dung dịch C và 1,232 lít NO (sản phẩm khử duy nhất).
Phần 2 : tác dụng với dung dịch NaOH dư đun nóng thu được 1,008 lít H2 và còn lại 7,56 gam chất rắn.
Biết các phản ứng xảy ra hoàn toàn, thể tích các khí đo ở đktc. Công thức FexOy là
-
A.
Fe3O4
-
B.
FeO
-
C.
Fe2O3
-
D.
FeO hoặc Fe3O4
Đáp án : A
Phần 2 : nAl dư = 2/3.nH2
Chất rắn còn lại là Fe => nFe = 0,135 mol
Phần 1 : Bảo toàn e : 3nAl + 3nFe = 3nNO
+) Bảo toàn nguyên tố oxi : ${n_{O(F{e_x}{O_y})}} = {\text{ }}{n_{O(A{l_2}{O_3})}}$
Phần 2 : ${n_{{H_2}}} = 0,045\,\,mol$ → nAl dư = $\frac{2}{3}.0,045 = 0,03\,\,mol$
Chất rắn còn lại là Fe => nFe = 0,135 mol
Phần 1 : nAl dư = 0,03k mol; nFe = 0,135k mol
Bảo toàn e : 3nAl + 3nFe = 3nNO => 0,03k + 0,135k = 0,055 => k = $\frac{1}{3}$
=>${m_{A{l_2}{O_3}}} = 4,83 - 0,03.\frac{1}{3}.27 - 56.0,135.\frac{1}{3} = 2,04\,\,gam$ => mAl2O3 = 0,02 mol
Bảo toàn nguyên tố oxi : ${n_{O(F{e_x}{O_y})}} = {\text{ }}{n_{O(A{l_2}{O_3})}}$ = 0,02.3 = 0,06 mol
${n_{Fe}} = 0,135.\frac{1}{3} = 0,045\,\,mol$
=>$\frac{{{n_{Fe}}{\text{ }}}}{{{n_O}}} = {\text{ }}\frac{{0,135}}{{0,18}} = \frac{3}{4}$ => oxit là Fe3O4
Điện phân dung dịch chứa a mol CuSO4 và b mol NaCl với 2a < b (điện cực trơ). Cho vài giọt quì vào dung dịch, màu của dung dịch sẽ biến đổi thế nào trong quá trình điện phân:
-
A.
Tím sang đỏ
-
B.
Đỏ sang tím rồi xanh
-
C.
Tím sang xanh
-
D.
Không đổi màu
Đáp án : B
Xem lại lý thuyết điện phân
Ở catot: Cu2+ + 2e → Cu
a 2a
2H2O + 2e → H2 + 2OH-
Ở anot: 2Cl- + 2e → Cl2
b b
Vì 2a < b => khi chưa điện phân hết Cl- ở anot thì ở catot nước đã bị điện phân tạo OH-
=> màu của dung dịch chuyển từ đỏ sang tím sang xanh
Cho m gam tinh thể CuSO4.5H2O vào dung dịch KCl thu được dung dịch X. Tiến hành điện phân dung dịch X với điện cực trơ, màng ngăn xốp và cường độ dòng điện không đổi, ở thời gian t giây thu được dung dịch Y đồng thời ở anot thu được 0,15 mol hỗn hợp khí. Nếu thời gian điện phân là 2t giây, tổng số mol khí thoát ra ở cả hai điện cực là 0,393 mol. Nhúng thanh Mg vào dung dịch Y, kết thúc phản ứng thấy khối lượng thanh không đổi so với trước phản ứng. Giá trị của m là
-
A.
70,5.
-
B.
71,0.
-
C.
73,0.
-
D.
73,5.
Đáp án : A
Trong t giây đầu tiên, tại anot thu được Cl2 (a mol) và O2 (b mol)
Từ tổng số mol khí => PT (1)
+) Tính số mol electron trao đổi trong t (s) theo a và b => số mol e trao đổi trong 2t (s)
+) Đặt \({{n}_{CuS{{O}_{4}}}}=x\) => trong t (s) tính nCuSO4 bị đp => nCuSO4 dư
+) Khi nhúng Mg vào Y, vì khối lượng thanh không đổi nên: mMg pứ = mCu bị Mg đẩy ra => PT (2)
+) Tính số mol H2 thu được sau 2t (s)
Khí trong 2t giây = khí trong t giây đầu (0,15 mol) + H2 + O2
=> tổng số mol khí = PT (3)
Giải hệ (1), (2), (3) => a; b ; x => \({{m}_{CuS{{O}_{4}}.5{{H}_{2}}O}}\)
Trong t giây đầu tiên, tại anot thu được Cl2 (a mol) và O2 (b mol)
=> a + b = 0,15 (1)
=> Số mol electron trao đổi trong t giây = 2a + 4b
Ban đầu đặt \({{n}_{CuS{{O}_{4}}}}=x\) => trong t giây thì nCuSO4 bị đp = a + 2b => nCuSO4 dư = x – a – 2b
\({{n}_{{{O}_{2}}}}=b=>{{n}_{{{H}^{+}}}}=4b\)
Khi nhúng Mg vào Y, vì khối lượng thanh không đổi nên: mMg pứ = mCu bị Mg đẩy ra
=> 24.(x – a – 2b + 2b) = 64.(x – a – 2b) (2)
Sau 2t giây thì ne = 4a + 8b => nH2 = 2a + 4b – x
Khí trong 2t giây = khí trong t giây đầu (0,15 mol) + H2 + O2
=> 0,15 + (2a + 4b – x) + (a/2 + b) = 0,393 (3)
Giải hệ (1), (2), (3) => a = 0,09; b = 0,06; x = 0,282
=> \({{m}_{CuS{{O}_{4}}.5{{H}_{2}}O}}=70,5\)
Chỉ dùng CO2 và nước có thể phân biệt được dãy các chất nào?
-
A.
Na, K, Ba
-
B.
Na, Ca, Al
-
C.
Ca, Fe; Cu
-
D.
K, Na, Ca
Đáp án : B
Xem lại lí thuyết kim loại kiềm thổ
Na, K, Ba đều hòa tan trong nước tạo dung dịch kiềm, nếu sục CO2 vào thì sẽ tạo kết tủa với dung dịch Ba(OH)2 => Không nhận biết được Na và K
Tương tự với K, Na, Ca.
Ca, Fe; Cu cho vào nước thì chỉ Ca tan thành Ca(OH)2 và sục CO2 vào thì tạo kết tủa còn Fe và Cu không hiện tượng => Không nhận biết được

Cho dd Ba(OH)2 lần lượt tác dụng với các dd sau: CaCl2, Ca(NO3)2, Ba(HSO4)2 , NaHSO4, Ca(HCO3)2, H2SO4, HCl. Số phản ứng tạo ra kết tủa là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Đáp án : B
Xem lại lí thuyết kim loại kiềm thổ
Ba(OH)2 phản ứng với các chất sinh ra kết tủa là: NaHSO4, Ba(HSO4)2, Ca(HCO3)2, H2SO4
Ba(OH)2 + 2NaHSO4 → BaSO4 ↓ + Na2SO4 + 2H2O
Ba(OH)2 + Ba(HSO4)2→ 2BaSO4 ↓ + 2H2O
Ba(OH)2 + H2SO4 → BaSO4 ↓ + 2CO2 + 2H2O
Ba(OH)2 + Ca(HCO3)2 → BaCO3 ↓ + CaCO3 + 2H2O
Nếu đun sôi nước cứng tạm thời sẽ thấy hiện tượng?
-
A.
Nước sôi.
-
B.
Chỉ thấy thoát khí CO2.
-
C.
Dung dịch chuyển màu xanh.
-
D.
Thấy thoát khí CO2 và đồng thời xuất hiện kết tủa trắng .
Đáp án : D
xem lại lí thuyết nước cứng
Mg(HCO3)2 \(\buildrel {{t^0}} \over
\longrightarrow \) MgCO3 ↓+ CO2 + H2O
Ca(HCO3)2 \(\buildrel {{t^0}} \over
\longrightarrow \) CaCO3 ↓+ CO2 + H2O
=> Hiện tượng là có khí CO2 bay ra và xuất hiện kết tủa của các ion Ca2+ và Mg2+
Sục từ từ V lít khí CO2 (đktc) từ từ vào 100 ml dung dịch hỗn hợp NaOH 2M; KOH 2M và Ba(OH)2 3 M. Kết thúc phản ứng thu được 39,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị lớn nhất của V thỏa mãn điều kiện của bài toán là
-
A.
8,96.
-
B.
4,48.
-
C.
17,92.
-
D.
13,44.
Đáp án : C
+) V lớn nhất khi có hiện tượng hòa tan kết tủa => thuộc trường hợp nCO2 < nOH- < 2.nCO2
nBaCO3 < nBa2+ => CO32- tạo hết thành kết tủa => nCO2 = nOH – nBaCO3
V lớn nhất khi có hiện tượng hòa tan kết tủa => thuộc trường hợp nCO2 < nOH- < 2.nCO2
nOH = nNaOH + nKOH + 2nBa(OH)2 = 1 mol
nBaCO3 = 0,2 mol < nBa2+ = 0,3 mol => CO32- tạo hết thành kết tủa
=> nCO2 = nOH – nBaCO3 = 1-0,2 = 0,8 mol
=> V = 17,92 lit
Cho Al đến dư vào dung dịch gồm NO3-, Cu2+, Fe3+, Ag+, sau phản ứng hoàn toàn thu được chất rắn X. Không kể phản ứng của Al với H2O trong X chứa
-
A.
Ag, Al
-
B.
Ag, Fe, Cu.
-
C.
Fe, Cu
-
D.
Ag, Fe, Cu, Al
Đáp án : D
xem lại lí thuyết nhôm
Al + 3Ag+ → Al3+ + Ag
Al + 3Fe3+ → Al3+ + 3Fe2+
2Al + 3Fe2+ → 3Fe + 2Al3+
2Al + 3Cu2+ → 2Al3+ + 3Cu
2Al + 3Fe2+ → 2Al3+ + 3Cu
Chất rắn gồm Ag, Fe, Cu, Al dư
Cho 8,6 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với lượng dư dung dịch HCl loãng, thu được 4,48 lít khí (đktc). Kim loại X, Y là
-
A.
Rb và Ba
-
B.
Liti và beri.
-
C.
Natri và Canxi.
-
D.
Ba và Cs.
Đáp án : C
+) ne nhận = ne cho = 2.nH2
+) \(\left\{ \matrix{
M = {m \over n} \hfill \cr
{n_{echo}} = n.\,hoa\,tri \hfill \cr} \right. = > M = {m \over {{n_{e.td}}}}hoa\,tri\)
Vì hh gồm 1 kim loại kiềm và 1 kim loại kiềm thổ => 1 < hóa trị trung bình < 2
=> khoảng giá trị M trung bình
2X + 2HCl → 2XCl + H2↑
Y + 2HCl → YCl2 + H2↑
nH2 = 0,2 mol
=> ne nhận = ne cho = 2.nH2 = 2.0,2= 0,4 mol
Ta có: \(\left\{ \matrix{
M = {m \over n} \hfill \cr
{n_{echo}} = n.\,hoa\,tri \hfill \cr} \right. = > M = {m \over {{n_{e.td}}}}hoa\,tri\)
Vì hh gồm 1 kim loại kiềm và 1 kim loại kiềm thổ => 1 < hóa trị trung bình < 2
=> 21,5 < ${\mathop M\limits^ - _{hh}}$ < 43
A sai vì cả hai kim loại đều có M > 43
B sai vì cả hai kim loại đều có M < 21,5
C đúng
D sai vì cả hai kim loại đều có M >43
→ Kim loại X, Y là Na, Ca
Trong các ion kim loại sau, ion kim loại có tính oxi hóa lớn nhất là?
-
A.
Na+
-
B.
Cu2+
-
C.
Al3+
-
D.
Fe3+
Đáp án : D
xem lại dãy điện hóa của kim loại
Theo dãy điện hóa, sắp xếp tính oxi hóa tăng dần : Na+< Al3+< Cu2+< Fe3+
=> ion kim loại có tính oxi hóa lớn nhất là Fe3+
Cho biết thế điện cực chuẩn của các cặp oxi hóa - khử Mg2+/Mg ; Zn2+/Zn ; Cu2+/Cu ; Ag+/Ag ; Hg2+/Hg lần lượt là –2,37 V; –0,76 V ; 0,34 V ; 0,8 V ; và 0,85 V. E0(pin) = 1,56 V là suất điện động chuẩn của pin nào trong số các pin sau ?
-
A.
Zn – Ag
-
B.
Mg – Zn
-
C.
Zn – Hg
-
D.
Mg – Hg
Đáp án : A
Công thức tính suất điện động của pin :Eopin = Eo(+) – Eo(-)
Ta có:\(\eqalign{
& {E^o}_{Zn - Ag}\; = {\rm{ }}{E^o}_{A{g^ + }/Ag}{\rm{ }}-{E^o}_{Z{n^{2 + }}/Zn}\;\,\, = 0,8{\rm{ }}-{\rm{ }}\left( {{\rm{ }} - {\rm{ }}0,76} \right){\rm{ }} = {\rm{ }}1,56{\rm{ }}V \cr
& {E^o}_{Mg - Zn}\; = {\rm{ }}{E^o}_{Z{n^{2 + }}/Zn}{\rm{ }}-{E^o}_{M{g^{2 + }}/Mg}\;\,\, = - {\rm{ }}0,76{\rm{ }}-{\rm{ }}\left( {{\rm{ }} - {\rm{ }}2,37} \right){\rm{ }} = {\rm{ }}1,61{\rm{ }}V \cr
& {E^o}_{Zn - Hg}\; = {\rm{ }}{E^o}_{H{g^{2 + }}/Hg}{\rm{ }}-{E^o}_{Z{n^{2 + }}/Zn}\;\,\, = 0,85{\rm{ }}-{\rm{ }}\left( {{\rm{ }}-{\rm{ }}0,76} \right){\rm{ }} = {\rm{ }}1,61{\rm{ }}V \cr
& {E^o}_{Mg - Hg}\; = {\rm{ }}{E^o}_{H{g^{2 + }}/Hg}{\rm{ }}-{E^o}_{M{g^{2 + }}/Mg}\;\,\, = 0,85{\rm{ }}-{\rm{ }}\left( {-2,37} \right){\rm{ }} = {\rm{ }}3,22{\rm{ }}V \cr} \)
Để điều chế K người ta có thể dùng phương pháp nào
-
A.
Điện phân dung dịch KCl có vách ngăn xốp.
-
B.
Dùng CO để khử K ra khỏi K2O.
-
C.
Điện phân nóng chảy KOH.
-
D.
Dùng Li để khử K ra khỏi dd KCl.
Đáp án : C
xem lại lí thuyết điều chế kim loại
Để điều chế K người ta dùng phương pháp điện phân nóng chảy muối và bazơ của Na
=>điện phân nóng chảy KOH
Phát biểu nào sau đây là đúng?
-
A.
Ăn mòn kim loại là sự phá hủy kim loại do tác động cơ học.
-
B.
Ăn mòn kim loại là sự hình thành kim loại do môi trường xung quanh tác dụng vào dung dịch muối.
-
C.
Ăn mòn kim loại là sự phá hủy kim loại do kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện.
-
D.
Ăn mòn kim loại là sự phá hủy kim loại do tác dụng hoá học của môi trường xung quanh.
Đáp án : D
xem lại lí thuyết ăn mòn kim loại
“Ăn mòn kim loại” là sự phá huỷ kim loại do tác dụng hoá học của môi trường xung quanh.
Al2O3 không tan được trong dung dịch chứa chất nào sau đây?
-
A.
HCl.
-
B.
NaCl.
-
C.
Ba(OH)2.
-
D.
HNO3
Đáp án : B
Dựa vào tính chất hóa học của Al2O3
+ Tác dụng được với dd axit, dd bazo
Al2O3 không phản ứng được với dd NaCl
Hòa tan hoàn toàn hỗn hợp gồm 0,25 mol Al2O3 và 0,4 mol BaO vào nước dư thu được dung dịch E. Nhỏ từ từ dung dịch HCl k (M) vào E, số mol kết tủa (y mol) thu được phụ thuộc vào số mol HCl phản ứng (x mol) được biểu diễn theo sơ đồ sau:

Giá trị của k là:
-
A.
2,0
-
B.
1,5
-
C.
2,5
-
D.
1,8
Đáp án : C
Nếu cho H+ tác dụng với dung dịch [Al(OH)4]- thì xảy ra 1 hoặc 2 phản ứng sau:
[Al(OH)4]- + H+ → Al(OH)3 + H2O (1)
Al(OH)3 + 3H+ → Al3+ + 3H2O (2)
*Phương pháp: Nếu đặt: n[Al(OH)4]- = a mol; nH+ = b mol thì:
+ Nếu b/a 1 thì: nAl(OH)3 = b
+ Nếu 1 < b/a < 4 thì kết tủa bị hoà tan 1 phần và: nAl(OH)3 = (4a – b)/3
+ Nếu b/a 4 thì không có kết tủa
BaO + H2O → Ba(OH)2
Mol 0,4 → 0,4
Al2O3 + Ba(OH)2 → Ba(AlO2)2 + H2O
Mol 0,25 → 0,25 → 0,25
=> số mol Ba(OH)2 dư = 0,4 – 0,25 = 0,15 mol
Vậy dung dịch E gồm: 0,3 mol OH- ; 0,5 mol AlO22- và Ba2+
Các phản ứng có thể xảy ra:
OH- + H+ → H2O
H+ + AlO2- + H2O → Al(OH)3
Al(OH)3 + 3H+ → Al3+ + 3H2O
Tại nHCl = 0,56k (mol) và 0,68k (mol) đều ở bên phải của đỉnh kết tủa (kết tủa max)
=> Lúc này, có sự hòa tan kết tủa bởi HCl nên ta sử dụng công thức:
nH+ = nOH- + 4nAlO2- - 3nAl(OH)3 => nAl(OH)3 = 1/3.[4nAlO2 - (nH+ - nOH)]
+ Tại nHCl = 0,56k (mol) => nAl(OH)3 = 3a (mol) = 1/3.[4nAlO2 - (nH+ - nOH)]
=> 3a.3 = 4.0,5 – (0,56k – 0,3) (1)
+ Tại nHCl = 0,68k (mol) => nAl(OH)3 = 2a (mol) = 1/3.[4nAlO2 - (nH+ - nOH)]
=> 2a.3 = 4.0,5 – (0,68k – 0,3) (2)
Giải hệ (1) và (2) => k = 2,5 (M)
Hòa tan hoàn toàn a gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO (trong đó oxi chiếm 7,99% về khối lượng) vào nước dư. Sau phản ứng, thu được dung dịch Y gồm NaOH, KOH và Ba(OH)2 có tỉ lệ mol tương ứng là 3: 2: 7 và 0,784 lít khí H2(đktc). Cho Y tác dụng với dung dịch gồm 0,02 mol Al2(SO4)3, 0,01 mol H2SO4 và 0,04 mol KHSO4 thu được m gam kết tủa. Giá trị của m là:
-
A.
24,17
-
B.
17,87
-
C.
17,09
-
D.
18,65
Đáp án : D
Cho biết nAl3+ = a và nOH- = b, tính số mol kết tủa:
+ Với muối nhôm
Các phản ứng xảy ra:
Al3+ + 3OH- → Al(OH)3 (1)
Al(OH)3 + OH- → [Al(OH)4]- (2)
Phương pháp:
Từ (1) và (2) ta rút ra kết luận:
+ Nếu b/a ≤ 3 thì kết tủa chưa bị hoà tan và
nAl(OH)3= b/3
+ Nếu 3 < b/a < 4 thì kết tủa bị hoà tan 1 phần
Al3+ + 3OH- → Al(OH)3 (1)
mol a → 3a → a
Al(OH)3 + OH- → [Al(OH)4]- (2)
Mol b-3a b-3a
nAl(OH)3= 4a-b
+ Nếu b/a ≥ 4 thì kết tủa bị hoà tan hoàn toàn
Qui đổi hỗn hơp thành Na (3u mol) ; K (2u mol) ; Ba (7u mol) và O (v mol)
(Vì sau khi cho vào nước thu được nNaOH: nKOH: nBa(OH)2 = 3: 2: 7 = 3u: 2u: 7u)
Bảo toàn electron: nNa + nK + 2nBa = 2nO + 2nH2
=> 3u + 2u + 2.7u = 2v + 0,035.2
Lại có: %mO = 7,99% => 16v = 7,99%.(23.3u + 39.2u + 137.7u + 16v)
Giải hệ PT => u = 0,01 ; v = 0,06 mol
=> nOH = 2v + 0,035.2 = 0,19 mol
nH+ = 2nH2SO4 + nKHSO4 = 2.0,01 + 0,04 = 0,06 mol
nAl3+ = 2nAl2(SO4)3 = 0,04 mol
=> nAl(OH)3 = 4nAl3+ - (nOH – nH+)
=> nAl(OH)3 = 0,03 mol
nBa2+ = 0,07 mol và nSO4 = 0,11 mol
=> nBaSO4 = nBa = 0,07 mol
=> mrắn = mBaSO4 + mAl(OH)3 = 18,65g
Kim loại nào sau đây không phải kim loại kiềm
-
A.
Ca
-
B.
K
-
C.
Cs
-
D.
Li
Đáp án : A
Xem lại các kim loại kiềm nhóm IA
Ca là kim loại kiềm thổ
Cho 1,82 g một kim loại kiềm tác dụng hết với 48,44 gam nước, sau phản ứng thu được 2,912 lít khí H2 (đktc) và dung dịch X. Kim loại kiềm và nồng độ phần trăm dung dịch X là
-
A.
Li; 44%.
-
B.
Na; 31,65 %.
-
C.
Li; 12,48 %.
-
D.
Na; 44%.
Đáp án : C
Viết PTHH và tính toán theo PTHH; bảo toàn khối lượng
nH2 = 2,912:22,4 = 0,13 mol
2A + 2H2O → 2AOH + H2
0,26 ← 0,26 ← 0,13 (mol)
=> MA = 1,82 : 0,26 = 7 (Li)
mLiOH = 0,26.24 = 6,24 (g)
BTKL: m dd sau pư = mKL + mH2O – mH2 = 1,82 + 48,44 – 0,13.2 = 50 (g)
C%LiOH = 6,24.100%/50 = 12,48%
Kim loại nào sau đây là kim loại kiềm?
-
A.
Ba.
-
B.
Ca.
-
C.
Al.
-
D.
Cs.
Đáp án : D
Dựa vào kiến thức về đại cương kim loại
Cs là kim loại kiềm
Dựa vào khối lượng riêng của kim loại, hãy tính thể tích mol kim loại và ghi kết quả vào bảng sau:

Chọn phát biểu không đúng trong các phát biểu sau:
-
A.
Thể tích mol của K là 45,46 cm3.
-
B.
Thể tích mol của Mg là 19,73 cm3.
-
C.
Thể tích mol của Al là 9,99 cm3.
-
D.
Thể tích mol của Au là 10,20 cm3.
Đáp án : B
Xét 1 mol chất có m = M (g)
Thể tích mol là: \(V = \frac{m}{D} \Leftrightarrow V = \frac{M}{D}\)
Chú ý: Lấy giá trị M các nguyên tố trong bảng tuần hoàn các nguyên tố hóa học.
Xét 1 mol chất có m = M (g)
Thể tích mol là: \(V = \frac{m}{D} \Leftrightarrow V = \frac{M}{D}\)
Chú ý: Lấy giá trị M các nguyên tố trong bảng tuần hoàn các nguyên tố hóa học.
Áp dụng công thức để tính thể tích mol ta được kết quả như bảng sau:
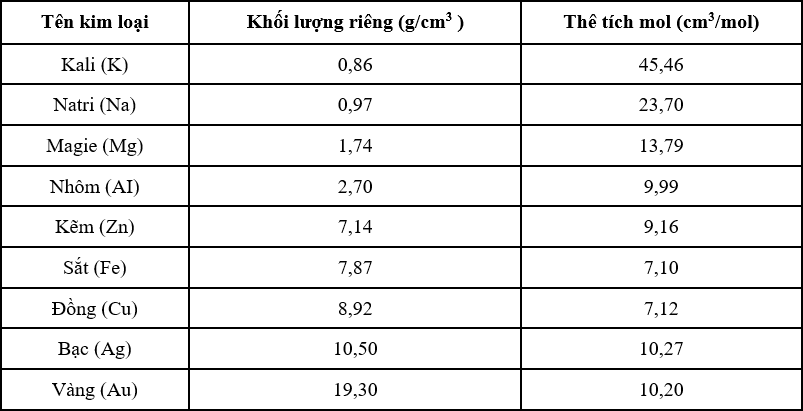
Từ bảng kết quả trên ta thấy thể tích mol của Mg là 13,79 cm3 không phải là 19,73 cm3.
Phát biểu nào sau đây là đúng khi nói về ăn mòn hoá học ?
-
A.
Ăn mòn hoá học làm phát sinh dòng điện một chiều.
-
B.
Kim loại tinh khiết sẽ không bị ăn mòn hoá học.
-
C.
Về bản chất, ăn mòn hóa học cũng là một dạng của ăn mòn điện hoá.
-
D.
Ăn mòn hoá học không làm phát sinh dòng điện.
Đáp án : D
A sai vì ăn mòn hóa học không làm phát sinh dòng điện.
B sai vì kim loại tinh khiết vẫn có thể bị ăn mòn hóa học.
C sai vì ăn mòn hóa học không phải là ăn mòn điện hóa.
D đúng
Hỗn hợp X gồm Fe3O4 và Al có tỉ lệ mol tương ứng là 1 : 3 thực hiện phản ứng nhiệt nhôm X (không có không khí) đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm
-
A.
Al,Fe,Fe3O4 và Al2O3.
-
B.
Al2O3,Fe và Fe3O4.
-
C.
Al2O3và Fe.
-
D.
Al,Fe và Al2O3.
Đáp án : D
Cách xác định chất hết - chất dư
Đề bài cho số mol của A và B.
PTHH: aA + bB → cC + dD
Ta so sánh tỉ lệ: \(\frac{{{n_A}}}{a}\) và \(\frac{{{n_B}}}{b}\). Nếu tỉ lệ nào nhỏ hơn thì chất đó phản ứng hết, chất còn lại dư.
3Fe3O4 + 8Al \(\xrightarrow{{{t^0}}}\) 9Fe + 4Al2O3
Ban đầu: 1 3
Ta thấy: 1/3 < 3/8 nên Fe3O4 phản ứng hết, Al còn dư.
Vậy sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm Fe, Al2O3 và Al dư.
Cho ba kim loại là Al, Fe, Cu và bốn dung dịch muối riêng biệt là ZnSO4, AgNO3, CuCl2, MgSO4. Kim loại nào tác dụng được với cả bốn dung dịch muối đã cho ?
-
A.
Al.
-
B.
Fe.
-
C.
Cu.
-
D.
Không kim loại nào tác dụng được.
Đáp án : D
Dựa vào lí thuyết bài tính chất của kim loại, dãy điện hóa của kim loại.

Kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối

→ Tính khử kim loại Mg > Al > Zn > Fe > Cu > Ag
Vậy nên không có kim loại nào tác dụng được với cả 4 dung dịch muối đã cho.
Hòa tan hoàn toàn m gam hỗn hợp X gồm Mg, Al, Zn trong 500 ml dung dịch HNO3 4M, sau phản ứng hoàn toàn thu được dung dịch Y và 4,48 lít (đktc) hỗn hợp gồm hai khí không màu có tỉ khối so với H2 là 18,5 trong đó có 1 khí hóa nâu ngoài không khí. Trung hòa dung dịch Y bằng lượng vừa đủ 100 ml dung dịch NaOH 1M, thu được dung dịch Z. Cô cạn Z, thu được 134,5 gam muối khan. Giá trị của m là
-
A.
30,0.
-
B.
29,4.
-
C.
30,6.
-
D.
29,0.
Đáp án : D
Từ dữ kiện bài toán => 2 khí
Sơ đồ bài toán:
\(m(g)\left\{ \matrix{
Mg \hfill \cr
Al \hfill \cr
Zn \hfill \cr} \right. + HN{O_3}:2 \to \left| \matrix{
{\rm{dd}}\,Y\left\{ \matrix{
M{g^{2 + }} \hfill \cr
A{l^{3 + }} \hfill \cr
Z{n^{2 + }} \hfill \cr
N{H_4}^ + \hfill \cr
{H^ + } \hfill \cr
N{O_3}^ - \hfill \cr} \right.\buildrel { + NaOH:0,1} \over
\longrightarrow \underbrace {Muoi}_{134,5(g)} + \underbrace {{H_2}O}_{0,1(mol)} \hfill \cr
Khi\left\{ \matrix{
NO \hfill \cr
{N_2}O \hfill \cr} \right. \hfill \cr} \right.\)
Áp dụng định luật bảo toàn khối lượng, bảo toàn nguyên tố, bảo toàn e để giải bài toán
M khí = 37
Khí hóa nâu ngoài không khí là NO (M = 30) => Khí còn lại có M > 37
Vì khí không màu nên khí đó là N2O
Giả sử khí gồm NO (x mol) và N2O (y mol)
Giải hệ: n khí = x + y = 0,2 và m khí = 30x + 44y = 0,2.27 được x = y = 0,1
Trung hòa dd Y cần vừa đủ 0,1 mol NaOH nên ta có nHNO3 = nNaOH = 0,1 mol
Sơ đồ bài toán:
\(m(g)\left\{ \matrix{
Mg \hfill \cr
Al \hfill \cr
Zn \hfill \cr} \right. + HN{O_3}:2 \to \left| \matrix{
{\rm{dd}}\,Y\left\{ \matrix{
M{g^{2 + }} \hfill \cr
A{l^{3 + }} \hfill \cr
Z{n^{2 + }} \hfill \cr
N{H_4}^ + \hfill \cr
{H^ + }:0,1 \hfill \cr
N{O_3}^ - \hfill \cr} \right.\buildrel { + NaOH:0,1} \over
\longrightarrow \underbrace {Muoi}_{134,5(g)} + \underbrace {{H_2}O}_{0,1(mol)} \hfill \cr
Khi\left\{ \matrix{
NO:0,1 \hfill \cr
{N_2}O:0,1 \hfill \cr} \right. \hfill \cr} \right.\)
+ Xét phản ứng của dd Y với NaOH:
m ion dd Y = m muối + mH2O - mNaOH = 134,5 + 0,1.18 - 0,1.40 = 132,3 (g)
+ Ta có công thức: nHNO3 = nHNO3 dư + 4nNO + 10nN2O + 10nNH4NO3
=> 2 = 0,1 + 4.0,1 + 10.0,1 + 10nNH4NO3 => nNH4NO3 = 0,05 mol
+ BTNT "N": nHNO3 = nNH4+ + nNO3- + nNO + 2nN2O
=> 2 = 0,05 + nNO3- (dd Y) + 0,1 + 2.0,1 => nNO3 (dd Y) = 1,65 mol
Ta có: m = mKL = m ion KL = m ion dd Y - mNH4+ - mH+ - mNO3-
= 132,3 - 0,05.18 - 0,1 - 1,65.62 = 29 gam
>> 2K8 Chú ý! Lộ Trình Sun 2026 - 3IN1 - 1 lộ trình ôn 3 kì thi (Luyện thi 26+ TN THPT, 90+ ĐGNL HN, 900+ ĐGNL HCM, 70+ ĐGTD - Click xem ngay) tại Tuyensinh247.com.Đầy đủ theo 3 đầu sách, Thầy Cô giáo giỏi, luyện thi theo 3 giai đoạn: Nền tảng lớp 12, Luyện thi chuyên sâu, Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |










Danh sách bình luận