30 bài tập luyện tập về tỉ khối của chất khí có lời giải
Làm đề thiCâu hỏi 1 :
Biểu thức tính tỉ khối của chất A đối với không khí là:
- A
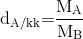
- B
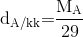
- C
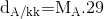
- D
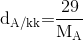
Đáp án: B
Lời giải chi tiết:
Biểu thức tính tỉ khối của chất A đối với không khí là: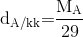
Đáp án B
Câu hỏi 2 :
Dãy các chất khí đều nặng hơn không khí là:
- A SO2, Cl2, H2S
- B N2, CO2, H2
- C CH4, H2S, O2
- D Cl2, SO2, N2
Đáp án: A
Lời giải chi tiết:
Dãy các chất khí đều nặng hơn không khí là: SO2, Cl2, H2S
B có N2( M=28) và H2(M=2) nhẹ hơn không khí
C có CH4 có M =16 nhẹ hơn không khí
D có N2 nhẹ hơn không khí
Đáp án A
Câu hỏi 3 :
Bằng cách nào có thể biết được khí A nặng hay nhẹ hơn khí B?
- A
Ta so sánh khối lượng mol của khí A với khối lượng mol của không khí.
- B
Ta so sánh khối lượng mol của khí A với khối lượng mol của khí B.
- C
Ta so sánh khối lượng mol của khí A với khối lượng mol của khí oxi.
- D Ta so sánh khối lượng mol của khí A với khối lượng mol của khí hiđro
Đáp án: B
Lời giải chi tiết:
Để có thể biết được khí A nặng hay nhẹ hơn khí B, ta so sánh khối lượng mol của khí A với khối lượng mol của khí B.
Đáp án B
Câu hỏi 4 :
Oxi có tỉ khối đối với không khí là:
- A
1,1
- B 1,2
- C 1,3
- D 1,4
Đáp án: A
Lời giải chi tiết:
MO2 = 32 => dO2/kk = 32/29 = 1,1
Câu hỏi 5 :
Tỉ khối của hỗn hợp chứa 3,36 lít khí H2 và 6,72 lít khí N2 ở đktc so với heli là:
- A 4,83
- B 18,33
- C 33,18
- D 33,19
Đáp án: A
Lời giải chi tiết:
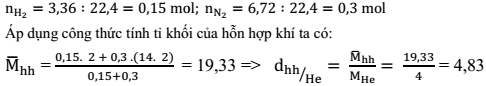
Câu hỏi 6 :
B là oxit của nitơ có tỷ khối hơi so với mêtan (CH4) là 1,875. B có công thức phân tử là:
- A NO2
- B N2O
- C N2O4
- D NO
Đáp án: D
Lời giải chi tiết:
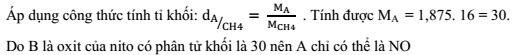
Câu hỏi 7 :
A là oxit của lưu huỳnh có tỉ khối hơi so với Ne là 3,2. Vậy A có công thức phân tử là:
- A SO2
- B CO2
- C SO3
- D NO2
Đáp án: A
Lời giải chi tiết:
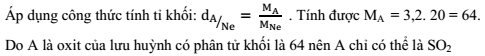
Câu hỏi 8 :
Tỉ khối của hỗn hợp chứa 4 g metan và 7 g khí etilen so với không khí là:
- A 22/28
- B 22/29
- C 29/21
- D 29/22
Đáp án: B
Lời giải chi tiết:
nCH4 = 4 : 16 = 0,25 mol; nC2H4 = 7 : 28 = 0,25 mol
\({\overline M _{hh}} = \frac{{{m_{C{H_4}}} + {m_{{C_2}{H_4}}}}}{{{n_{C{H_4}}} + {n_{{C_2}{H_4}}}}} = \frac{{4 + 7}}{{0,25 + 0,25}} = 22\)
\( \Rightarrow {d_{hh/kk}} = \frac{{{{\overline M }_{hh}}}}{{{M_{kk}}}} = \frac{{22}}{{29}}\)
Đáp án B
Câu hỏi 9 :
B là oxit của nitơ có tỷ khối hơi so với khí cacbonic (CO2) là 1. B có công thức phân tử là:
- A NO2
- B N2O
- C N2O4
- D NO
Đáp án: B
Lời giải chi tiết:
Đáp án B
Áp dụng công thức tính tỉ khối:
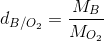
Tính được MB = 1. 44 = 44
Do B là oxit của nito có phân tử khối là 44 nên A chỉ có thể là N2O
Câu hỏi 10 :
A là oxit của lưu huỳnh có tỉ khối hơi so với phân tử oxi là 2. Vậy A có công thức phân tử là:
- A S
- B SO2
- C SO3
- D NO2
Đáp án: B
Lời giải chi tiết:
Đáp án: B
Áp dụng công thức tính tỉ khối: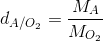 . Tính được MA = 2. 32 = 64.
. Tính được MA = 2. 32 = 64.
Do A là oxit của lưu huỳnh có phân tử khối là 64 nên A chỉ có thể là SO2
Câu hỏi 11 :
Một halogen X có tỉ khối hơi đối với canxi bằng 4. Xác định ký hiệu và tên gọi.
- A Clo, Cl
- B Brom, Br
- C iot, I
- D Flo, F
Đáp án: B
Lời giải chi tiết:
Đáp án: B
Halogen có công thức phân tử là X2.
Áp dụng công thức tính tỉ khối:
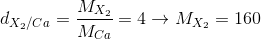
X2 = 160 => 2X = 160 => X = 80X là brom, kí hiệu Br
Câu hỏi 12 :
Có những khí sau: N2, O2, Cl2, CO, CO2,SO2. Những khí nặng hơn không khí là:
- A
N2, O2, Cl2, CO
- B
O2, Cl2, CO2 , SO2
- C N2, O2, Cl2, SO2.
- D N2, Cl2, CO, SO2
Đáp án: B
Lời giải chi tiết:
Không khí có khối lượng mol là 29
Những khí nặng hơn không khí là: O2, Cl2, CO2 , SO2
Đáp án B
Câu hỏi 13 :
Có thể thu được những khí nào vào bình ( từ những thí nghiệm trong phòng thí nghiệm): khí H2, N2, CH4, O2 bằng cách đặt đứng bình?
- A H2
- B CH4
- C N2
- D O2
Đáp án: D
Lời giải chi tiết:
Những chất khí nặng hơn không khí thì ta thu bằng cách đặt đứng bình
→ O2 có khối lượng mol là 32 nặng hơn không khí
Đáp án D
Câu hỏi 14 :
Cho hình vẽ thu khí như sau: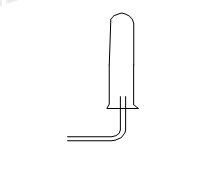
Những khí nào trong số các khí H2, N2, NH3 ,O2, Cl2, CO2,HCl, SO2, H2S có thể thu được theo cách trên?
- A
Chỉ có khí H2
- B
H2, N2, NH3,
- C O2, N2, H2,Cl2, CO2
- D Tất cả các khí trên.
Đáp án: B
Lời giải chi tiết:
Để thu khí bằng úp ngược bình thì khí đấy phải nhẹ hơn không khí
→ chọn khí H2, N2, NH3
Đáp án B
Câu hỏi 15 :
Khí N2 nặng hơn khí H2 bằng bao nhiêu lần? (N = 14, H = 1)
- A 10 lần.
- B 12 lần.
- C 8 lần.
- D 14 lần.
Đáp án: D
Phương pháp giải:
Lấy phân tử khối của N2 chia cho phân tử khối của H2
Lời giải chi tiết:
Phân tử khối của N2 = 14×2 = 28 (gam/mol)
Phân tử khối của H2 = 2×1 = 2 (gam/mol)
Suy ra
\({d_{{N_2}/{H_2}}} = {{28} \over 2} = 14\)
Vậy N2 nặng hơn H2 14 lần
Đáp án D
Câu hỏi 16 :
Khí nào có thể thu được bằng cách đặt ngược bình (hình vẽ):
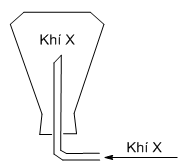
- A Khí Cacbonic (CO2).
- B Khí Oxi (O2).
- C Khí Clo (Cl2).
- D Khí Hiđro (H2).
Đáp án: A
Phương pháp giải:
Khí thu được bằng cách đặt úp bình => khí này có phân tử khối nặng hơn không khí (Mkk≈ 29 g/mol)
Lời giải chi tiết:
Khí thu được bằng cách đặt úp bình => khí này có phân tử khối nặng hơn không khí
=> khí X là khí CO2 (MCO2 = 44 g/mol)
Đáp án A
Câu hỏi 17 :
Biết d A/B = 1,5 nhận xét không đúng là:
- A Khí A nhẹ hơn khí B 1,5 lần
- B Khí A nặng hơn khí B 1,5 lần
- C MA =1,5.MB
- D cả B và C đều đúng
Đáp án: A
Phương pháp giải:
Dựa vào kiến thức được học về tỉ khối của chất khí sgk hóa 8 – trang 68
Lời giải chi tiết:
Vì d A/B =1,5 nên A nặng hơn khí B 1,5 lần
Vậy phát biểu không đúng là A
Đáp án A
Câu hỏi 18 :
Khí nào trong số các khí sau được thu bằng cách đẩy kk úp bình?
- A
Khí CO2
- B Khí Cl2
- C Khí H2
- D Khí O2
Đáp án: C
Lời giải chi tiết:
Vì khí hiđrô có MH2 = 2 , nhẹ hơn kk; Khí CO2, Cl2 đều nặng hơn kk nên không thu được bằng cách trên mà phải ngửa ống nghiệm.
Câu hỏi 19 :
Tỉ khối của hỗn hợp chứa N2 và O2 theo tỉ lệ vê thể tích là 1: 2 so với không khí là:
- A 92/87
- B 87/92
- C 82/97
- D 97/82
Đáp án: A
Lời giải chi tiết:
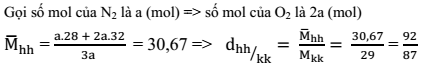
Câu hỏi 20 :
Tỉ khối của hỗn hợp chứa N2 và O3 theo tỉ lệ 1: 2 so với không khí là:
- A 128/47
- B 124/87
- C 127/48
- D 148/27
Đáp án: B
Lời giải chi tiết:
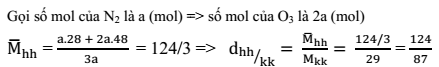
Câu hỏi 21 :
Ở đktc, 0,5 lít khí X có khối lượng là 1,25 (g)
Câu 1: Khối lượng mol phân tử của khí X là:
- A 24
- B 65
- C 56
- D 64
Đáp án: C
Lời giải chi tiết:
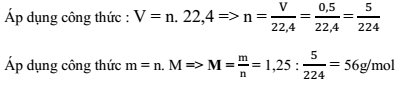
Câu 2: Tỉ khối hơi của X đối với không khí với CO2 và đối với CH4 lần lượt là:
- A 1,93; 1,27; 3,5
- B 1,92; 1,25; 3,7
- C 1,25; 3,6; 1,92
- D 3,5; 1,27; 1,93
Đáp án: A
Lời giải chi tiết:

Câu hỏi 22 :
A là hợp chất CxHy có tỷ khối hơi đối với H2 là 15 biết cacbon chiếm 80% khối lượng phân tử. Công thức phân tử của CxHy là:
- A CH4
- B C2H6
- C C3H8
- D C2H2
Đáp án: B
Lời giải chi tiết:
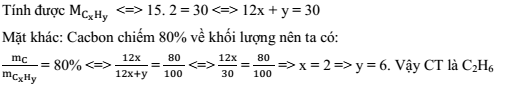
Câu hỏi 23 :
Tỉ khối của khí B đối với oxi là 0,5 và tỉ khối của khí A đối với khí B là 2,125. Tìm khối lượng mol của khí A.
- A 34
- B 43
- C 35
- D 53
Đáp án: A
Lời giải chi tiết:
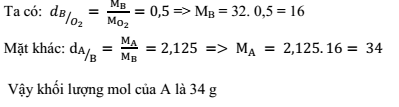
Câu hỏi 24 :
A và B đều là oxit được tạo bởi nguyên tố X và oxi có dạng XOm. Biết trong B có nhiều nguyên tử oxi hơn trong A là 1. Trong A phần trăm khối lượng của oxi chiếm 50% và tỉ khối của A so với phân tử O2 bằng 2. Công thức của A và B lần lượt là:
- A CO và CO2
- B NO và NO2
- C SO2 và SO3
- D FeO và Fe2O3
Đáp án: C
Lời giải chi tiết:
Đáp án: C
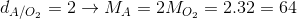
Trong hợp chất A:\(\% {\text{ }}{m_O} = \frac{{16m}}{{64}}.100\% {\text{ }} = {\text{ }}50\% {\text{ }} = > {\text{ }}m{\text{ }} = {\text{ }}2\)
Lại có: M A = X + 16 . 2 = 64 => X = 32 là lưu huỳnh
Vậy CTHH của A là: SO2 => B là: SO3
Câu hỏi 25 :
Một halogen X có tỉ khối hơi đối với khí axetilen (C2H2) bằng 2,731). Xác định ký hiệu và tên gọi.
- A Clo, Cl
- B Brom, Br
- C iot, I
- D Flo, F
Đáp án: A
Lời giải chi tiết:
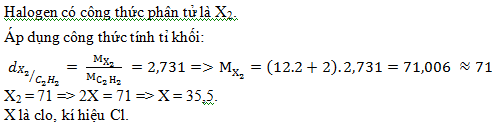
Câu hỏi 26 :
Hợp chất A gồm 2 nguyên tố lưu huỳnh và oxi có dA/ H2 = 32.
Câu 1: Công thức của A là:
- A SO2
- B SO3
- C SO
- D S2O
Đáp án: A
Phương pháp giải:
Phương pháp :
→ MA→ thử chọn đáp án
Lời giải chi tiết:
Hướng dẫn giải
MA = 32 .2 =64
→A là SO2
Đáp án A
Câu 2: Phần trăm nguyên tố lưu huỳnh có trong hợp chất A là:
- A 25%
- B 75%
- C 50%
- D 60%
Đáp án: C
Phương pháp giải:
Phương pháp:
Lời giải chi tiết:
Hướng dẫn giải :
Phần trăm nguyên tố lưu huỳnh có trong hợp chất A là: 32 : 64 .100% =50%
Đáp án C
Câu hỏi 27 :
Khí nào trong số các khí sau được thu bằng cách đẩy không khí để ngửa bình
- A Khí CO2
- B Khí N2
- C Khí H2
- D Khí NH3
Đáp án: A
Phương pháp giải:
Để ngửa bình chỉ áp dụng trong trường hợp khí nặng hơn không khí (tức có khối lượng phân tử > 29)
Lời giải chi tiết:
Để ngửa bình chỉ áp dụng trong trường hợp khí nặng hơn không khí
Trong các khí trên chỉ có khí CO2 nặng hơn không khí
Đáp án A
Câu hỏi 28 :
Khí nào trong số các khí sau được thu bằng cách đẩy không khí úp bình?
- A Khí CO2
- B Khí CuCl2
- C H2
- D Khí O2
Đáp án: C
Phương pháp giải:
Ta chỉ thu khí bằng cách úp bình khi khí đó nhẹ hơn không khí (tức phân tử khối nhỏ hơn 29)
Lời giải chi tiết:
Ta chỉ thu khí bằng cách úp bình khi khí đó nhẹ hơn không khí
Chỉ có khí H2 nhẹ hơn không khí
Đáp án C
Câu hỏi 29 :
Hỗn hợp khí SO2 và O2 có tỉ khối so với CH4 là 3. Thể tích khí O2 cần thêm vào 4,48 lít hỗn hợp trên (đktc) để có tỉ khối so với CH4 giảm còn 2,8 là:
- A 2,24 lít
- B 1,12 lít
- C 11,2 lít
- D 22,4 lít
Đáp án: B
Lời giải chi tiết:
Gọi số mol của SO2 và O2 lần lượt là a, b (mol)
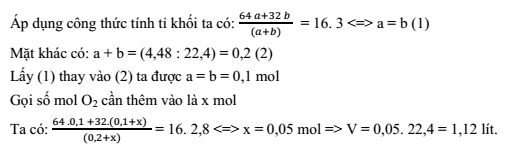
Câu hỏi 30 :
Hỗn hợp khí CO và CO2 có tỉ khối so với O2 là 1. Thể tích khí CO2 cần thêm vào 8,96 lít hỗn hợp trên (đktc) để có tỉ khối so với O2 tăng lên bằng 1,075 là:
- A 2,24 lít
- B 1,12 lít
- C 11,2 lít
- D 22,4 lít
Đáp án: A
Lời giải chi tiết:
Đáp án: A
Gọi số mol của CO và CO2 lần lượt là a, b (mol)
Áp dụng công thức tính tỉ khối ta có: \(\frac{{28a + 44b}}{{\left( {a + b} \right)}} = {\text{ }}1\,.\,32 < = > {\text{ }}a{\text{ }} = {\text{ }}3b{\text{ }}\left( 1 \right)\)
Mặt khác có: a + b = (8,96 : 22,4) = 0,4 (2)
Lấy (1) thay vào (2) ta được b = 0,1 mol và a=0,3 mol
Gọi số mol CO2 cần thêm vào là x mol
Ta có:\(\frac{{28.0,3 + 44\left( {0,1 + x} \right)}}{{\left( {0,4 + x} \right)}} = {\text{ }}1,075.32{\text{ }} < = > {\text{ }}x{\text{ }} = {\text{ }}0,1{\text{ }}mol\)
=> V = 0,1. 22,4 = 2,24 lít.
Các bài khác cùng chuyên mục
- 20 câu hỏi vận dụng về cân bằng phương trình hóa học có lời giải
- 15 câu hỏi cân bằng phương trình hóa học theo phương pháp chẵn lẽ có lời giải
- 20 bài tập vận dụng về định luật bảo toàn khối lượng có lời giải (phần 2)
- 20 bài tập vận dụng về định luật bảo toàn khối lượng có lời giải (phần 1)
- 20 câu hỏi luyện tập về mol có lời giải













