20 bài tập vận dụng về định luật bảo toàn khối lượng có lời giải (phần 2)
Làm đề thiCâu hỏi 1 :
Đốt cháy hoàn toàn 13,4 gam hỗn hợp X gồm: Fe, Al và Cu trong 2,24 lít khí O2 (đktc), sau phản ứng thu được m gam chất rắn. Giá trị của m là: (biết oxi phản ứng hết)
- A 16,6 gam.
- B 13,4 gam.
- C 22,2 gam.
- D 14,8 gam.
Đáp án: A
Phương pháp giải:
Áp dụng định luật bảo toàn khối lượng: mRắn = m hh X + mO2 = ? (gam)
Lời giải chi tiết:
\({n_{{O_2}}} = \frac{{2,24}}{{22,4}} = 0,1\,(mol)\) => mO2 = 0,1.32 = 3,2 (g)
Hỗn hợp X + O2 → hỗn hợp oxit
Áp dụng định luật bảo toàn khối lượng ta có:
mRắn = m hh X + mO2 = 13,4 + 3,2 = 16,6 (g)
Đáp án A
Câu hỏi 2 :
Đốt cháy hoàn toàn 4,5 gam kim loại Mg trong khí oxi, sau phản ứng được 7,5 gam hợp chất MgO. Khối lượng của oxi đã tham gia phản ứng là
- A 12,0 gam.
- B 3,0 gam.
- C 4,5 gam.
- D 5,5 gam.
Đáp án: B
Phương pháp giải:
Áp dụng định luật bảo toàn khối lượng ta có:
mMg + mO2 = mMgO
=> mO2 = mMgO - mMg = ? (g)
Lời giải chi tiết:
2Mg + O2 \(\xrightarrow{{{t^0}}}\) 2MgO
Áp dụng định luật bảo toàn khối lượng ta có:
mMg + mO2 = mMgO
=> mO2 = mMgO - mMg = 7,5 – 4,5 = 3 (gam)
Đáp án B
Câu hỏi 3 :
Đốt cháy hoàn toàn 12 gam cacbon trong không khí thu được 44 gam khí cacbon đioxit (CO2). Khối lượng oxi đã tham gia phản ứng là:
- A 3,2 gam
- B 32 gam
- C 0,32 gam
- D 1,6 gam
Đáp án: B
Phương pháp giải:
áp dụng định luật bảo toàn khối lượng.
Lời giải chi tiết:
Bảo toàn khối lượng có mO2 = mCO2 –mC = 44-12 =32 g
Đáp án B
Câu hỏi 4 :
Cho 16,8 kg khí cacbon oxit (CO) tác dụng hết với 32 kg sắt (III) oxit Fe2O3 thì thu được kim loại sắt và 26,4 kg CO2. Khối lượng sắt thu được là:
- A 2,24 kg
- B 22,8 kg
- C 29,4 kg
- D 22,4 kg
Đáp án: D
Phương pháp giải:
Phương pháp :
Bảo toàn khối lượng
Lời giải chi tiết:
Hướng dẫn giải
Bảo toàn khối lượng có mCO + moxit sắt = mCO2 +mFe → mFe = 22,4
Đáp án D
Câu hỏi 5 :
Cho hỗn hợp gồm 2 muối A2SO4 và BSO4 có khối lượng 44,2 gam tác dụng vừa đủ với 62,4 gam BaCl2 trong dung dịch thì cho 69,9 gam kết tủa BaSO4 và 2 muối tan. Tính khối lượng của 2 muối tan ?
Lời giải chi tiết:
Phương pháp giải : áp dụng định luật bảo toàn khối lượng
Lời giải :
Áp dụng định luật bảo toàn khối lượng ta có
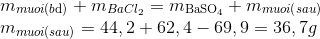
Câu hỏi 6 :
Đốt cháy hoàn toàn m (g) C2H2 cần 8 (g) khí O2 thu được 8,8 (g) khí CO2 và 1,8 (g) H2O. Giá trị của m là:
- A 2,6 gam
- B 15,2 gam
- C 1 gam
- D 6,2 gam
Đáp án: A
Phương pháp giải:
áp dụng định luật bảo toàn khối lượng
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng ta có m+ 8= 8,8 +1,8 => m=2,6 g
Đáp án A
Câu hỏi 7 :
Đốt cháy hoàn toàn m gam CH4 cần dùng 0,4 gam O2 thu được 1,4 gam CO2 và 1,6 gam H2O. Giá trị của m là:
- A 2,6 g
- B 1,7 g
- C 2,5 g
- D 1,6 g
Đáp án: A
Phương pháp giải:
bảo toàn khối lượng
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng thì \({m_{C{H_4}}} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}\)
Suy ra m =1,6 +1,4 -0,4 =2,6 g
Đáp án A
Câu hỏi 8 :
Đốt cháy hoàn toàn m gam kim loại Na bằng 3,2 gam oxi thu được 12,4 gam natri oxit. Gía trị m là:
- A 2,9 gam
- B 9,2 gam
- C 15,6 gam
- D 16,5 gam
Đáp án: B
Phương pháp giải:
Bảo toàn khối lượng
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng thì mNa + mO2= moxit
Ta có m = 12.4-3.2=9.2 g
Đáp án B
Câu hỏi 9 :
Đốt cháy 4 g chất M cần 12,8 g khí oxi và thu được khí CO2 và hơi nước theo tỉ lệ mCO2 : mH2O = 11 : 3. Khối lượng của CO2 và H2O lần lượt là:
- A 11g và 3g
- B 13,2 g và 3,6g
- C 12,32g và 3,36
- D 5,5 g và 1,5 g
Đáp án: B
Phương pháp giải:
PTHH: M + O2 → CO2 + H2O
Gọi khối lượng của CO2 và H2O lần lượt là 11a và 9a
BTKL ta có: mM + mO2 = mCO2 + mH2O → thay số vào tìm được a = ?
Lời giải chi tiết:
Gọi khối lượng của CO2 và H2O lần lượt là 11a và 3a
Áp dụng định luật bảo toàn khối lượng
mM + mO2 = mCO2 + mH2O
=> 4 + 12,8 = 11a + 3a
=> 16,8 = 14a => a = 1,2
=> mCO2 = 13,2g và mH2O = 3,6g
Đáp án B
Câu hỏi 10 :
Cho 6,5 gam kẽm vào dung dịch axit clohiđric sẽ tạo thành 13,6 gam muối kẽm clorua và 0,2 gam khí hiđro. Khối lượng dung dịch axit clohiđric đã dùng là:
.
- A 6,9g
- B 7,3 g
- C 9,6 g
- D 19,9 g
Đáp án: B
Phương pháp giải:
BTKL ta có: mZn + mHCl phản ứng = mZnCl2 + mH2 => mHCl = ?
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng
mZn + mHCl phản ứng = mZnCl2 + mH2
=> mHCl = mZnCl2 + mH2 – mZn = 13,6+ 0,2 – 6,5= 7,3(g)
Đáp án B
Câu hỏi 11 :
Cho biết khối lượng canxi cacbonat bằng 100 kg, khối lượng khí cacbonic sinh ra bằng 44 kg. Khối lượng vôi sống tạo thành là:
- A 55 kg
- B 60 kg
- C 56 kg
- D 60kg
Đáp án: C
Phương pháp giải:
áp dụng định luật bảo toàn khối lượng
mCaCO3 = mCaO + mCO2 => mCaO = ?
Lời giải chi tiết:
PTHH CaCO3 \(\buildrel {{t^0}} \over\longrightarrow \)CaO + CO2
Áp dụng định luật bảo toàn khối lượng cho phương trình trên ta có
mCaCO3 = mCaO + mCO2
=> mCaO = 100 - 44 = 56 (kg)
Đáp án C
Câu hỏi 12 :
Khi nung canxi cacbonat CaCO3 người ta thu được canxi oxit CaO và khí cacbonic. Cho biết khối lượng vôi sống sinh ra bằng 140 kg, khối lượng khí cacbonic bằng 110 kg. Tính khối lượng canxi cacbonat phản ứng?
- A 30 kg.
- B 140 kg
- C 110 kg
- D 250 kg.
Đáp án: D
Phương pháp giải:
Áp dụng định luật bảo toàn khối lượng cho phương trình mCaCO3 = mCaO + mCO2 = ?
Lời giải chi tiết:
PTHH CaCO3 \(\buildrel {{t^0}} \over\longrightarrow \) CaO + CO2
Áp dụng định luật bảo toàn khối lượng cho phương trình trên ta có
mCaCO3 = mCaO + mCO2 = 140 + 110 = 250 (kg)
Đáp án D
Câu hỏi 13 :
Cho 11,2 g sắt tác dụng với dung dịch axit clohiđric HCl tạo ra 25,4 g sắt (II) clorua FeCl2 và 0,4 g khí hiđro. Tính khối lượng HCl đã dùng
- A 14,6 g
- B 16,4 g
- C 36,2 g.
- D 13,8 g
Đáp án: A
Phương pháp giải:
Áp dụng định luật bảo toàn khối lương
mFe+ mHCl = mH2+ msắt II clorua
=> mHCl= ?
Lời giải chi tiết:
PTHH
Fe + 2HCl → FeCl2 + H2
Áp dụng định luật bảo toàn khối lương
mFe+ mHCl = mH2+ msắt II clorua
=> mHCl= 25,4 + 0,4 -11,2 =14,6 (g)
Đáp án A
Câu hỏi 14 :
Đốt cháy hoàn toàn m (g) CH4 cần dùng 0,4 (g) khí O2 thu được 1,4 (g) CO2 và 1,6(g) H2O. m có giá trị là:
- A 2,6g
- B 2,5g
- C 1,7g
- D 1,6g
Đáp án: A
Phương pháp giải:
áp dụng định luật bảo toàn khối lượng vào tính toán
Lời giải chi tiết:
PTHH chữ: m(g) CH4 + 0,4 (g) O2 → 1,4 (g) CO2 + 1,6 (g) H2O
Bảo toàn khối lượng ta có: mCH4 + mO2 = mCO2 + mH2O
→ mCH4 = mCO2 + mH2O – mO2 = 1,4 + 1,6 – 0,4 = 2,6 (g)
Đáp án A
Câu hỏi 15 :
Người ta dùng 490 kg than để đốt lò chạy máy. Sau khi lò nguội, thấy còn 49 kg than chưa cháy. Tính hiệu suất phản ứng
- A 90%
- B 75%
- C 25%
- D 10%
Đáp án: A
Phương pháp giải:
m than phản ứng = mthan bđ – mthan còn lại = ?
% H = (mthan pư : mthan bđ)×100% = ?
Lời giải chi tiết:
m than phản ứng = mthan bđ – mthan còn lại = 490 – 49 = 441 kg
% H = (mthan pư : mthan bđ)×100% = (441 : 490)×100% = 90%
Đáp án A
Câu hỏi 16 :
Thành phần chính của đất đèn là caxicacbua. Khi cho đất đèn hợp nước có phản ứng sau:
Canxicacbua+ nước→ canxi hiđroxit+ khí axetilen.
Biết rằng cho 80kg đất đèn hợp với 36 kg nước tạo thành 74kg canxi hi droxit và 26 kg khí axetilen.
Tỉ lệ phần trăm khối lượng canxicacbua có trong đất đèn là:
- A 64%
- B 74%
- C 80%
- D 90%
Đáp án: C
Phương pháp giải:
BTKL ta có: mcanxicacbua + mnước → mcanxi hi đroxit+ mkhí axetilen => mcanxicacbua = ?\(\% {m_{canxi\,cacbua}} = \frac{{{m_{canxi\,cacbua}}}}{{m{\,_{dat\,den}}}} \times 100\% = ?\)
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng ta có:
mcanxicacbua + mnước → mcanxi hi đroxit+ mkhí axetilen
=> mcanxicacbua = 74+ 26 – 36 = 64(kg)
Phần trăm khối lượng canxicacbua có trong đất đèn là: \(\% {m_{canxi\,cacbua}} = \frac{{{m_{canxi\,cacbua}}}}{{m{\,_{dat\,den}}}} \times 100\% = \frac{{64}}{{80}} \times 100\% = {\rm{ }}80\% \)
Đáp án C
Câu hỏi 17 :
Khi nung đá vôi tới 90% khối lượng (chính bằng phần trăm chứa canxicacbonat) thu được 11,2 tấn canxi oxit và 8,8 tấn cacbonic. Khối lượng đá vôi lấy đem nung là:
- A 18 tấn
- B 20 tấn
- C 22,22 tấn
- D 33,33 tấn
Đáp án: C
Phương pháp giải:
BTKL ta có: mcanxi cacbonat = mcanxi oxit + mcacbonic => mcanxi cacbonat = ?\(\% {m_{da\,voi}} = \frac{{m{\,_{canxi\,cacbonat}}}}{{{\% _{da\,voi\,chiem}}}} \times 100\% = ?\left( {{\rm{ }}tan} \right)\)
Lời giải chi tiết:
Canxi cacbonat \(\buildrel {{t^0}} \over\longrightarrow \) Canxi oxit + cacbonic
Áp dụng định luật bảo toàn khối lượng ta có:
mcanxi cacbonat = mcanxi oxit + mcacbonic
=> mcanxi cacbonat = 11,2 + 8,8 = 20 (tấn)
Vì canxi cacbonat chỉ chiếm 90% đá vôi nên khối lượng đá vôi đem lấy nung là:
\(\% {m_{da\,voi}} = \frac{{m{\,_{canxi\,cacbonat}}}}{{{\% _{da\,voi\,chiem}}}} \times 100\% = \frac{{20}}{{90\% }} \times 100\% = 22,22\left( {{\rm{ }}tan} \right)\)
Đáp án C
Câu hỏi 18 :
Cho hỗn hợp gồm hai muối A2SO4 và BSO4 có khối lượng 44,2 g tác dụng vừa đủ với 62,4 g BaCl2 trong dung dịch thì cho 69,9 g kết tủa BaSO4 và 2 muối tan. Khối lượng 2 muối tan sau phản ứng là:
- A 36,8 g
- B 36,7 g
- C 38 g
- D 40 g
Đáp án: B
Phương pháp giải:
BTKL ta có: mA2SO4 + mBSO4 + mBaCl2 = mBaSO4 + m muối tan => m muối tan = ?
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng
mA2SO4 + mBSO4 + mBaCl2 = mBaSO4 + m muối tan
=> m muối tan = mA2SO4 + mBSO4 + mBaCl2 - mBaSO4 = 44,2 + 62,4 – 69,9 = 36,7g
Đáp án B
Câu hỏi 19 :
Than cháy theo phản ứng hoá học: Cacbon + khí oxi -> khí cacbonic
Cho biết khối lượng cacbon là 4,5 kg, khối lượng oxi là 12 kg. Khối lượng khí cacbonic tạo thành là:
- A 16,5 kg
- B 16,6 kg
- C 17 kg
- D 20 kg
Đáp án: A
Phương pháp giải:
BTKL có: m cacbon + m khí oxi = m khí cacbonic => m khí cacbonic = ?
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng
m cacbon + m khí oxi = m khí cacbonic
=> m khí cacbonic = 4,5 + 12 = 16,5kg
Đáp án A
Câu hỏi 20 :
Cho 11,2 g sắt tác dụng với dung dịch axit clohiđric HCl tạo ra 25,4 g sắt (II) clorua FeCl2 và 0,4 g khí hiđro. Khối lượng axit HCl đã dùng là:
- A 14,7 g
- B 15 g
- C 14,6 g
- D 26 g
Đáp án: C
Phương pháp giải:
BTKL ta có: mFe + mHCl phản ứng = mFeCl2 + mH2 => mHCl = ?
Lời giải chi tiết:
Áp dụng định luật bảo toàn khối lượng
mFe + mHCl phản ứng = mFeCl2 + mH2
=> mHCl = mFeCl2 + mH2 – mFe = 25,4 + 0,4 – 11,2 = 14,6g
Đáp án C
Các bài khác cùng chuyên mục
- 20 câu hỏi vận dụng về cân bằng phương trình hóa học có lời giải
- 15 câu hỏi cân bằng phương trình hóa học theo phương pháp chẵn lẽ có lời giải
- 20 bài tập vận dụng về định luật bảo toàn khối lượng có lời giải (phần 2)
- 20 bài tập vận dụng về định luật bảo toàn khối lượng có lời giải (phần 1)
- 20 câu hỏi luyện tập về mol có lời giải













