Đề kiểm tra 1 tiết Hóa 12 chương 6: Kim loại kiềm - Kim loại kiềm thổ - Nhôm - Đề số 3
Đề bài
Để sản xuất nhôm từ quặng boxit người ta sử dụng phương pháp:
-
A.
Nhiệt luyện
-
B.
Thủy luyện
-
C.
Điện phân dung dịch
-
D.
Điện phân nóng chảy
Cho p mol Na[Al(OH)4] tác dụng với dung dịch chứa q mol HCl. Để thu được kết tủa thì cần có tỉ lệ
-
A.
p : q < 1: 4
-
B.
p : q = 1: 2
-
C.
p : q > 1: 4
-
D.
p : q = 1: 4
Dãy gồm các chất đều là kim loại kiềm thổ là
-
A.
Be, Ca, Sr, Ba
-
B.
Na, K, Mg, Ca
-
C.
Li, Na, K, Cs
-
D.
Be, Ca, K, Cs
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
-
A.
a : b < 1 : 4
-
B.
a : b = 1 : 3
-
C.
a : b = 1 : 4
-
D.
a : b > 1 : 4
Trong nhóm IA đi từ đầu đến cuối các nguyên tố được sắp xếp theo chiều… của điện tích hạt nhân. Trong dấu “…” là?
-
A.
Không đổi.
-
B.
Tăng dần.
-
C.
Giảm dần.
-
D.
Không so sánh được.
Công thức của phèn chua là :
-
A.
K2SO4.Al2(SO4)3.24H2O
-
B.
K2SO4.Al2(SO4)3.nH2O
-
C.
Li2SO4.Al2(SO4)3.24H2O
-
D.
Na2SO4.Al2(SO4)3.24H2O
Phản ứng hoá học nào dưới đây không thuộc loại phản ứng nhiệt nhôm ?
-
A.
Al tác dụng với Fe3O4 nung nóng
-
B.
Al tác dụng với CuO nung nóng
-
C.
Al tác dụng với Fe2O3 nung nóng
-
D.
Al tác dụng với axit H2SO4 đặc, nóng
Hỗn hợp X gồm Fe3O4 và Al có tỉ lệ mol tương ứng 1 : 3. Thực hiện phản ứng nhiệt nhôm X (không có không khí) đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm
-
A.
Al2O3 và Fe
-
B.
Al, Fe và Al2O3
-
C.
Al, Fe, Fe3O4 và Al2O3
-
D.
Al2O3, Fe và Fe3O4
Từ hỗn hợp Al2O3 và Fe2O3, muốn tách Al2O3 người ta thực hiện phản ứng :
-
A.
Dùng H2 (to) cao rồi dung dịch NaOH (dư)
-
B.
Dùng H2 (to) cao rồi dùng dung dịch HCl (dư)
-
C.
Dùng dung dịch NaOH (dư), dung dịch HCl dư rồi nung nóng
-
D.
Dùng dịch NaOH dư, CO2 dư, tách kết tủa rồi đem nung nóng
Để bảo quản các kim loại kiềm, ta cần phải
-
A.
ngâm chúng trong rượu nguyên chất
-
B.
ngâm chúng trong dầu hỏa
-
C.
ngâm chúng vào nước
-
D.
giữ trong lọ có nắp đậy kín
Nước cứng là nước chứa nhiều:
-
A.
muối CaCl2
-
B.
muối CaSO4
-
C.
muối Ca(HCO3)2
-
D.
Ion Ca2+ , Mg2+
Cho các dung dịch sau: Ba(OH)2, NaHSO4, K2CO3, Ba(HCO3)2. Đổ lần lượt các dung dịch vào nhau. Số phản ứng xảy ra là
-
A.
8
-
B.
6
-
C.
4
-
D.
5
Công thức hóa học của thạch cao khan là?
-
A.
CaSO4.2H2O.
-
B.
CaSO4.3H2O.
-
C.
CaSO4.
-
D.
CaSO4.H2O.
Cho chuỗi biến hóa sau :
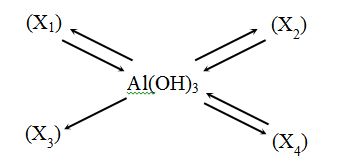
Vậy X1, X2, X3, X4 lần lượt là :
-
A.
Al2(SO4)3, KAlO2, Al2O3, AlCl3
-
B.
AlCl3, Al(NO3)3, Al2O3, Al
-
C.
Al2O3, NaAlO2, AlCl3, Al(NO3)3
-
D.
NaAlO2, Al2O3, Al2(SO4)3, AlCl3
Cho biết số thứ tự của Al trong bảng tuần hoàn là 13. Phát biểu nào sau đây đúng ?
-
A.
Trong các hạt Na+, Mg2+, Al3+, O, F thì Al3+ có bán kính lớn nhất
-
B.
Al thuộc chu kì 3, nhóm IIIB
-
C.
So với các kim loại khác trong cùng chu kì, nhôm có tính khử mạnh hơn
-
D.
Al thuộc chu kì 3, nhóm IIIA
NaCl có lẫn tạp chất Na2CO3. Cách nào sau đây có thể dùng để thu được NaCl tinh khiết ?
-
A.
Cho hỗn hợp đó vào dung dịch HCl dư, sau đó cô cạn dung dịch.
-
B.
Nung hỗn hợp ở nhiệt độ cao.
-
C.
Cho hỗn hợp tác dụng với BaCl2 .
-
D.
Cả A và C đều đúng.
Cho 10 gam một kim loại kiềm thổ M tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
-
A.
Ba
-
B.
Mg
-
C.
Ca
-
D.
Sr
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào V ml dung dịch chứa NaOH 2,75M và K2CO3 1M. Cô cạn dung dịch sau phản ứng ở nhiệt độ thường thu được 64,5 gam chất rắn khan gồm 4 muối. Giá trị của V là
-
A.
150
-
B.
180
-
C.
140
-
D.
200
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
-
A.
2,58 gam
-
B.
2,22 gam
-
C.
2,31 gam
-
D.
2,44 gam
Dung dịch X chứa 0,6 mol NaHCO3 và 0,3 mol Na2CO3. Thêm rất từ từ dung dịch chứa 0,8 mol HCl vào dung dịch X được dung dịch Y và V lít khí CO2 (đktc). Thêm vào dung dịch Y nước vôi trong dư thấy tạo thành m gam kết tủa. Tính thể tích V và khối lượng m.
-
A.
11,2 lít CO2 ; 40 gam CaCO3
-
B.
11,2 lít CO2 ; 90 gam CaCO3
-
C.
16,8 lít CO2 ; 60 gam CaCO3
-
D.
11,2 lít CO2 ; 60 gam CaCO3
Cho V lít dung dịch NaOH 1M vào dung dịch chứa 0,14 mol AlCl3, thu được m gam kết tủa. Mặt khác, cho 1,5V lít dung dịch NaOH 1M vào dung dịch chứa 0,14 mol AlCl3, thu được 0,75m gam kết tủa. Giá trị của V là
-
A.
0,32
-
B.
0,40
-
C.
0,36
-
D.
0,28
Cần ít nhất bao nhiêu ml dung dịch HCl 1M cần cho vào 500 ml dung dịch Na[Al(OH)4] 0,1M để thu được 0,78 g chất kết tủa?
-
A.
10 ml
-
B.
100 ml
-
C.
15 ml
-
D.
170 ml
Nung nóng m gam hỗn hợp Al và Fe2O3 (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau
Phần 1: tác dụng với dung dịch H2SO4 loãng dư sinh ra 3,08 lít khí H2 (ở đktc).
Phần 2: tác dụng với dung dịch NaOH dư sinh ra 0,84 lít khí H2 (ở đktc).
Giá trị của m là
-
A.
22,75
-
B.
21,40
-
C.
29,40
-
D.
29,43
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Fe2O3 và Al trong điều kiện không có không khí thu được hỗn hợp chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2. Mặt khác nếu cho Y tác dụng với dung dịch HCl dư sẽ thu được 0,4 mol H2. Số mol Al trong X là
-
A.
0,30 mol
-
B.
0,60 mol
-
C.
0,40 mol
-
D.
0,25 mol
Cho hỗn hợp gồm Na và Ba vào dung dịch chứa HCl 1M và H2SO4 0,6M. Sau khi kết thúc phản ứng thấy thoát ra 3,36 lít khí H2 (đktc) đồng thời thu được 13,98 gam kết tủa và dung dịch X có khối lượng giảm 0,1 gam so với dung dịch ban đầu. Cô cạn dung dịch X thu được m gam chất rắn. Giá trị của m là
-
A.
10,87
-
B.
7,45
-
C.
9,51
-
D.
10,19
Lời giải và đáp án
Để sản xuất nhôm từ quặng boxit người ta sử dụng phương pháp:
-
A.
Nhiệt luyện
-
B.
Thủy luyện
-
C.
Điện phân dung dịch
-
D.
Điện phân nóng chảy
Đáp án : D
Để sản xuất nhôm từ quặng boxit người ta sử dụng phương pháp điện phân nóng chảy
Cho p mol Na[Al(OH)4] tác dụng với dung dịch chứa q mol HCl. Để thu được kết tủa thì cần có tỉ lệ
-
A.
p : q < 1: 4
-
B.
p : q = 1: 2
-
C.
p : q > 1: 4
-
D.
p : q = 1: 4
Đáp án : C
Ta có: Na[Al(OH)4]= NaAlO2 + 2 H2O
NaAlO2 + H+ + H2O → Al(OH)3
Al(OH)3 + 3H+ → Al3+ + H2O
=> Thu được kết tủa thì quan hệ giữa H+ và NaAlO2
Na[Al(OH)4]= NaAlO2 + 2 H2O
NaAlO2 + H+ + H2O → Al(OH)3
Al(OH)3 + 3H+ → Al3+ + H2O
=> Để thu được kết tủa thì nH+ (Hay nHCl)< 4.nNa[Al(OH)4] => q< 4p => p/q > 1/4
Dãy gồm các chất đều là kim loại kiềm thổ là
-
A.
Be, Ca, Sr, Ba
-
B.
Na, K, Mg, Ca
-
C.
Li, Na, K, Cs
-
D.
Be, Ca, K, Cs
Đáp án : A
Dãy gồm các chất đều là kim loại kiềm thổ là Be, Ca, Sr, Ba
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
-
A.
a : b < 1 : 4
-
B.
a : b = 1 : 3
-
C.
a : b = 1 : 4
-
D.
a : b > 1 : 4
Đáp án : D
xem lại lí thuyết nhôm và hợp chất tác dụng với dung dịch kiềm
Nếu b ≥ 4a thì kết tủa bị hoà tan hoàn toàn => để thu được kết tủa thì b < 4a
Trong nhóm IA đi từ đầu đến cuối các nguyên tố được sắp xếp theo chiều… của điện tích hạt nhân. Trong dấu “…” là?
-
A.
Không đổi.
-
B.
Tăng dần.
-
C.
Giảm dần.
-
D.
Không so sánh được.
Đáp án : B
xem lại lí thuyết kim loại kiềm
Những nguyên tố trong nhóm IA của bảng tuần hoàn được sắp xếp từ trên xuống dưới theo thứ tự tăng dần của điện tích hạt nhân nguyên tử.
Công thức của phèn chua là :
-
A.
K2SO4.Al2(SO4)3.24H2O
-
B.
K2SO4.Al2(SO4)3.nH2O
-
C.
Li2SO4.Al2(SO4)3.24H2O
-
D.
Na2SO4.Al2(SO4)3.24H2O
Đáp án : A
Công thức của phèn chua là : K2SO4.Al2(SO4)3.24H2O
Phản ứng hoá học nào dưới đây không thuộc loại phản ứng nhiệt nhôm ?
-
A.
Al tác dụng với Fe3O4 nung nóng
-
B.
Al tác dụng với CuO nung nóng
-
C.
Al tác dụng với Fe2O3 nung nóng
-
D.
Al tác dụng với axit H2SO4 đặc, nóng
Đáp án : D
Phản ứng nhiệt nhôm là cho nhôm khử các oxit của kim loại => Phản ứng hoá học không thuộc loại phản ứng nhiệt nhôm là Al tác dụng với axit H2SO4 đặc, nóng.
Hỗn hợp X gồm Fe3O4 và Al có tỉ lệ mol tương ứng 1 : 3. Thực hiện phản ứng nhiệt nhôm X (không có không khí) đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm
-
A.
Al2O3 và Fe
-
B.
Al, Fe và Al2O3
-
C.
Al, Fe, Fe3O4 và Al2O3
-
D.
Al2O3, Fe và Fe3O4
Đáp án : B
xem lại lí thuyết nhôm
nFe3O4 = 1 mol => nAl = 3 mol
PTHH: 3Fe3O4 + 8Al → 9Fe + 4Al2O3
1 → 8/3 → 3 → 4/3
=> sau phản ứng Al còn dư, hỗn hợp thu được gồm Al, Fe, Al2O3
Từ hỗn hợp Al2O3 và Fe2O3, muốn tách Al2O3 người ta thực hiện phản ứng :
-
A.
Dùng H2 (to) cao rồi dung dịch NaOH (dư)
-
B.
Dùng H2 (to) cao rồi dùng dung dịch HCl (dư)
-
C.
Dùng dung dịch NaOH (dư), dung dịch HCl dư rồi nung nóng
-
D.
Dùng dịch NaOH dư, CO2 dư, tách kết tủa rồi đem nung nóng
Đáp án : D
Xem lại lí thuyết hợp chất nhôm
Để tách Al2O3 người ta dùng dung dịch NaOH dư dể hòa tan Al2O3, sau đó sục CO2 vào dung dịch thu được kết tủa Al(OH)3. Nung nóng Al(OH)3 thu được Al2O3
Để bảo quản các kim loại kiềm, ta cần phải
-
A.
ngâm chúng trong rượu nguyên chất
-
B.
ngâm chúng trong dầu hỏa
-
C.
ngâm chúng vào nước
-
D.
giữ trong lọ có nắp đậy kín
Đáp án : B
Để bảo quản các kim loại kiềm, ta cần phải ngâm chúng trong dầu hỏa
Nước cứng là nước chứa nhiều:
-
A.
muối CaCl2
-
B.
muối CaSO4
-
C.
muối Ca(HCO3)2
-
D.
Ion Ca2+ , Mg2+
Đáp án : D
Nước cứng là nước chứa nhiều ion Ca2+ , Mg2+
Cho các dung dịch sau: Ba(OH)2, NaHSO4, K2CO3, Ba(HCO3)2. Đổ lần lượt các dung dịch vào nhau. Số phản ứng xảy ra là
-
A.
8
-
B.
6
-
C.
4
-
D.
5
Đáp án : B
Xem lại lí thuyết kim loại kiềm thổ
+) Ba(OH)2 phản ứng với NaHSO4, K2CO3, Ba(HCO3)2
+) NaHSO4 phản ứng với K2CO3, Ba(HCO3)2
+) K2CO3 phản ứng với Ba(HCO3)2
=> có tất cả 6 phản ứng
Công thức hóa học của thạch cao khan là?
-
A.
CaSO4.2H2O.
-
B.
CaSO4.3H2O.
-
C.
CaSO4.
-
D.
CaSO4.H2O.
Đáp án : C
Xem lại lí thuyết kim loại kiềm thổ
Thạch cao khan có công thức hóa học là CaSO4.
Cho chuỗi biến hóa sau :

Vậy X1, X2, X3, X4 lần lượt là :
-
A.
Al2(SO4)3, KAlO2, Al2O3, AlCl3
-
B.
AlCl3, Al(NO3)3, Al2O3, Al
-
C.
Al2O3, NaAlO2, AlCl3, Al(NO3)3
-
D.
NaAlO2, Al2O3, Al2(SO4)3, AlCl3
Đáp án : A
xem lại lí thuyết hợp chất nhôm
Vì Al(OH)3 tạo ra X3 mà X3 không tạo được ra Al(OH)3 => X3 là Al2O3
Cho biết số thứ tự của Al trong bảng tuần hoàn là 13. Phát biểu nào sau đây đúng ?
-
A.
Trong các hạt Na+, Mg2+, Al3+, O, F thì Al3+ có bán kính lớn nhất
-
B.
Al thuộc chu kì 3, nhóm IIIB
-
C.
So với các kim loại khác trong cùng chu kì, nhôm có tính khử mạnh hơn
-
D.
Al thuộc chu kì 3, nhóm IIIA
Đáp án : D
Cấu hình electron của Al: 1s22s22p63s23p1
=> Số hiệu nguyên tử 13, thuộc nhóm IIIA, chu kì 3
NaCl có lẫn tạp chất Na2CO3. Cách nào sau đây có thể dùng để thu được NaCl tinh khiết ?
-
A.
Cho hỗn hợp đó vào dung dịch HCl dư, sau đó cô cạn dung dịch.
-
B.
Nung hỗn hợp ở nhiệt độ cao.
-
C.
Cho hỗn hợp tác dụng với BaCl2 .
-
D.
Cả A và C đều đúng.
Đáp án : A
xem lại lí thuyết kim loại kiềm
Để thu được NaCl tinh khiết, ta cho hỗn hợp đó vào dung dịch HCl dư, sau đó cô cạn dung dịch.
PTHH: NaHCO3 + HCl → NaCl + CO2 + H2O
B sai vì nung hỗn hợp thì Na2CO3 không bị phân hủy.
C sai vì BaCl2 + Na2CO3 → BaCO3 + 2NaCl
Nếu BaCl2 dư thì NaCl vẫn không tinh khiết
Cho 10 gam một kim loại kiềm thổ M tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
-
A.
Ba
-
B.
Mg
-
C.
Ca
-
D.
Sr
Đáp án : C
Bảo toàn e: 2nM = 2nH2
nH2 = 0,25 mol
Bảo toàn e: 2nM = 2nH2 => nM = 0,25 mol
=> M = 10 / 0,25 = 40 => M là Ca
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào V ml dung dịch chứa NaOH 2,75M và K2CO3 1M. Cô cạn dung dịch sau phản ứng ở nhiệt độ thường thu được 64,5 gam chất rắn khan gồm 4 muối. Giá trị của V là
-
A.
150
-
B.
180
-
C.
140
-
D.
200
Đáp án : D
+) mrắn = mNa + mK + mCO3 + mHCO3 => 64,5 (1)
+) Bảo toàn điện tích : ${n_{N{a^ + }}} + {\text{ }}{n_{{K^ + }}} = {\text{ }}{n_{HCO_3^ - }} + 2.{n_{CO_3^{2 - }}}$ (2)
+) Bảo toàn C : nCO2 + nK2CO3 = x + y (3)
Từ (1), (2) và (3) ta có : v = 0,2 lít = 200 ml
Vì phản ứng tạo 4 muối => có tạo x mol CO32- và y mol HCO3-
=> mrắn = mNa + mK + mCO3 + mHCO3 => 64,5 = 23.2,75V + 39.2V + 60x + 61y (1)
Bảo toàn điện tích : ${n_{N{a^ + }}} + {\text{ }}{n_{{K^ + }}} = {\text{ }}{n_{HCO_3^ - }} + 2.{n_{CO_3^{2 - }}}$ => 2,75V + 2V = 2x + y (2)
Bảo toàn C : nCO2 + nK2CO3 = x + y = 0,4 + V (3)
Từ (1), (2) và (3) ta có : V = 0,2 lít = 200 ml
Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH 0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan?
-
A.
2,58 gam
-
B.
2,22 gam
-
C.
2,31 gam
-
D.
2,44 gam
Đáp án : C
+) nOH > 2nCO2=> OH‑ dư
=> nCO3 = nCO2 = 0,015 mol
Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -$2{n_{CO_3^{2 - }}}$
+) mrắn = mNa + mK + mCO3 + mOH dư
nCO2 = 0,015 mol; nOH = nNaOH + nKOH = 0,04 mol > 2nCO2
=> OH‑ dư
=> nCO3 = nCO2 = 0,015 mol
Và nOH- dư = nOH- ban đầu – nOH- phản ứng = nOH- ban đầu -$2{n_{CO_3^{2 - }}}$= 0,01 mol
=> mrắn = mNa + mK + mCO3 + mOH dư = 2,31 gam
Dung dịch X chứa 0,6 mol NaHCO3 và 0,3 mol Na2CO3. Thêm rất từ từ dung dịch chứa 0,8 mol HCl vào dung dịch X được dung dịch Y và V lít khí CO2 (đktc). Thêm vào dung dịch Y nước vôi trong dư thấy tạo thành m gam kết tủa. Tính thể tích V và khối lượng m.
-
A.
11,2 lít CO2 ; 40 gam CaCO3
-
B.
11,2 lít CO2 ; 90 gam CaCO3
-
C.
16,8 lít CO2 ; 60 gam CaCO3
-
D.
11,2 lít CO2 ; 60 gam CaCO3
Đáp án : A
Với bài toán nhỏ từ từ axit vào muối cacbonat và ngược lại . Ta có :
+) Nhỏ từ từ axit vào muối cacbonat thì ban đầu H+ thiếu nên thứ tự phản ứng là:
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
Thêm từ từ HCl vào X thì sẽ xảy ra phản ứng theo thứ tự sau :
CO32- + H+ → HCO3-
HCO3- + H+ → CO2 + H2O
=> nCO2 = nH+ - nCO3 = 0,8 – 0,3 = 0,5 mol
Và nHCO3(Y) = nCO3 + nHCO3(X) – nCO2 = 0,3 + 0,6 – 0,5 = 0,4 mol
=> VCO2 = 11,2 lít
Và nCaCO3 = nHCO3 = 0,4 mol => m = 40 gam
Cho V lít dung dịch NaOH 1M vào dung dịch chứa 0,14 mol AlCl3, thu được m gam kết tủa. Mặt khác, cho 1,5V lít dung dịch NaOH 1M vào dung dịch chứa 0,14 mol AlCl3, thu được 0,75m gam kết tủa. Giá trị của V là
-
A.
0,32
-
B.
0,40
-
C.
0,36
-
D.
0,28
Đáp án : A
Bài toán muối nhôm tác dụng với dd kiềm
+ Nếu b/a ≤ 3 thì kết tủa chưa bị hoà tan và nAl(OH)3= b/3
+ Nếu 3 < b/a < 4 thì kết tủa bị hoà tan 1 phần nAl(OH)3= 4a-b
+ Nếu b/a ≥ 4 thì kết tủa bị hoà tan hoàn toàn
Giả sử thí nghiệm 1 Al3+ dư => nNaOH = 3nkết tủa (1)
Thí ngiệm 2 : có sự hòa tan kết tủa vì NaOH tăng mà lượng kết tủa giảm
=> nkết tủa = 4.nAlCl3 – nOH- (2)
Từ (1),(2) : $\left\{ \begin{gathered}V = 3.\dfrac{m}{{78}} \hfill \\\dfrac{{0,75m}}{{78}} = 4.0,14 - 1,5V \hfill \\ \end{gathered} \right.$ => V = 0,32 lit
Cần ít nhất bao nhiêu ml dung dịch HCl 1M cần cho vào 500 ml dung dịch Na[Al(OH)4] 0,1M để thu được 0,78 g chất kết tủa?
-
A.
10 ml
-
B.
100 ml
-
C.
15 ml
-
D.
170 ml
Đáp án : A
+ Nếu b/a $ \leqslant $ 1 thì nAl(OH)3 = b
+ Nếu 1 < b/a < 4 thì kết tủa bị hoà tan 1 phần và nAl(OH)3 = (4a – b)/3
+ Nếu b/a $\geqslant $ 4 thì không có kết tủa
Ta có: a = 0,05 mol; b = 0,01 mol => b < a
Đề bài yêu cầu tính VHCl nhỏ nhất có nghĩa là phải tính nH+ min thì nH+ = b = 0,01
=> V = 0,01 lít = 10 ml
Nung nóng m gam hỗn hợp Al và Fe2O3 (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau
Phần 1: tác dụng với dung dịch H2SO4 loãng dư sinh ra 3,08 lít khí H2 (ở đktc).
Phần 2: tác dụng với dung dịch NaOH dư sinh ra 0,84 lít khí H2 (ở đktc).
Giá trị của m là
-
A.
22,75
-
B.
21,40
-
C.
29,40
-
D.
29,43
Đáp án : A
+) phần 2 : Bảo toàn e :$3{n_{Al}} = 2{n_{{H_2}}}$
+) phần 1 : Bảo toàn e :$3{n_{Al}} + 2{n_{Fe}} = 2{n_{{H_2}\,(1)}}$
+) Bảo toàn nguyên tố Fe : ${n_{F{e_2}{O_3}}} = \frac{{{n_{Fe}}}}{2}$
+) Bảo toàn nguyên tố O :${n_{A{l_2}{O_3}}}\; = {\text{ }}{n_{F{e_2}{O_3}}}\;$
+) Bảo toàn khối lượng : mtrước phản ứng = msau phản ứng = ${m_{A{l_2}{O_3}}} + {m_{Fe}} + {m_{Al}}$
Y tác dụng với NaOH giải phóng H2 → hỗn hợp rắn Y gồm Al2O3, Fe và Al dư
Xét phần 2 : Bảo toàn e : $3{n_{Al}} = 2{n_{{H_2}}}\,\, \to \,\,{n_{Al}} = \frac{2}{3}{n_{{H_2}\,(2)}} = \,\,0,025\,\,mol$
Xét phần 1 : Bảo toàn e :
$3{n_{Al}} + 2{n_{Fe}} = 2{n_{{H_2}\,(1)}}\,\, \to \,\,{n_{Fe}} = \frac{{2{n_{{H_2}(1)}} - 3{n_{Al}}}}{2} = \frac{{2.0,1375 - 3.0,025}}{2} = 0,1\,\,mol$
Bảo toàn nguyên tố Fe :${n_{F{e_2}{O_3}}} = \frac{{{n_{Fe}}}}{2} = 0,05\,\,mol$
Bảo toàn nguyên tố O :${n_{A{l_2}{O_3}}}\; = {\text{ }}{n_{F{e_2}{O_3}}}\; = {\text{ }}0,05{\text{ }}mol\;$
Bảo toàn khối lượng : mtrước phản ứng = msau phản ứng = ${m_{A{l_2}{O_3}}} + {m_{Fe}} + {m_{Al}}$
→ m = (0,05.102 + 0,1.56 + 0,025.27).2 = 22,75 gam
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Fe2O3 và Al trong điều kiện không có không khí thu được hỗn hợp chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2. Mặt khác nếu cho Y tác dụng với dung dịch HCl dư sẽ thu được 0,4 mol H2. Số mol Al trong X là
-
A.
0,30 mol
-
B.
0,60 mol
-
C.
0,40 mol
-
D.
0,25 mol
Đáp án : A
+) Chất rắn Y có thể gồm Al2O3, Fe, Fe2O3 và Al
Y tác dụng với NaOH : nAl (trong Y) = $\frac{2}{3}{n_{{H_2}}}$
Y tác dụng với HCl :$2{n_{{H_2}}}$ = 3nAl + 2nFe
+) ${n_{A{l_2}{O_3}}} = \frac{1}{2}{n_{Fe}}$
+) Bảo toàn nguyên tử Al : nAl ban đầu = 2nAl2O3+ nAl dư
2Al + Fe2O3 $\xrightarrow{{{t^o}}}$ Al2O3 + 2Fe
Chất rắn Y có thể gồm Al2O3, Fe, Fe2O3 và Al
Y tác dụng với NaOH : nAl (trong Y) = $\frac{2}{3}{n_{{H_2}}}$ = 0,2 mol
Y tác dụng với HCl :$2{n_{{H_2}}}$ = 3nAl + 2nFe → 2.0,4 = 3.0,2 + 2nFe → nFe = 0,1 mol
${n_{A{l_2}{O_3}}} = \frac{1}{2}{n_{Fe}}$= 0,05 mol
Bảo toàn nguyên tử Al : nAl ban đầu = 2nAl2O3+ nAl dư = 2.0,05 + 0,2 = 0,3 mol
Cho hỗn hợp gồm Na và Ba vào dung dịch chứa HCl 1M và H2SO4 0,6M. Sau khi kết thúc phản ứng thấy thoát ra 3,36 lít khí H2 (đktc) đồng thời thu được 13,98 gam kết tủa và dung dịch X có khối lượng giảm 0,1 gam so với dung dịch ban đầu. Cô cạn dung dịch X thu được m gam chất rắn. Giá trị của m là
-
A.
10,87
-
B.
7,45
-
C.
9,51
-
D.
10,19
Đáp án : A
+) Đặt a và b là số mol của Na, Ba => a + 2b = 0,15.2 (1)
mdung dịch giảm = 23a + 137b – 13,98 – 0,15.2 = - 0,1 (2)
+) nBaSO4 = 0,06 mol => Ba2+ còn dư
=> nH2SO4 = 0,06 mol => nHCl = 0,06.1/0,6
+) Dung dịch X chứa Ba2+ (0,02), Na+ (0,14 mol); Cl- (0,1 mol) và OH-
Bảo toàn điện tích => nOH- = 0,08 mol
Đặt a và b là số mol của Na, Ba
=> a + 2b = 0,15.2 (1)
mdung dịch giảm = 23a + 137b – 13,98 – 0,15.2 = - 0,1 (2)
Từ (1) và (2) => a = 0,14; b = 0,08
nBaSO4 = 0,06 mol => Ba2+ còn dư 0,08 – 0,06 = 0,02 mol
=> nH2SO4 = 0,06 mol => nHCl = 0,06.1/0,6 = 0,1
Dung dịch X chứa Ba2+ (0,02), Na+ (0,14 mol); Cl- (0,1 mol) và OH-
Bảo toàn điện tích => nOH- = 0,08 mol
=> mrắn = 10,87 gam
















