Bài 11. Liên kết Hydrogen và tương tác van der Waals trang 39, 40, 41 SBT Hóa 10 Chân trời sáng tạo
Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử? Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
11.1
Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử?
A. H2S.
B. PH3.
C. HI.
D. CH3OH.
Phương pháp giải:
Dựa vào
- Định nghĩa liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết
- Phân loại liên kết hydrogen:
+ Liên kết hydrogen nội phân tử: là liên kết hydrogen được tạo thành trong chính phân tử chất đó
Điều kiện để có liên kết hydrogen nội phân tử:
· Hợp chất phải chứa từ 2 nhóm chức trở lên
· Khi tạo thành liên kết hydrogen phải tạo được vòng 5 hoặc 6 cạnh
+ Liên kết hydrogen liên phân tử: là liên kết hydrogen được tạo thành giữa phân tử này và phân tử khác
Lời giải chi tiết:
- Đáp án: D
- Giải thích: Trong 4 đáp án trên, chỉ có đáp án D thỏa mãn điều kiện để tạo liên kết hydrogen liên phân tử: Có nguyên tử H (đã liên kết với nguyên tố có độ âm điện cao là O) liên kết với một nguyên tử khác có độ âm điện lớn là O
11.2
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
A. độ âm điện của chlorine nhỏ hơn của nitrogen.
B. phân tử NH3 chứa nhiều nguyên tử hydrogen hơn phân tử HCl.
C. tổng số nguyên tử trong phân tử NH3 nhiều hơn so với phân tử HCl.
D. kích thước nguyên tử chlorine lớn hơn nguyên tử nitrogen nên mật độ điện tích âm trên chlorine không đủ lớn để hình thành liên kết hydrogen.
Phương pháp giải:
Dựa vào kích thước nguyên tử chlorine lớn hơn kích thước nguyên tử nitrogen => mật độ điện tích trên nguyên tử chlorine không đủ lớn
Lời giải chi tiết:
- Đáp án: D
11.3
Sơ đồ nào sau đây thể hiện đúng liên kết hydrogen giữa 2 phân tử hydrogen fluoride (HF)?
A. \({H^{\delta + }} - {F^{\delta - }}...{H^{\delta + }} - {F^{\delta - }}\).
B. \({H^{\delta + }} - {F^{\delta + }}...{H^{\delta - }} - {F^{\delta - }}\).
C. \({H^{\delta - }} - {F^{\delta + }}...{H^{\delta - }} - {F^{\delta + }}\).
D. \({H^{\delta + }} - {F^{\delta - }}...{H^{\delta - }} - {F^{\delta + }}\).
Phương pháp giải:
Dựa vào độ âm điện để xác định nguyên tử nào mang điện tích âm hay dương
Lời giải chi tiết:
- Vì nguyên tử hydrogen có độ âm điện nhỏ hơn nguyên tử fluorine " nguyên tử hydrogen mang một phần điện tích dương và nguyên tử fluorine mang một phần điện tích âm
=> Đáp án: A
11.4
Điều nào sau đây đúng khi nói về liên kết hydrogen liên phân tử?
A. Là lực hút tĩnh điện giữa nguyên tử H (thường trong các liên kết H-F, H-N, H-O ở phân tử này) với một trong các nguyên tử có độ âm điện mạnh (thường là N, O, F) ở một phân tử khác.
B. Là lực hút giữa các phân tử khác nhau.
C. Là lực hút tĩnh điện giữa các ion trái dấu.
D. Là lực hút giữa các nguyên tử trong một hợp chất cộng hoá trị.
Phương pháp giải:
- Định nghĩa liên kết hydrogen: Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết
Lời giải chi tiết:
- Đáp án: A
11.5
Điều nào sau đây đúng khi nói về liên kết hydrogen nội phân tử?
A. Là lực hút giữa các proton của nguyên tử này với các electron ở nguyên tử khác.
B. Là lực hút tĩnh điện giữa nguyên tử H (thường trong các liên kết H-F, H-N, H-O) ở một phân tử với một trong các nguyên tử có độ âm điện mạnh (thường là N, O, F) ở ngay chính phân tử đó.
C. Là lực hút giữa các ion trái dấu.
D. Là lực hút giữa các phân tử có chứa nguyên tử hydrogen.
Phương pháp giải:
Dựa vào
- Phân loại liên kết hydrogen:
+ Liên kết hydrogen nội phân tử: là liên kết hydrogen được tạo thành trong chính phân tử chất đó
Điều kiện để có liên kết hydrogen nội phân tử:
· Hợp chất phải chứa từ 2 nhóm chức trở lên
· Khi tạo thành liên kết hydrogen phải tạo được vòng 5 hoặc 6 cạnh
+ Liên kết hydrogen liên phân tử: là liên kết hydrogen được tạo thành giữa phân tử này và phân tử khác
Lời giải chi tiết:
- Đáp án: B
11.6
Tương tác van der Waals xuất hiện là do sự hình thành các lưỡng cực tạm thời cũng như các lưỡng cực cảm ứng. Các lưỡng cực tạm thời xuất hiện là do sự chuyển động của
A. các nguyên tử trong phân tử.
B. các electron trong phân tử.
C. các proton trong hạt nhân.
D. các neutron và proton trong hạt nhân
Phương pháp giải:
Dựa vào: lưỡng cực tạm thời xuất hiện là do sự chuyển động của các electron di chuyển tập trung về một phía bất kì của phân tử
Lời giải chi tiết:
- Đáp án: B
11.7
Trong các khí hiếm sau, khí hiếm có nhiệt độ sôi cao nhất là
A. Ne.
B. Xe.
C. Ar.
D. Kr.
Phương pháp giải:
Dựa vào đặc điểm của tương tác van der Waals
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
- Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
- Đáp án: B
- Giải thích: Khối lượng của nguyên tố Xe là lớn nhất " tương tác van der Waals lớn nhất " nhiệt độ sôi của Xe cao nhất
11.8
Biểu diễn liên kết hydrogen giữa các phân tử sau:
a) methanol (CH3OH) và nước.
b) ethylene glycol (HOCH2CH2OH) và nước.
Phương pháp giải:
Dựa vào
- Liên kết hydrogen thường được biểu diễn bằng dấu ba chấm (…)
- Phân tử có chứa liên kết hydrogen thì tan tốt trong nước
Lời giải chi tiết:
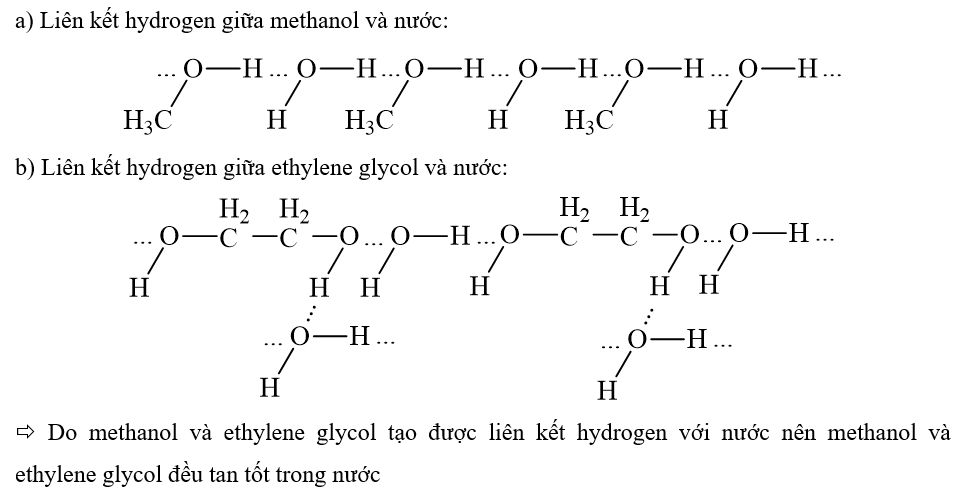
11.9
Ethylene glycol (HOCH2CH2OH) là một chất chống đông trong công nghiệp ô tô, hàng không do có khả năng can thiệp vào liên kết hydrogen của nước, làm các phân tử nước khó liên kết hơn, khiến nước khó đóng băng hơn. Biểu diễn liên kết hydrogen liên phân tử và nội phân tử trong ethylene glycol.
Phương pháp giải:
Dựa vào liên kết hydrogen thường được biểu diễn bằng dấu ba chấm (…)
Lời giải chi tiết:
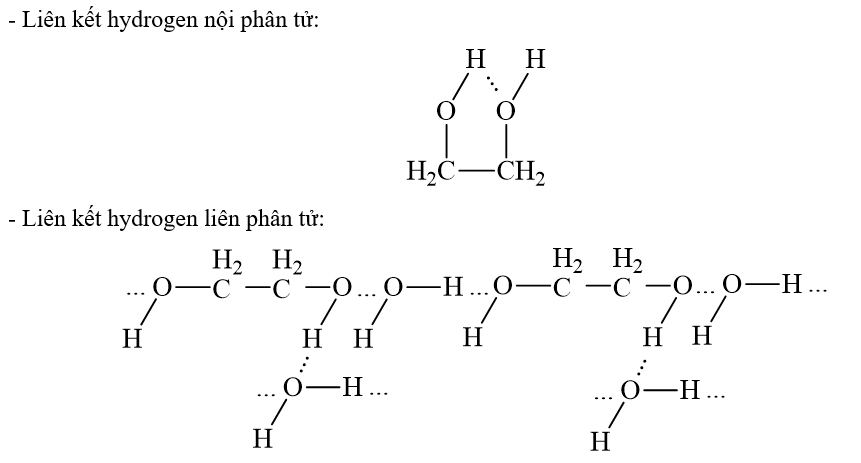
11.10
Hãy so sánh tương tác van der Waals với liên kết ion.
Phương pháp giải:
- Giống nhau: đều là các lực hút tĩnh điện
- Khác nhau: đặc điểm các phân tử/ ion liên kết
Lời giải chi tiết:
- Giống nhau: tương tác van der Waals với liên kết ion đều là các lực hút tĩnh điện
- Khác nhau:
+ Tương tác van der Waals là lực hút tĩnh điện giữa các phân tử trung hòa
+ Liên kết ion là lực hút tĩnh điện giữa các ion trái dấu
11.11
Thiết bị chụp cộng hưởng từ hạt nhân (NMR) sử dụng nitrogen lỏng để làm mắt nam châm siêu dẫn. Nitrogen lỏng sôi ở -195,8°C. Dự đoán nhiệt độ sôi của oxygen lỏng sẽ cao hay thấp hơn so với nitrogen lỏng? Giải thích.
Phương pháp giải:
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
- Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
- Do oxygen có khối lượng phân tử (32) lớn hơn khối lượng phân tử của nitrogen (28) => Tương tác van der Waals giữa các phân tử oxygen lớn hơn giữa các phân tử nitrogen
=> Oxygen lỏng có nhiệt độ sôi cao hơn nitrogen lỏng
11.12
Giải thích vì sao các tương tác van der Waals giữa các phân tử có kích thước lớn lại mạnh hơn so với các phân tử có kích thước nhỏ.
Phương pháp giải:
- Định nghĩa của tương tác van der Waals: là lực tương tác yếu giữa các phân tử, được hình thành do sự xuất hiện của các lưỡng cực tạm thời và lưỡng cực cảm ứng
- Đặc điểm của tương tác van der Waals:
+ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
+ Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
- Nguyên nhân: Vì phân tử có kích thước lớn thường sẽ có nhiều electron => Khả năng tạo lưỡng cực tạm thời và lưỡng cực phản ứng sẽ nhanh và nhiều hơn => Các tương tác van der Waals giữa các phân tử cũng mạnh hơn
11.13
Giải thích tại sao ở điều kiện thường, các nguyên tố trong nhóm halogen như fluorine và chlorine ở trạng thái khí, còn bromine ở trạng thái lỏng và iodine ở trạng thái rắn.
Phương pháp giải:
Dựa vào
- Định nghĩa của tương tác van der Waals: là lực tương tác yếu giữa các phân tử, được hình thành do sự xuất hiện của các lưỡng cực tạm thời và lưỡng cực cảm ứng
- Đặc điểm của tương tác van der Waals:
+ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
+ Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
- Phân tử khối từ F2 đến I2 tăng dần => Tương tác van der Waals giữa các phân tử cũng tăng dần => các phân tử liên kết với nhau chặt chẽ hơn vậy nên F2 và Cl2 ở trạng thái khí, còn Br2 ở trạng thái lỏng và I2 ở trạng thái rắn
11.14
Nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố nhóm VA, VIA và VIIA được biểu diễn qua đồ thị sau:
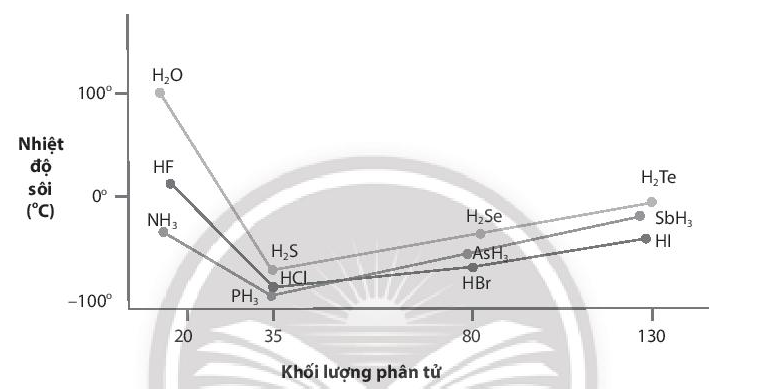
a) Giải thích nhiệt độ sôi cao bất thường của các hợp chất với hydrogen của các nguyên tố đầu tiên trong mỗi nhóm.
b) Nhận xét nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố còn lại ở mỗi nhóm và giải thích nguyên nhân sự biến đổi nhiệt độ sôi của chúng.
Phương pháp giải:
Dựa vào ảnh hưởng của liên kết hydrogen và tương tác van der Waals đến nhiệt độ sôi và nhiệt độ nóng chảy của các chất
- Các chất có liên kết hydrogen đều có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn các chất không có liên kết hydrogen
- Đặc điểm của tương tác van der Waals:
+ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
+ Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
a) Các nguyên tố đầu tiên trong mỗi nhóm VA, VIA và VIIA lần lượt là N, O và F đều là những nguyên tố có kích thước nhỏ và độ âm điện lớn vậy nên trong các phân tử NH3, H2O và HF có liên kết hydrogen => khiến nhiệt độ sôi cao bất thường so với các hợp chất còn lại trong nhóm.
b) Khối lượng của các hợp chất với hydrogen của các nguyên tố còn lại trong mỗi nhóm tăng dần => tương tác van der Waals giữa các phân tử trong hợp chất cũng tăng dần => Nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố còn lại trong mỗi nhóm tăng dần.
11.15
So sánh nhiệt độ nóng chảy và nhiệt độ sôi của pentane (CH3CH2CH2CH2CH3) và neopentane ((CH3)4C). Giải thích nguyên nhân sự khác biệt trên.
Phương pháp giải:
- Các yếu tố ảnh hưởng đến tương tác van der Waals
+ Số electron trong các phân tử: Phân tử nào có nhiều electron hơn => tương tác van der Waals mạnh hơn
+ Kích thước/ diện tích tiếp xúc của phân tử: Phân tử nào có kích thước/ diện tích tiếp xúc lớn hơn => tương tác van der Waals mạnh hơn
+ Độ phân cực của phân tử: Phân tử nào phân cực hơn => tương tác van der Waals mạnh hơn
Lời giải chi tiết:

11.16
Giải thích vì sao tetrachloromethane (CCl4) tuy là phân tử không cực nhưng có nhiệt độ sôi cao hơn trichloromethane (CHCl3) là phân tử có cực.
Phương pháp giải:
- Các yếu tố ảnh hưởng đến tương tác van der Waals
+ Số electron trong các phân tử: Phân tử nào có nhiều electron hơn => tương tác van der Waals mạnh hơn
+ Kích thước/ diện tích tiếp xúc của phân tử: Phân tử nào có kích thước/ diện tích tiếp xúc lớn hơn => tương tác van der Waals mạnh hơn
+ Độ phân cực của phân tử: Phân tử nào phân cực hơn => tương tác van der Waals mạnh hơn
- Đặc điểm của tương tác van der Waals:
+ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất
+ Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng
Lời giải chi tiết:
- CCl4 có kích thước lớn hơn CHCl3 và
- CCl4 có số electron nhiều hơn so với CHCl3
=> tương tác van der Waals giữa các phân tử CCl4 mạnh hơn so với giữa các phân tử CHCl3 => CCl4 có nhiệt độ sôi cao hơn CHCl3.
Luyện Bài Tập Trắc nghiệm Hóa 10 - Chân trời sáng tạo - Xem ngay
Các bài khác cùng chuyên mục
- Ôn tập chương 7 trang 83, 84 SBT Hóa 10 Chân trời sáng tạo
- Bài 18. Hydrogen halide và một số phản ứng của ion halide trang 79, 80, 81 SBT Hóa 10 Chân trời sáng tạo
- Bài 17. Tính chất vật lí và hóa học các đơn chất nhóm VIIA trang 75, 76, 77 SBT Hóa 10 Chân trời sáng tạo
- Ôn tập chương 6 trang 73, 74 SBT Hóa 10 Chân trời sáng tạo
- Bài 16. Các yếu tố ảnh hường đến tốc độ phản ứng hóa học trang 67, 68, 69 SBT Hóa 10 Chân trời sáng tạo













Danh sách bình luận