Bài 1. Mở đầu về cân bằng hóa học trang 6, 7, 8, 9, 10, 11, 12, 13, 14 Hóa học 11 Cánh diều
Khí NO2 (màu nâu đỏ) liên tục chuyển hoá thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định. Tại điều kiện này, khí NO2 cũng như khí N2O4 trong các bình riêng biệt (Hình 1.1), sau một thời gian đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian.
CH tr 6
Video hướng dẫn giải
| Câu hỏi mở đầu: Khí NO2 (màu nâu đỏ) liên tục chuyển hoá thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định. Tại điều kiện này, khí NO2 cũng như khí N2O4 trong các bình riêng biệt (Hình 1.1), sau một thời gian đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian.
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, có phản ứng diễn ra trong hai bình này hay không? |
Phương pháp:
Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Lời giải chi tiết:
Phản ứng: 2NO2(g) ⇌ N2O4(g)
(nâu đỏ) (không màu)
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, có hai phản ứng diễn ra trong hai bình này:
- Phản ứng chuyển hóa NO2 thành N2O4.
- Phản ứng chuyển hóa N2O4 thành NO2.
CH tr 7
Video hướng dẫn giải
| Câu hỏi 1: Hãy nêu một số ví dụ về phản ứng thuận nghịch mà em biết. |
Phương pháp:
Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Lời giải chi tiết:
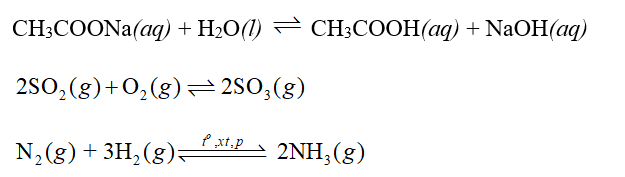
| Câu hỏi 2: Phản ứng thuận nghịch có xảy ra hoàn toàn được không? Vì sao? |
Phương pháp:
Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Chiều từ trái sang phải (chiều các chất ban đầu tạo thành chất sản phẩm) được gọi là chiều thuận.
Chiều từ phải sang trái (chiều các chất sản phẩm tạo thành chất ban đầu) được gọi là chiều nghịch.
Lời giải chi tiết:
Phản ứng thuận nghịch không xảy ra hoàn toàn được vì khi các chất ban đầu phản ứng với nhau tạo sản phẩm thì các sản phẩm lại phản ứng với nhau để tạo thành chất phản ứng.
| Câu hỏi 3: Xét Ví dụ 2:
a) Giải thích vì sao màu tím của hỗn hợp khí lại nhạt dần so với lúc mới bắt đầu trộn hai khí H2 và I2, với nhau. b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của chất nào không thay đổi? |
Phương pháp:
Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Tuy nhiên, ở trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn tiếp diễn với tốc độ bằng nhau nhưng nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó là bằng nhau. Như vậy, cân bằng hoá học là cân bằng động.
Lời giải chi tiết:
H2(g) + I2(g) ⇌ 2HI(g)
Không màu Tím Không màu
a) Màu tím của hỗn hợp khí lại nhạt dần so với lúc mới bắt đầu trộn hai khí H2 và I2, với nhau vì khi trộn H2 và I2 phản ứng thuận diễn ra tạo khí HI không màu.
b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của I2 không thay đổi
CH tr 8
Video hướng dẫn giải
|
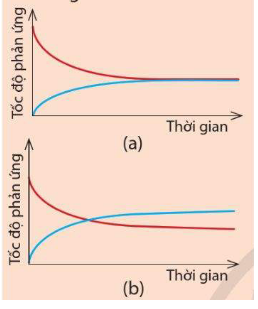
Câu hỏi 1: Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian.
Hãy cho biết đồ thị nào thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị đó biểu diễn tốc độ phản ứng thuận hay tốc độ phản ứng nghịch? |
Phương pháp:
Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Tuy nhiên, ở trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn tiếp diễn với tốc độ bằng nhau nhưng nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó là bằng nhau. Như vậy, cân bằng hoá học là cân bằng động.
Lời giải chi tiết:
Sau một khoảng thời gian, màu tím của hỗn hợp khí không thay đổi, chứng tỏ nồng độ I2 không thay đổi. Nghĩa là sau một thời gian, lượng I2 sinh ra từ phản ứng nghịch và lượng I2 mất đi từ phản ứng thuận bằng nhau. Hay tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Do đó đồ thị (a) thể hiện đúng Ví dụ 2.
Đường màu xanh biểu diễn tốc độ phản ứng nghịch. Ban đầu phản ứng, chưa sinh ra HI nên tốc độ phản ứng nghịch bằng 0. Sau một thời gian, lượng HI sinh ra càng nhiều, tốc độ phản ứng nghịch tăng. Sau đó, lượng HI sinh ra từ phản ứng thuận bằng lượng HI mất đi từ phản ứng nghịch, tức tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch nên đường đồ thị màu xanh trùng với đường đồ thị màu đỏ.
| Câu hỏi 2: Vì sao giá trị \[\frac{{{{\rm{k}}_{\rm{t}}}}}{{{{\rm{k}}_{\rm{n}}}}}\] là một hằng số ở nhiệt độ xác định? |
Phương pháp:
- Công thức tính tốc độ phản ứng aA+bB → cC + dD dựa vào định luật tác dụng khối lượng: \[{\rm{v = kC}}_{\rm{A}}^{\rm{a}}{\rm{C}}_{\rm{B}}^{\rm{b}}\]
Lời giải chi tiết:
H2(g) + I2(g) ⇌ 2HI
\[\begin{array}{l}{{\rm{v}}_{\rm{t}}}{\rm{ = }}{{\rm{k}}_{\rm{t}}}{{\rm{C}}_{{{\rm{H}}_{\rm{2}}}}}{{\rm{C}}_{{{\rm{I}}_{\rm{2}}}}}\\{{\rm{v}}_{\rm{n}}}{\rm{ = }}{{\rm{k}}_{\rm{n}}}{\rm{C}}_{{\rm{HI}}}^{\rm{2}}\end{array}\]
Với kt và kn lần lượt là hằng số tốc độ phản ứng thuận và hằng số tốc độ phản ứng nghịch.
kt và kn chỉ phụ thuộc vào nhiệt độ nên giá trị \[\frac{{{{\rm{k}}_{\rm{t}}}}}{{{{\rm{k}}_{\rm{n}}}}}\] là một hằng số ở nhiệt độ xác định.
CH tr 9
Video hướng dẫn giải
| Câu hỏi 1: Viết biểu thức hằng số cân bằng KCcho phản ứng thuận nghịch:
a, N2(g) + 3H2(g) ⇌ 2NH3(g) b, CaCO3 (s) ⇌ CaO (s) + CO2 (g) |
Phương pháp:
Với một phản ứng thuận nghịch bất kì:
aA + bB ⇌ mM + nM
KC được gọi là hằng số cân bằng (tính theo nồng độ mol), giá trị của KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ.
Khi đó biểu thức tính KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; [A], [B], [M], [N] lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Lưu ý: Trong công thức tính hằng số cân bằng KC, chỉ xét những chất ở thể khí và chất tan trong dung dịch.
Lời giải chi tiết:
a) a, N2(g) + 3H2(g) ⇌ 2NH3(g)
\[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[N}}{{\rm{H}}_3}{\rm{]}}}^2}}}{{{\rm{[}}{{\rm{N}}_2}{\rm{][}}{{\rm{H}}_2}{{\rm{]}}^3}}}\]
b) CaCO3 (s) ⇌ CaO (s) + CO2 (g)
\[{{\rm{K}}_{\rm{C}}}{\rm{ = [C}}{{\rm{O}}_{\rm{2}}}{\rm{]}}\]
| Câu hỏi 2: Viết biểu thức hằng số cân bằng KCcho phản ứng (*), (**) dưới đây.
H2 (g) + I2 (g) ⇌ 2HI(g) (*) 1/2 H2(g) + 1/2 I2 (g) ⇌ HI (g) (**) Theo em, giá trị hai hằng số cân bằng này có bằng nhau không? |
Phương pháp:
Với một phản ứng thuận nghịch bất kì:
aA + bB ⇌ mM + nM
KC được gọi là hằng số cân bằng (tính theo nồng độ mol), giá trị của KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ.
Khi đó biểu thức tính KC như sau: \({{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{(M)}}}^{\rm{m}}}{{{\rm{(N)}}}^{\rm{n}}}}}{{{{{\rm{(A)}}}^{\rm{a}}}{{{\rm{(B)}}}^{\rm{b}}}}}\)
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Lưu ý: Trong công thức tính hằng số cân bằng KC, chỉ xét những chất ở thể khí và chất tan trong dung dịch.
Lời giải chi tiết:
- Trong phản ứng (*): \({{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{(HI)}}}^{\rm{2}}}}}{{{\rm{(}}{{\rm{H}}_{\rm{2}}}{\rm{)(}}{{\rm{I}}_{\rm{2}}}{\rm{)}}}}\)
- Trong phản ứng (**): \({{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{\rm{(HI)}}}}{{{{{\rm{(}}{{\rm{H}}_{\rm{2}}}{\rm{)}}}^{\frac{1}{2}}}{{{\rm{(}}{{\rm{I}}_{\rm{2}}}{\rm{)}}}^{\frac{1}{2}}}}}\)
Giá trị hai hằng số cân bằng này không bằng nhau.
| Câu hỏi 3: Trong công nghiệp, hydrogen được sản xuất từ phản ứng:
CH4 (g) + H2O (g) ⇌ 3H2 (g) + CO (g) a) Tính hằng số cân bằng KC của phản ứng trên ở 760 °C. Biết ở nhiệt độ này, tất cả các chất đều ở thể khí và nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cần bằng lần lượt là 0,126 M; 0,242 M; 1,150 M và 0,126 M. b*) Ở 760 °C, giả sử ban đầu chỉ có CH4, H2O có nồng độ bằng nhau và bằng x M. Xác định x, biết nồng độ của H2 ở trạng thái cân bằng là 0,6 M. |
Phương pháp:
Với một phản ứng thuận nghịch bất kì:
aA + bB ⇌ mM + nM
KC được gọi là hằng số cân bằng (tính theo nồng độ mol), giá trị của KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ.
Khi đó biểu thức tính KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Lưu ý: Trong công thức tính hằng số cân bằng KC, chỉ xét những chất ở thể khí và chất tan trong dung dịch.
Lời giải chi tiết:
a) \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[}}{{\rm{H}}_{\rm{2}}}{\rm{]}}}^{\rm{3}}}{\rm{[CO]}}}}{{{\rm{[C}}{{\rm{H}}_{\rm{4}}}{\rm{][}}{{\rm{H}}_{\rm{2}}}{\rm{O]}}}} = \frac{{{{1,150}^3}.0,126}}{{0,126.0,242}} \approx 6,285\]
b) CH4 (g) + H2O (g) ⇌ 3H2 (g) + CO (g)
Ban đầu: x x
Phản ứng: 0,2 ← 0,2 ← 0,6 → 0,2
Cân bằng: (x – 0,2) (x - 0,2) 0,6 0,2
Ở 760 °C:
\[\begin{array}{l}{{\rm{K}}_{\rm{C}}}{\rm{ = }}6,285\\ \Leftrightarrow \frac{{{{{\rm{[}}{{\rm{H}}_{\rm{2}}}{\rm{]}}}^{\rm{3}}}{\rm{[CO]}}}}{{{\rm{[C}}{{\rm{H}}_{\rm{4}}}{\rm{][}}{{\rm{H}}_{\rm{2}}}{\rm{O]}}}} = 6,285\\ \Leftrightarrow \frac{{{{0,6}^3}.0,2}}{{(x - 0,2)(x - 0,2)}} = 6,285\\ \Rightarrow x \approx 0,283(M)\end{array}\]
CH tr 10
Video hướng dẫn giải
| Câu hỏi 1: Hãy cho biết trong công nghiệp, để thu được nhiều NH3 hơn thì cần tăng hay giảm nồng độ N2 và H2. |
Phương pháp:
aA + bB ⇌ mM + nM
Khi đó biểu thức tính hằng số cân bằng KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Hằng số cân bằng càng lớn (hay nhỏ) cho biết mức độ phản ứng thuận diễn ra thuận lợi hay không thuận lợi.
Lời giải chi tiết:
N2 (g) + 3H2 (g) ⇌ 2NH3 (g)
\[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[N}}{{\rm{H}}_3}{\rm{]}}}^2}}}{{{\rm{[}}{{\rm{N}}_2}{\rm{][}}{{\rm{H}}_2}{{\rm{]}}^3}}}\]
Ta thấy, KC càng lớn, phản ứng thuận tạo ra NH3 diễn ra càng thuận lợi, các chất ở trạng thái cân bằng chủ yếu là chất sản phẩm. Do đó người ta tăng nồng độ N2 và H2 để lượng NH3 sinh ra nhiều hơn.
| Câu hỏi 2: Hai acid HA và HB cùng nồng độ ban đầu là 0,5 M, phân li trong nước theo các cân bằng:
HA ⇌ H+ + A- HB ⇌ H+ + B- Với các hằng số cân bằng (hay gọi là hằng số phân li acid) tương ứng là KC(HA) = 0,2 và KC(HB) = 0,1. Tính nồng độ H+ của mỗi dung dịch acid. Rút ra kết luận về mối liên hệ giữa độ mạnh của acid với độ lớn của hằng số phân li acid. Biết rằng acid càng mạnh khi càng dễ tạo ra H+. |
Phương pháp:
Với một phản ứng thuận nghịch bất kì:
aA + bB ⇌ mM + nM
KC được gọi là hằng số cân bằng (tính theo nồng độ mol), giá trị của KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ.
Khi đó biểu thức tính KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Lưu ý: Trong công thức tính hằng số cân bằng KC, chỉ xét những chất ở thể khí và chất tan trong dung dịch.
Lời giải chi tiết:
HA ⇌ H+ + A-
Ban đầu: 0,5
Phản ứng: x → x → x
Cân bằng: (0,5 – x) x x
\[\begin{array}{l}{\rm{ }}{{\rm{K}}_{{\rm{C(HA)}}}} = {\rm{ }}0,2\\ \Leftrightarrow \frac{{{\rm{[}}{{\rm{H}}^{\rm{ + }}}{\rm{][}}{{\rm{A}}^{\rm{ - }}}{\rm{]}}}}{{{\rm{[HA]}}}}{\rm{ = 0}}{\rm{,2}}\\ \Leftrightarrow \frac{{{\rm{x}}{\rm{.x}}}}{{{\rm{(0}}{\rm{,5 - x)}}}}{\rm{ = 0}}{\rm{,2}}\\ \Rightarrow {\rm{x}} \approx {\rm{0}}{\rm{,232 (M) = [}}{{\rm{H}}^{\rm{ + }}}{\rm{]}}\end{array}\]
HB ⇌ H+ + B-
Ban đầu: 0,5
Phản ứng: y → y → y
Cân bằng: (0,5 – y) y y
\[\begin{array}{l}{\rm{ }}{{\rm{K}}_{{\rm{C(HB)}}}} = {\rm{ }}0,1\\ \Leftrightarrow \frac{{{\rm{[}}{{\rm{H}}^{\rm{ + }}}{\rm{][}}{{\rm{B}}^{\rm{ - }}}{\rm{]}}}}{{{\rm{[HB]}}}}{\rm{ = 0}}{\rm{,1}}\\ \Leftrightarrow \frac{{{\rm{y}}{\rm{.y}}}}{{{\rm{(0}}{\rm{,5 - y)}}}}{\rm{ = 0}}{\rm{,1}}\\ \Rightarrow {\rm{y}} \approx {\rm{0}}{\rm{,179 (M) = [}}{{\rm{H}}^{\rm{ + }}}{\rm{]}}\end{array}\]
Ta thấy nồng độ H+ trong sinh ra trong phản ứng phân li HA lớn hơn nồng độ nồng độ H+ trong sinh ra trong phản ứng phân li HB và KC(HA) > KC(HB), chứng tỏ hằng số cân bằng (hằng số phân li acid) càng lớn, acid càng dễ tạo thành H+, acid càng mạnh.
CH tr 11
Video hướng dẫn giải
| Câu hỏi 1: Methanol (CH3OH) là nguyên liệu quan trọng trong công nghiệp hoá học. Dựa vào hằng số cân bằng của các phản ứng ở 25 °C, hãy lựa chọn phản ứng thích hợp để điều chế CH3OH. Giải thích. |
Phương pháp:
aA + bB ⇌ mM + nM
Khi đó biểu thức tính hằng số cân bằng KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Hằng số cân bằng càng lớn (hay nhỏ) cho biết mức độ phản ứng thuận diễn ra thuận lợi hay không thuận lợi.
Lời giải chi tiết:
Ở 25oC, K(C) (1) > K(C) (2) nên tốc độ xảy ra phản ứng thuận (tạo thành methanol) của phản ứng (1) lớn hơn phản ứng (2). Do đó phản ứng thích hợp để điều chế CH3OH là phản ứng (1).
| Câu hỏi 2: Từ Thí nghiệm 1, hãy cho biết:
a) Dựa vào dấu hiệu nào để biết trạng thái cân bằng của phản ứng (8) bị chuyển dịch khi thay đổi nhiệt độ. b*) Khi tăng nhiệt độ hoặc giảm nhiệt độ, cân bằng chuyển dịch theo chiều thu nhiệt hay toả nhiệt? |
Phương pháp:
Khi một phản ứng thuận nghịch ở trạng thái cân bằng, nếu thay đổi nhiệt độ thì cân bằng cũ sẽ bị phá vỡ, cân bằng mới được hình thành theo chiều làm giảm sự thay đổi nhiệt độ đó. Ta gọi đây là sự chuyển dịch cân bằng (từ cân bằng cũ sang cân bằng mới).
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
\[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\] > 0: Phản ứng thu nhiệt.
\[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\] < 0: Phản ứng tỏa nhiệt.
Lời giải chi tiết:
a) Dựa vào màu sắc của hỗn hợp khí, ta biết được trạng thái cân bằng của phản ứng (8) bị chuyển dịch khi thay đổi nhiệt độ.
b) 2NO2(g) ⇌ N2O4(g) (8) \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= -58 kJ
(nâu đỏ) (không màu)
Theo chiều thuận: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= -58 kJ < 0 → Chiều thuận tỏa nhiệt.
Theo chiều nghịch: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= 58 kJ > 0 → Chiều nghịch thu nhiệt.
Khi tăng nhiệt độ, hỗn hợp có màu nâu đậm hơn, cân bằng chuyển dịch theo tạo ra NO2 hay cân bằng chuyển dịch theo chiều thu nhiệt.
Khi hạ nhiệt độ, hỗn hợp trở nên nhạt màu hơn, cân bằng chuyển dịch theo chiều tạo ra N2O4 hay cân bằng chuyển dịch theo chiều tỏa nhiệt.
CH tr 12
Video hướng dẫn giải
| Câu hỏi 1: Dựa vào thí nghiệm 2, cho biết khi tăng nhiệt độ thì cân bằng (9) chuyển dịch theo chiều thuận hay chiều nghịch? |
Phương pháp:
Khi một phản ứng thuận nghịch ở trạng thái cân bằng, nếu thay đổi nhiệt độ thì cân bằng cũ sẽ bị phá vỡ, cân bằng mới được hình thành theo chiều làm giảm sự thay đổi nhiệt độ đó. Ta gọi đây là sự chuyển dịch cân bằng (từ cân bằng cũ sang cân bằng mới).
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
CH3COO- + H2O ⇌ CH3COOH + OH- (9)
Sau khi đun nóng ống nghiệm B, màu hồng trong ống nghiệm B đậm hơn ống nghiệm A. Chứng tỏ, trong ống nghiệm B, khi tăng nhiệt độ cân bằng chuyển dịch theo chiều thuận tạo NaOH, nồng độ NaOH tăng, làm chỉ thị phenolphthalein hóa hồng đậm hơn.
| Câu hỏi 2: Cân bằng sau chuyển dịch theo chiều nào khi tăng nhiệt độ?
2SO2 (g) + O2 (g) ⇌ 2SO3 (g) \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}{\rm{ = - 197}}{\rm{,8 kJ}}\] |
Phương pháp:
Khi một phản ứng thuận nghịch ở trạng thái cân bằng, nếu thay đổi nhiệt độ thì cân bằng cũ sẽ bị phá vỡ, cân bằng mới được hình thành theo chiều làm giảm sự thay đổi nhiệt độ đó. Ta gọi đây là sự chuyển dịch cân bằng (từ cân bằng cũ sang cân bằng mới).
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
Theo chiều thuận: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= -197,8 kJ < 0 → Chiều thuận tỏa nhiệt.
Theo chiều nghịch: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= 197,8 kJ > 0 → Chiều nghịch thu nhiệt.
Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm tác động của việc tăng nhiệt độ, nghĩa là cân bằng chuyển dịch theo chiều thu nhiệt (chiều nghịch).
| Câu hỏi 3: Cân bằng 2NO2 (g) ⇌ N2O4 (g) chuyển dịch theo chiều nào khi tăng áp suất của hỗn hợp (bằng cách nén hỗn hợp) ở điều kiện nhiệt độ không đổi. Biết rằng áp suất tỉ lệ với số mol chất khí. |
Phương pháp:
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
Số mol khí vế trái: 2 mol.
Số mol khí vế phải: 1 mol.
Khi tăng áp suất của hỗn hợp (bằng cách nén hỗn hợp) ở điều kiện nhiệt độ không đổi, cân bằng chuyển dịch theo chiều làm giảm áp suất, nghĩa là cân bằng chuyển dịch theo chiều làm giảm số mol khí - cân bằng chuyển dịch theo chiều thuận.
CH tr 13
Video hướng dẫn giải
| Câu hỏi 1: Quá trình tổng hợp NH3 trong công nghiệp từ N2, và H2 nên thực hiện ở áp suất cao hay áp suất thấp? Giải thích. Tìm hiểu thông tin, cho biết phản ứng tổng hợp NH3 ở các nhà máy thường được thực hiện ở áp suất nào. |
Phương pháp:
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Tổng số mol khí ở vế trái: 1 + 3 = 4 (mol)
Số mol khí ở vế phải: 2 (mol)
Khi tăng áp suất, hệ cân bằng chuyển dịch theo chiều làm giảm áp suất của hệ (giảm số mol khí của hệ). Cân bằng trên chuyển dịch theo chiều thuận (chiều tạo NH3). Khi giảm áp suất, hệ cân bằng chuyển dịch theo chiều làm tăng áp suất của hệ (tăng số mol khí của hệ). Cân bằng trên chuyển dịch theo chiều nghịch (chiều phân hủy NH3).
Vậy để thu được NH3 với hiệu suất cao, người ta thực hiện phản ứng ở áp suất cao.
Thực tế, phản ứng tổng hợp NH3 ở các nhà máy thường được thực hiện ở áp suất 200 – 300 atm.
| Câu hỏi 2: Thành phần chính của tinh dầu chuối là ester CH3COOCH2CH2CH(CH3)2. Để thu được hỗn hợp chất chứa nhiều ester này thì cần thay đổi nồng độ các chất như thế nào trong cân bằng:
CH3COOOH (aq) + ROH (aq) ⇌ CH3COOR (aq) + H2O (l) Với R là (CH3)2 CH CH2CH2- |
Phương pháp:
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
Khi tăng nồng độ của các chất phản ứng như \[{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}{\rm{, ROH}}\]- cân bằng chuyển dịch theo chiều làm giảm nồng độ \[{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}{\rm{, ROH}}\]nghĩa là cân bằng chuyển dịch theo chiều thuận (chiều tạo thành ester).
Khi giảm nồng độ của các chất \[{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOR}}{\rm{, }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\]- cân bằng chuyển dịch theo chiều làm tăng nồng độ \[{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOR}}{\rm{, }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\]nghĩa là cân bằng cân bằng chuyển dịch theo chiều thuận (chiều tạo thành ester).
CH tr 14
Video hướng dẫn giải
| Câu hỏi 2: Phát biểu nào sau đây về một phản ứng thuận nghịch tại trạng thái cân bằng là sai?
A. Tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch. B. Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi. C. Nồng độ mol của chất phản ứng luôn bằng nồng độ mol của chất sản phẩm phản ứng. D. Phản ứng thuận và phản ứng nghịch vẫn diễn ra. |
Phương pháp:
Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Tuy nhiên, ở trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn tiếp diễn với tốc độ bằng nhau nhưng nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó là bằng nhau. Như vậy, cân bằng hoá học là cân bằng động.
Lời giải chi tiết:
Phát biểu sai: C
Khi phản ứng thuận nghịch đạt trạng thái cân bằng, nồng độ mol của chất phản ứng và các chất sản phẩm không đổi. Tùy thuộc vào hệ số tỉ lượng của phương trình phản ứng và thời điểm đạt trạng thái cân bằng, không phải lúc nồng độ mol của chất phản ứng cũng bằng nồng độ mol của chất sản phẩm phản ứng.
| Câu hỏi 2: Cho 0,4 mol SO2 và 0,6 mol O2vào một bình dung tích 1 lít được giữ ở một nhiệt độ không đổi. Phản ứng trong bình xảy ra như sau:
2SO2 (g) + O2 (g) ⇌ 2SO3 (g) Khi phản ứng đạt đến trạng thái cân bằng, lượng SO3 trong bình là 0,3 mol. Tính hằng số cân bằng KC của phản ứng tổng hợp SO3 ở nhiệt độ trên. |
Phương pháp:
aA + bB ⇌ mM + nM
Khi đó biểu thức tính hằng số cân bằng KC như sau: \[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[M]}}}^{\rm{m}}}{{{\rm{[N]}}}^{\rm{n}}}}}{{{{{\rm{[A]}}}^{\rm{a}}}{{{\rm{[B]}}}^{\rm{b}}}}}\]
Trong đó: a, b, m, n lần lượt là hệ số tỉ lượng tương ứng của các chất A, B, M, N trong phương trình hoá học; (A), (B), (M), (N) lần lượt là nồng độ mol của các chất A, B, M, N ở trạng thái cân bằng.
Lời giải chi tiết:
\[{{\rm{C}}_{{\rm{M(S}}{{\rm{O}}_{\rm{2}}}{\rm{)}}}}{\rm{ = }}\frac{{{\rm{0}}{\rm{,4}}}}{{\rm{1}}}{\rm{ = 0}}{\rm{,4 (M); }}{{\rm{C}}_{{\rm{M(}}{{\rm{O}}_{\rm{2}}}{\rm{)}}}}{\rm{ = }}\frac{{{\rm{0}}{\rm{,6}}}}{{\rm{1}}}{\rm{ = 0}}{\rm{,6 (M); [S}}{{\rm{O}}_{\rm{3}}}{\rm{] = }}\frac{{{\rm{0}}{\rm{,3}}}}{{\rm{1}}}{\rm{ = 0}}{\rm{,3(M)}}\]
Theo tỉ lệ phản ứng; 2 : 1 : 2
2SO2 (g) + O2 (g) ⇌ 2SO3 (g)
Ban đầu: 0,4 0,6
Phản ứng: 0,3 ← 0,15 ← 0,3
Cân bằng: 0,1 0,45 0,3
\[{{\rm{K}}_{\rm{C}}}{\rm{ = }}\frac{{{{{\rm{[S}}{{\rm{O}}_{\rm{3}}}{\rm{]}}}^{\rm{2}}}}}{{{{{\rm{[S}}{{\rm{O}}_{\rm{2}}}{\rm{]}}}^{\rm{2}}}{\rm{[}}{{\rm{O}}_{\rm{2}}}{\rm{]}}}} = \frac{{{{0,3}^2}}}{{{{0,1}^2}.0,45}} = 20\]
| Câu hỏi 3: Nhũ đá được hình thành trong các hang động liên quan đến cân bằng sau đây:
Ca(HCO3)2(aq) ⇌ CaCO3(s) + CO2(aq) + H2O(1) Nếu nồng độ CO2 hoà tan trong nước tăng lên thì có thuận lợi cho sự hình thành nhũ đá hay không? Giải thích. |
Phương pháp:
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Lời giải chi tiết:
Phản ứng hình thành thạch nhũ là phản ứng xảy ra theo chiều thuận. Nếu nồng độ CO2 hoà tan trong nước tăng lên, cân bằng chuyển dịch theo chiều làm giảm nồng độ CO2 – cân bằng chuyển dịch theo chiều nghịch, không thuận lợi cho sự hình thành nhũ đá.
Các bài khác cùng chuyên mục
- Bài 19: Carboxylic acid trang 132, 133, 134, 135, 136, 137, 138, 139 Hóa học 11 Cánh diều
- Bài 18: Hợp chất carbonyl trang 122, 123, 124, 125, 126, 127, 128, 129, 130, 131 Hóa học 11 Cánh diều
- Bài 17: Phenol trang 116, 117, 118, 119, 120, 121 Hóa học 11 Cánh diều
- Bài 16: Alcohol trang 107, 108, 109, 110, 111, 112, 113, 114, 115 Hóa học 11 Cánh diều
- Bài 15: Dẫn xuất halogen trang 100, 101, 102, 103, 104, 105, 106 Hóa học 11 Cánh diều













Danh sách bình luận