 Đề thi khoa học tự nhiên 7, đề kiểm tra khoa học tự nhiên 7 kết nối tri thức với cuộc sống có đáp án và lời giải chi tiết
Đề thi khoa học tự nhiên 7, đề kiểm tra khoa học tự nhiên 7 kết nối tri thức với cuộc sống có đáp án và lời giải chi tiết
 Đề thi giữa kì 1 KHTN 7 - Kết nối tri thức
Đề thi giữa kì 1 KHTN 7 - Kết nối tri thức Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 8
“Trên cơ sở các sổ liệu và phân tích số liệu, con người có thể đưa ra các dự báo hay dự đoán tính chất của sự vật, hiện tượng, nguyên nhân của hiện tượng!” Đó là kĩ năng nào?
Đề thi
Câu 1: “Trên cơ sở các sổ liệu và phân tích số liệu, con người có thể đưa ra các dự báo hay dự đoán tính chất của sự vật, hiện tượng, nguyên nhân của hiện tượng!” Đó là kĩ năng nào?
A. Kĩ năng quan sát, phân loại. B. Kĩ năng liên kết tri thức.
C. Kĩ năng dự báo. D. Kĩ năng đo.
Câu 2: Nguyên tử luôn trung hoà về điện nên
A. số hạt proton = số hạt neutron.
B. số hạt electron = số hạt neutron.
C. số hạt electron = số hạt proton.
D. số hạt proton = số hạt electron = số hạt neutron.
Câu 3: Nguyên tử của nguyên tố X có tổng số hạt là 40 .Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. X có số đơn vị điện tích hạt nhân là
A. 12. B. 13. C. 14. D. 15.
Câu 4: Đây là sơ đồ nguyên tử nguyên tố nào?
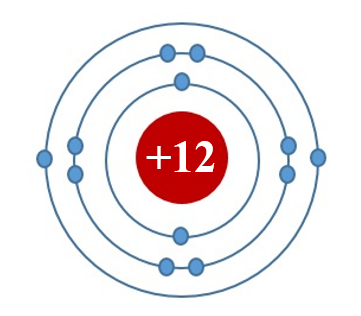
A. Na. B. N.
C. Mg. D. Al.
Câu 5: Trong số các chất dưới đây, thuộc loại hợp chất có:
A. Khí hidro. B. Nhôm.
C. Photpho. D. Đá vôi.
Câu 6: Liên kết cộng hóa trị được hình thành do
A. lực hút tĩnh điện yếu giữa các nguyên tử.
B. các cặp electron dùng chung.
C. các đám mây electron.
D. các electron hoá trị.
Câu 7: Số thứ tự chu kì trong bảng hệ thống tuần hoàn cho biết:
A. Số thứ tự của nguyên tố B. số hiệu nguyên tử
C. Số electron lớp ngoài cùng D. số lớp electron
Câu 8: Chu kì 3 của bảng hệ thống tuần hoàn có
A. 2 nguyên tố. B. 8 nguyên tố. C. 10 nguyên tố. D. 18 nguyên tố.
Câu 9: Nguyên tử của nguyên tố Y có 2 lớp electron, trong đó lớp ngoài cùng có 4 electron. Vị trí
của Y trong bảng tuần hoàn là
A. chu kỳ 2, nhóm IVA. B. chu kỳ 4, nhóm IIA.
C. chu kỳ 2, nhóm IIA. D. chu kỳ 4, nhóm IVA.
Câu 10: Nguyên tố nào sau đây là nguyên tố là phi kim?
A. Na. B. S. C. Al. D. Be.
Câu 11: Phát biểu nào sau đây là đúng?
A. Bảng tuần hoàn gồm 116 nguyên tố hóa học.
B. Bảng tuần hoàn gồm 6 chu kì.
C. Bảng tuần hoàn gồm 8 nhóm A và 8 nhóm B.
D. Các nguyên tố trong bảng tuần hoàn được xếp theo chiều tăng dần khối lượng nguyên tử.
Câu 12: Cho các nguyên tố sau: Ge, S, Br, Pb, C, Mo, Ba, Ar, Hg. Số nguyên tố kim loại, phi kim,
khí hiếm lần lượt là
A. 4, 4, 1. B. 4, 3, 2. C. 5, 2, 2. D. 5, 3, 1.
II. TỰ LUẬN
Câu 1: Nguyên tử của nguyên tố X có tổng số hạt p, n và e là 40, số hạt không mang điện nhiều hơn số hạt mang điện dương là 1. Tính số hạt p, n, e
Câu 2: Nguyên tố phosphorus (P) có Z = 15, có trong thành phần một loại phân bón, diêm, pháo hoa; nguyên tố calcium (Ca) có Z = 20 đóng vai trò quan trọng đối với cơ thể, đặc biệt là xương và răng.
(a) Hãy xác định vị trí của hai nguyên tố trên trong bảng tuần hoàn.
(b) Cho biết chúng thuộc loại nguyên tố kim loại, phi kim hay khí hiếm?
Đáp án
Phần trắc nghiệm
|
1C |
2C |
3B |
4C |
5D |
6B |
|
7D |
8D |
9A |
10B |
11C |
12D |
Câu 1: “Trên cơ sở các sổ liệu và phân tích số liệu, con người có thể đưa ra các dự báo hay dự đoán tính chất của sự vật, hiện tượng, nguyên nhân của hiện tượng!” Đó là kĩ năng nào?
A. Kĩ năng quan sát, phân loại. B. Kĩ năng liên kết tri thức.
C. Kĩ năng dự báo. D. Kĩ năng đo.
Lời giải chi tiết
Đáp án C
Câu 2: Nguyên tử luôn trung hoà về điện nên
A. số hạt proton = số hạt neutron.
B. số hạt electron = số hạt neutron.
C. số hạt electron = số hạt proton.
D. số hạt proton = số hạt electron = số hạt neutron.
Phương pháp giải
Hạt proton mang điện tích dương, hạt electron mang điện tích âm vì vậy nguyên tử trung hòa về điện khi p = e
Lời giải chi tiết
Đáp án C
Câu 3: Nguyên tử của nguyên tố X có tổng số hạt là 40 .Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. X có số đơn vị điện tích hạt nhân là
A. 12. B. 13. C. 14. D. 15.
Phương pháp giải
Dựa vào tổng số hạt của nguyên tố X
Lời giải chi tiết
(1) P + E + N = 40
(2) P + E = 12 + N
=> P = 13
Đáp án B
Câu 4: Đây là sơ đồ nguyên tử nguyên tố nào?
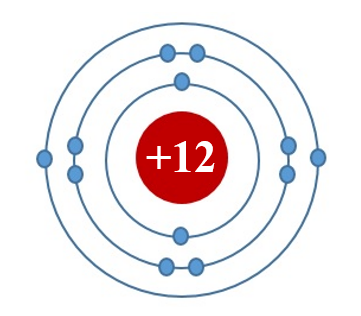
A. Na. B. N.
C. Mg. D. Al.
Phương pháp giải
Dựa vào điện tích hạt nhân
Lời giải chi tiết
Đáp án C
Câu 5: Trong số các chất dưới đây, thuộc loại hợp chất có:
A. Khí hidro. B. Nhôm.
C. Photpho. D. Đá vôi.
Phương pháp giải
Hợp chất được cấu tạo từ nguyên tử của 2 nguyên tố trở lên
Lời giải chi tiết
Đáp án D
Câu 6: Liên kết cộng hóa trị được hình thành do
A. lực hút tĩnh điện yếu giữa các nguyên tử.
B. các cặp electron dùng chung.
C. các đám mây electron.
D. các electron hoá trị.
Lời giải chi tiết
Đáp án B
Câu 7: Số thứ tự chu kì trong bảng hệ thống tuần hoàn cho biết:
A. Số thứ tự của nguyên tố B. số hiệu nguyên tử
C. Số electron lớp ngoài cùng D. số lớp electron
Phương pháp giải
Số thứ tự chu kì = số lớp electron
Lời giải chi tiết
Đáp án D
Câu 8: Chu kì 3 của bảng hệ thống tuần hoàn có
A. 2 nguyên tố. B. 8 nguyên tố. C. 10 nguyên tố. D. 18 nguyên tố.
Lời giải chi tiết
Đáp án D
Câu 9: Nguyên tử của nguyên tố Y có 2 lớp electron, trong đó lớp ngoài cùng có 4 electron. Vị trí
của Y trong bảng tuần hoàn là
A. chu kỳ 2, nhóm IVA. B. chu kỳ 4, nhóm IIA.
C. chu kỳ 2, nhóm IIA. D. chu kỳ 4, nhóm IVA.
Phương pháp giải
Dựa vào số lớp electron và số electron lớp ngoài cùng để xác định vị trí của Y
Lời giải chi tiết
Đáp án A
Câu 10: Nguyên tố nào sau đây là nguyên tố là phi kim?
A. Na. B. S. C. Al. D. Be.
Phương pháp giải
Kim loại có 1, 2, 3 hoặc 4 e lớp ngoài cùng
Phi kim có 4, 5, 6, 7 e lớp ngoài cùng
Lời giải chi tiết
Đáp án B
Câu 11: Phát biểu nào sau đây là đúng?
A. Bảng tuần hoàn gồm 116 nguyên tố hóa học.
B. Bảng tuần hoàn gồm 6 chu kì.
C. Bảng tuần hoàn gồm 8 nhóm A và 8 nhóm B.
D. Các nguyên tố trong bảng tuần hoàn được xếp theo chiều tăng dần khối lượng nguyên tử.
Lời giải chi tiết
Đáp án C
Câu 12: Cho các nguyên tố sau: Ge, S, Br, Pb, C, Mo, Ba, Ar, Hg. Số nguyên tố kim loại, phi kim,
khí hiếm lần lượt là
A. 4, 4, 1. B. 4, 3, 2. C. 5, 2, 2. D. 5, 3, 1.
Phương pháp giải
Kim loại có 1, 2, 3 hoặc 4 e lớp ngoài cùng
Phi kim có 4, 5, 6, 7 e lớp ngoài cùng
Lời giải chi tiết
Đáp án D
II. Tự luận
Câu 1: Nguyên tử của nguyên tố X có tổng số hạt p, n và e là 40, số hạt không mang điện nhiều hơn số hạt mang điện dương là 1. Tìm số hạt p, n, e
Lời giải chi tiết
(1) P + E + N = 40
(2) N = P + 1
Thay (2) vào (1) ta được: P + E + P + 1 = 40
Mà P = E => 3P = 30 => P = E = 13; N = 14
Câu 2: Nguyên tố phosphorus (P) có Z = 15, có trong thành phần một loại phân bón, diêm, pháo hoa; nguyên tố calcium (Ca) có Z = 20 đóng vai trò quan trọng đối với cơ thể, đặc biệt là xương và răng.
(a) Hãy xác định vị trí của hai nguyên tố trên trong bảng tuần hoàn.
(b) Cho biết chúng thuộc loại nguyên tố kim loại, phi kim hay khí hiếm?
Lời giải chi tiết
a) Nguyên tố P: ô số 15, nhóm VA, chu kì 3
b) Nguyên tố Ca: sô số 20, nhóm IIA, chu kì 4
b) Nguyên tố P thuộc phi loại vì có 5 electron lớp ngoài cùng; Ca thuộc kim loại vì có 2 electron lớp ngoài cùng
- Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 9
- Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 10
- Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 11
- Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 12
- Đề thi giữa kì 1 KHTN 7 Kết nối tri thức - Đề số 13
>> Xem thêm
Luyện Bài Tập Trắc nghiệm KHTN 7 - Kết nối tri thức - Xem ngay












Danh sách bình luận