10 câu hỏi vận dụng áp dụng phương pháp biện luận có lời giải
Làm đề thiCâu hỏi 1 :
Hòa tan hoàn toàn 2,4 gam kim loại M bằng dung dịch HCl vừa đủ thu được 2,24 lít H2(đktc)
Kim loại M là
- A Mg
- B Al
- C Zn
- D Fe
Đáp án: A
Phương pháp giải:
nH2 = VH2/ 22,4 = 0,1 mol
2M + 2nHCl →2MCln + nH2
0,1.2/n 0,1
\(\begin{gathered}
{n_M} = \frac{2}{n}{n_{{H_2}}} = \frac{2}{n}.0,1 \hfill \\
\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, = \frac{{0,2}}{n} \hfill \\
M = \frac{{2,4}}{{0,2}}.n = 12n \hfill \\
\end{gathered} \)
Biện luận M theo n
Lời giải chi tiết:
nH2 = VH2/ 22,4 = 0,1 mol
2M + 2nHCl →2MCln + nH2
0,1.2/n 0,1
\(\begin{gathered}
{n_M} = \frac{2}{n}{n_{{H_2}}} = \frac{2}{n}.0,1 \hfill \\
\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, = \frac{{0,2}}{n} \hfill \\
M = \frac{{2,4}}{{0,2}}.n = 12n \hfill \\
\end{gathered} \)

=> M =24 (Mg)
Đáp án A
Câu hỏi 2 :
Cho 13 gam kim loại M tác dụng với dung dịch H2SO4 loãng dư thu được dung dịch chứa 32,2 gam muối khan. Xác định M
- A Cu
- B Fe
- C Zn
- D Mg
Đáp án: C
Phương pháp giải:
2M+n H2SO4 →M2(SO4)n + nH2
mmuối = mKl + mSO4
32,2 = 13 + mSO4
=> mSO4 = 19,2 gam
=> nSO4= 0,2 mol
nM = \(\frac{2}{n}{n_{S{O_4}}} = \frac{{0,4}}{n}\)
=> M= 32,5 n
=> biện luận M theo n
Lời giải chi tiết:
2M+n H2SO4 →M2(SO4)n + nH2
mmuối = mKl + mSO4
32,2 = 13 + mSO4
=> mSO4 = 19,2 gam
=> nSO4= 0,2 mol
nM = \(\frac{2}{n}{n_{S{O_4}}} = \frac{{0,4}}{n}\)
=> M= 32,5 n
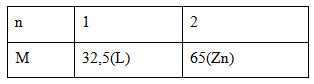
=> M: Zn
Đáp án C
Câu hỏi 3 :
Cho 2,016 gam kim loại X tác dụng hết với oxi thu được 2,784 gam chất rắn . Kim loại M là
- A Cu
- B Fe
- C Zn
- D Mg
Đáp án: B
Phương pháp giải:
Gọi công thức phải tìm là MxOy
BTKL mX + mO2 = mchất rắn
=> mO2 = 2,784-2,016= 0,768 g
=> nO2= 0,024 mol => nO (oxit) = 0,048
\(\frac{x}{y} = \frac{{{n_M}}}{{{n_O}}} = \frac{{2,016}}{{0,048M}} \to M = \frac{{42y}}{x}\)
=> biện luận M theo x,y
Lời giải chi tiết:
Gọi công thức phải tìm là MxOy
BTKL mX + mO2 = mchất rắn
=> mO2 = 2,784-2,016= 0,768 g
=> nO2= 0,024 mol => nO (oxit) = 0,048
\(\frac{x}{y} = \frac{{{n_M}}}{{{n_O}}} = \frac{{2,016}}{{0,048M}} \to M = \frac{{42y}}{x}\)
Xét cá tỉ số \(\frac{x}{y} = \frac{1}{1},\frac{1}{2},\frac{1}{3},\frac{2}{1},\frac{2}{3},\frac{3}{4}\) chỉ có x=3, y=4 thỏa mãn
M= 42.4/3= 56 (Fe)
Đáp án B
Câu hỏi 4 :
Hoà tan hoàn toàn 19,5 g một kim loại R hóa trị không đổi tác dụng hết với 300 mldung dịch CuCl2 1M Tìm kim loại R.
- A Mg
- B Al
- C Zn
- D Fe
Đáp án: C
Phương pháp giải:
nCuCl2 = CM.V= 0,3 mol
2R + nCuCl2 →2RCln +n Cu
0,6/n 0,3
R = m/n = 19,5n/0,6= 32,5n
biện luận R theo n
Lời giải chi tiết:
nCuCl2 = CM.V= 0,3 mol
2R + nCuCl2 →2RCln +n Cu
0,6/n 0,3
R = m/n = 19,5n/0,6= 32,5n
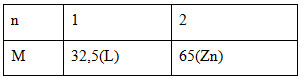
Đáp án C
Câu hỏi 5 :
Cho 4,75 g muối clorua của kim loại R (hóa trị không đổi) tác dụng với dung dịch AgNO3 thì thu được 14,35 g kết tủa AgCl. Công thức muối sắt là
- A Mg
- B Al
- C Zn
- D Fe
Đáp án: A
Phương pháp giải:
gọi công thức của muối cần tìm là RClx ( x là hóa trị của Fe)
nAgCl = m/M = 0,1 mol
RClx +x AgNO3 →R(NO3)x + xAgCl
0,1/x 0,1
=> R + 35,5x = 4,75x/0,1= 47,5
=> M= 12n
biện luận M theo n
Lời giải chi tiết:
gọi công thức của muối cần tìm là RClx ( x là hóa trị của Fe)
nAgCl = m/M = 0,1 mol
RClx +x AgNO3 →R(NO3)x + xAgCl
0,1/x 0,1
=> R + 35,5x = 4,75x/0,1= 47,5
=> M= 12n

Đáp án A
Câu hỏi 6 :
Hoà tan 3,06g oxit MxOy bằng dung dich HNO3 dư sau đó cô cạn thì thu được 5,22g muối khan. Hãy xác định kim loại M biết nó chỉ có một hoá trị duy nhất.
- A Ca
- B Ba
- C Mg
- D Al
Đáp án: B
Phương pháp giải:
MxOy + 2yHNO3 → xM(NO3)2y/x + yH2O
\(\frac{{5,22}}{{M{\text{x}} + 124y}}\) \(\frac{{5,22}}{{M + 62.2y/x}}\)
noxit =\(\frac{{5,22}}{{M{\text{x}} + 124y}}\) = \(\frac{{3,06}}{{M{\text{x}} + 16y}}\)
=> M= 137y/x
Biện luận giá trị x, y =?
Lời giải chi tiết:
MxOy + 2yHNO3 → xM(NO3)2y/x + yH2O
\(\frac{{5,22}}{{M{\text{x}} + 124y}}\) \(\frac{{5,22}}{{M + 62.2y/x}}\)
noxit =\(\frac{{5,22}}{{M{\text{x}} + 124y}}\) = \(\frac{{3,06}}{{M{\text{x}} + 16y}}\)
=> M= 137y/x
=> y = 2, x= 2 thỏa mãn
M= 137 (Ba)
Đáp án B
Câu hỏi 7 :
Cho 29,4 gam hỗn hợp X gồm 2 muối A2SO4 và BSO4 (MA = MB +15) tác dụng với dung dịch BaCl2 dư thu được 46,6 gam kết tủa. Xác định 2 kim loại A và B
- A Na, Mg
- B K, Mg
- C Na, Ba
- D K, Ba
Đáp án: B
Phương pháp giải:
\(\begin{gathered}
\overline M S{O_4} + BaC{l_2} \to \overline M C{l_2} + Ba\,S{O_4} \hfill \\
0,2\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,2 \hfill \\
\overline M + 96 = \frac{{29,4}}{{0,2}} = 147 \hfill \\
\overline M = 51 \hfill \\
\end{gathered} \)
\(\begin{gathered}
\left\{ \begin{gathered}
2{\text{A}} > 51 \hfill \\
B < 51 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
2{\text{A > 51}} \hfill \\
A - 15 < 51 \hfill \\
\end{gathered} \right. \hfill \\
25,5 < A < 66 \hfill \\
\end{gathered} \)
Lời giải chi tiết:
\(\begin{gathered}
\overline M S{O_4} + BaC{l_2} \to \overline M C{l_2} + Ba\,S{O_4} \hfill \\
0,2\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,2 \hfill \\
\overline M + 96 = \frac{{29,4}}{{0,2}} = 147 \hfill \\
\overline M = 51 \hfill \\
\end{gathered} \)
\(\begin{gathered}
\left\{ \begin{gathered}
2{\text{A}} > 51 \hfill \\
B < 51 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
2{\text{A > 51}} \hfill \\
A - 15 < 51 \hfill \\
\end{gathered} \right. \hfill \\
25,5 < A < 66 \hfill \\
\end{gathered} \)
=> A=39(K)
=> B= 24 (Mg)
Đáp án B
Câu hỏi 8 :
Hòa tan hết 16,2 gam kim loại X bằng 5 lít HNO3 0,5 M. Sau phản ứng kết thúc thu được 5,6 lít hỗn hợp khí NO và N2 (đktc) nặng 7,2 gam. Kim loại X là
- A Mg
- B Al
- C Zn
- D Fe
Đáp án: B
Phương pháp giải:
Gọi số mol của NO và N2 lần lượt là x,y
\(\left\{ \begin{gathered}
x + y = 0,3 \hfill \\
30{\text{x}} + 28y = 7,2 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x = 0,1 \hfill \\
y = 0,15 \hfill \\
\end{gathered} \right.\)
X - ne →X+n
1,8/n 1,8
N+5 + 3e →N+2
0,3 0,1
2N+5 + 10e →N20
1,5 0,15
=> X= 16,2n/1,8 = 9n
Lời giải chi tiết:
Gọi số mol của NO và N2 lần lượt là x,y
\(\left\{ \begin{gathered}
x + y = 0,3 \hfill \\
30{\text{x}} + 28y = 7,2 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x = 0,1 \hfill \\
y = 0,15 \hfill \\
\end{gathered} \right.\)
X - ne →X+n
1,8/n 1,8
N+5 + 3e → N+2
0,3 0,1
2N+5 + 10e →N20
1,5 0,15
=> X= 16,2n/1,8 =9n

Đáp án B
Câu hỏi 9 :
Hòa tan 9,6 gam hỗn hợp gồm kim loại M hóa trị II (không đổi) và oxit của nó bằng dung dịch HCl dư thu được dung dịch chứa 22,2 gam muối khan. Xác định M
- A Al
- B Mg
- C Ca
- D Ba
Đáp án: C
Phương pháp giải:
M + 2HCl →MCl2 +H2
x x
MO + 2HCl →MCl2 +H2O
y y
Mx+ (M+16)y= 9,4
<=> M(x+y) +16y=9,4
(M+71)(x+y)=22,2
<=> M(x+y)+ 71(x+y)=22,2
=> 71x+ 55y=12,8
55(x+y) < 12,8 < 71(x+y)
0,1803 < x+y < 0,2327
=> 0,1803.(M+71) < 22,2 < 0,2327.(M+71)
=> 24,4 < M < 52,13
Lời giải chi tiết:
M + 2HCl →MCl2 +H2
x x
MO + 2HCl →MCl2 +H2O
y y
Mx+ (M+16)y= 9,4
<=> M(x+y) +16y=9,4
(M+71)(x+y)=22,2
<=> M(x+y)+ 71(x+y)=22,2
=> 71x+ 55y=12,8
55(x+y) < 12,8 < 71(x+y)
0,1803 < x+y < 0,2327
=> 0,1803.(M+71) < 22,2 < 0,2327.(M+71)
=> 24,4 < M < 52,13
M hóa trị II không đổi => M= 40 (Ca)
Đáp án C
Câu hỏi 10 :
Cho 16,2 gam một hỗn hợp gồm kim loại kiềm A và oxit của nó tan hết trong nước thu được dung dịch B và trung hòa hết 1/10 dung dịch B cần 200 ml H2SO4 0,15M. Kim loại A là
- A Li
- B Na
- C K
- D Rb
Đáp án: B
Phương pháp giải:
nH2SO4 = 10.(CM.V) = 10.(0,2.0,15)=0,3 mol
2AOH + H2SO4 →A2SO4 + 2H2O
0,6 0,3
A + H2O →AOH + 0,5 H2
x x
A2O + H2O →2AOH
y 2y
\(\left\{ \begin{gathered}
x + 2y = 0,6 \hfill \\
A.x + (2{\text{A}} + 16)y = 16,2 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x + 2y = 0,6 \hfill \\
A.(x + 2y) + 16y = 16,2 \hfill \\
\end{gathered} \right. \to y = \frac{{(16,2 - 0,6{\text{A}})}}{{16}}\)
Ta có 0 < y < 0,3
* 0 < y => 0< 16,2-0,6A => A < 27
* y < 0,3 => \(\frac{{(16,2 - 0,6{\text{A}})}}{{16}} < 0,3 \to A > 19\)
19 < A < 27
Lời giải chi tiết:
nH2SO4 = 10.(CM.V) = 10.(0,2.0,15)=0,3 mol
2AOH + H2SO4 →A2SO4 + 2H2O
0,6 0,3
A + H2O →AOH + 0,5 H2
x x
A2O + H2O →2AOH
y 2y
\(\left\{ \begin{gathered}
x + 2y = 0,6 \hfill \\
A.x + (2{\text{A}} + 16)y = 16,2 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x + 2y = 0,6 \hfill \\
A.(x + 2y) + 16y = 16,2 \hfill \\
\end{gathered} \right. \to y = \frac{{(16,2 - 0,6{\text{A}})}}{{16}}\)
Ta có 0 < y < 0,3
* 0 < y => 0< 16,2-0,6A => A < 27
* y < 0,3 => \(\frac{{(16,2 - 0,6{\text{A}})}}{{16}} < 0,3 \to A > 19\)
19 < A < 27
Vì A là kim loại kiềm => chỉ có A=23 thỏa mãn => A: Na
Đáp án B
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 20 bài tập vận dụng áp dụng định luật bảo toàn khối lượng có lời giải
- 15 bài tập áp dụng định luật tăng giảm khối lượng có lời giải
- 10 bài tập vận dụng áp dụng phương pháp tương đương (công thức trung bình) có lời giải
- 10 câu hỏi vận dụng áp dụng phương pháp biện luận có lời giải
- 10 bài tập vận dụng áp dụng phương pháp bảo toàn nguyên tố có lời giải
- 10 bài tập vận dụng về phương pháp qui đổi có lời giải
- 10 bài tập vận dụng áp dụng phương pháp bảo toàn nguyên tố có lời giải
- 10 câu hỏi vận dụng áp dụng phương pháp biện luận có lời giải
- 10 bài tập vận dụng áp dụng phương pháp tương đương (công thức trung bình) có lời giải
- 15 bài tập áp dụng định luật tăng giảm khối lượng có lời giải







