10 bài tập về mối quan hệ giữa các hợp chất vô cơ có lời giải
Làm đề thiCâu hỏi 1 :
Cặp chất nào sau đây có thể phản ứng với nhau:
- A HCl và Na2SO4
- B NaOH và BaCl2
- C AgCl và NaNO3
- D H2SO4 và BaCO3
Đáp án: D
Lời giải chi tiết:
A sai 2 chất này không pư
B sai 2 chất này không pư
C sai 2 chất này không pư
D đúng vì BaCO3 + H2SO4 → BaSO4 + H2O + CO2
Đán án D
Câu hỏi 2 :
Viết 01 phương trình hóa học của phản ứng giữa các chất sau với tỉ lệ mol đã cho (các phản ứng là hoàn toàn, vừa đủ)
a.\(S{O_2}{\rm{ }} + {\rm{ }}Ca{\left( {OH} \right)_2}\buildrel {1:1} \over\longrightarrow \)
b. \(Ba{\left( {HC{O_3}} \right)_2}{\rm{ }} + {\rm{ }}NaOH\buildrel {1:1} \over\longrightarrow \)
c.\(P{\rm{ }} + {\rm{ }}C{l_2}\buildrel {2:3} \over\longrightarrow \)
d. \(C{a_3}{\left( {P{O_4}} \right)_2}{\rm{ }} + {\rm{ }}{H_2}S{O_4}\buildrel {1:2} \over\longrightarrow \)
e. \({H_3}P{O_4}{\rm{ }} + {\rm{ }}KOH\buildrel {1:3} \over\longrightarrow \)
g. \(C{O_2}{\rm{ }} + {\rm{ }}NaOH\buildrel {1:1} \over\longrightarrow \)
Lời giải chi tiết:
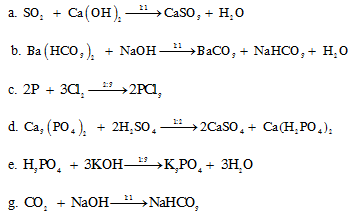
Câu hỏi 3 :
Cho dãy chuyển hóa sau: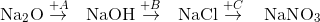 . Các chất A, B, C trong dãy trên lần lượt là:
. Các chất A, B, C trong dãy trên lần lượt là:
- A H2O, HCl, KNO3
- B H2O, HCl, HNO3
- C H2O, HCl, AgNO3
- D H2O, HCl, Ba(NO3)2
Đáp án: C
Lời giải chi tiết:
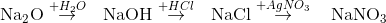
Đáp án C
Câu hỏi 4 :
1. Nêu hiện tượng và viết phương trình hóa học của phản ứng xảy ra trong các thí nghiệm sau:
a) Nhỏ vài giọt dung dịch NaOH vào ống nghiệm có chứa 1 ml dung dịch FeCl3, lắc nhẹ ống nghiệm.
b) Đốt một ít photpho đỏ (bằng hạt đậu xanh) trong bình thủy tinh miệng rộng. Sau khi photpho cháy hết, cho 2-3 ml nước vào nình, đậy nút, lắc nhẹ. Thử dung dịch trong bình bằng quỳ tím.
2. Trong quá trình tiến hành thí nghiệm, một học sinh không may bị axit H2SO4 đặc dây vào tay, học sinh này cần làm gì để hạn chế tối đa tác hại của tai nạn không mong muốn này?
Phương pháp giải:
1. a), b) hiện tượng quan sát được là những gì bằng mắt thường có thể nhìn thấy, hoặc mũi có thể ngửi thấy: đó là sự thay đổi về màu sắc, xuất hiện kết tủa hay không, kết tủa màu gì, có khí thoát ra hay không, khí màu hay mùi gì, các chất tan hay không tan...
2. Dựa vào kiến thức thực tế và tính chất hóa học của H2SO4 đặc để tìm cách khắc phục tối ưu.
Lời giải chi tiết:
1.
a) Hiện tượng: xuất hiện kết tủa màu nâu đỏ của Fe(OH)3 do xảy ra phương trình hóa học
3NaOH + FeCl3 → Fe(OH)3↓(nâu đỏ) + 3NaCl
b) Hiện tượng: Photpho đỏ (bằng hạt đậu xanh) cháy với ngọn lửa sáng chói, tạo ra khói trắng dày đặc bám vào thành lọ đó chính là P2O5. Cho 2-3 ml nước vào bình, đậy nút, lắc nhẹ thì bột trắng này tan dần, tạo thành dung dịch không màu đó chính là dd axit H3PO4. Cho quỳ tím vào dung dịch này quỳ tím chuyển sang màu đỏ.
PTHH: 4P(r) + 5O2(k) \(\buildrel {{t^0}} \over\longrightarrow \) 2P2O5(khói trắng)
P2O5 + H2O → H3PO4 (dd không màu)
2. Khi học sinh không may bị axit H2SO4 đặc dây vào tay thì học sinh cần làm để giảm tối đa tác hại của tai nạn:
+ Đầu tiên cần xả nước lạnh mạnh vào phần vết thương bị dây axit H2SO4 đặc
+ Sau đó rửa vết thương bằng dung dịch NaHCO3 để trung hòa axit còn lại trên da
PTHH: 2NaHCO3 + H2SO4 → Na2SO4 + 2CO2↑ + 2H2O
Câu hỏi 5 :
Viết phương trình hóa học thực hiện chuỗi phản ứng sau:
Zn → ZnO → ZnCl2 → Zn(NO3)2 → Zn(OH)2 → ZnSO4
Phương pháp giải:
Dựa vào sơ đồ viết chuyển hóa các chất từ kim loại ra oxit bazo, ra muối, bazo
Lời giải chi tiết:
PTHH
\(\eqalign{
& Zn + {O_2}\buildrel {{t^0}} \over
\longrightarrow ZnO \cr
& ZnO + 2HCl\buildrel {} \over
\longrightarrow ZnC{l_2} + {H_2}O \cr
& ZnC{l_2} + 2AgN{O_3}\buildrel {} \over
\longrightarrow Zn{(N{O_3})_2} + 2AgCl \downarrow \cr
& Zn{(N{O_3})_2} + 2NaOH\,vua\,du\buildrel {} \over
\longrightarrow Zn{(OH)_2} \downarrow + NaN{O_3} \cr
& Zn{(OH)_2} + {H_2}S{O_4}\buildrel {} \over
\longrightarrow ZnS{O_4} + 2{H_2}O \cr} \)
Câu hỏi 6 :
Từ các chất Na, Fe2O3, Al, H2O và dung dịch HCl. Viết các phương trình hóa học điều chế AlCl3, Fe(OH)3
(Cho biết:K = 39; H = 1; Mg = 24; O = 16; S = 32)
Phương pháp giải:
Điều chế muối AlCl3 cho kim loại Al tác dụng với axit hoặc muối
Điều chế Fe(OH)3 cho dd muối sắt (III) tác dụng với dd bazơ
Lời giải chi tiết:
Điều chế AlCl3
2Al + 6HCl → 2AlCl3 + 3H2↑
Điều chế Fe(OH)3
2Na + 2H2O → 2NaOH + H2↑
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl
Câu hỏi 7 :
Viết phương trình hóa học biểu diễn các chuyển đổi sau đây:
Fe → FeCl3 → Fe(OH)3→ Fe2O3 → Fe2(SO4)3
Phương pháp giải:
Dựa vào tính chất hóa học của sắt đã được học và sơ đồ chuyển hóa từ oxit bazo sang muối, bazo.
Lời giải chi tiết:
PTHH:
\(\eqalign{
& 2Fe + 3C{l_2}\buildrel {{t^0}} \over
\longrightarrow 2FeC{l_3} \cr
& FeC{l_3} + 3NaOH\buildrel {} \over
\longrightarrow Fe{(OH)_3} + 3NaCl \cr
& 2Fe{(OH)_3}\buildrel {{t^0}} \over
\longrightarrow F{e_2}{O_3} + 3{H_2}O \cr
& F{e_2}{O_3} + 3{H_2}S{O_4}\buildrel {} \over
\longrightarrow F{e_2}{(S{O_4})_3} + 3{H_2}O \cr} \)
Câu hỏi 8 :
Hoàn thành các phương trình hóa học theo sơ đồ sau: (Ghi rõ điều kiện nếu có)
\(Zn\buildrel {(1)} \over
\longrightarrow ZnC{l_2}\buildrel {(2)} \over
\longrightarrow Zn{(OH)_2}\buildrel {(3)} \over
\longrightarrow ZnO\buildrel {(4)} \over
\longrightarrow ZnS{O_4}\buildrel {(5)} \over
\longrightarrow Zn\)
Phương pháp giải:
Dựa vào tính chất hóa học của kim loại, bazo, muối để viết được phương trình.
Lời giải chi tiết:
\(\eqalign{
& (1)\,Zn + 2HCl\buildrel {} \over
\longrightarrow ZnC{l_2} + {H_2} \cr
& (2)\,ZnC{l_2} + NaOH\,vua\,du\buildrel {} \over
\longrightarrow Zn{(OH)_2} \downarrow + 2NaCl \cr
& (3)\,Zn{(OH)_2}\buildrel {{t^0}} \over
\longrightarrow ZnO + {H_2}O \cr
& (4)\,ZnO + {H_2}S{O_4}\buildrel {} \over
\longrightarrow ZnS{O_4} + {H_2}O \cr
& (5)\,ZnS{O_4} + Mg\buildrel {} \over
\longrightarrow Zn + Mg{(N{O_3})_2} \cr} \)
Câu hỏi 9 :
Viết các phương trình hóa học thực hiện chuỗi biến hóa sau đây, ghi rõ điều kiện phản ứng (nếu có):
\(Mg\buildrel {(1)} \over
\longrightarrow Mg{\rm{S}}{O_4}\buildrel {(2)} \over
\longrightarrow Mg{(OH)_2}\buildrel {(3)} \over
\longrightarrow MgC{l_2}\buildrel {(4)} \over
\longrightarrow Mg{(N{O_3})_2}\)
Phương pháp giải:
Xem lại tính chất hóa học của các hợp chất vô cơ
Lời giải chi tiết:
\(\begin{array}{l}(1)Mg + {H_2}S{O_4} \to Mg{\rm{S}}{O_4} + {H_2}\\(2)\,Mg{\rm{S}}{O_4} + 2NaOH \to Mg{(OH)_2} + N{a_2}S{O_4}\\(3)Mg{(OH)_2} + 2HCl \to MgC{l_2} + 2{H_2}O\\(4)MgC{l_2} + 2AgN{O_3} \to 2AgCl + Mg{(N{O_3})_2}\end{array}\)
Câu hỏi 10 :
Thực hiện chuỗi phương trình hóa học sau, ghi rõ điều kiện phản ứng (nếu có)
\(Cu\buildrel {(1)} \over
\longrightarrow CuO\buildrel {(2)} \over
\longrightarrow CuS{O_4}\buildrel {(3)} \over
\longrightarrow CuC{l_2}\buildrel {(4)} \over
\longrightarrow Cu{(OH)_2}\)
Phương pháp giải:
Xem lại tính chất hóa học của các hợp chất vô cơ.
Lời giải chi tiết:
(1) \(2Cu + {O_2}\buildrel {{t^0}} \over\longrightarrow 2CuO\)
(2) \(CuO + {H_2}S{O_4} \to CuS{O_4} + {H_2}O\)
(3) \(CuS{O_4} + BaC{l_2} \to CuC{l_2} + BaS{O_4} \downarrow \)
(4) \(CuC{l_2} + 2NaOH \to Cu{(OH)_2} \downarrow + 2NaCl\)
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Các bài khác cùng chuyên mục
- 20 bài tập vận dụng áp dụng định luật bảo toàn khối lượng có lời giải
- 15 bài tập áp dụng định luật tăng giảm khối lượng có lời giải
- 10 bài tập vận dụng áp dụng phương pháp tương đương (công thức trung bình) có lời giải
- 10 câu hỏi vận dụng áp dụng phương pháp biện luận có lời giải
- 10 bài tập vận dụng áp dụng phương pháp bảo toàn nguyên tố có lời giải
- 10 bài tập vận dụng về phương pháp qui đổi có lời giải
- 10 bài tập vận dụng áp dụng phương pháp bảo toàn nguyên tố có lời giải
- 10 câu hỏi vận dụng áp dụng phương pháp biện luận có lời giải
- 10 bài tập vận dụng áp dụng phương pháp tương đương (công thức trung bình) có lời giải
- 15 bài tập áp dụng định luật tăng giảm khối lượng có lời giải







