Lý thuyết bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Lý thuyết: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
I. Định luật tuần hoàn
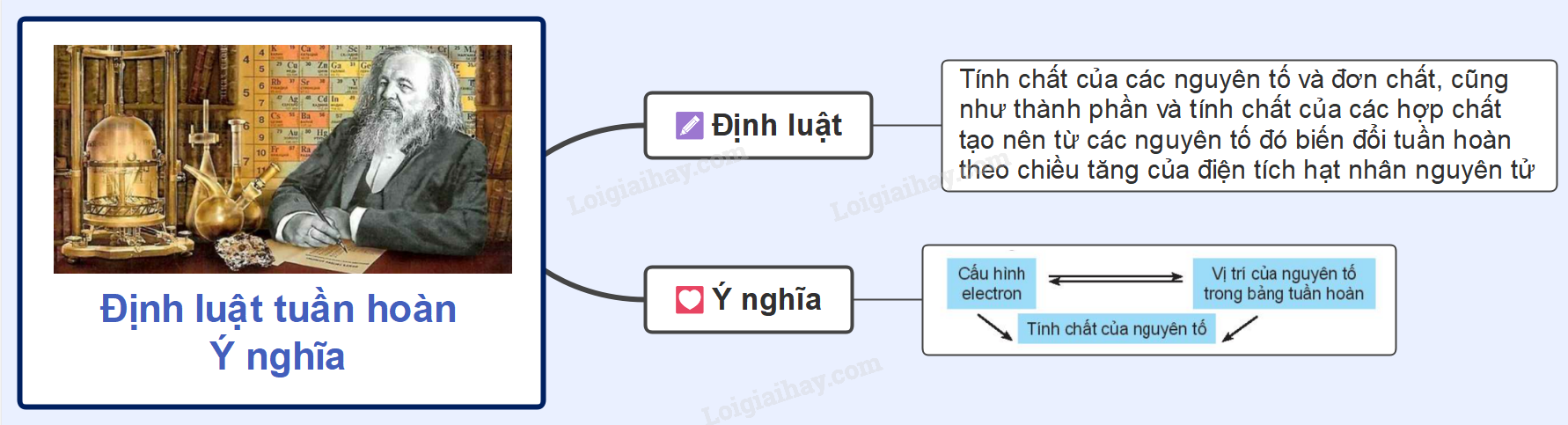
- Nội dung: "Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử."
Em có biết:

- Dựa trên xu hướng biến đổi tính chất của các nguyên tố hóa học khi sắp xếp theo chiều tăng dần khối lượng nguyên tử D. I. Mendeleev đã đưa ra 2 quyết định quan trọng:
+ Ông đã dành chỗ trống cho các nguyên tố khi đó chưa được tìm ra và dự đoán tính chất của chúng
Ví dụ: nguyên tố gallium và germanium
+ Ông bỏ qua trật tự cứng nhắc theo chiều tăng của khối lượng nguyên tử để sắp xếp các nguyên tố theo hướng biến đổi tính chất
Ví dụ: nguyên tố terillium có số khối lớn hơn được xếp trước nguyên tố iodine trong bảng tuần hoàn các nguyên tố
- Các quyết định này của ông phù hợp với nguyên tắc sắp xếp các nguyên tố theo chiều tăng của điện tích hạt nhân
II. Ý nghĩa của bảng tuần hoàn

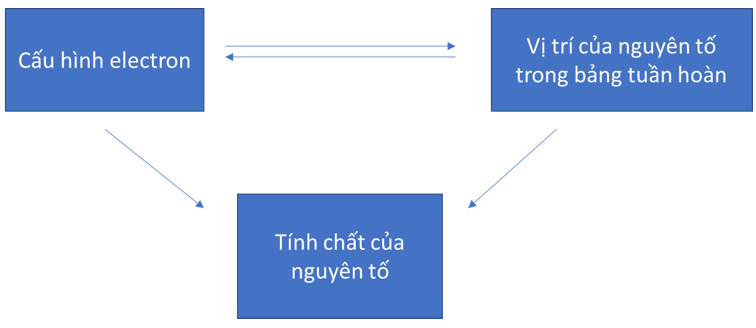
- Vị trí của nguyên tố trong bảng tuần hoàn các nguyên tố hóa học cho biết cấu hình electron nguyên tử, cấu hình electron nguyên tử quyết định tính chất của các nguyên tố. Vì vậy, có thể dự đoán tính chất hóa học của các nguyên tố khi biết vị trí của nó trong bảng tuần hoàn các nguyên tố hóa học hay cấu hình electron của nó
Ví dụ 1: Nguyên tố sulfur (S) ở ô số 16, nhóm VIA, chu kì 3
- Nguyên tử S có:
+ 16 proton, 16 electron (do số proton = số electron = Z)
+ 3 lớp electron (do số lớp electron bằng số thứ tự chu kì)
+ 6 electron lớp ngoài cùng (do số electron lớp ngoài cùng bằng số thứ tự nhóm A)
=> Cấu hình electron của S: 1s22s22p63s23p4
Luyện Bài Tập Trắc nghiệm Hóa 10 - Kết nối tri thức - Xem ngay












Danh sách bình luận