Bài 18. Hydrogen halide và hydrohalic acid trang 109, 110, 111, 112, 113, 114 Hóa 10 Cánh diều
Tải vềKhi hòa tan mỗi hydrogen halide HF, HCl, HBr và HI vào nước thì thu được các dung dịch hydrohalic acid. Dung dịch nào có tính acid yếu nhất? Vì sao? Giải thích tại sao xu hướng phân cực của các phân tử HX giảm dần từ HF đến HI
CH tr 109 MĐ
| Khi hòa tan mỗi hydrogen halide HF, HCl, HBr và HI vào nước thì thu được các dung dịch hydrohalic acid. Dung dịch nào có tính acid yếu nhất? Vì sao? |
Lời giải chi tiết:
- Tính acid phụ thuộc vào khả năng tách H của acid. Phân tử nào càng dễ tách H thì tính acid càng mạnh
- Trong nhóm halogen, từ F đến I có độ âm điện giảm dần
=> Khả năng liên kết H-X giảm dần
=> Khả năng tách H trong HX tăng dần
=> Tính acid tăng dần
=> Dung dịch HF có tính acid yếu nhất
CH tr 109 CH
| 1. Giải thích tại sao xu hướng phân cực của các phân tử HX giảm dần từ HF đến HI |
Phương pháp giải:
Độ âm điện giảm dần
Lời giải chi tiết:
Trong nhóm halogen, từ F đến I có độ âm điện giảm dần
=> Sự chênh lệch độ âm điện giữa H và X giảm dần
=> Độ phân cực H-X giảm dần từ F đến I
CH tr 109 CH
|
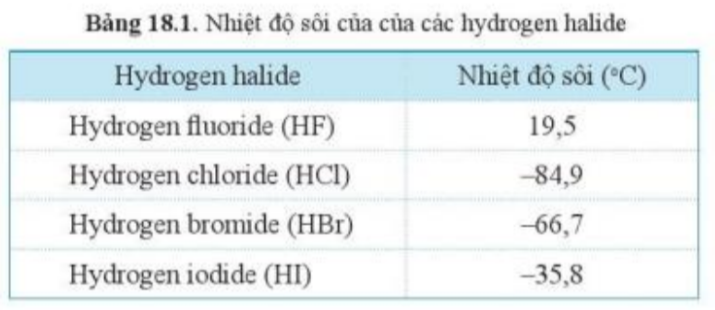
2. Dựa vào Bảng 18.1, hãy cho biết khí hydrogen halide nào sẽ hóa lỏng trước tiên khi nhiệt độ được hạ xuống thấp dần |
Phương pháp giải:
Nhiệt độ sôi = Nhiệt độ hóa lỏng
Lời giải chi tiết:
- Ở điều kiện thường, nhiệt độ là 25oC, tất cả các hydrogen halide đều ở thể khí
=> Khi hạ nhiệt độ xuống thấp dần, hydrogen fluoride sẽ được hóa lỏng đầu tiên
CH tr 111 CH
| 3. Phản ứng của sodium chloride rắn, hay của sodium iodide rắn với sulfuric acid đặc là phản ứng oxi hóa – khử? Vì sao? |
Phương pháp giải:
Tham khảo Bảng 18.2:
Lời giải chi tiết:
- Xét phản ứng của NaCl với H2SO4:
NaCl(s) + H2SO4(l) \(\xrightarrow{{{t^o}}}\) NaHSO4(s) + HCl(g)
=> Ion Cl- không thể hiện tính khử, không có sự thay đổi số oxi hóa
=> Không phải phản ứng oxi hóa – khử
- Xét phản ứng của NaI với H2SO4:
8NaI(s) + 9H2SO4(l) → 8NaHSO4(s) + I2(g) + H2S(g) + 4H2O(g)
=> Ion I- thể hiện tính khử và khử sulfur trong H2SO4 từ số oxi hóa +6 về số oxi hóa -2 trong H2S
- Giải thích: Do ion Cl- có tính khử yếu hơn ion I-
CH tr 111 LT
| 1. Có thể điều chế được hydrogen bromide từ phản ứng giữa potassium bromide với sulfuric acid đặc, đun nóng không? Vì sao? |
Phương pháp giải:
Tham khảo Bảng 18.2
Lời giải chi tiết:
- Khi potassium bromide phản ứng với sulfuric acid đặc, đun nóng. Ta có phương trình:
2NaBr(s) + 3H2SO4(l) \(\xrightarrow{{{t^o}}}\) 2NaHSO4(s) + Br2(g) + SO2(g) + 2H2O(g)
=> Sản phẩm tạo thành không có HBr
=> Không thể điều chế hydrogen bromide từ phản ứng giữa potassium bromide với sulfuric acid đặc
CH tr 112 VD
| 1. Vật dụng bằng kim loại đồng dễ bị phủ bởi lớp copper(II) oxide
a) Vì sao có thể sử dụng dung dịch hydrochloric acid để tẩy rửa copper (II) oxide? b) Có thể sử dụng một số dung dịch thường có sẵn trong gia đình để tẩy rửa copper(II) oxide. Đó có thể là dung dịch nào? Vì sao? |
Phương pháp giải:
a) Oxide + acid → Muối + Nước
b) Giấm ăn, chanh
Lời giải chi tiết:
a)
- Dung dịch hydrochloric acid được dùng để trung hòa môi trường base: oxide base, base
=> Sử dụng dung dịch hydrochloric acid để tẩy rửa lớp copper(II) oxide tạo thành dung dịch muối và nước
- Phương trình hóa học:
CuO + HCl → CuCl2 + H2O
b) Các dung dịch có sẵn trong gia đình để tẩy rửa copper(II) oxide là: nước chanh, giấm ăn. Vì chúng có tính acid, có thể loại bỏ được lớp copper(II) oxide:
Acid + Oxide base → Muối + Nước
CH tr 113 TH
| Nhận biết các dung dịch
Có bốn bình nhỏ được đậy bằng nút có ổng nhỏ giọt. Mỗi bình chứa một trong các dung dịch sodium chloride, sodium bromide, sodium iodide, hydrochlodric acid nhưng tên hóa chất ghi trên nhãn đã bị nhòe. Hãy thảo luận về hóa chất, dụng cụ cần dùng và trình tự tiến hành thí nghiệm để nhận ra mỗi bình chứa dung dịch gì. Tiến hành thí nghiệm, ghi lại kết quả. Lặp lại thí nghiệm để kiểm tra kết quả |
Phương pháp giải:
- Bước 1: Sử dụng quỳ tím để nhận biết hydrochlodric acid
- Bước 2: Sử dụng silver nitrate
Lời giải chi tiết:
- 4 dung dịch cần nhận biết là: NaCl, NaBr, NaI, HCl
- Hóa chất: Giấy quỳ tím, dung dịch silver nitrate
- Dụng cụ: 4 ống nghiệm
- Tiến hành thí nghiệm và kết quả:
Bước 1: Lấy ở mỗi bình khoảng 2 mL dung dịch vào 4 ống nghiệm tương ứng
Bước 2: Sử dụng quỳ tím nhúng vào 4 dung dịch trong 4 ống nghiệm. Ống nghiệm nào làm quỳ tím hóa đỏ => Dung dịch hydrochlodric acid
Bước 3: Nhỏ khoảng 2 mL dung dịch silver nitrate vào 3 ống nghiệm còn lại và có những hiện tượng sau:
Ống nghiệm xuất hiện kết tủa trắng AgCl => Ống nghiệm đó chứa NaCl
NaCl + AgNO3 → AgCl↓ + NaNO3
Ống nghiệm xuất hiện kết tủa vàng nhạt AgBr => Ống nghiệm đó chứa NaBr
NaBr + AgNO3 → AgBr↓ + NaNO3
Ống nghiệm xuất hiện kết tủa vàng AgI => Ống nghiệm đó chứa NaI
NaI + AgNO3 → AgI↓ + NaNO3
CH tr 113 LT
| 1. Hãy mô tả hiện tượng và viết phương trình hóa học khi cho từ từ vài giọt dung dịch silver nitrate vào ống nghiệm chứa từng dung dịch potassium fluoride, hydrochloric acid, sodium bromide |
Phương pháp giải:
Khi nhỏ dung dịch silver nitrate vào dung dịch chứa ion X-
+ Nếu xuất hiện kết tủa trắng => Cl-
+ Nếu xuất hiện kết tủa vàng nhạt => Br-
+ Nếu không thấy sự biến đổi => F-
Lời giải chi tiết:
- Khi cho từ từ vài giọt dung dịch silver nitrate vào ống nghiệm chứa từng dung dịch potassium fluoride, hydrochloric acid, sodium bromide:
+ Ống nghiệm xuất hiện kết tủa trắng AgCl => Ống nghiệm đó chứa HCl
HCl + AgNO3 → AgCl↓ + HNO3
+ Ống nghiệm xuất hiện kết tủa vàng nhạt AgBr => Ống nghiệm đó chứa NaBr
NaBr + AgNO3 → AgBr↓ + NaNO3
+ Ống nghiệm không có sự biến đổi do không có phản ứng hóa học xảy ra => Ống nghiệm chứa KF
Bài tập 1
|
Bài 1. Hãy giải thích vì sao nhiệt độ sôi của hydrogen bromide cao hơn nhiệt độ sôi của hydrogen chloride |
Phương pháp giải:
Nhiệt độ sôi phụ thuộc vào:
+ Khối lượng phân tử
+ Lực van der Waals
Lời giải chi tiết:
Nhiệt độ sôi của hydrogen bromide cao hơn nhiệt độ sôi của hydrogen chloride được giải thích như sau:
+ Khối lượng phân tử HBr (81) cao hơn khối lượng phân tử HCl (36,5)
+ Br có bán kính nguyên tử lớn, có nhiều electron hơn Cl => Tăng khả năng lưỡng cực HX => Làm tăng tương tác van der Waals giữa các phân tử
Bài tập 2
|
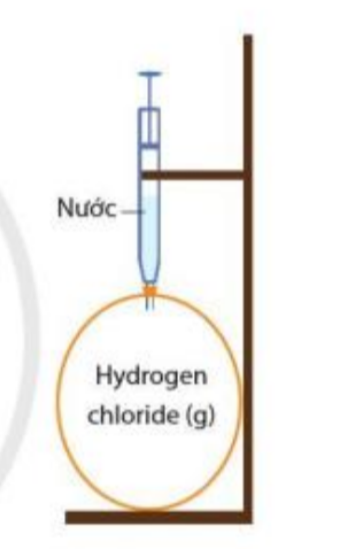
Bài 2. Quan sát hình bên, nếu bơm từ từ cho đến hết lượng nước trong xi – lanh vào bong bóng chứa khí hydrogen chloride thì hiện tượn gì sẽ xảy ra. Giải thích |
Phương pháp giải:
Quả bóng xẹp vào
Lời giải chi tiết:
Khí hydrogen chloride tan nhiều trong nước tạo thành dung dịch hydrochloric acid
=> Khi bơm nước vào, khí hydrogen chloride bị hòa tan hết
=> Quả bóng bị xẹp vào
Bài tập 3
|
Bài 3. Phản ứng dưới đây có thể được thực hiện để điều chế khí chlorine trong phòng thí nghiệm 4HCl + MnO2 → Cl2 + MnCl2 + 2H2O a) Trong phản ứng trên, hãy xác định chất khử và chất oxi hóa b) Hãy dự đoán, hydroiodic acid có phản ứng được với mangan(IV) oxide không. Giải thích |
Phương pháp giải:
- Chất khử là chất nhường electron
- Chất oxi hóa là chất nhận electron
Lời giải chi tiết:
\(4H\mathop {Cl}\limits^{ - 1} {\text{ }} + {\text{ }}\mathop {Mn}\limits^{ + 4} {O_2} \to {\mathop {Cl}\limits^0 _2} + {\text{ }}\mathop {Mn}\limits^{ + 2} C{l_2} + {\text{ }}2{H_2}O\)
a)
\(\mathop {Mn}\limits^{ + 4} + 2e \to \mathop {Mn}\limits^{ + 2} \) => MnO2 là chất oxi hóa
\(\mathop {2Cl}\limits^{ - 1} \to \mathop {C{l_2}}\limits^0 + 2e\) => HCl là chất khử
b) HI có tính khử mạnh hơn HCl
=> HI có thể phản ứng được với MnO2
4HI + MnO2 → I2 + MnI2 + 2H2O
Bài tập 4
|
Bài 4. Dung dịch hydrobromic acid không màu, để lâu trong không khí thí chuyển sang màu vàng nâu do phản ứng với oxygen trong không khí a) Từ hiện tượng được mô tả trên, hãy dự đoán sản phẩm của quá trình dung dịch hydrobromic acid bị oxi hóa bởi oxygen trong không khí b) Thực tế, hydrobromic acid được bảo quản trong các lọ tối màu. Giải thích |
Phương pháp giải:
a) Màu vàng nâu là màu của nước bromine
b) Sẽ bị oxi hóa
Lời giải chi tiết:
a)
Khi để lâu trong không khí thì chuyển sang màu vàng nâu => Sản phẩm có sự tạo thành nước Bromine
4HBr + O2 → 2Br2 + 2H2O
b)
Hydrobromic acid được bảo quản trong các lọ tối màu, nếu để nơi có ánh sáng hoặc trong bình sáng thì khí oxygen sẽ được tạo ra do thành phần của acid HBrO
=> HBr bị oxi hóa bởi oxygen












Danh sách bình luận